
- •Лекций по курсу «методы получения биологически активных соединений» Электронный вариант на основе учебника: в.С. Мокрушин, г.А. Вавилов
- •Предисловие
- •Введение
- •Глава 1
- •Классификация лекарственных средств
- •Действие лекарственных средств на метаболизм живых организмов
- •1.2. Методы поиска новых препаратов
- •1.2.1. Основные этапы создания лекарственных препаратов, подходы к получению и отбору лекарственных средств
- •1.2.2. Разработка плана синтеза
- •1.3. Сырьевая база химико-фармацевтической промышленности
- •1.3.1. Продукты переработки твердого топлива и коксохимического производства
- •1.3.2. Продукты нефтеоргсинтеза
- •1.3.3. Лесохимическое сырье
- •1.3.4. Некоторые продукты многотоннажных производств
- •1.4. Теоретические аспекты выбора метода синтеза
- •1.4.1. Энергетические факторы
- •1.4.2. Классификация реакций
- •1.4.3. Механизм и кинетика реакций
- •1.4.4. Уравнения Гаммета, Тафта
- •1.4.5. Квантово-химические расчеты
- •1.4.6. Выбор растворителя
- •Характеристики растворителей
- •1.5. Разработка технологической схемы производства
- •1.5.1. Категории и типы технологических схем
- •1.5.2. Правила составления и основные требования к технологическим схемам
- •1.5.3. Оформление чертежей технологических схем
- •1.5.4. Типовое оснащение и привязка химического реактора к конкретному производству
- •Глава 2 методы получения промежуточных продуктов и синтетических лекарственных препаратов
- •2.1. Реакции электрофильного замещения
- •2.1.1. Нитрование
- •2.1.1.1. Реакции нитрования в синтезе некоторых лекарственных препаратов
- •2.1.1.2. Химические особенности реакций нитрования, реагенты, механизм
- •2.1.1.3. Нитрование арил и гетариламинов
- •2.1.1.4. Нитрование азотной кислотой
- •2.1.1.5. Технологические аспекты нитрования
- •2.1.1.6. Использование реакции нитрования для получения полупродуктов и лекарственных средств
- •2.1.1.7. Получение нитроэфиров и n-нитросоединений Так же как и при нитровании ароматических соединений, при получении нитроэфиров используют смесь азотной и серной кислот:
- •2.1.2. Нитрозирование
- •2.1.2.1. Механизм нитрозирования, реагенты
- •2.1.2.2. Особенности проведения реакции
- •2.1.2.3. Особенности структуры и свойств нитрозосоединений
- •2.1.2.4. Практика проведения реакции нитрозирования
- •2.1.2.5. Техника безопасности, экология
- •2.1.3. Сульфирование
- •2.1.3.2. Реагенты, использующиеся при проведении реакции сульфирования, механизм реакции
- •2.1.3.3. Особенности сульфирования, побочные реакции
- •2.1.3.4. Влияние температуры
- •2.1.3.5. Сульфирование бензола и его производных
- •2.1.3.6. Сульфирование анилина и его производных
- •2.1.3.8. Сульфирование хлорсульфоновой кислотой
- •2.1.3.9. Техника безопасности, экология
- •2.1.4. Сульфохлорирование
- •2.1.4.1. Химические особенности реакции
- •2.1.4.2. Технологические аспекты сульфохлорирования
- •2.1.4.3. Синтез сульфаниламидных препаратов
- •2.1.4.4. Техника безопасности, экология
- •2.1.5. Введение углеродных остатков в Ароматическое и гетероциклическое ядро
- •2.1.5.1. Реакции с-алкилирования
- •Реагенты, катализаторы. Как отмечалось, реагентами могут быть алкилгалогениды, олефины и спирты:
- •Механизм реакции. При взаимодействии реагента и катализатора быстро образуется карбокатион, его присутствие зафиксировано с помощью спектроскопии ямр:
- •2.1.5.2. Реакции гидроксиалкилирования
- •2.1.5.3. Реакции хлоралкилирования
- •2.1.5.4. Реакции аминоалкилирования
- •2.1.5.5. Реакции с-ацилирования
- •2.1.5.6. Реакции с-формилирования
- •2.1.5.7. Реакция карбоксилирования
- •2.1.5.8. Карбоксилирование алифатических соединений
- •2.1.5.9. Техника безопасности, экология
- •2.1.6. Галогенирование
- •2.1.6.1. Препараты, содержащие в молекуле атомы галогенов
- •2.1.6.2. Реагенты, механизм реакций галогенирования
- •2.1.6.3. Хлорирование ароматических соединений
- •2.1.6.4. Бромирование, иодирование
- •2.1.6.5. Технологические аспекты галогенирования
- •2.1.6.7. Галогенирование альдегидов, кетонов и кислот
- •2.1.6.8. Свободнорадикальное галогенирование
- •Энергия стадий процесса
- •2.1.6.10. Получение галогенамидов
- •2.1.6.11. Окислительное хлорирование
- •2.1.6.12. Меры предосторожности при проведении реакций галогенирования
- •2.1.6.13. Экология
- •2.2. Реакции нуклеофильного замещения
- •Реакции нуклеофильного замещения у насыщенного атома углерода
- •2.2.1.1. Типы реакций
- •Реагенты для проведения реакций алкилирования
- •Механизмы реакций
- •Алкилирование аминов
- •Селективные методы синтеза первичных аминов
- •Селективные методы синтеза вторичных аминов
- •Алкилирование спиртов и фенолов
- •Алкилирование сн кислот
- •Алкилирование гетероциклических соединений
- •Техника безопасности, экология
- •2.2.2. Реакции нуклеофилов с соединениями,
- •2.2.2.1. Обзор реакций, их кинетика и механизм
- •2.2.2.2. Реакции ацилирования
- •2.2.2.3. Реакции нитрилов с нуклеофилами
- •2.2.2.4. Реакции этерификации, получение амидов и гидразидов кислот
- •2.2.2.5. Получение азометинов и гидразонов
- •2.2.2.6. Методы получения первичных аминов с помощью перегруппировок
- •2.2.2.7. Использование реакций в основном органическом синтезе
- •2.2.2.8. Технология, техника безопасности, экология
- •2.2.3. Нуклеофильное замещение в ряду ароматическИх и гетероциклических оединений
- •2.2.3.1. Нуклеофильное замещение по типу sn1
- •2.2.3.2. Ариновое замещение
- •2.2.3.3. Реакции нуклеофилов с ипсо-замещением нуклеофугных групп
- •Получение полупродуктов и лекарственных препаратов. В отсутствие электроноакцепторных заместителей замещение атома хлора происходит при высокой температуре и в присутствии катализатора:
- •2.2.3.4. Нуклеофильное замещение водорода
- •Еще в начале хх в. Было найдено, что реакция хинолина (изохинолина, фенантридина) с хлорангидридами кислот и цианидом натрия дает устойчивые соединения Райсерта (реакция Райсерта):
- •2.2.3.5. Замещение гидроксигрупп
- •2.2.3.6. Замещение по механизму anrorc
- •2.2.3.7. Технологические аспекты проведения реакций, техника безопасности, экология
1.3. Сырьевая база химико-фармацевтической промышленности
Основные продукты, которые получают с помощью тонкого, основного, нефтеоргсинтеза, лесохимии, коксохимического и микробиологического производства.
Для планирования синтеза конкретного лекарственного препарата и технологического оформления процессов необходимо в первую очередь обратиться к литературе и выяснить состояние промышленной разработки в нашей стране и за рубежом. Вторым шагом является оценка имеющихся либо вновь разработанных альтернативных методов получения препарата с точки зрения использования различных видов сырья в каждом методе, его стоимость и доступность. Для примера: в синтезе препарата необходимо использовать п-нитрохлорбензол. Его производят на Березниковском химзаводе, Рубежанском химкомбинате (Украина) и фирме Merk (Германия). Стоимость 1 т продукта одинакова, но транспортные расходы весьма отличаются. К тому же необходимо оценить и надежность поставщика. Безусловно, самым надежным будет его производство на своем заводе, но стоимость крупнотоннажного производства, конечно же ниже, чем своего небольшого.
Основные отрасли промышленности, которые поставляют сырье для промышленного получения синтетических ЛС в химико-фармацевтической промышленности (ХФП):
1) химическая переработка каменного угля, нефти, газа, древесины;
2) выделение продуктов из сырья растительного и животного происхож-дения;
3) микробиологический синтез.
Рассмотрим более подробно каждый из источников.
1.3.1. Продукты переработки твердого топлива и коксохимического производства
Переработка коксующихся углей при температуре 1 000 – 1 250 ОС без доступа воздуха в коксовых батареях дает кокс, являющийся важнейшим сырьем для производства чугуна. Кроме того, кокс служит исходным продуктом для получения карбида кальция и сероуглерода (CS2). При коксовании происходит отгонка летучих веществ, охлаждение уходящих газов и поглощение растворителем продуктов. Из 1 т каменного угля получают следующие продукты:
1) кокс, практически чистый углерод (выход – 730 – 780 кг). Газы – H2, H2S, CO, HCN, CH4 и др. (150 – 180 кг);
2) сырой бензол (легкое масло, Ткип < 200 ОС): бензол, толуол, ксилолы, сольвент (этилбензол, этилтолуолы, мезитилен, инден, кумарон, стирол и др.), фенол, крезолы, ксиленолы, пиридин, пиколины (2-, 3-, 4-метилпиридины), диметилпиридины (лутидины), (80 – 110 кг на 1 т шихты);
3) каменноугольная смола – сложная смесь соединений (около 10 000 веществ). Выделено и идентифицировано около 500 веществ, составляющих около 50 % общей массы. Каменноугольная смола имеет три основных летучих фракции и пек: среднее масло, Ткип 200 – 250 оС (состав: фенол, крезолы, пиридиновые основания, нафталин); тяжелое масло, Ткип 250 – 300 оС (состав: нафталин, крезолы, ксиленолы, хинолин, изохинолин и их производные); антраценовое масло (состав: антрацен, фенантрен, карбазол и их производные). Выход каменноугольной смолы составляет 28 – 35 кг. Масштаб коксохимического производства в мире около 350 млн. т. Россия в настоящее время занимает одно из ведущих мест по его производству. При содержании одного из компонентов хотя бы 1 %, его масса составляет сотни тонн в год, что вполне может удовлетворить потребности ХФП. Однако сложность ситуации с продуктами коксохимпроизводства заключается в том, что компоненты находятся в смеси. Для ХФП необходимо иметь продукты высокой чистоты. Разделение сложных смесей является одной из труднейших задач химического производства. Так довольно долгое время при получении никотиновой и изоникотиновой кислот использовались синтетические 3- и 4-метилпириди-ны (пиколины). Долгое время эти пиколины, продукты коксохимического производства, уходили в отходы, т. к. не удавалось достичь их высокой чистоты. Сегодня эта задача решена.
Рассмотрим пример переработки легкого и среднего масла. В их составе имеются ароматические углеводороды, фенолы и пиридиновые основания. Фенолы и пиридиновые основания можно разделить за счет их различной основности. Так при обработке щелочью фенол и крезолы переходят в водный раствор. В органической фазе остаются ароматические углеводороды и пиридины. При подкислении водного раствора выделяются в твердом виде фенол и крезолы, разделить которые можно с помощью ректификации.
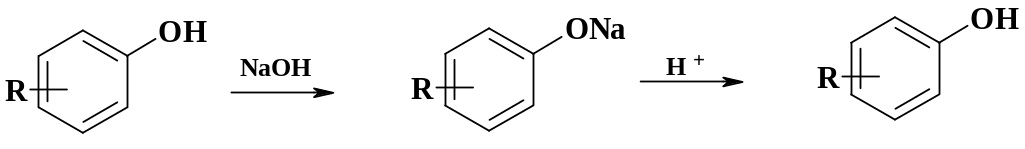
Выделение пиридиновых оснований основано на их способности образовывать водорастворимые соли с минеральными кислотами. При обработке оставшейся органической фазы водным раствором минеральной кислоты они переходят в водную фазу, после подщелачивания водной фазы выделяют производные пиридина.

Ректификацией разделяют пиридин, пиколины и лутидин. Оставшуюся органическую фазу также разгоняют, получают бензол, толуол и смесь ксилолов.
Таким образом сложную смесь с близкими температурами кипения компонентов разделяют с помощью химических методов. При ректификации из смеси производных пиридина отделяют 2-пиколин (2-метилпиридин). Фракция с Ткип 140 – 150 0С содержит 3- и 4-пиколины, и 2,6-лутидин, которые разделяют также с помощью химических методов. В реакцию с формальдегидом вступает только -пиколин, давая смесь метилольных производных. Лутидин и -пиколин не вступают в реакцию и их отгоняют острым паром. С помощью комплексообразования с солями меди отделяют 2,6-лутидин. Оставшийся -пиколин очищают перегонкой, при его окислении перманганатом калия в щелочи получают никотиновую кислоту. Окислением водного раствора метилольных производных получают изоникотиновую кислоту.

2,6-Лутидин используют в синтезе антисклеротического препарата пармидин (продектин). Пиридин применяют в качестве растворителя, кислотосвязывающего средства и при получении пиперидина. Бензол и толуол используют в качестве растворителей и как промежуточные продукты, ксилолы в качестве растворителей. Нафталин является сырьем в синтезе фталевого и малеинового ангидрида, а также нитро-, амино- и сульфопроизводных, которые служат промежуточными продуктами. Из антрацена получают антрахинон. Смесь хинолина и изохинолина, фенантрен и карбазол пока не нашли квалифицированного использования. Нерешенных проблем остается еще очень много.
