
- •Лекций по курсу «методы получения биологически активных соединений» Электронный вариант на основе учебника: в.С. Мокрушин, г.А. Вавилов
- •Предисловие
- •Введение
- •Глава 1
- •Классификация лекарственных средств
- •Действие лекарственных средств на метаболизм живых организмов
- •1.2. Методы поиска новых препаратов
- •1.2.1. Основные этапы создания лекарственных препаратов, подходы к получению и отбору лекарственных средств
- •1.2.2. Разработка плана синтеза
- •1.3. Сырьевая база химико-фармацевтической промышленности
- •1.3.1. Продукты переработки твердого топлива и коксохимического производства
- •1.3.2. Продукты нефтеоргсинтеза
- •1.3.3. Лесохимическое сырье
- •1.3.4. Некоторые продукты многотоннажных производств
- •1.4. Теоретические аспекты выбора метода синтеза
- •1.4.1. Энергетические факторы
- •1.4.2. Классификация реакций
- •1.4.3. Механизм и кинетика реакций
- •1.4.4. Уравнения Гаммета, Тафта
- •1.4.5. Квантово-химические расчеты
- •1.4.6. Выбор растворителя
- •Характеристики растворителей
- •1.5. Разработка технологической схемы производства
- •1.5.1. Категории и типы технологических схем
- •1.5.2. Правила составления и основные требования к технологическим схемам
- •1.5.3. Оформление чертежей технологических схем
- •1.5.4. Типовое оснащение и привязка химического реактора к конкретному производству
- •Глава 2 методы получения промежуточных продуктов и синтетических лекарственных препаратов
- •2.1. Реакции электрофильного замещения
- •2.1.1. Нитрование
- •2.1.1.1. Реакции нитрования в синтезе некоторых лекарственных препаратов
- •2.1.1.2. Химические особенности реакций нитрования, реагенты, механизм
- •2.1.1.3. Нитрование арил и гетариламинов
- •2.1.1.4. Нитрование азотной кислотой
- •2.1.1.5. Технологические аспекты нитрования
- •2.1.1.6. Использование реакции нитрования для получения полупродуктов и лекарственных средств
- •2.1.1.7. Получение нитроэфиров и n-нитросоединений Так же как и при нитровании ароматических соединений, при получении нитроэфиров используют смесь азотной и серной кислот:
- •2.1.2. Нитрозирование
- •2.1.2.1. Механизм нитрозирования, реагенты
- •2.1.2.2. Особенности проведения реакции
- •2.1.2.3. Особенности структуры и свойств нитрозосоединений
- •2.1.2.4. Практика проведения реакции нитрозирования
- •2.1.2.5. Техника безопасности, экология
- •2.1.3. Сульфирование
- •2.1.3.2. Реагенты, использующиеся при проведении реакции сульфирования, механизм реакции
- •2.1.3.3. Особенности сульфирования, побочные реакции
- •2.1.3.4. Влияние температуры
- •2.1.3.5. Сульфирование бензола и его производных
- •2.1.3.6. Сульфирование анилина и его производных
- •2.1.3.8. Сульфирование хлорсульфоновой кислотой
- •2.1.3.9. Техника безопасности, экология
- •2.1.4. Сульфохлорирование
- •2.1.4.1. Химические особенности реакции
- •2.1.4.2. Технологические аспекты сульфохлорирования
- •2.1.4.3. Синтез сульфаниламидных препаратов
- •2.1.4.4. Техника безопасности, экология
- •2.1.5. Введение углеродных остатков в Ароматическое и гетероциклическое ядро
- •2.1.5.1. Реакции с-алкилирования
- •Реагенты, катализаторы. Как отмечалось, реагентами могут быть алкилгалогениды, олефины и спирты:
- •Механизм реакции. При взаимодействии реагента и катализатора быстро образуется карбокатион, его присутствие зафиксировано с помощью спектроскопии ямр:
- •2.1.5.2. Реакции гидроксиалкилирования
- •2.1.5.3. Реакции хлоралкилирования
- •2.1.5.4. Реакции аминоалкилирования
- •2.1.5.5. Реакции с-ацилирования
- •2.1.5.6. Реакции с-формилирования
- •2.1.5.7. Реакция карбоксилирования
- •2.1.5.8. Карбоксилирование алифатических соединений
- •2.1.5.9. Техника безопасности, экология
- •2.1.6. Галогенирование
- •2.1.6.1. Препараты, содержащие в молекуле атомы галогенов
- •2.1.6.2. Реагенты, механизм реакций галогенирования
- •2.1.6.3. Хлорирование ароматических соединений
- •2.1.6.4. Бромирование, иодирование
- •2.1.6.5. Технологические аспекты галогенирования
- •2.1.6.7. Галогенирование альдегидов, кетонов и кислот
- •2.1.6.8. Свободнорадикальное галогенирование
- •Энергия стадий процесса
- •2.1.6.10. Получение галогенамидов
- •2.1.6.11. Окислительное хлорирование
- •2.1.6.12. Меры предосторожности при проведении реакций галогенирования
- •2.1.6.13. Экология
- •2.2. Реакции нуклеофильного замещения
- •Реакции нуклеофильного замещения у насыщенного атома углерода
- •2.2.1.1. Типы реакций
- •Реагенты для проведения реакций алкилирования
- •Механизмы реакций
- •Алкилирование аминов
- •Селективные методы синтеза первичных аминов
- •Селективные методы синтеза вторичных аминов
- •Алкилирование спиртов и фенолов
- •Алкилирование сн кислот
- •Алкилирование гетероциклических соединений
- •Техника безопасности, экология
- •2.2.2. Реакции нуклеофилов с соединениями,
- •2.2.2.1. Обзор реакций, их кинетика и механизм
- •2.2.2.2. Реакции ацилирования
- •2.2.2.3. Реакции нитрилов с нуклеофилами
- •2.2.2.4. Реакции этерификации, получение амидов и гидразидов кислот
- •2.2.2.5. Получение азометинов и гидразонов
- •2.2.2.6. Методы получения первичных аминов с помощью перегруппировок
- •2.2.2.7. Использование реакций в основном органическом синтезе
- •2.2.2.8. Технология, техника безопасности, экология
- •2.2.3. Нуклеофильное замещение в ряду ароматическИх и гетероциклических оединений
- •2.2.3.1. Нуклеофильное замещение по типу sn1
- •2.2.3.2. Ариновое замещение
- •2.2.3.3. Реакции нуклеофилов с ипсо-замещением нуклеофугных групп
- •Получение полупродуктов и лекарственных препаратов. В отсутствие электроноакцепторных заместителей замещение атома хлора происходит при высокой температуре и в присутствии катализатора:
- •2.2.3.4. Нуклеофильное замещение водорода
- •Еще в начале хх в. Было найдено, что реакция хинолина (изохинолина, фенантридина) с хлорангидридами кислот и цианидом натрия дает устойчивые соединения Райсерта (реакция Райсерта):
- •2.2.3.5. Замещение гидроксигрупп
- •2.2.3.6. Замещение по механизму anrorc
- •2.2.3.7. Технологические аспекты проведения реакций, техника безопасности, экология
Глава 2 методы получения промежуточных продуктов и синтетических лекарственных препаратов
2.1. Реакции электрофильного замещения
Реакции электрофильного замещения в ряду ароматических соединений широко используются для получения лекарственных средств. Эти реакции легко идут с производными фурана, тиофена, имидазола, пиразола, тиазола и некоторых других гетероциклов. Азины обычно реагируют в более жестких условиях, чем азолы. В данном разделе будут рассмотрены также и процессы, имеющие другой механизм реакции, но связанные с использованием общего реагента. Такое расположение материала обусловлено тем, что технологические и экологические особенности для них сходны.
К процессам электрофильного замещения относятся следующие реакции: нитрование, нитрозирование, азосочетание, сульфирование, сульфохлорирование, галогенирование (хлорирование, бромирование и иодирование, но не фторирование), реакции введения углеродных остатков (С-алкилирование и С-ацилирование, гидроксиметилирование, хлорметилирование, карбоксилирование и др.).
Одной из важных задач в синтезе лекарственных препаратов является введение в ароматическое или гетероциклическое ядро аминогруппы. Основные методы получения арил- и гетариламинов:

За исключением прямого нуклеофильного замещения водорода, все промежуточные продукты в их синтезе получают с помощью реакций электрофильного замещения. В первую очередь будут рассмотрены методы синтеза нитропроизводных.
2.1.1. Нитрование
Использование реакции нитрования в синтезе лекарственных препаратов, реагенты, механизм реакции, химические особенности нитрования различных органических соединений, технологические аспекты проведения нитрования. Получение нитроэфиров и N-нитросоединений, техника безопасности и экология.
Реакция нитрования имеет большое значение для производства химфармпрепаратов. Если в лекарственном препарате в ароматическом ядре содержатся NH2-, NHR-, NR2- группы, то промежуточным продуктом в их синтезе с большой долей вероятности является нитропроизводное.
2.1.1.1. Реакции нитрования в синтезе некоторых лекарственных препаратов
На примере получения ряда лекарственных средств рассмотрим использование реакции нитрования. Так в препарате прокаинамид (новокаинамид), который обладает местноанестезирующим действием, снижает возбудимость сердечной мышцы, используется при лечении аритмии, в ароматическом ядре имеется аминогруппа. Ретросинтетический анализ синтеза:

Аминогруппа может быть получена восстановлением соответствующего нитропроизводного, которое синтезируют из хлорангидрида п-нитробензойной кислоты. Его невозможно получить из амида бензойной кислоты, т. к. амидная группа является электроноакцепторным заместителем. Поэтому при нитровании нитрогруппа будет вступать преимущественно в м-положение. Аналогично п-нитробензойную кислоту не синтезируют из бензойной кислоты, а получают окислением п-нитротолуола.
На следующей схеме представлен ретросинтетический анализ получения мефенаминовой кислоты. Мефенаминовая кислота (мефенаминат натрия) проявляет противовоспалительное, анальгезирующее, жаропонижающее действие, ингибирует синтез простагландинов. Применяется при лечении ревматизма, полиартрита, зубной боли, невралгии, парадонтоза.
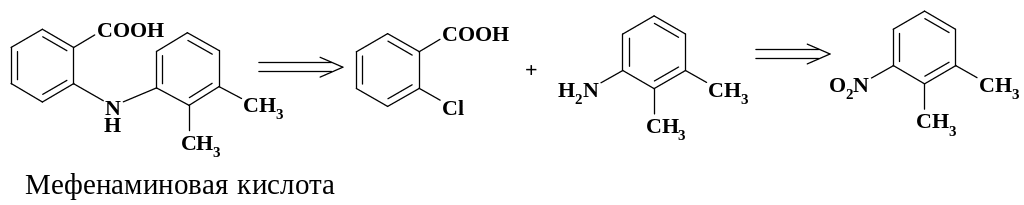
При синтезе этого препарата используют ксилидин-3, который получают восстановлением нитропроизводного. Нитрование ксилола дает 3- и 4-нитро-производные о-ксилола, которые разделяют вакуум ректификацией. Ксилидин-4 применяют при получении рибофлавина (витамина В2).
Еще один пример – синтез парацетамола (акамол, далерол, панадол), обладающего жаропонижающим, болеутоляющим, противовоспалительным действием. Ретросинтез рассмотрен в разделе 1.2. Препарат получают ацилированием п-аминофенола, который синтезируют из п-нитрофенола. Это соединение может быть получено как из фенола, так и из п-нитрохлорбензола. Сравнение двух альтернативных путей синтеза парацетамола позволяет отдать предпочтение гидролизу нитрохлорбензола щелочью, т. к. при нитровании фенола выход п-нитрофенола составляет лишь 30 % и разделение п- и о-нитрофенола требует больших энергозатрат (технологические особенности реакции нитрования различных ароматических производных рассмотрены ниже в данном разделе).
Азатиоприн (имуран) применяется как иммунодепрессант при трансплантации тканей, при красной волчанке, ревматическом полиартрите. В синтезе этого препарата используют нитрование 1-метил-5-хлоримидазола. Фрагмент ретросинтетического анализа приведен на схеме:

Нитрогруппа содержится в ряде лекарственных препаратов и является фармакофорной. В частности, она имеется в препарате аминитрозол (нитазол), который обладает широким спектром антибактериального действия и применяется для лечения острого и хронического мочеполового трихомониаза у мужчин и женщин.
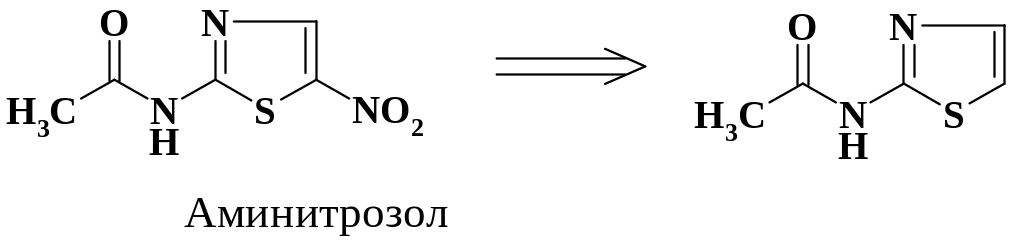
Метронидазол также применяют при лечении острого и хронического мочеполового трихомониаза у мужчин и женщин, а также лямблиоза. Препарат снижает влечение к алкоголю. Фрагмент ретросинтетического анализа получения субстанции препарата приведен на схеме.
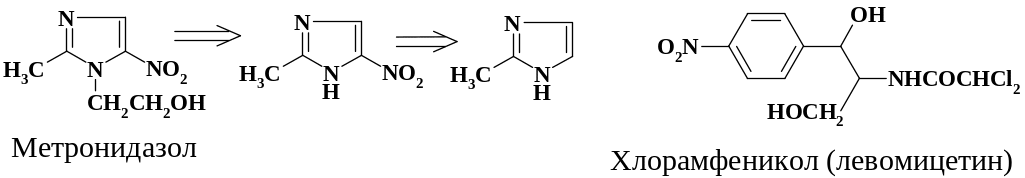
Антибиотик хлорамфеникол (левомицетин) – D-(-)-трео-1-п-нитро-фенил-2-дихлорацетиламинопропандиол-1,3. Применяют для лечения дизентерии, брюшного тифа, паратифа, бруцеллеза, туляремии, гонореи и других заболеваний. Этот антибиотик вначале был выделен из культуральной жидкости Streptomyces venezuelae, в настоящее время его получают синтетическим путем (рацемат называют синтомицин). Стадии синтеза препарата рассмотрены в разделах данного учебника.
Большая группа антибактериальных средств является производными нитрофурана. Они эффективны в отношении грамположительных и грамотрицательных микробов, а также некоторых крупных вирусов, трихомонад и лямблий.

Из перечисленных примеров видно, что нитрогруппа является фармакофорной, т. е. ее введение в соединение приводит к появлению биологической активности.
Таким образом, реакции нитрования имеют большое значение в синтезе ЛС. Однако нитрование относится к процессам, имеющим химические и технологические особенности, которые необходимо подробно рассмотреть при разработке оптимального метода синтеза целевого соединения.
