
- •Лекций по курсу «методы получения биологически активных соединений» Электронный вариант на основе учебника: в.С. Мокрушин, г.А. Вавилов
- •Предисловие
- •Введение
- •Глава 1
- •Классификация лекарственных средств
- •Действие лекарственных средств на метаболизм живых организмов
- •1.2. Методы поиска новых препаратов
- •1.2.1. Основные этапы создания лекарственных препаратов, подходы к получению и отбору лекарственных средств
- •1.2.2. Разработка плана синтеза
- •1.3. Сырьевая база химико-фармацевтической промышленности
- •1.3.1. Продукты переработки твердого топлива и коксохимического производства
- •1.3.2. Продукты нефтеоргсинтеза
- •1.3.3. Лесохимическое сырье
- •1.3.4. Некоторые продукты многотоннажных производств
- •1.4. Теоретические аспекты выбора метода синтеза
- •1.4.1. Энергетические факторы
- •1.4.2. Классификация реакций
- •1.4.3. Механизм и кинетика реакций
- •1.4.4. Уравнения Гаммета, Тафта
- •1.4.5. Квантово-химические расчеты
- •1.4.6. Выбор растворителя
- •Характеристики растворителей
- •1.5. Разработка технологической схемы производства
- •1.5.1. Категории и типы технологических схем
- •1.5.2. Правила составления и основные требования к технологическим схемам
- •1.5.3. Оформление чертежей технологических схем
- •1.5.4. Типовое оснащение и привязка химического реактора к конкретному производству
- •Глава 2 методы получения промежуточных продуктов и синтетических лекарственных препаратов
- •2.1. Реакции электрофильного замещения
- •2.1.1. Нитрование
- •2.1.1.1. Реакции нитрования в синтезе некоторых лекарственных препаратов
- •2.1.1.2. Химические особенности реакций нитрования, реагенты, механизм
- •2.1.1.3. Нитрование арил и гетариламинов
- •2.1.1.4. Нитрование азотной кислотой
- •2.1.1.5. Технологические аспекты нитрования
- •2.1.1.6. Использование реакции нитрования для получения полупродуктов и лекарственных средств
- •2.1.1.7. Получение нитроэфиров и n-нитросоединений Так же как и при нитровании ароматических соединений, при получении нитроэфиров используют смесь азотной и серной кислот:
- •2.1.2. Нитрозирование
- •2.1.2.1. Механизм нитрозирования, реагенты
- •2.1.2.2. Особенности проведения реакции
- •2.1.2.3. Особенности структуры и свойств нитрозосоединений
- •2.1.2.4. Практика проведения реакции нитрозирования
- •2.1.2.5. Техника безопасности, экология
- •2.1.3. Сульфирование
- •2.1.3.2. Реагенты, использующиеся при проведении реакции сульфирования, механизм реакции
- •2.1.3.3. Особенности сульфирования, побочные реакции
- •2.1.3.4. Влияние температуры
- •2.1.3.5. Сульфирование бензола и его производных
- •2.1.3.6. Сульфирование анилина и его производных
- •2.1.3.8. Сульфирование хлорсульфоновой кислотой
- •2.1.3.9. Техника безопасности, экология
- •2.1.4. Сульфохлорирование
- •2.1.4.1. Химические особенности реакции
- •2.1.4.2. Технологические аспекты сульфохлорирования
- •2.1.4.3. Синтез сульфаниламидных препаратов
- •2.1.4.4. Техника безопасности, экология
- •2.1.5. Введение углеродных остатков в Ароматическое и гетероциклическое ядро
- •2.1.5.1. Реакции с-алкилирования
- •Реагенты, катализаторы. Как отмечалось, реагентами могут быть алкилгалогениды, олефины и спирты:
- •Механизм реакции. При взаимодействии реагента и катализатора быстро образуется карбокатион, его присутствие зафиксировано с помощью спектроскопии ямр:
- •2.1.5.2. Реакции гидроксиалкилирования
- •2.1.5.3. Реакции хлоралкилирования
- •2.1.5.4. Реакции аминоалкилирования
- •2.1.5.5. Реакции с-ацилирования
- •2.1.5.6. Реакции с-формилирования
- •2.1.5.7. Реакция карбоксилирования
- •2.1.5.8. Карбоксилирование алифатических соединений
- •2.1.5.9. Техника безопасности, экология
- •2.1.6. Галогенирование
- •2.1.6.1. Препараты, содержащие в молекуле атомы галогенов
- •2.1.6.2. Реагенты, механизм реакций галогенирования
- •2.1.6.3. Хлорирование ароматических соединений
- •2.1.6.4. Бромирование, иодирование
- •2.1.6.5. Технологические аспекты галогенирования
- •2.1.6.7. Галогенирование альдегидов, кетонов и кислот
- •2.1.6.8. Свободнорадикальное галогенирование
- •Энергия стадий процесса
- •2.1.6.10. Получение галогенамидов
- •2.1.6.11. Окислительное хлорирование
- •2.1.6.12. Меры предосторожности при проведении реакций галогенирования
- •2.1.6.13. Экология
- •2.2. Реакции нуклеофильного замещения
- •Реакции нуклеофильного замещения у насыщенного атома углерода
- •2.2.1.1. Типы реакций
- •Реагенты для проведения реакций алкилирования
- •Механизмы реакций
- •Алкилирование аминов
- •Селективные методы синтеза первичных аминов
- •Селективные методы синтеза вторичных аминов
- •Алкилирование спиртов и фенолов
- •Алкилирование сн кислот
- •Алкилирование гетероциклических соединений
- •Техника безопасности, экология
- •2.2.2. Реакции нуклеофилов с соединениями,
- •2.2.2.1. Обзор реакций, их кинетика и механизм
- •2.2.2.2. Реакции ацилирования
- •2.2.2.3. Реакции нитрилов с нуклеофилами
- •2.2.2.4. Реакции этерификации, получение амидов и гидразидов кислот
- •2.2.2.5. Получение азометинов и гидразонов
- •2.2.2.6. Методы получения первичных аминов с помощью перегруппировок
- •2.2.2.7. Использование реакций в основном органическом синтезе
- •2.2.2.8. Технология, техника безопасности, экология
- •2.2.3. Нуклеофильное замещение в ряду ароматическИх и гетероциклических оединений
- •2.2.3.1. Нуклеофильное замещение по типу sn1
- •2.2.3.2. Ариновое замещение
- •2.2.3.3. Реакции нуклеофилов с ипсо-замещением нуклеофугных групп
- •Получение полупродуктов и лекарственных препаратов. В отсутствие электроноакцепторных заместителей замещение атома хлора происходит при высокой температуре и в присутствии катализатора:
- •2.2.3.4. Нуклеофильное замещение водорода
- •Еще в начале хх в. Было найдено, что реакция хинолина (изохинолина, фенантридина) с хлорангидридами кислот и цианидом натрия дает устойчивые соединения Райсерта (реакция Райсерта):
- •2.2.3.5. Замещение гидроксигрупп
- •2.2.3.6. Замещение по механизму anrorc
- •2.2.3.7. Технологические аспекты проведения реакций, техника безопасности, экология
2.2.1.1. Типы реакций
Реакции нуклеофильного замещения имеют большое разнообразие и в общем виде они представлены в табл. 2.10.
Таблица 2.10
|
Субстрат (электрофил) |
Нуклеофил |
Продукты реакции |
1. |
(R)3C-OH |
H-Hal (F, Cl, Br, J) |
(R)3C-Hal + H2O |
2. |
(R)3C-Hal |
H2O |
(R)3C-OH + HHal |
3. |
(R)3C-Hal |
R`SO3 - |
(R)3C-O-SO2R` + HCl |
4. |
(R)3C-Hal |
R`-OH |
(R)3C-O-R` + HHal |
5. |
(R)3C-OSO2R`` |
R`OH |
(R)3C-O-R` + R``SO3H |
6. |
(R)3C-Hal |
R`-O- (Na+) |
(R)3C-O-R` + NaHal |
7. |
(R)3C-OSO2R`` |
R`-O- (Na+) |
(R)3C-O-R` + R``SO3Na |
8. |
(R)3C-Hal |
R`COO- |
(R)3C-O-OR` Hal- |
9. |
(R)3C-OSO2R`` |
R`COO- |
(R)3C-O-OR` + R``SO3- |
10. |
(R)3C-Hal |
R-SH |
(R)3C-S-R` + HHal |
11. |
(R)3C-OSO2R`` |
R-SH |
(R)3C-S-R` + R``SO3H |
12. |
(R)3C-Hal |
R-S- (Na+) |
(R)3C-S-R` + Hal- |
13. |
(R)3C-OSO2R`` |
R-S- (Na+) |
(R)3C-S-R` + R``SO3- |
14. |
(R)3C-Hal, (R)3C-OH, (R)3C-OSO2R`` |
NH3, R`NH2, (R`)2NH, (R`)3N |
(R)3C-NH2, (R)3C-NHR`, (R)3C-N(R`)2, (R)3C-N+(R`)3 |
15. |
(R)3C-N+(R`)3 |
ОН- |
(R)3C-ОН + N(R`)3 |
16. |
(R)3C-Hal |
NaCN |
(R)3C-CN + NaHal, [(R)3C-N=C:] |
17. |
(R)3C-Hal |
NaSCN |
(R)3C-SCN + NaHal, [(R)3C-NCS] |
18. |
|
R`OH |
R-CH(OH)-CH2-OR` |
19. |
|
R`NH2 |
R-CH(OH)-CH2-NHR` |
20. |
|
R`SH |
R-CH(OH)-CH2-SR` |
21. |
|
R`OH |
R-CH(OR`)-CH2OH |
22. |
|
R`OH |
(R)3C-O-R` + H2O |
23. |
(R)3C-Cl(Br) |
J- |
(R)3C-J + Cl- (Br-) |
24. |
(R)3C-OSO2R` |
Hal- |
(R)3C-Hal + R`SO3- |
25. |
(R)3C-Hal |
|
(R)3CH-(R`)(R``) |
Из табл. 2.10 видно, что при всем разнообразии реакции можно разделить на следующие группы: синтез галогенопроизводных из спиртов; алкилирование спиртов, фенолов, аминов, цианистого и роданистого калия, меркаптопроизводных и СН-кислот.
При рассмотрении методов получения лекарственных средств следует отметить большое количество препаратов, в синтезе которых используются реакции нуклеофильного замещения. В качестве примеров можно привести ряд из них – димедрол, хлорпромазин (аминазин), анальгин, папаверин, барбитураты, фенилэфрин (мезатон), в синтезе которых особенно наглядно видно применение этих реакций. Пунктирной линией выделены фрагменты молекулы, введенные с помощью реакций нуклеофильного замещения.



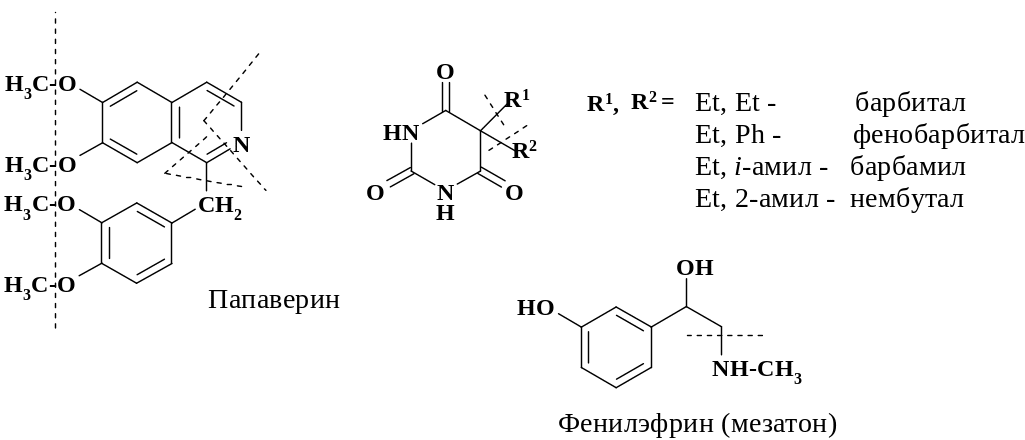
Препарат димедрол (дифенгидрамин), как ранее уже упоминалось, экранирует Н1-гистаминовые рецепторы и устраняет эффекты гистамина, опосредуемые через этот тип рецепторов. Действие на ЦНС обусловлено блокадой Н3-гистаминовых рецепторов. Применяют дифенгидрамин (димедрол) при различных видах аллергии. Он входит в качестве одной из компонент в средство от морской и воздушной болезни – авиоморин. Препарат хлорпромазин (аминазин, действие рассмотрено в разделе 2.1.6). Препарат анальгин (международное название – метамизол натрия) обладает анальгезирующим, жаропонижающим и противовоспалительным действием. Угнетает активность циклооксигеназы, тем самым снижает уровень свободных радикалов в организме, ингибирует перекисное окисление липидов. Препятствует проведению болевых импульсов, повышает порог болевой чувствительности, увеличивает теплоотдачу. Тонкий механизм болеутоляющего действия неизвестен. Применяют для снятия головной и зубной боли, при коликах, хорее, ревматизме и инфарктах легкого и миокарда, травмах, ожогах и т. д. Препарат папаверин (опийный алкалоид) обладает спазмолитическим и гипотензивным эффектом. Ингибирует фосфодиэстеразу, повышает в клетках концентрацию ц-АМФ и понижает уровень кальция. Применяют для снятия спазма сосудов головного мозга, при лечении стенокардии, эндатериита и колик. Является одной из компонент композиций, например папазола. Еще одной группой препаратов, в синтезе которых используются реакции нуклеофильного замещения, являются снотворные средства ряда производных барбитуровой кислоты (фенобарбитал, нембутал и др.). Они взаимодействуют с мембранами клеток, изменяя их физико-химические свойства, снижают возбудимость нейронов и подавляют сенсорные зоны головного мозга. Вызывают сон, отличающийся от физиологического. В качестве одной из компонент фенобарбитал входит в состав корвалола (валокордина). Препарат нембутал (пентотал натрия) совместно с кофеином вызывает состояние, которое называют «сывороткой правды». Применение барбитуратов несовместимо с приемом алкоголя, т. к. вызывает усиление его действия. Действие фенилэфрина описано в разделе 2.1.1. Подробный синтез препаратов приведен далее.
