
- •Механизм:
- •Нитриты
- •Гидразиды
- •3) Из сл.Эфиров
- •Дикарбоновые кислоты
- •Ненасыщенные дикарбоновые кислоты
- •Ароматические дикарбоновые кислоты
- •Сульфоновые кислоты
- •Ароматические (фенолокислоты)
- •Производные солициловой кислоты
- •1) Произ-ые по –cooh:
- •2) Ппроизв-ые по –oh:
- •Оксокислоты
- •Алкилирование
- •Природные α-аминокислоты
- •Специфич.Св-ва аминокислот.
- •Пептиды и белки
- •С троение пептидной группы
- •Химический метод синтеза пептидов(классич)
- •Твердофазный синтез пептидов (тфсп)
- •Важнейшие пентозы:
- •Важнейшие гeксозы:
- •Стереоизомерия
- •Таутомерия
- •Конформации моносахаридов.
- •Конформация галактоперонозы
- •Химические св-ва моносахаридов.
- •Качественные реакции обнаружения гексоз., и пентоз.,
- •Другие представители моносахаридов.
- •Аминосахара
- •Дисахариды
- •Химические св-ва:
- •Полисахариды
- •Крахмал
- •Аминопектин
- •Декстраны
- •Пособы получения:
- •Галогенирование
- •Специфич.Реакции
- •Пятичленные гетероциклы с 2-мя гетероатомами
- •Имидазол. Получение:
- •Важнейшие производные:
- •Производные пиразола.
- •3(5)-Оксипиразол пиразолон-3(5)
- •Синтез антипирина
- •Синтез амидо из антипирина
- •Хинолин
- •Производные хинолина
- •Производные пиримидина
- •Синтез барбитуровой к-ты.
- •Оксазины
- •Тиазины
- •Производные фенотиазина
- •Мочевая к-та.
- •Метилированные ксантины
- •Птеридин
- •Аллоксазин изоаллоксазин.
- •Алкалоиды
- •**Морфин
- •** Кокаин
- •Нуклеиновые ( азотистые основания)
- •Нуклеозиды:
- •Нуклеотиды
- •2 Цепи в этой спирали антипараллельны, т.Е.Их 5’ и 3’-межнуклеотидные фосфодиэфир.Мостики параллельны противоположно.
- •Коферментные нуклеотиды
- •2)Флавиновые ( фмн и фад)
- •Терпены
- •Циклические
- •Производные камфана :
- •Стероидные гормоны (половые г.И г.Коры надпочечников)
- •Желчные кислоты
- •Стерины
- •Омыляемые липиды
- •Простые липиды
- •Обзорная лекция
- •Задачи:
Природные α-аминокислоты
Большое зн.имеет 20 α-аминок-т, входящих в состав пептидов и белков,т.е.
α
H 2N-CH-COOH - общая формула.
R
Стереоизомерия. Все кроме глицина имеют хиральный атом С и сущ-ют в виде пары энантиомеров.
(природные отн-ся к 4-ряду)
 COOH COOH
COOH COOH
H
 NH2
NH2
H
NH2
NH2
H
R R
Д-α-АК 4-α-АК
Изолицин и трионин имеют по 2 хиральных центра из 4-х изомеров, в пр-де встр-ся следующие:
COOH COOH
H

 2N
H H2N
H
2N
H H2N
H
H 3C
H H OH
3C
H H OH
CH2CH3 CH3
4-изолейцин 4-треонин
Классификация: 1. Моноаминомонокарбоновые (1 NH2, 1-COOH, нейтр. )
** H2N-CH2COOH глицин (гли)
* * H2N-CH-COOH аланин (ала)
CH3
* *H2N-CH-COOH валин (вал)
CH-CH3
CH3
* * H2N-CH-COOH лейцин (лей)
CH2
CH-CH3
CH3
* * H2N-CH-COOH изолейцин (илей)
CH-CH3
CH2
CH3
Оксо аминокислот
* * H2N-CH-COOH серин (сер)
CH2OH
* *H2N-CH-COOH треонин (тре)
CHOH
CH3
Серусодержащие аминокислоты
* *H2N-CH-COOH цистеин (цис)
CH2-SH
H2N
* *H2N-CH-COOH
CH-COOH
*H2N-CH-COOH
CH-COOH
CH2SH – SCH2 цистин (цис – S-S-цис)
* * H2N-CH-COOH метионин (мет)
CH2
CH2SCH3
Ароматические
* * H2N-CH-COOH фенилаланин (фен)
CH2


* * H2N-CH-COOH тирозин (тир)
 CH2
CH2


OH
Гетероциклические
*


 *
СH2-CH-COOH
*
СH2-CH-COOH
 NH2
триптофан (три)
NH2
триптофан (три)
N
H
*

 *
N
*
N
- CH2-CH-COOH гистидин (гис)
N NH2
H
2. Моноаминодикарбон-ые к-ты (1-NH2, 2-COOH, кислые)
H 2N-CH-COOH
CH2-COOH аспарагиновая к-та (АСП)
* * H2N-CH-COOH
 O
O
 CH2C
аспарагин (асн)
CH2C
аспарагин (асн)
NH2
* *H2N-CH-COOH глутаминовая к-та (глу)
CH2
CH2COOH
* *H2N-CH-COOH
 CH2
O глутамин
(глн)
CH2
O глутамин
(глн)
 CH2C
CH2C
NH2
3. Диаминомонокарбон. к-ты. (2-NH2, 1-COOH)
* *H2N-CH-COOH
(CH2)3 орнитин ( орн)
NH2
* *
H2N-CH-COOH
*
H2N-CH-COOH
(CH2)4 лизин (лиз)
NH2
* * H2N-CH-COOH
(CH2)3 аргинин (арг)
NH
C=NH
NH2
4.Иминокислота
*
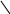
 *
*
COOH пролин (про)
N
H
* * HO

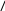
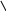 COOH
оксипролин (про-н)
COOH
оксипролин (про-н)

 N
N
H
Незаменимые АМК (не синтезир-ся в орг-ме, должны поступ.в орг)
-вал
-лей
-илей
-тре
-мет
-лиз
-фен
-три
Остальные синтез-ся в орг-ме в процессе след.реак:
1. Трансамнирование (переом-ие)
C
 OOH
COOH
COOH
COOH
OOH
COOH
COOH
COOH
C =O + CH-NH2 F C=O + CH-NH2
R1 кето R2 амино R2 нов.кето R1 нов.амино
2 . COOH COOH
 C=O +NH3,
+H2
CHNH2
C=O +NH3,
+H2
CHNH2
R R
Химические свойства: 1. Получение произ-ых по карбоксильн.группе
-соли (со щелоч)
-амиды (с NH3)
-сл.эфиры (со спиртами)
-ангидриды ( с карб.к-ми)
-хлорангидриды ( с PCl5, PCl3, SOCl2)
-декарбоксилирование


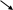 In Vitro
Ba(OH)2 to
In Vitro
Ba(OH)2 to
H
 2N-CH-COOH
- H2N-CH2-R
2N-CH-COOH
- H2N-CH2-R
R in Vivo биогенные амины (коламин, гистамин)

2. Реакции по аминогруппе
-об-ие солей (с мин.к-ми)
-алкилирование (с алкилгалоген.)
O
- ацилир-ие
(с R-C
/ (CH3CO)2O)
ацилир-ие
(с R-C
/ (CH3CO)2O)
Cl
-дезаминирование:
In Vitro;
H
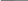 2N-CH-COOH+HONOHO–CH–COOH+N2+H2O
2N-CH-COOH+HONOHO–CH–COOH+N2+H2O
R R
Метод Ван-Слайка (исп-ся для комп.опред.АМК)
In Vivo; окиси-ое:
H

 2N-CH-COOH
HAД+
R-CHCOOHR-C-COOH
2N-CH-COOH
HAД+
R-CHCOOHR-C-COOH
R HAДН NH O
Неокислит:
R -CH-CH-COOH R-CH=CH-COOH
H Nh2 -NH3
3. Реак. с формальдегидом (для опред.колич.АМК)
R
 -CH-COOH
O
-CH-COOH
O
 NH2
+ H-C
R-CH-COOH
NH2
+ H-C
R-CH-COOH
H NHCH2OH
Реак.с фенилизатиоцианатом
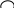
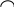
C 6Hб-5N=Cб+
=Sб-+
H2N-CH-COOH
C6H5NH–C–NH–CH–COOH
6Hб-5N=Cб+
=Sб-+
H2N-CH-COOH
C6H5NH–C–NH–CH–COOH
R R
HCl
-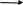 H2O
S
H2O
S
 C
C

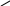 C6H5-NH
NH фенилтиогидантаиновое
произ-ое.
C6H5-NH
NH фенилтиогидантаиновое
произ-ое.
 C-CH-R
C-CH-R
O
