
- •Механизм:
- •Нитриты
- •Гидразиды
- •3) Из сл.Эфиров
- •Дикарбоновые кислоты
- •Ненасыщенные дикарбоновые кислоты
- •Ароматические дикарбоновые кислоты
- •Сульфоновые кислоты
- •Ароматические (фенолокислоты)
- •Производные солициловой кислоты
- •1) Произ-ые по –cooh:
- •2) Ппроизв-ые по –oh:
- •Оксокислоты
- •Алкилирование
- •Природные α-аминокислоты
- •Специфич.Св-ва аминокислот.
- •Пептиды и белки
- •С троение пептидной группы
- •Химический метод синтеза пептидов(классич)
- •Твердофазный синтез пептидов (тфсп)
- •Важнейшие пентозы:
- •Важнейшие гeксозы:
- •Стереоизомерия
- •Таутомерия
- •Конформации моносахаридов.
- •Конформация галактоперонозы
- •Химические св-ва моносахаридов.
- •Качественные реакции обнаружения гексоз., и пентоз.,
- •Другие представители моносахаридов.
- •Аминосахара
- •Дисахариды
- •Химические св-ва:
- •Полисахариды
- •Крахмал
- •Аминопектин
- •Декстраны
- •Пособы получения:
- •Галогенирование
- •Специфич.Реакции
- •Пятичленные гетероциклы с 2-мя гетероатомами
- •Имидазол. Получение:
- •Важнейшие производные:
- •Производные пиразола.
- •3(5)-Оксипиразол пиразолон-3(5)
- •Синтез антипирина
- •Синтез амидо из антипирина
- •Хинолин
- •Производные хинолина
- •Производные пиримидина
- •Синтез барбитуровой к-ты.
- •Оксазины
- •Тиазины
- •Производные фенотиазина
- •Мочевая к-та.
- •Метилированные ксантины
- •Птеридин
- •Аллоксазин изоаллоксазин.
- •Алкалоиды
- •**Морфин
- •** Кокаин
- •Нуклеиновые ( азотистые основания)
- •Нуклеозиды:
- •Нуклеотиды
- •2 Цепи в этой спирали антипараллельны, т.Е.Их 5’ и 3’-межнуклеотидные фосфодиэфир.Мостики параллельны противоположно.
- •Коферментные нуклеотиды
- •2)Флавиновые ( фмн и фад)
- •Терпены
- •Циклические
- •Производные камфана :
- •Стероидные гормоны (половые г.И г.Коры надпочечников)
- •Желчные кислоты
- •Стерины
- •Омыляемые липиды
- •Простые липиды
- •Обзорная лекция
- •Задачи:
Таутомерия
Моносахариды на ряду с открытой могут сущ-ть и в циклич.формах. такой вид таутомерии наз-ся кольчато-цепной (цикло-оксотаутомерия)
O OH
 R-C
+ R’OHб+
FR-C-OR’
R-C
+ R’OHб+
FR-C-OR’
H H полуацеталь
O
 С
С
H
H-C-OH
HO-C-H
H-C-OH
H-C-OH
CH2OH
Молекулы моносахар.в пр-ве имеют клешневидную конформ.в α-oй альдегидная и –OH группа. Особенно у CH, C5 снижены в пр-ве.
Если в реакц.вступает –OH при С5, то обр-ся шестичлен.цикл наз-ый пиранозным, а если –OH при СН, -то пятичн.цикл наз-ый фуранозным.
Вновь образ-ый гидроксил наз-ся полуацетальным, при образ-ии полуацет. возник.еще один хиральный центр
α-ый наз-ся аномерным.
H
 O
H H OH
O
H H OH
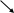
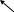



 C*
O
C*
C*
O
C*

 H-C-OH C H-C-OH
H-C-OH C H-C-OH
H O-C-H
O H HO-C-H O
O-C-H
O H HO-C-H O
H-C-OH H-C-OH H-C-OH
C HO-C-H C
CH2OH H-C-OH CH2OH
H-C-OH
CH2OH
β-амомер α-Аномер
β-Д-глюкопираноза α-Д-глюкопираноза
H

 O
H H
OH
O
H H
OH


 C
C
C
C
H-C-OH H-C-OH
H O-C-H O HO-C-H O
H-C H-C
H-C-OH H-C-OH
CH2OH CH2OH
β-Д-глюкофураноза α-Д-глюкофураноза
Автор: Колли-Толлекс
Хеуорс предложил цикл.формы изобразить след.образом.

 O
O
O
O

Пиронозы фуранозы
 СH2OH
CH2OH
СH2OH
CH2OH
H H O H H H O OH

OH OH H OH OH OH H H
H OH H OH
α-Д-глюкопираноза β-Д-глюкопираноза
C H2OH CH2OH
C
 HOH
O OH CHOH O H
HOH
O OH CHOH O H
H H
H OH
OH H OH H
H OH H OH
β-Д-глюкофураноза α-Д-глюкофураноза
В тв.состоянии моносахариды имеют цикл.строение, а в водном р-ре сущ-ют в виде 5-таутомерных форм.(1-ой открытой,2-пиранозных,2-фуранозных)
С явлением этого вида таутомерии связано явление мутаротации- изменение во времени угла вращения плоскости поляризации света р-рами сахаром.
Это объясняется установлением равновесия между таутомерами.
У Д-глюкозы в р-ре преобладает β-пиранозная.
