
- •Механизм:
- •Нитриты
- •Гидразиды
- •3) Из сл.Эфиров
- •Дикарбоновые кислоты
- •Ненасыщенные дикарбоновые кислоты
- •Ароматические дикарбоновые кислоты
- •Сульфоновые кислоты
- •Ароматические (фенолокислоты)
- •Производные солициловой кислоты
- •1) Произ-ые по –cooh:
- •2) Ппроизв-ые по –oh:
- •Оксокислоты
- •Алкилирование
- •Природные α-аминокислоты
- •Специфич.Св-ва аминокислот.
- •Пептиды и белки
- •С троение пептидной группы
- •Химический метод синтеза пептидов(классич)
- •Твердофазный синтез пептидов (тфсп)
- •Важнейшие пентозы:
- •Важнейшие гeксозы:
- •Стереоизомерия
- •Таутомерия
- •Конформации моносахаридов.
- •Конформация галактоперонозы
- •Химические св-ва моносахаридов.
- •Качественные реакции обнаружения гексоз., и пентоз.,
- •Другие представители моносахаридов.
- •Аминосахара
- •Дисахариды
- •Химические св-ва:
- •Полисахариды
- •Крахмал
- •Аминопектин
- •Декстраны
- •Пособы получения:
- •Галогенирование
- •Специфич.Реакции
- •Пятичленные гетероциклы с 2-мя гетероатомами
- •Имидазол. Получение:
- •Важнейшие производные:
- •Производные пиразола.
- •3(5)-Оксипиразол пиразолон-3(5)
- •Синтез антипирина
- •Синтез амидо из антипирина
- •Хинолин
- •Производные хинолина
- •Производные пиримидина
- •Синтез барбитуровой к-ты.
- •Оксазины
- •Тиазины
- •Производные фенотиазина
- •Мочевая к-та.
- •Метилированные ксантины
- •Птеридин
- •Аллоксазин изоаллоксазин.
- •Алкалоиды
- •**Морфин
- •** Кокаин
- •Нуклеиновые ( азотистые основания)
- •Нуклеозиды:
- •Нуклеотиды
- •2 Цепи в этой спирали антипараллельны, т.Е.Их 5’ и 3’-межнуклеотидные фосфодиэфир.Мостики параллельны противоположно.
- •Коферментные нуклеотиды
- •2)Флавиновые ( фмн и фад)
- •Терпены
- •Циклические
- •Производные камфана :
- •Стероидные гормоны (половые г.И г.Коры надпочечников)
- •Желчные кислоты
- •Стерины
- •Омыляемые липиды
- •Простые липиды
- •Обзорная лекция
- •Задачи:
2) Ппроизв-ые по –oh:



 COOH
(CH3CO)2O
COOH
ацетилсалециловая к-та.(аспирин)
COOH
(CH3CO)2O
COOH
ацетилсалециловая к-та.(аспирин)


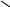
 OH
–CH3COOH
OCOCH3
OH
–CH3COOH
OCOCH3
Это анельгетич., противосп-st? жаропонижающие ср-ва.
Оксокислоты
Альдегидокислоты кетокислоты
O
 O
СН3=С-СООН
O
СН3=С-СООН
 C-C
О
C-C
О
H OH
OH
Глиаксалевая к-та.
(оксо-этановая) пировиноградная к-та. (ПВК)
**СН3-С-СН2-COOH ацетоуксусная (АУК)
O
** O
HOOC-C-CH2-COOH щавелевоуксусная к-та. ЩУК)
** HOOC-C-CH2- CH2-COOH α-кетоглутаровая
O
По взаимному расположению – COOH и –OH различают: α, β, γ.
Способы получения: ** Окисление гидроксикислот.
C H3-C-COOH
[O] CH3-C-COOH
ПВК
H3-C-COOH
[O] CH3-C-COOH
ПВК
 OH
O
OH
O
Молоч.к-та
** Гидролиз геминальных дигалогенопроизводных
С





 H3-C-COOH
3NaOH CH3-C-COONa
CH3-C-COONa
+HCl CH3CCOOH
H3-C-COOH
3NaOH CH3-C-COONa
CH3-C-COONa
+HCl CH3CCOOH
Cl Cl -2NaCl OH HO -H2O O -NaCl O
-2H2O
Химические свойства: *по –COOH
 O
O
 *по –С
*по –С
H
Альдегидок-ты легко окис-ся образуя дикарбоновые к-ты.
α и β оксок-ты сравнительно легко декарбоксилируются.
 O
Но сл.эфиры α/β-оксокислот сравнительно
устойчивы.
O
Но сл.эфиры α/β-оксокислот сравнительно
устойчивы.
С
 H3-C-COOH
H2SO4,
to
CH3-C
H3-C-COOH
H2SO4,
to
CH3-C
 O
-CO2
H
O
-CO2
H
Ацетоуксусный эфир
Это этиловый эфир ацетоуксусной кислоты; получается при сложной эфирной конденсации кляйзена.(см.лекции сл.эф)
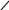
 Н О
Н О
С

 Н3-С
CC
FCH3–C=H–COOC2H5
Н3-С
CC
FCH3–C=H–COOC2H5
О Н ОС2Н5 ОН
СН-кислотный центр
Кето-форма(92%) енольная форма 8%
Сравнительно большое кол-во ен.ф образованием сопряж.сист. и наличие внутримолек. Водород связи.

 СН
СН
Н3С-СН С-ОС2Н5
 О :О
О :О
Н…
**Реакции по кето-форме.
[H]
С

 Н3-С-СН2СООС2Н5
восс-ие CH3CHCH2COOC2H5
Н3-С-СН2СООС2Н5
восс-ие CH3CHCH2COOC2H5
О ОН
СNH CN
 CH3–C–CH2COOC2H5
CH3–C–CH2COOC2H5
OH
SO3Na
NaHSO3 CH3–C–CH2COOC2H5
 OH
OH
** Реакции по енольной форме.
+Br2
C

 H3C=CH–COOC2H5
CH3–C–CH–COOC2H5
H3C=CH–COOC2H5
CH3–C–CH–COOC2H5
OH O Br
Na
 -H2
CH3–C=CHCOOC2H5
-H2
CH3–C=CHCOOC2H5
ONa
+FeCl3 окраш. в фиолет.цвет. продукт реакции.
+CH3COH
-HCl CH3–C=CHCOOC2H5
 Ацил-ие
OCOCH3
Ацил-ие
OCOCH3
