
- •Механизм:
- •Нитриты
- •Гидразиды
- •3) Из сл.Эфиров
- •Дикарбоновые кислоты
- •Ненасыщенные дикарбоновые кислоты
- •Ароматические дикарбоновые кислоты
- •Сульфоновые кислоты
- •Ароматические (фенолокислоты)
- •Производные солициловой кислоты
- •1) Произ-ые по –cooh:
- •2) Ппроизв-ые по –oh:
- •Оксокислоты
- •Алкилирование
- •Природные α-аминокислоты
- •Специфич.Св-ва аминокислот.
- •Пептиды и белки
- •С троение пептидной группы
- •Химический метод синтеза пептидов(классич)
- •Твердофазный синтез пептидов (тфсп)
- •Важнейшие пентозы:
- •Важнейшие гeксозы:
- •Стереоизомерия
- •Таутомерия
- •Конформации моносахаридов.
- •Конформация галактоперонозы
- •Химические св-ва моносахаридов.
- •Качественные реакции обнаружения гексоз., и пентоз.,
- •Другие представители моносахаридов.
- •Аминосахара
- •Дисахариды
- •Химические св-ва:
- •Полисахариды
- •Крахмал
- •Аминопектин
- •Декстраны
- •Пособы получения:
- •Галогенирование
- •Специфич.Реакции
- •Пятичленные гетероциклы с 2-мя гетероатомами
- •Имидазол. Получение:
- •Важнейшие производные:
- •Производные пиразола.
- •3(5)-Оксипиразол пиразолон-3(5)
- •Синтез антипирина
- •Синтез амидо из антипирина
- •Хинолин
- •Производные хинолина
- •Производные пиримидина
- •Синтез барбитуровой к-ты.
- •Оксазины
- •Тиазины
- •Производные фенотиазина
- •Мочевая к-та.
- •Метилированные ксантины
- •Птеридин
- •Аллоксазин изоаллоксазин.
- •Алкалоиды
- •**Морфин
- •** Кокаин
- •Нуклеиновые ( азотистые основания)
- •Нуклеозиды:
- •Нуклеотиды
- •2 Цепи в этой спирали антипараллельны, т.Е.Их 5’ и 3’-межнуклеотидные фосфодиэфир.Мостики параллельны противоположно.
- •Коферментные нуклеотиды
- •2)Флавиновые ( фмн и фад)
- •Терпены
- •Циклические
- •Производные камфана :
- •Стероидные гормоны (половые г.И г.Коры надпочечников)
- •Желчные кислоты
- •Стерины
- •Омыляемые липиды
- •Простые липиды
- •Обзорная лекция
- •Задачи:
Галогенирование
Тиофен можно: Hal – (Cl2 или Br2) на холоде










 Cl
Cl
Cl
Cl
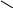
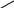
 S + Cl2
S -Cl +Cl2
Cl S - Cl +
2Cl Cl Cl
S + Cl2
S -Cl +Cl2
Cl S - Cl +
2Cl Cl Cl

 -HCl
-HCl
-2HCl S
-HCl
-HCl
-2HCl S
С J2 р-ия идет труднее, в присутств. Hgo.
Пирроз с Hal –реагир.легко с образованием сразу тетрагалогенпиррала.
Для полдг.моно/ди исп-ся сульфохлорид

 Cl
Cl
Cl
Cl









 SO2Cl2
- Cl SOCl2
Cl - Cl SOCl2
Cl- - Cl
SO2Cl2
- Cl SOCl2
Cl - Cl SOCl2
Cl- - Cl
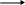
 N N
N
N
N N
N
N
H H H H
Галогенир.фурана происх.сложно, т.к. с замещ.водорода на Hal – идет 2,5 – присоединение



 O +Cl2
Cl - O
-Cl
O +Cl2
Cl - O
-Cl
Нитрование
Учитывая ацедовобность пиррола и фурана для нитр.исп.ацетилнитрат.




 ..
..
 Х + СР3-С=O
X -NO2
+CH3COOH
Х + СР3-С=O
X -NO2
+CH3COOH
ONO2
X=0; NH
Тиофен можно нитрировать азотной к-ой в мягк.усл.
Сульфирование
В виду ацедофобности пиррола и фурана для их сульфирования исп.перидиксульфотриоксид.(Терентьев).



+ - SO3H +

Х N X
SO3H
X=0; NH
Тиофен легко сульфир. H2SO4 (k)
Ацилирование
Используют ангидриды к-т в присутств.к-т Льюиса ( ZnCl2, SnCl4)
+ (Cu3CO)2O SnCl4 -COCH3 + CH3COOH
X S
Тиофен можно ацилир.хлорангидр.в присут. AlCl3
** Восстановление
CH2 CH2
+2H2 to, 140-150 атм. Н2С- CH2
 Кат(М)
Кат(М)
O O тетрагидрофуран
Фуран
H2C CH2
+ 2H2 to, 2-4 атм.Pd H2C CH2

S S тетрагидротиофен
Тиофен
N
H
п ирролин
ирролин
[H] CH2 CH2
 ( Zn+CH3COOH)
+H2,
Pd/Pt H2C
CH2
( Zn+CH3COOH)
+H2,
Pd/Pt H2C
CH2
N N
H H
** Окисление
Пиррол и фуран очень чувств.к действ.окис-ей.
Окисл-ся даже O2 (возд), при этом происходит разрыв кольца.
В присут.катал.об-ся
 + O2
V2O5,
to
O= = O
+ O2
V2O5,
to
O= = O
O O малеиновый ангидрид
+ O2 V2O5 O= = O
O N
H малеинимид
