
- •Механизм:
- •Нитриты
- •Гидразиды
- •3) Из сл.Эфиров
- •Дикарбоновые кислоты
- •Ненасыщенные дикарбоновые кислоты
- •Ароматические дикарбоновые кислоты
- •Сульфоновые кислоты
- •Ароматические (фенолокислоты)
- •Производные солициловой кислоты
- •1) Произ-ые по –cooh:
- •2) Ппроизв-ые по –oh:
- •Оксокислоты
- •Алкилирование
- •Природные α-аминокислоты
- •Специфич.Св-ва аминокислот.
- •Пептиды и белки
- •С троение пептидной группы
- •Химический метод синтеза пептидов(классич)
- •Твердофазный синтез пептидов (тфсп)
- •Важнейшие пентозы:
- •Важнейшие гeксозы:
- •Стереоизомерия
- •Таутомерия
- •Конформации моносахаридов.
- •Конформация галактоперонозы
- •Химические св-ва моносахаридов.
- •Качественные реакции обнаружения гексоз., и пентоз.,
- •Другие представители моносахаридов.
- •Аминосахара
- •Дисахариды
- •Химические св-ва:
- •Полисахариды
- •Крахмал
- •Аминопектин
- •Декстраны
- •Пособы получения:
- •Галогенирование
- •Специфич.Реакции
- •Пятичленные гетероциклы с 2-мя гетероатомами
- •Имидазол. Получение:
- •Важнейшие производные:
- •Производные пиразола.
- •3(5)-Оксипиразол пиразолон-3(5)
- •Синтез антипирина
- •Синтез амидо из антипирина
- •Хинолин
- •Производные хинолина
- •Производные пиримидина
- •Синтез барбитуровой к-ты.
- •Оксазины
- •Тиазины
- •Производные фенотиазина
- •Мочевая к-та.
- •Метилированные ксантины
- •Птеридин
- •Аллоксазин изоаллоксазин.
- •Алкалоиды
- •**Морфин
- •** Кокаин
- •Нуклеиновые ( азотистые основания)
- •Нуклеозиды:
- •Нуклеотиды
- •2 Цепи в этой спирали антипараллельны, т.Е.Их 5’ и 3’-межнуклеотидные фосфодиэфир.Мостики параллельны противоположно.
- •Коферментные нуклеотиды
- •2)Флавиновые ( фмн и фад)
- •Терпены
- •Циклические
- •Производные камфана :
- •Стероидные гормоны (половые г.И г.Коры надпочечников)
- •Желчные кислоты
- •Стерины
- •Омыляемые липиды
- •Простые липиды
- •Обзорная лекция
- •Задачи:
Химический метод синтеза пептидов(классич)
При обычном смещении 2-х АМК возможны след.затруднения:
1. Из-за диполярной структуры проведение реак.требует высоких температур, что приводит к побочным продуктам(дикетопиперацин)
2. АМК необходимо соед-ть в строгой опред-ой последовательности
 Классич.метод всключает несколько
стадий:
Классич.метод всключает несколько
стадий:
1. Защита аминогруппы N-канцевой АМК чаще используют реак.ацилирования след.реагентами:
O O
С6H5CH2O-C бензоксикарбонихлорид;(CH3)3COC
Cl N3
Т ретбутоксикарбоксазид
O
O
ретбутоксикарбоксазид
O
O
H
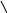
 2N-CH-COOH+C6H5CH2O-C
C6H5CH2OC-NH-CH-COOH
2N-CH-COOH+C6H5CH2O-C
C6H5CH2OC-NH-CH-COOH
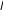 CH3
Cl -HCl
CH3
O
CH3
Cl -HCl
CH3
O
2 .
Активация карбоксильной группы,
N-защищенной АМК. Для
актив.исп-ют либо PCl5,
либо SOCl2, C2H5O-C
.
Активация карбоксильной группы,
N-защищенной АМК. Для
актив.исп-ют либо PCl5,
либо SOCl2, C2H5O-C
Этилхлорформиат Cl
 O
O
O
O
O
O
C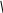
 6H5CH2OC–NH–CH–COOH+SOCl2C6H5CH2OC–NH–CH–C
+ SO2
+HCl
6H5CH2OC–NH–CH–COOH+SOCl2C6H5CH2OC–NH–CH–C
+ SO2
+HCl
CH3 CH3
3. Защита карб-ой гр, С-канцевой АМК.
H
 2N-CH-COOH
+ C2H5OH
F
H2N-CH-COOC2H5+H2O
2N-CH-COOH
+ C2H5OH
F
H2N-CH-COOC2H5+H2O
CH2OH CH2OH
4
 .Синтез
.Синтез

 O O
O CH3
O H
O O
O CH3
O H
C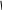




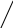 6H5CH2OC–NH–CH–C
+ HNH–CH–COOC2H5C6H5CH2OC–NH–CH–C–N–CH–COOC2H5
6H5CH2OC–NH–CH–C
+ HNH–CH–COOC2H5C6H5CH2OC–NH–CH–C–N–CH–COOC2H5
 CH3
Cl CH2OH
CH3
Cl CH2OH
5-6. Снятие защиты с N и С концов.
 O O
O
O O
O
С
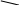 6H5-CH2O-C-NH-CH-C-N-CH-C
6H5-CH2O-C-NH-CH-C-N-CH-C
CH3 CH2OH OC2H5
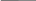
 H2
P H2O,OH-
H2
P H2O,OH-
C6H5CH3 -C2H5OH
 O H
O H
 H2N-CH-C-N-CH-COOH
H2N-CH-C-N-CH-COOH
CH3 CH2OH
Твердофазный синтез пептидов (тфсп)
Полипептидная цепь наращивается на тв.основе без выделения промеж.продуктов.
O
с

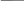
 мола
–СH2Cl
+ HOOCCH-NH2
смола CH2OC-CH-NH2
мола
–СH2Cl
+ HOOCCH-NH2
смола CH2OC-CH-NH2
R -HCl R
На конце свободная аминогруппа ацилир-ся след.АМК, у α-ой защищена аминогр.(бок-группы) в присутствии активатора карбоксильной группы N-N’, где карбоксил N-N- дициклогексилкарбодисемид.
O
 -СH2OCCH-NH2+HOOC-CH-NHБОК
+ C6H5N=C=N-C6H11
-СH2OCCH-NH2+HOOC-CH-NHБОК
+ C6H5N=C=N-C6H11
R R (ДЦГК)
O O

CH2OCCH-NH-C-CHNHБОК+C6H11NH—C-NHC6H11
CH2OCCH-NH-C-CHNHБОК+C6H11NH—C-NHC6H11
R R’ O дициклогексилмочевина
Далее удаляют защиту действ.3-фторуксус.к-ты, пролив-ют от избыт.реагентов и побочных продуктов. Таким образом конденсируются и след.АМК.
После присоед. послед. Кисл. остатка и снятия защиты обрабатывают бромоводор.к-ой в р-те полипептид отдел. От полимера.
Все стадии автоматизированы.
Белки
** Первичная структура белка-это послед.распол.аминокислотных остатков полипептидной цепи.
АМК строго соед.в послед.с кодом белкового синтеза.
Для опред.первич.структуры сначала опред.аминокислотный состав, проведя гидролиз и проведя хроматографич.способ анализа.
Затем опред.N-C-концевые кислоты.
Природа N-конц.АМК опр-ся чаще финилтиогедантоиновым методом эдмона(деградация по эдману)
C

 6H5N=C=S+H2N–CH–C–NH–CH–CO–OH
6H5N=C=S+H2N–CH–C–NH–CH–CO–OH
R1 O Rx n
S O
C

 6H5NH–C–NH–CH–C–NH–CH–CO–OH
–HCl
ФРГ произв.N-конц.
6H5NH–C–NH–CH–C–NH–CH–CO–OH
–HCl
ФРГ произв.N-конц.
R1 Rx n
S



 C O
C O

С6H5-N
NH+H2N-CH-C-NH-CH-CO—OH
С6H5-N
NH+H2N-CH-C-NH-CH-CO—OH
 C-CH-R1
R2 Rx-1
n
C-CH-R1
R2 Rx-1
n
O
Полипептид укороченный на 1 АМК
Таким способом опиц.остаток за отстатком и опред.всю послед.
С N-конца можно опред.послед.с помощью 1-фтор-2,4-динитробензола.
Для опред.С-конца исп.ферментативный путь: фермет карбоксипептидаза отщепляет цепь с С-конца и природа устанавл.хромотографически.
** Вторичная структура-конфигурация полипептидной цепи.
Наиболее изучены α-спираль и β-структура.
α-спираль –характерна для глобулярных белков закручивания по часовой стрелке, что связано с 4-аминокислотным сост.
На кажд.витог(шаг) приход.3,6 АМК остатка.
Li подъема ≈26о
Через кажд.5 витков (18 АМК остатка) структ.конфиг.повторяется.
Причиной возникновения стабильной вторичной структуры является способность обр-ть в связи между отд.участками белка.
β-структура-фибрилярные белки остов перпендикулярной цепи имеет зигзагообраз.кофм. эти зигзагообразные полипептидные цепи уложены II друг другу в виде складок, в них об-ся межцепочечные в св. вместо внутрицепочечных.
**Третичная структура –способ укладки полипептид.цепи в опред.v
В стабилизации третич.стр осн.роль играют вод.связи; электростатич.взаим., гдрофобные взаим., дисульфидное взаим.
** Четвертичная структура-способ укладки в пространстве единого в структурном и функц-ом отнош.макромолек.обр-ия, сст.из неск.поппептидных цепей.
Углеводы
Это соед. состава Сх(Н2О)у
Они образ-ся в процессе фотосинтеза
хCO2+yH2O+солн.энергия Сх(Н2О)у+хО2


 Углеводы
Углеводы
Моносахариды Олигосахариды Полисахариды
(однокомп., (от 2х до 10 (более 10 моносахар.звеньев)
не гидролизуются) моносахар.звеньев)
Моносахариды (простые сахара)
1.молекула моносахар.содержит в своем составе несколько –OH групп и одну –COH., в зависимости от налич.альд.или кетонной группы их делят на альдозы и кетозы.
К лассификация:
O
CH2OH
лассификация:
O
CH2OH
 C
C=O
C
C=O
 H
(CHOH)n
H
(CHOH)n
(CHOH)n CH2OH
CH2OH
Альдозы кетозы
2. По числу углер.атомов:
-триозы
-тетрозы
-пентозы
-гексозы и др.
3. В зависимости от строения у послед.ассим.атома С делят на Д и Li-ряды.
