
- •Механизм:
- •Нитриты
- •Гидразиды
- •3) Из сл.Эфиров
- •Дикарбоновые кислоты
- •Ненасыщенные дикарбоновые кислоты
- •Ароматические дикарбоновые кислоты
- •Сульфоновые кислоты
- •Ароматические (фенолокислоты)
- •Производные солициловой кислоты
- •1) Произ-ые по –cooh:
- •2) Ппроизв-ые по –oh:
- •Оксокислоты
- •Алкилирование
- •Природные α-аминокислоты
- •Специфич.Св-ва аминокислот.
- •Пептиды и белки
- •С троение пептидной группы
- •Химический метод синтеза пептидов(классич)
- •Твердофазный синтез пептидов (тфсп)
- •Важнейшие пентозы:
- •Важнейшие гeксозы:
- •Стереоизомерия
- •Таутомерия
- •Конформации моносахаридов.
- •Конформация галактоперонозы
- •Химические св-ва моносахаридов.
- •Качественные реакции обнаружения гексоз., и пентоз.,
- •Другие представители моносахаридов.
- •Аминосахара
- •Дисахариды
- •Химические св-ва:
- •Полисахариды
- •Крахмал
- •Аминопектин
- •Декстраны
- •Пособы получения:
- •Галогенирование
- •Специфич.Реакции
- •Пятичленные гетероциклы с 2-мя гетероатомами
- •Имидазол. Получение:
- •Важнейшие производные:
- •Производные пиразола.
- •3(5)-Оксипиразол пиразолон-3(5)
- •Синтез антипирина
- •Синтез амидо из антипирина
- •Хинолин
- •Производные хинолина
- •Производные пиримидина
- •Синтез барбитуровой к-ты.
- •Оксазины
- •Тиазины
- •Производные фенотиазина
- •Мочевая к-та.
- •Метилированные ксантины
- •Птеридин
- •Аллоксазин изоаллоксазин.
- •Алкалоиды
- •**Морфин
- •** Кокаин
- •Нуклеиновые ( азотистые основания)
- •Нуклеозиды:
- •Нуклеотиды
- •2 Цепи в этой спирали антипараллельны, т.Е.Их 5’ и 3’-межнуклеотидные фосфодиэфир.Мостики параллельны противоположно.
- •Коферментные нуклеотиды
- •2)Флавиновые ( фмн и фад)
- •Терпены
- •Циклические
- •Производные камфана :
- •Стероидные гормоны (половые г.И г.Коры надпочечников)
- •Желчные кислоты
- •Стерины
- •Омыляемые липиды
- •Простые липиды
- •Обзорная лекция
- •Задачи:
Производные камфана :
Эти спирты могут превращ.взаимно друг с друглм при кипяч.с Na мет.
Спирты
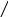
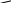

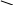 OH
- борнеол
OH
- борнеол
 H
H
Терпингидрат
H - изоборнеол
OH
Диантиомеры и рацематы содерж.в раст.в свободном виде, так и в виде
(-)левовращ.-в эфиро-пихтовых маслах.
(+)правовращ.
Борнеолы проявл.св-ва втор.спиртов при их окисл.обр-ся камфора.
 *
*
=O

Комфора содерж.в эфир.маслах камфорного дерева, с др.вр.исп-ся для стимуляции сердеч.деятельности.
2 хир.центра, 2 энантиомера:

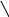 =O O=
=O O=


Особенности:
1) в молек.2 ассиметр.атома С, но вместо 4-х изомеров известно 2, что связано с жестк.системы, конфигурации обеих хир.центров изменяется одновременно.
2)шестичн.кольцо в пр-ве занимает комформ-ванну синтез комфоры из α-пирена по Тищенко:




 TiO2*H2O
CH3COOH
OCOCH3
TiO2*H2O
CH3COOH
OCOCH3


 180
180
Камф-ен (очень бормилацитал
реакц.спосб)

H
 2O
OH [O]
=O
2O
OH [O]
=O
- CH3COOH
CH3COOH
Бормеол
Хим.реакц.многих терпенов сложны и часто сопровожд.перегруппир.скелета.
Гидрохлорирование пинена приводит к борнилхлориду.
+


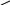 +H+
перегруп-ка
+ +Сl-
Cl
+H+
перегруп-ка
+ +Сl-
Cl



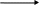

Третичный катион II борнилхлорид
Карбокатион I более устойчив
Чем карбокатион I
По хим.св-ам типичный кетон ( все реак.AN, присоед.-отщеп.аксимы, гидразоны, фенилгидразон), кроме того метиленовая гр.в α-полож.проявл. CH-кисл.св-ва.
=O +Br2 =O + HBr
 C-H
Br
C-H
Br
H бромкасфона
Улучш.серд.деятельность.
Секстерпены
Сантонин
O =O
O CH3
CH3
CH3
CH3
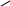


Содерж.в раст.рода Artemisia, яв-ся сост.частью лекарств.средств.
В настоящее время исп-ся как антигельм.ср-во.
Дитерпены
Ретинол (витамин А)


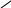








 CH2OH
CH2OH
Участв.в кисл.в орг-ме в ретиналь, участв.в пр-се световосприятия.
К

 онифоль
онифоль


H3C COOH
Содержит абиетиновую к-ту, относ-ся в дитерпенам.
Исп-ся в пр-ве лаков, хоз.мыла и т.д.
Тритерпены(ациклические)
Сквален























 23 (C30H50)
23 (C30H50)
Содежр.в дрожжах, пшенич.зарод.оливк.масле. яв-ся биолог.предшествстероидов.
Тетратерпены
Каротиноиды
 Β-каротин(предшественник
витамина А)
Β-каротин(предшественник
витамина А)






















 19
19
При окисл.обр-ся β-ианон.


CH=CH-C-CH3
 O
O
Запах фиалок.
Стероиды
К ним относят в-ва живот.и раст.происхожд.в основе α-ых нах-ся система циклопентанопергидридофенантрена(стренана)
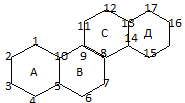
Общая формула стероидов.
CH3 R
CH3
X-либо –OH, OR, C3=C
У 13,10-CH3; 17-R

X
Стереохимия
Стиран имеет 6-ассим.атомов углерода(№5,8,9,10,13,14) к теоретич.он может сущ-ть в виде 64 стереоизомеров, но в живой природе.встр.лишь некотр.из стереоизомер.форм.
Кольца А и В могут сочленятся таким образом:
1) в обр-ии конденс.сист.участ.2 эквитер.связи цикла А при этом от.Н у С5 и С10 нах-ся в транс.-полож.относ.друг др.
10



 А В
А В

 Транс-сочитание
Транс-сочитание
5
2) в связыв.двух циклов участв.1 аксиальная и 1 эквост.связь кольца А, водород.связи у С5 и С10 расп-ся по одну сторону колец.

 H
H
 В
В
 А
А
 Цис-сочитание
Цис-сочитание
Теорет.возможно 8 комбинаций цис, транс-сочленении 3-х пар колец.
В природе:
1) А/В, В/С, С/Д –транс сочлен.
H
 H
H
H C Д



 А В H
5-α-стеран
А В H
5-α-стеран

 H
H
H
2) А-В-цис; В/С, С/Д. – транс.сочлен.
H
H
H C Д
 В H H
В H H
H
 А
А
По типу сочлен.А и В стероиды делятся:
- 5 - α- стероиды ( А/В- транс)
- 5 – β- стероиды (А/В цис)
На плоскости
R
 CH3
CH3

 H3C
H 5-α-стероид
H3C
H 5-α-стероид
H H

 Х
Х
R
CH3
СН3 H 5-β-стероид
H H
Х
H

X (e) A

 3
3
3(β) –заместит.занимает экватр.полож.
3 A
α
X 3α-замест.заним.аксиальн.полож.
