
- •Механизм:
- •Нитриты
- •Гидразиды
- •3) Из сл.Эфиров
- •Дикарбоновые кислоты
- •Ненасыщенные дикарбоновые кислоты
- •Ароматические дикарбоновые кислоты
- •Сульфоновые кислоты
- •Ароматические (фенолокислоты)
- •Производные солициловой кислоты
- •1) Произ-ые по –cooh:
- •2) Ппроизв-ые по –oh:
- •Оксокислоты
- •Алкилирование
- •Природные α-аминокислоты
- •Специфич.Св-ва аминокислот.
- •Пептиды и белки
- •С троение пептидной группы
- •Химический метод синтеза пептидов(классич)
- •Твердофазный синтез пептидов (тфсп)
- •Важнейшие пентозы:
- •Важнейшие гeксозы:
- •Стереоизомерия
- •Таутомерия
- •Конформации моносахаридов.
- •Конформация галактоперонозы
- •Химические св-ва моносахаридов.
- •Качественные реакции обнаружения гексоз., и пентоз.,
- •Другие представители моносахаридов.
- •Аминосахара
- •Дисахариды
- •Химические св-ва:
- •Полисахариды
- •Крахмал
- •Аминопектин
- •Декстраны
- •Пособы получения:
- •Галогенирование
- •Специфич.Реакции
- •Пятичленные гетероциклы с 2-мя гетероатомами
- •Имидазол. Получение:
- •Важнейшие производные:
- •Производные пиразола.
- •3(5)-Оксипиразол пиразолон-3(5)
- •Синтез антипирина
- •Синтез амидо из антипирина
- •Хинолин
- •Производные хинолина
- •Производные пиримидина
- •Синтез барбитуровой к-ты.
- •Оксазины
- •Тиазины
- •Производные фенотиазина
- •Мочевая к-та.
- •Метилированные ксантины
- •Птеридин
- •Аллоксазин изоаллоксазин.
- •Алкалоиды
- •**Морфин
- •** Кокаин
- •Нуклеиновые ( азотистые основания)
- •Нуклеозиды:
- •Нуклеотиды
- •2 Цепи в этой спирали антипараллельны, т.Е.Их 5’ и 3’-межнуклеотидные фосфодиэфир.Мостики параллельны противоположно.
- •Коферментные нуклеотиды
- •2)Флавиновые ( фмн и фад)
- •Терпены
- •Циклические
- •Производные камфана :
- •Стероидные гормоны (половые г.И г.Коры надпочечников)
- •Желчные кислоты
- •Стерины
- •Омыляемые липиды
- •Простые липиды
- •Обзорная лекция
- •Задачи:
Птеридин
5
N 4

 6 N 3
6 N 3
 7 2
7 2

 N 8 N
1
N 8 N
1
Ядро ядро
пирозина пиримидина
Входит в состав фолиевой к-ты. В большом кол-ве содержится в листьях шпината, моркови. Биол.связана 5,6,7,8-тетрагидрофоливой к-ой.
-стимулир.кроветворение
-участ.в биосинт.к-те.
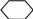


 OH N
O
OH N
O

 N CH2-NH-
- C-NH-CH-CH2CH2COOH
N CH2-NH-
- C-NH-CH-CH2CH2COOH
H2N COOH
N N
Ядро птеридина параамино- остаток 4-глутам.к-ты.
Бензон.к-та.
ПАВК
Аллоксазин изоаллоксазин.
Легко вступает в ОВР.входит в состав вит.В2(рибофлавина),содерж.в мясе,бобах,дрожжах,яич.желтке.
 N O
N
O
N O
N
O


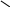
N-H азольная N-H флавин (желт.цвета)
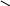
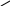
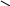
 =O
таутом.
=O
=O
таутом.
=O

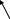 N N
N
N
N N
N
N
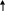 H
H
H
H
Бензольное ядро гидрированый
Кольцо пирозина пиримидин Легко вступает в ОВР.входит в состав
вит.В2(рибофлавина),содерж.в
мясе,бобах,дрожжах,яич.желтке.
N =O

 H3C
N-H
H3C
N-H

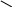 H3C
=O
H3C
=O
N N
 CH2CHCHCHCH2OH
CH2CHCHCHCH2OH
OHOHOH спирт рибитол
Алкалоиды
Наз-ся азотсодерж.орган.соед,преимущ.растит.происхожд.проявл.основные св-ва и высокою биологич.активногсть. по хим.строению большинство относит.к гетероцикл.соед. алкалоидами богаты растении: 1) маковые; 2) лютиковые; 3)бобовые; и др.,
Большие дозы часто яв-ся ядами, но в малых дозах часто исп-ся как ценные лекарств.в-ва.
В раст.содержатся в виде солей орган.к-т-щавел, лимон,яблоч.,винной.
По физическим св-ам это бесцветные крист.в-ва горького вкуса, практичлекартсв.в H2O, но хорошо раств-ся в орган.р-лях: хлороформ, бензол, диэтиловый эфир.
Соли р-ся в H2O, но не яв-ся в орган.р-лях.
Методы обнаружения.
Для обнаруж.алкал.исп-ся общие групповые реакции присущие группе алкалоидов и специфич.реак, хар-ые для индивид.алкалоидов.
** наиболее часто, для осаж-ия применяют:
Р-ры J2-в KJ ( реактив)
Р-ры PbJ2 в KJ ( реактив Маера)
Р-ры BiJ3 в KJ ( реактив Драгендорфа)
Р-р пикриновой к-ы.
Р-р Тонина.
**реакции окрашевания
Р -в
Марке ( смесь H2SO4+H-C=O)
-в
Марке ( смесь H2SO4+H-C=O)
H
Р-в Эртермана ( смесь HNO3(k) + H2SO4(k))
Классифик.
1. по ботанич.признаку
2. химическая – по природе гетероцикла.
Алкалоиды гр.пиридина, пипиридина.
Никотин-содер-ся в листьях табака, в виде солей яблоч.и лимонной к-ты.
Никотин.
Его молек.состоит из пиридинового и N-метилпирролидиного цикла, связан.простой связью.

 Легко окисл-ся.
Легко окисл-ся.


 N
[O]
N
[O]
 CH3
CH3
N

 COOH
COOH
 Никотиновая кислота
Никотиновая кислота
N
Никотин очень токсичен!
Смерт.доза=40мг.
Никотин исп-ся в качестве иксиктицида для борьбы с вред.в с/х.
Анабазин
Сод-ся в ежовнике безлистом, произрост.в Ср.Азии. молек.состоит из пиридинового и пипирид.цикла, связанного простой связью.

N
N H
Так же очень ядовит. Обладает высоким инсиктицидным св-ом в виде HCl соли прим.в медицине, в качест.ср-ва против курения.
Предполагается, что эффект основан на конкур.воздейств.с никот.на нерв.рецепторах.
Алкалоиды. Группы хинолина
Впервые был выделен в 1820г.с коры хинного дерева.(малярия).
Хинин
+Na
+окисл.
+
 обр.пр.эф.
–CH=CH2
непредельный виниловый фрагмент
обр.пр.эф.
–CH=CH2
непредельный виниловый фрагмент
+ обр.сл.эф. вторич. CH2 +Br2
Спирт.гидроксил CH2 +KMnO4

 HO-CH -
+H2O
HO-CH -
+H2O

 CH3O
..N
CH3O
..N
Простая ядро хинукледина
эфир.связь
 (+HJ) ..N
(+HJ) ..N
Ядро хинолина
Алкалоиды. Гр.изохинолина и фенонтрена.
Высуш.млечн.сок опинного мака содерж.2гр.алкалоидов; к 1гр.-бензилизохинолин.алкалоидов относ-я пдповерин и наркотин.
2гр.с фенантреновой структ.:
-кодеин.
-морфин.
** пуповерин
CH3



 CH3O
CH3O
+
CH3O
CH3O
+
 CH3O
N CH3O
N OCH3
CH3O
N CH3O
N OCH3
CH2 OCH3

 6.7-диметокси-изо-хинолин
6.7-диметокси-изо-хинолин
 OCH3
OCH3
OCH3
В виде хлороводор.соли примен.в медицине в качестве смазмалит.и сосудорасш.ср-ва.
