
- •Механизм:
- •Нитриты
- •Гидразиды
- •3) Из сл.Эфиров
- •Дикарбоновые кислоты
- •Ненасыщенные дикарбоновые кислоты
- •Ароматические дикарбоновые кислоты
- •Сульфоновые кислоты
- •Ароматические (фенолокислоты)
- •Производные солициловой кислоты
- •1) Произ-ые по –cooh:
- •2) Ппроизв-ые по –oh:
- •Оксокислоты
- •Алкилирование
- •Природные α-аминокислоты
- •Специфич.Св-ва аминокислот.
- •Пептиды и белки
- •С троение пептидной группы
- •Химический метод синтеза пептидов(классич)
- •Твердофазный синтез пептидов (тфсп)
- •Важнейшие пентозы:
- •Важнейшие гeксозы:
- •Стереоизомерия
- •Таутомерия
- •Конформации моносахаридов.
- •Конформация галактоперонозы
- •Химические св-ва моносахаридов.
- •Качественные реакции обнаружения гексоз., и пентоз.,
- •Другие представители моносахаридов.
- •Аминосахара
- •Дисахариды
- •Химические св-ва:
- •Полисахариды
- •Крахмал
- •Аминопектин
- •Декстраны
- •Пособы получения:
- •Галогенирование
- •Специфич.Реакции
- •Пятичленные гетероциклы с 2-мя гетероатомами
- •Имидазол. Получение:
- •Важнейшие производные:
- •Производные пиразола.
- •3(5)-Оксипиразол пиразолон-3(5)
- •Синтез антипирина
- •Синтез амидо из антипирина
- •Хинолин
- •Производные хинолина
- •Производные пиримидина
- •Синтез барбитуровой к-ты.
- •Оксазины
- •Тиазины
- •Производные фенотиазина
- •Мочевая к-та.
- •Метилированные ксантины
- •Птеридин
- •Аллоксазин изоаллоксазин.
- •Алкалоиды
- •**Морфин
- •** Кокаин
- •Нуклеиновые ( азотистые основания)
- •Нуклеозиды:
- •Нуклеотиды
- •2 Цепи в этой спирали антипараллельны, т.Е.Их 5’ и 3’-межнуклеотидные фосфодиэфир.Мостики параллельны противоположно.
- •Коферментные нуклеотиды
- •2)Флавиновые ( фмн и фад)
- •Терпены
- •Циклические
- •Производные камфана :
- •Стероидные гормоны (половые г.И г.Коры надпочечников)
- •Желчные кислоты
- •Стерины
- •Омыляемые липиды
- •Простые липиды
- •Обзорная лекция
- •Задачи:
Ненасыщенные дикарбоновые кислоты
Н
 ООС-СН=СН-СООН
бутендиовая кислота
ООС-СН=СН-СООН
бутендиовая кислота
цис транс


 Н Н НООС H
Н Н НООС H


 С=С C=C
С=С C=C
НООС СООН H COOH
Малейновая к-та Фумаровая кислота
Получение: 1) Малеиновая к-та:
1. Дегидратация яблочной к-ты(в лаборат.)
О
Н О-СН-СООН to СН-С НОН СН-СООН
О
Н-С-СООН -2Н2О СН-С СН-СООН
О
Маллеин.ангидрид
2. В промышленности
 О2V2O5
to
О2V2O5
to
3. Из бутена -2
C H3–CH=CH–CNH3
+О.2,
V2O5,
to
H3–CH=CH–CNH3
+О.2,
V2O5,
to
2) Фумаровая кислота
1. Встречается во многих растениях
2. Синтетически, по клюве-нагелю.
 О Н СООН
to
СООН to
Н СООН
О Н СООН
to
СООН to
Н СООН
Н ООС-С + С -Н2О НООС-СН=С -СО2 С=С
Н Н СООН СООН НООС Н
3. Изомеризация малеиновой кислоты (to=150о С)
Химические свойства: 1) по – СООН
- кислые и средние соли
- полные и неполные: галогенангидриды, амиды, сл.эфиры.
2) по двойной связи (+H2, +HAl2, +HAl, +HOH, +KMnO4(H2O))
3) Особенности: проявляют более кислотные свойства, чем соотв.насыщ.к-ты,т.к. взаимное сливание передается по сопряженной системе=св
О О

 С-СН=СН-С
С-СН=СН-С
НО О-
Малеиновая кислота сильнее фумаровой и кислотность . Особенно по первой ступени, что обусловлено стабилизацией за счет внутримолек.взаим. ионизированной и неионизированной карбоксильными группами, через водородную связь.
О
С Н-С
Н-С
О-
СН
![]()

 С-О-Н
С-О-Н
О Малеиновая к-та в отличии от фумаровой при нагревании обесцвечивает циклический ангидрид.
 О
О

 СН-С O
СН-С O
ОН to CH-C
ОН -Н2О O
СН-С CH-C
О O
Ароматические дикарбоновые кислоты
COOH COOH COOH

 COOH
COOH
COOH
COOH
Фталевая изофталевая терефталевая
(фто) (мета) (пара)
Получение: ** Каталитическое окисление ксилолов кислородом воздуха
** Окисление нафталина О2, V2O5
Химические свойства: Образуют ряда производных по 2-м - COOH
(у фталевой кислоты полный дихлорангидрид не получ. из-за внутримолекулярного взаимодействия)
О O




 С Сl to C
С Сl to C
OH -HCl O фталевый ангидрид


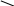
 C
C
C
C
O O
Фталевая кислота в отличие от других при to образует фталевый ангидрид.
Фталевый ангидрид используют для получения фенолфталеина.







Н

 О
Н Н
О
Н Н





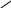 О
О





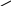

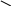 С
С




 О С
О С



 -Н2О
О
-Н2О
О


 С
бесцветный
С
бесцветный
С
 О
О
О
О
ОН-
Н+

О= - С - - О-



 СОО-
СОО-
Угольная кислота и ее функц.производные
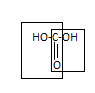 Ведет себя как дикарбоновая кислота.
Образует 2 ряда производных.
Ведет себя как дикарбоновая кислота.
Образует 2 ряда производных.
Хлорангидриды: а) монохлорангдрид
О
НО-С-Сl хлоругольная кислота- в свободном виде не существует, к-та в момент образования сразу распадается на : HCl и CO2, но ее эфиры существуют и устойчивы.
 О
О
R-C-Cl
б) дихлорангидрид
Cl-C-Cl фосген
О
СО2+Сl –h СОСl2 проявляется св-ва как у галогенангидрид. карбоновых кислот.
 +НОН
СО2+НCl
+НОН
СО2+НCl
O проявляет св-ва как сл.эфиры, так и ангидр.
O +ROH (1 моль) Cl-C-OR
O
Cl-C-Cl +ROH (2 моль) R-C-OR
O
+2NH3 NH2-C-NH2
+2НCl
Амиды
а) неполный
H O-C-NH2 карбаминовая к-та- в свободном виде неизвестна, но ее соли и эфиры сущ-ют.
O Устойчив.эфиры- уретаны.
O CH3 O мепротан(мепробамат)
С -О-СН2-С-СН2-О-С-NH2 дикарбомат – 2 – метил-2-пропилпропандиола-1,3
NH2 CH2CH2CH3
б) полный
H N2-C-NH2 мочевина
O
Получение:CO2+2NH3 –t,PCO(NH2)2+H2O
Химические свойства: ** Основные свойства:


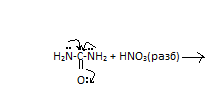
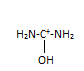 NO3
NO3
** Гидролиз мочевины
CO(NH2)2+HOHCO2+NH2
** Реак. связанные с нуклеиновыми св-ми:
1. Алкилирование O
H 2N-C-NH2+RCl
NH2-C-NH-R
2N-C-NH2+RCl
NH2-C-NH-R
-HCl
O
2. Ацилирование
 O O
O O
O O
O O
 R-C
+ H2N-C-NH2
R-C-NH-C-NH2
R-C
+ H2N-C-NH2
R-C-NH-C-NH2
Cl -HCl
N- ацильные производные-уреиды.
Брамизовал (уреид-α-бромизовалерианой к-ты)
 CH3
O
CH3
O
H 3C-CH-CH-C
3C-CH-CH-C
Br NH-C-NH2
O
** Действие азотистой кислоты
H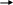
 2N-C-NH2+HNO2
CO2+N2+H2O
2N-C-NH2+HNO2
CO2+N2+H2O
O использ.в количеств.анализе.
** Разложение гипобромида
H 2N-C–NH2+NaOBrCO2+N2+H2O+NaBr
O
** Образование биурета
H 2N–C–NH2+H–N–C–NH2 –toH2N–C–NH–C–NH2
O H O O O
Биурет в щелочной среде вместе с Cu+2 образует комплекс красно-фиолетового цвета(биуретовая реакция; для обнаружения мочевины и белков)
H

 2N
H2N
NH2
2N
H2N
NH2




 C=O
C-O O=C
C=O
C-O O=C
2

 NH + Cu(OH)2
N Cu N
NH + Cu(OH)2
N Cu N





 C=O
C=O O-C
C=O
C=O O-C
H2N H2N N2H
** Образование урендокислот
O O
H

 2N-C-NH2+Cl-CH2-C
H2N-C-NH-CH2-C
+ HCl
2N-C-NH2+Cl-CH2-C
H2N-C-NH-CH2-C
+ HCl
O OH O OH
Урендоугольная к-та
Важным производным мочевины яв-ся иминамочевина(гуанидин)-это сильные однокислотные основания.


H
 2N-C-NH2+HCl
H2N-C+-NH2
Cl-‑
2N-C-NH2+HCl
H2N-C+-NH2
Cl-‑
NH NH2
Входит в состав к-т: анбилина, антибиотика стрептомицилина, нукл.осн: гуанина.
