
- •Механизм:
- •Нитриты
- •Гидразиды
- •3) Из сл.Эфиров
- •Дикарбоновые кислоты
- •Ненасыщенные дикарбоновые кислоты
- •Ароматические дикарбоновые кислоты
- •Сульфоновые кислоты
- •Ароматические (фенолокислоты)
- •Производные солициловой кислоты
- •1) Произ-ые по –cooh:
- •2) Ппроизв-ые по –oh:
- •Оксокислоты
- •Алкилирование
- •Природные α-аминокислоты
- •Специфич.Св-ва аминокислот.
- •Пептиды и белки
- •С троение пептидной группы
- •Химический метод синтеза пептидов(классич)
- •Твердофазный синтез пептидов (тфсп)
- •Важнейшие пентозы:
- •Важнейшие гeксозы:
- •Стереоизомерия
- •Таутомерия
- •Конформации моносахаридов.
- •Конформация галактоперонозы
- •Химические св-ва моносахаридов.
- •Качественные реакции обнаружения гексоз., и пентоз.,
- •Другие представители моносахаридов.
- •Аминосахара
- •Дисахариды
- •Химические св-ва:
- •Полисахариды
- •Крахмал
- •Аминопектин
- •Декстраны
- •Пособы получения:
- •Галогенирование
- •Специфич.Реакции
- •Пятичленные гетероциклы с 2-мя гетероатомами
- •Имидазол. Получение:
- •Важнейшие производные:
- •Производные пиразола.
- •3(5)-Оксипиразол пиразолон-3(5)
- •Синтез антипирина
- •Синтез амидо из антипирина
- •Хинолин
- •Производные хинолина
- •Производные пиримидина
- •Синтез барбитуровой к-ты.
- •Оксазины
- •Тиазины
- •Производные фенотиазина
- •Мочевая к-та.
- •Метилированные ксантины
- •Птеридин
- •Аллоксазин изоаллоксазин.
- •Алкалоиды
- •**Морфин
- •** Кокаин
- •Нуклеиновые ( азотистые основания)
- •Нуклеозиды:
- •Нуклеотиды
- •2 Цепи в этой спирали антипараллельны, т.Е.Их 5’ и 3’-межнуклеотидные фосфодиэфир.Мостики параллельны противоположно.
- •Коферментные нуклеотиды
- •2)Флавиновые ( фмн и фад)
- •Терпены
- •Циклические
- •Производные камфана :
- •Стероидные гормоны (половые г.И г.Коры надпочечников)
- •Желчные кислоты
- •Стерины
- •Омыляемые липиды
- •Простые липиды
- •Обзорная лекция
- •Задачи:
Конформации моносахаридов.
Как известно 6 членные циклы в пр-ве принимают дермодинамич.выгодную конформацию кресла, а заместители предпочтительно заним.экваториальное полож(более выгодное)
У α –анамера полуацет.гидроксил занимает аксиальное положение, а у β-экватор.

 H
H
H
H

 CH2OH
HO
CH2OH
CH2OH
HO
CH2OH
O

 H
O
O
H
O
O
H







 O
H H e OH HO
H H
O
H H e OH HO
H H
H OH H OH H
H OH(a)
β-Д-глюкопираноза α-Д-глюкопираноза
69% 31%
Конформация галактоперонозы
У галактоперенозы спирт.гидроксил у С4 расположен аксиально, в р-ре преобр.β –анамер.
(а)OH OH




H CH2OH O H CH2OH O


 H H
H H
H H
H H
H



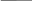
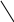
 O
HO
O
HO
 H HO
(e)OH
H OH
H HO
(e)OH
H OH
 H
H
H
H
β-Д-галактопиранозы. OH
У маннопиранозы спирт.гидроксил при С2 расположен аксиально.
H H
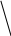
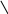



H O CH2OH O HO



 H OH(a)
CH2OH
O
H OH(a)
CH2OH
O
H


 O
HO H OH
O
HO H OH
H 2H OH H H
 H
H
H
H
OH
β-Д-маннопираноза (31%) α-Д-маннопираноза (69%)
В р-ре преобл.α-аномер, у α-ого гидроксилы при С1 и С2 наиболее удалены, что искл.отталк.е- 3-х атом.О2
