
- •Механизм:
- •Нитриты
- •Гидразиды
- •3) Из сл.Эфиров
- •Дикарбоновые кислоты
- •Ненасыщенные дикарбоновые кислоты
- •Ароматические дикарбоновые кислоты
- •Сульфоновые кислоты
- •Ароматические (фенолокислоты)
- •Производные солициловой кислоты
- •1) Произ-ые по –cooh:
- •2) Ппроизв-ые по –oh:
- •Оксокислоты
- •Алкилирование
- •Природные α-аминокислоты
- •Специфич.Св-ва аминокислот.
- •Пептиды и белки
- •С троение пептидной группы
- •Химический метод синтеза пептидов(классич)
- •Твердофазный синтез пептидов (тфсп)
- •Важнейшие пентозы:
- •Важнейшие гeксозы:
- •Стереоизомерия
- •Таутомерия
- •Конформации моносахаридов.
- •Конформация галактоперонозы
- •Химические св-ва моносахаридов.
- •Качественные реакции обнаружения гексоз., и пентоз.,
- •Другие представители моносахаридов.
- •Аминосахара
- •Дисахариды
- •Химические св-ва:
- •Полисахариды
- •Крахмал
- •Аминопектин
- •Декстраны
- •Пособы получения:
- •Галогенирование
- •Специфич.Реакции
- •Пятичленные гетероциклы с 2-мя гетероатомами
- •Имидазол. Получение:
- •Важнейшие производные:
- •Производные пиразола.
- •3(5)-Оксипиразол пиразолон-3(5)
- •Синтез антипирина
- •Синтез амидо из антипирина
- •Хинолин
- •Производные хинолина
- •Производные пиримидина
- •Синтез барбитуровой к-ты.
- •Оксазины
- •Тиазины
- •Производные фенотиазина
- •Мочевая к-та.
- •Метилированные ксантины
- •Птеридин
- •Аллоксазин изоаллоксазин.
- •Алкалоиды
- •**Морфин
- •** Кокаин
- •Нуклеиновые ( азотистые основания)
- •Нуклеозиды:
- •Нуклеотиды
- •2 Цепи в этой спирали антипараллельны, т.Е.Их 5’ и 3’-межнуклеотидные фосфодиэфир.Мостики параллельны противоположно.
- •Коферментные нуклеотиды
- •2)Флавиновые ( фмн и фад)
- •Терпены
- •Циклические
- •Производные камфана :
- •Стероидные гормоны (половые г.И г.Коры надпочечников)
- •Желчные кислоты
- •Стерины
- •Омыляемые липиды
- •Простые липиды
- •Обзорная лекция
- •Задачи:
Специфич.Св-ва аминокислот.
Аминокислоты –это амф-ые соединения.
** образование внутр.солей
R
 -CH-COOH
-CH-COOH
NH2
R
H+
 -CH-COOH
R-CH-COO-
OH-
R-CH-COO-
-CH-COOH
R-CH-COO-
OH-
R-CH-COO-
NH+3 NH3 NH2 анион
Катион внутр.соль
(биополярный ион) цвиттерион
Р-р каждой аминокислоты харак-ся своим значением
Рн характер q зависит от строен. R и рН среды.
В опред.среед сумма «+» q и «-» q могут быть равными. Это значение рн, получило название – изоэлектрической точки. (ИЭТ)
* *взаим.с
Сu(OH)2
O
*взаим.с
Сu(OH)2
O

 H2N
HO-C
H2N
HO-C

 R-CH
OH-Cu-OH-
CH-R
R-CH
OH-Cu-OH-
CH-R
 C-OH NH2
-H2O
C-OH NH2
-H2O
O
 O
O



 H2N
O-C
H2N
O-C
R

 -CH
CH CH-R
-CH
CH CH-R
 C-O
C-O
O NH2
** Обр-ие пептидов.
 O
O H
O
O H
H
 2N-CH-C
+ HNH – CH-COOH H2N-CH-C-N-CH-COOH
2N-CH-C
+ HNH – CH-COOH H2N-CH-C-N-CH-COOH
R1 R2 -H2O R1 R2
Пептидная связь.(дипептид)
**Нингидридовые реакции-качеств.реак.на α-АМК

 O
NH2
O
O
NH2
O



 OH +R-CH-COOH
R-C
OH +R-CH-COOH
R-C


 OH -CO2
H
OH -CO2
H
 O O
O O

 O
=N-
O
=N-
O O
Пурпур Расмана
Пептиды и белки
Пептиды-продукты взаим-ия АМК. Образуются либо при гидролизе белков, либо много пептидов, облад-их биол.активностью. N-концевая АМК амидная связь.


 O H
O
O H
O
O H
O
O H
O
H


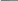 2N-CH-C
+ H-N-CH-C
H2N-CH-C-N-CH-CH-C
2N-CH-C
+ H-N-CH-C
H2N-CH-C-N-CH-CH-C
CH3 OH CH2OH OH -H2O CH3 CH3OH OH С-кольц.АМК
Аланин сирин аланилсерин
N-концевая (не участв.в об-ие пептид.связи)
COOH-не уч-ет в об-ие пептид.связи.
С троение пептидной группы
R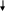 2
H
2
H

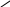
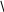
 Cl N
Cl N
 C C2
C C2
O R2 H пептидная связь яв-ся плоской копланарной
Неопределенная пара е-атома N нах-ся в сопряжении с П-связью карбонильной группы в р-те чего связь с-N укорачивается и имеет характер двойной связи, вокруг α-ой нет свободного вращения.
П ,р-сопряж.
O O O-
-



 C-N-
-C=N-
C=N+-
C-N-
-C=N-
C=N+-
H H H Благодаря наличию электронного резонанса возможно об-ие водор.связей, и возможно сущ-ие цис и транс изомеров. В природных пептидах и белках встречается транс расп-ие радикалов.
