
- •Содержание contents
- •Онкологические заболевания органов мочеполовой системы
- •1.1. Эпидемиология
- •1.2. Этиология, факторы риска
- •1.3. Профилактика
- •1.4. Скрининг
- •1.5. Топографическая и клиническая анатомия предстательной железы
- •1.6. Патоморфологическая характеристика рака предстательной железы
- •1.7. Экстрапростатическое распространение опухоли
- •1.8. Международная классификация рака предстательной железы по системе tnm
- •1.9. Диагностика рака предстательной железы
- •1.9.1. Методы диагностики отдаленных метастазов
- •1.9.2. Диагностика и степень распространенности опухолевого процесса
- •1.9.3. Клинические проявления ограниченного и местно распространенного рака предстательной железы
- •1.10. Клинические проявления диссеминированного рака предстательной железы
- •1.11. Оценка степени распространенности рака предстательной железы
- •1.12. Прогноз
- •1.13. Лечение рака предстательной железы
- •1.13.1. Выжидательная тактика
- •1.13.2. Радикальная простатэктомия
- •1.13.3. Неоадъювантная гормонотерапия
- •1.13.4. Адъювантная гормонотерапия
- •1.13.6. Альтернативные методы лечения локализованного рака предстательной железы
- •1.14. Контрольные вопросы
- •1.15. Тестовые задания
- •1.16. Рекомендуемая литература
- •2.1. Эпидемиология
- •2.2. Факторы риска
- •2.3. Патоморфологическая характеристика рака яичка
- •2.4. Клинические проявления
- •2.5. Диагностика рака яичка
- •Уровень хгт и альфа-фп в зависимости от нозологической формы опухоли яичка
- •2.6. Международная классификация рака предстательной железы по системе tnm
- •2.7. Лечение рака яичка
- •2.8. Контрольные вопросы
- •2.9. Тестовые задания
- •2.10. Рекомендуемая литература
- •3.1. Эпидемиология
- •3.2. Патоморфологическая характеристика рака яичка
- •3.3. Диагностика рака яичка
- •3.3.1. Рекомендации по диагностике рака полового члена
- •3.4. Международная классификация рака полового члена по системе tnm
- •3.5. Лечение рака полового члена
- •3.5.1. Первичная опухоль
- •3.5.2. Регионарные метастазы
- •3.5.3. Рекомендации по лечению рака полового члена
- •3.5.4. Качество жизни
- •3.5.5. Технические аспекты оперативного лечения рака полового члена
- •3.5.6. Химиотерапия
- •3.5.7. Прогностические факторы
- •3.6. Диспансеризация
- •3.6.1. Рекомендации по диспансеризации больных раком полового члена
- •3.7. Контрольные вопросы
- •3.8. Тестовые задания
- •3.9. Рекомендуемая литература
- •4.1. Эпидемиология
- •4.2. Этиология и патогенез
- •4.3. Патоморфологическая характеристика рака почки
- •4.4. Метастазирование рака почки
- •4.5. Спонтанная регрессия
- •4.6. Диагностика рака почки
- •4.7. Дифференциальная диагностика рака почки
- •4.8. Клинические проявления рака почки
- •4.9. Классификация рака почки
- •4.10. Прогноз
- •4.11. Хирургическое лечение рака почки
- •4.11.1. Хирургическое лечение локального рака почки
- •4.11.2. Выбор хирургического доступа
- •4.11.3. Хирургическое лечение местно распространенного рака почки
- •I. Опухолевое распространение на магистральные сосуды
- •II. Опухолевое распространение на соседние органы
- •III. Хирургическое лечение отдаленных метастазов
- •4.11.4. Паллиативные хирургические вмешательства
- •4.11.5. Осложнения при хирургическом лечении рака почки
- •4.11.6. Органосохраняющее лечение при раке почки
- •4.11.7. Эндоскопические операции
- •4.11.8. Хирургическое лечение солитарных и единичных метастазов рака почки
- •4.11.9. Хирургическое лечение местных рецидивов после нефрэктомии
- •4.12. Лекарственное лечение метастатического рака почки
- •4.13. Лучевая терапия
- •4.14. Контрольные вопросы
- •4.15. Тестовые задания
- •4.16. Рекомендуемая литература
- •5.7. Контрольные вопросы
- •5.8. Тестовые задания
- •5.9. Рекомендуемая литература
- •6.1. Эпидемиология
- •6.2. Факторы риска
- •6.3. Патоморфологическая характеристика
- •6.4. Классификация tnm
- •6.5. Клиническая картина
- •6.6. Диагностика опухолей мочевого пузыря
- •6.7. Лечение рака мочевого пузыря
- •6.7.1. Лечение поверхностного переходно-клеточного рака мочевого пузыря
- •6.7.2. Лечение инвазивного рака мочевого пузыря
- •6.7.3. Сравнительная оценка органосохраняющих и органоуносящих методов хирургического лечения рака мочевого пузыря
- •6.7.4. Вопросы пластики и протезирования мочевого пузыря
- •6.8. Лечение инвазивного рмп
- •6.9. Лучевая терапия
- •6.10. Генерализованный рак мочевого пузыря
- •6.11. Контрольные вопросы
- •6.12. Тестовые задания
- •6.13. Рекомендуемая литература
- •Первый вариант
- •Второй вариант
- •Глоссарий
- •Интернет ресурсы
- •Онкологические заболевания органов мочеполовой системы
- •644043 Г. Омск, ул. Ленина, 12; тел. 23-05-98
1.6. Патоморфологическая характеристика рака предстательной железы
Невозможно правильно установить диагноз рака предстательной железы без гистологического и цитологического исследования биопсийного и операционного материала, целью которого является стадирование РПЖ в целях определения дальнейшей тактики лечения, прогноза заболевания для каждого конкретного больного.
Пролиферативные изменения железистого эпителия предстательной железы периферической зоны обозначаются как простатическая интраэпителиальная неоплазия (PIN), центральной зоны – атипическая аденоматозная гиперплазия. Все виды атипической гиперплазии являются факультативным предраком и рассматриваются как предшественники аденокарциномы.
I. Пролиферативная воспалительная атрофия (PIA) – локальные участки эпителиальной атрофии, близкие к PIN или карциноме. Эти повреждения демонстрируют генетическую альтерацию, связанную с раком простаты и признаками клеточного стресса.
II. Простатическая интраэпителиальная неоплазия (PIN) – клеточная пролиферация ацинарного эпителия на разных стадиях клеточных отклонений, характеризуется прогрессирующей утратой маркеров секреторной дифференцировки и патологическим изменением ядер и ядрышек, плотности микрососудов, генетической нестабильностью и содержанием ДНК. PIN бывает высокой и низкой степени. PIN высокой степени делится на 6 типов (пучковидный, микропапиллярный, плоский, крибриформный, мелкоклеточный, инвертированный).
Больным с изолированной PIN высокой степени в течение 6 месяцев выполняется повторная полифокальная биопсия, независимо от уровня ПСА и результатов пальцевого ректального исследования. В настоящее время при обнаружении PIN лечение больному не показано. PIN является прогностическим фактором развития рака простаты.
III. Злокачественные образования:
А. Аденокарцинома – мелкоацинарный рак (small acinar carcinoma), составляет 95-97% всех случаев РПЖ, происходит из ацинарного эпителия преимущественно периферической зоны предстательной железы, но около 20-25% аденокарцином возникает в переходной зоне простаты. В этих случаях рак может быть диагностирован в ходе гистологического исследования после трансуретральной резекции предстательной железы. Как правило, он соответствует стадиям Т1а или Т1b.
Выделяют несколько гистологических вариантов аденокарциномы.
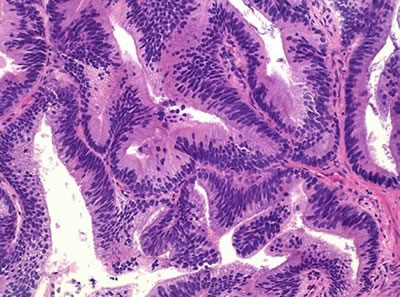
1. Протоковый (эндометриоидный) рак (ductal or endometriod carcinoma) – характеризуется папиллярным ростом, локализуется в протоках простаты (рис. 3а).
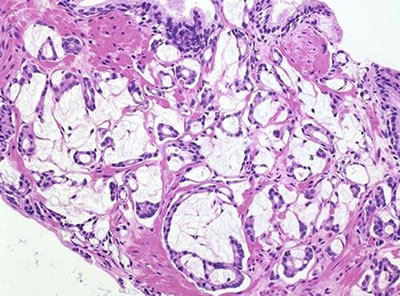
2. Муцинозная аденокарцинома (или коллоидная) (mucinous adenocarcinoma) – характеризуется тем, что 25% и более желез в просвете содержит слизь (муцин) или железы «плавают» в большом количестве слизи (рис. 3б). Однако такая форма расположения муцина может быть найдена при атипичной аденоматозной гиперплазии, PIN, что стимулирует рак простаты.
Для муцинозной аденокарциномы характерно:
1) клетки не имеют рецепторов к андрогенам; 2) критерии Глисона неприменимы; 3) прогноз такой формы рака простаты более неблагоприятный по сравнению с обычной аденокарциномой; 4) устойчива к традиционной терапии; 5) средняя продолжительность жизни не более 3 лет.
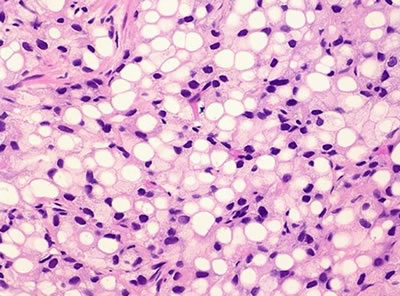
3. Перстневидноклеточный рак (signet cell carcinoma) – характеризуется наличием клеток в виде «перстня», кольца с камнем, что является результатом наличия цитоплазматического просвета, интрацитоплазматической слизи и липидных вакуолей (рис. 3в). Крайне неблагоприятный вид рака, больные погибают в течение 3х лет после установления диагноза.
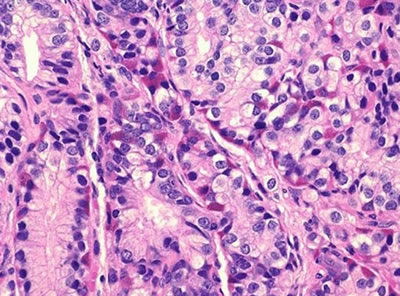
4. Мелкоклеточный рак – нейроэндокринный рак (small cell carcinoma, neuroendocrine carcinoma), который трудно отличить от низкодифференцированной аденокарциномы. Характерны большие нейроэндокринные клетки с большими эозинофильными гранулами (рис. 3г). Гранулы содержат хромогранин А, серотонин, бомбезин, васкулярный эндотелиальный фактор роста (VEGF).
Нейроэндокринные клетки андрогеннезависимы и не вызывают повышения ПСА. Клетки-предшественницы выделяют нейропептиды, что может иметь значение в клинике в виде формирования гормонорефрактерного фенотипа рака простаты. Однако клетки могут быть чувствительными к лучевой и химиотерапии (VP-16 этопозид, цисплатин).
Наряду с типичными признаками аденокарциномы предстательной железы могут иметь место паранеопластические синдромы в виде синдрома Кушинга, злокачественной гиперкальциемии, синдрома неадекватной секреции антидиуретического гормона, миастенический синдром; средняя выживаемость – менее 1 года.
5. Плоскоклеточный рак (железисто-плоскоклеточный) – опухоли с плоскоклеточной дифференцировкой, возникающие из выстилающих базальных клеток в периуретральных железах, простатических ацинусах, не содержат железистых элементов. Для данного вида опухоли характерно агрессивное течение.
Вариант плоскоклеточной опухоли – аденоакантокарцинома – менее 0,6% опухолей простаты. Для плоско-клеточного рака характерно: 1) возраст больных 50-80 лет; 2) около 50% аденоакантокарцином возникает у больных карциномой после гормональной и лучевой терапии; 3) описаны случаи взаимосвязи с инфекцией – шистосомозом; 4) проявляется мочевой обструкцией, болью в костях, гематурией; 5) быстро метастазирует в кости, вызывая остеолитическое их поражение; 6) не вызывает повышение ПСА; 7) гормональная, лучевая и химиотерапия не эффективны. В случае наличия данной опухоли рекомендуется выполнить радикальную простатэктомию, цистопростэктомию, тотальную уретроэктомию.
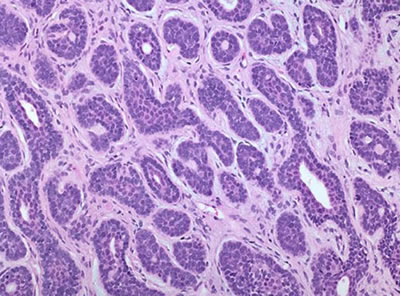
6. Базалоидный рак (базальноклеточная карцинома) – солидные скопления крупных базалоидных клеток, часто с периферическим некрозом, растет по периневральным пространствам (рис. 3д). Клетки не имеют рецепторов к андрогенам, но имеют к эстрогенам и прогестерону. Опухоль характеризуется высоким потенциалом быстрого злокачественного роста и образования отдаленных метастазов (биологическое поведение изучено недостаточно из-за малого количества случаев и непродолжительности наблюдений).
а
 б
б
в
 г
г
д
 е
е
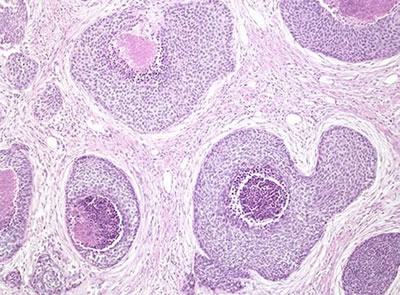
Рис. 3. Патоморфологическая характеристика различных форм рака предстательной железы. а - протоковая (эндометриоидная) аденокарцинома; б - коллоидная аденокарцинома; в - перстневидноклеточная карцинома; г - нейроэндокринная аденокарцинома; д - базальноклеточная карцинома; е - переходноклеточный рак.
Кроме выше названных форм, к злокачественным образованиям предстательной железы относится аденосквамозный рак и кистозная аденокарцинома.
Б. Переходноклеточный (уротелиальный) рак – происходит из главных протоков предстательной железы, которые лежат вблизи мочеиспускательного канала, что и обусловливает его название (рис. 3е). Может быть самостоятельным очагом рака простаты и одним из вариантов перехода рака из мочевого пузыря. Первичный рак встречается в 0,7-2,8% случаев всех видов РПЖ, происходит из уротелиальной выстилки простатической уретры и проксимальной части простатических протоков. Вторичный – обусловлен прорастанием уроуротелиальных опухолей мочевого пузыря и уретры в простату. Может наблюдаться сочетание инвазивной уротелиальной карциномы мочевого пузыря и вторичной уротелиальной карциномы предстательной железы.
В. Мезенхимальные опухоли – саркомы (лейомиосаркома, рабдомиосаркома) – встречаются редко (0,1-0,2% всех опухолей предстательной железы).
1. Лейомиосаркома – чаще встречается у взрослых (40-70 лет), однако 20% лейомиосарком может встречаться в молодом возрасте. Прогноз крайне неблагоприятный, часто и быстро метастазирует (чаще в легкие), рецидивирует. 5-летняя выживаемость составляет около 40%.
2. Рабдомиосаркома – встречается у детей, относится к эмбриональному подтипу опухолей, для подтверждения необходимо иммуногистохимическое подтверждение. Отдаленные метастазы встречаются редко. Наиболее агрессивный тип – альвеолярная рабдомиосаркома. Отдаленные метастазы встречаются редко, прогноз крайне неблагоприятный, 5-летняя выживаемость составляет 0-10%. После биопсии и гистологического подтверждения проводится интенсивная лучевая и химиотерапия.
Г. Лимфоэпителиальный рак.
1.6.1. Гистологическая степень (индекс Глисона)
Наиболее значимым предиктором прогрессирования РПЖ после биопсии и радикальной простатэктомии является сумма Глисона, определенная в препарате (табл. 1, 2). Исследование индекса Глисона выполняется в случаях, если опухоль происходит из секреторных клеток. Сумма Глисона состоит из двух слагаемых: первичного (наиболее распространенного) и вторичного (второй по распространенности) показателей Глисона. Если в препарате не выявляется вторичный показатель Глисона, то для получения суммы Глисона первичный показатель Глисона удваивается. Первичный и вторичный показатели Глисона должны указываться в скобках после указания суммы Глисона (например, сумма Глисона 7 [3+ 4]).
Таблица 1
Степени злокачественности по Глисону (Gleason grade)
Grade 1 – одиночные, отдельные, плотно расположенные железы |
Grade 2 – одиночные железы, более тесно располагающиеся, менее единообразные |
Grade 3 – одиночные железы различного размера и взаимоотношения, крибриформные и папиллярные структуры |
Grade 4 – неправильные скопления желез и сливающиеся пласты эпителия, могут наблюдаться светлые клетки |
Grade 5 – анапластический рак |
Таблица 2
Группировка сумм Глисона по прогностическим категориям
2–4: |
Высокодифференцированный РПЖ |
5–6: |
Умеренно-высокодифференцированный РПЖ |
7: |
Умеренно-низкодифференцированный РПЖ |
8–10: |
Низкодифференцированный РПЖ |
Или |
|
2–6: |
Высокодифференцированный РПЖ |
7: |
Умеренно дифференцированный РПЖ |
8–10: |
Низко дифференцированный РПЖ |
