
- •Научные консультанты:
- •Сокращения и глоссарий
- •Введение
- •Обзор литературы
- •1.1 Торможение в гиппокампе
- •1.1.1 ГамКергическая синаптическая передача
- •1.1.2 ГамКергические рецепторы
- •1.1.3 Разнообразие форм торможения
- •1.1.4 Механизмы и функциональное значение тонического торможения
- •1.2 Взаимодействие между глутамат и гамКергической системами
- •1.2.1 Гетеросинаптические взаимодействия
- •1.2.2 Критерии гетеросинаптической депрессии
- •1.2.3 Метаботропные рецепторы группы III в гиппокампе
- •1.2.4 Каинатные рецепторы в гиппокампе
- •1.3 Механизмы фокального эпилептогенеза
- •1.3.1 Исследования эпилептогенеза
- •1.3.2 Критерии развития эпилептиформной активности
- •1.3.3 Возбуждающие механизмы в эпилептогенезе
- •1.3.4 Тормозные механизмы в эпилептогенезе
- •1.4 Постановка цели и задач исследования
- •2. Материалы и методы
- •2.1 Срезы гиппокампа
- •2.1.1 Приготовление и растворы
- •2.1.2 Рабочая установка для поддержания срезов и манипуляторы
- •2.1.3 Идентификация клеток с помощью световой микроскопии
- •2.2 Регистрация и анализ полевых потенциалов
- •2.3 Записи и анализ токов (потенциалов) в режиме фиксации потенциала (тока) с одиночных нейронов
- •2.3.1 Электроды и внутриклеточные растворы
- •2.3.2 Проведение регистраций и сохранение данных
- •2.3.2 Анализ спонтанных и вызванных ответов в режиме фиксации потенциала
- •2.4 Записи и анализ ответов на ионтофоретические аппликации
- •2.5 Записи и анализ токов с outside-out patch
- •2.5.1 Приготовление outside-out patch
- •2.5.2 Система быстрой аппликации веществ
- •2.5.3 Определение биофизических свойств рецепторов с использованием анализа токов, полученных с outside-out пейчей
- •2.6 Модели эпилептогенеза in vivo
- •2.6.1 Электрический киндлинг
- •2.6.2 Модель аудиогенной судорожной активности. Аудиогенный киндлинг
- •2.7 Использованные вещества
- •2.8 Статистический анализ
- •3 Результаты исследованИй и их обсуждение
- •3.1 Нетипичные фармакологические свойства гамКергических рецепторов в гиппокампальных интернейронах
- •3.1.1 Различная чувствительность ионотропных гамКергических рецепторов к пикротоксину в интернейронах и пирамидных клетках
- •3.1.2 Ионные каналы ионотропных гамКергических рецепторов в интернейронах и пирамидных клетках имеют различную проводимость
- •3.1.3 Ионотропные гамКергические рецепторы как в интернейронах, так и пирамидных клетках чувствительны к агонисту гамкс рецепторов
- •3.1.4 Пентобарбитал по-разному модулирует гамКергические токи, вызываемые аппликацией caca (50 м)
- •3.1.5 Тпст в интернейронах, регистрируемые в присутствии 100 м пикротоксина, обладают повышенной чувствительностью к антагонисту гамкс рецепторов
- •3.1.6 Токи, опосредованные гамКергическими рецепторами, в присутствии 100 м пикротоксина возникают за счет характерной Cl-/hco3- ионой проводимости
- •3.1.7 Эффект аллостерических модуляторов гамка рецепторов на устойчивые к пикротоксину токи, опосредованные гамКергическими рецепторами
- •3.1.8 Сравнение эффективности антагонистов гамка и гамкс рецепторов на устойчивые к пикротоксину токи, опосредованные гамКергическими рецепторами
- •3.1.9 Интернейроны содержат рецепторы, обладающие нетипичными фармакологическими свойствами
- •3.1.10 Нетипичные гамКергические рецепторы и традиционные типы рецепторов (гамка и гамкс)
- •3.1.11 Возможная субъединичная композиция нетипичных гамКергических рецепторов в интернейронах
- •Заключение
- •3.2 Регуляция возбудимости нейронов гиппокампа за счет гамКергического тонического торможения
- •3.2.1 Базовый тонический гамКергический ток специфичен для интернейронов, но не пирамидных клеток
- •3.2.2 Увеличение внеклеточной концентрации гамк ведет к возникновению тонического тока в пирамидных клетках и повышению в интернейронах
- •3.2.3 Температурная зависимость тонического гамКергического тока и фазических спонтанных тпст
- •3.2.4 Возможная роль тонического торможения в эпилептогенезе
- •3.2.5 Заключение
- •3.3 Модуляция гамКергической передачи в гиппокампе метаботропными рецепторами
- •3.3.1 L-ap4 подавляет и тормозные, и возбуждающие синаптические токи в интернейронах
- •Демонстрирующих отсутствие метаботропных рецепторов группы III на терминалях коллатералей Шаффера, оканчивающихся на пирамидных клетках са1.
- •3.3.2 Синаптически высвобождаемый глутамат снижает тпст
- •3.3.3 Глутамат опосредует гетеросинаптическую депрессию тпст
- •3.3.4 Изменения в эффективности обратного захвата глутамата влияет на гетеросинаптическую депрессию
- •3.3.5 Метаботропные рецепторы группы III опосредуют гетеросинаптическую депрессию по двум различным механизмам
- •3.3.6 Метаботропные рецепторы группы III модулируют частоту спонтанных тпст
- •3.3.7 Возможные молекулярные механизмы депрессии тпст при активации mGluR группы III
- •3.3.8 Последствия активации mGluR группы III для общей возбудимости нейрональной сети поля са1
- •3.3.9 Гетеросинаптическая депрессия, опосредованная метаботропными гамкb рецепторами
- •3.3.10 Заключение
- •3.4 Каинатные рецепторы модулируют гамКергическое торможение в гиппокампальных интернейронах
- •3.4.1 Каинат увеличивает частоту и амплитуду спонтанных тпст в интернейронах
- •3.4.2 Каинат увеличивает вероятность генерации антидромных потенциалов действия в интернейронах
- •3.4.3 Каинат вызывает спонтанные аксональные потенциалы действия
- •3.4.4 Спилловер глутамата активирует аксональные каинатные рецепторы
- •3.4.5 Последствия аксональной деполяризации, вызываемой каинатными рецепторами, для гамКергической передачи
- •3.4.6 Каинат усиливает вызванные тпст в интернейронах
- •3.4.7 Каинат приводит к увеличению гамКергического тонического тока
- •3.4.8 Последствия усиления гамКергической передачи в интернейронах, вызываемой каинатными рецепторами, для возбудимости нейрональной сети
- •3.4.9 Заключение
- •3.5 Оказывают ли метаботропные рецепторы группы III и каинатные рецепторы противоположное действие на гамКергическую передачу?
- •3.6 Механизмы развития пачечной активности в гиппокампе
- •3.6.1 Кратковременные увеличения внеклеточной концентрации калия создают долговременное снижение порога развития пачечных разрядов в поле са1 гиппокампа
- •3.6.2 Развитие пачечных разрядов в поле са1 гиппокампа не зависит от активности нейронов поля са3
- •3.6.3 Окклюзия развития пачечных разрядов в поле са1 в ответ на кратковременные увеличения внеклеточной концентрации калия в моделях эпилептогенеза in vivo
- •3.6.4 Является ли пачечная активность в поле са1 гиппокампа эпилептиформной?
- •3.6.5 Способность пирамидных нейронов поля са1 генерировать пачечные разряды сопровождается повышением возбудимости этих клеток
- •3.6.6 Роль nmda рецепторов и l-типа кальциевых каналов в повышение возбудимости пирамидных клеток и генерации пачечных разрядов
- •3.6.7 Заключение
- •Заключение
- •Клеткоспецифичность гамКергического торможения в гиппокампе
- •Клеткоспецифичность модуляции гамКергического торможения в гиппокампе
- •Возбудимость и торможение в эпилептогенезе
- •Эффектов веществ влияющих на гамКергические механизмы, описанные в данной диссертационной работе, представлена втаблице 4.1 (см также Рис. 4.1). Выводы
- •Список рисунков
- •Список литературы
3.4.4 Спилловер глутамата активирует аксональные каинатные рецепторы
Полученные в предыдущих разделах результаты демонстрируют эффект аппликации экзогенного агониста каинатных рецепторов. Однако, из них не ясно может ли эндогенный глутамат, высвобождаемый синаптически, приводить к активации аксональных каинатных рецепторов. Для ответа на этот вопрос мы воспользовались протоколом аналогичным тому, который использовался для исследования гетеросинаптической депрессии ТПСТ, опосредованной метаботропными рецепторами. Мы стимулировали коллатерали Шаффера серией стимулов (5 стимулов при частоте 5 Гц), которая должна была вызвать значительный
контроль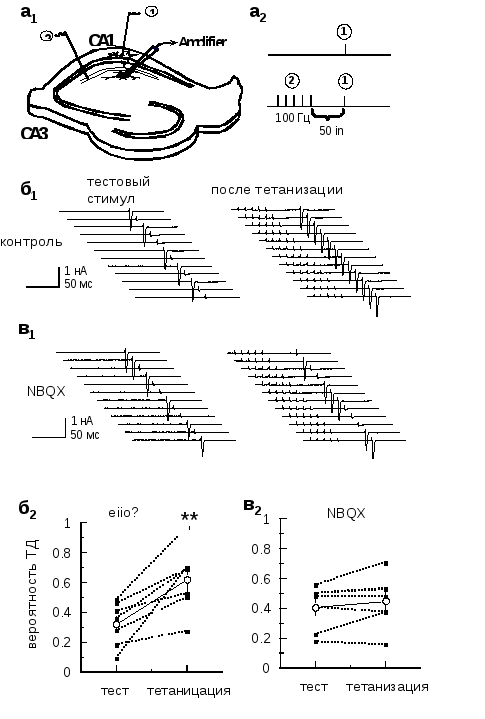
Рис. 3.4.4 Синаптически высвобождаемый глутамат увеличивает возбудимость аксонов через каинатные рецепторы
а, Экспериментальный протокол. Позиции стимулирующих и регистрирующего электродов показаны на рисункеа1. Тестовый стимул, инициирующий антидромный ТД (а2) подавался через электрод (1) либо сам по себе, либо после серии стимулов (5 стимулов при частоте 100 Гц) через дистальный электрод (2).б, Оригинальные записи, полученные в одном интернейроне, показывают, что вероятность генерации ТД увеличивается после высокочастотной стимуляции глутаматергических терминалей. Это увеличение подавлялось при блокаде каинатных рецепторов с помощью NBQX (100 μМ).в, Данные, усреденные по 7 интернейронам. **: p<0,01
выброс глутамата. Затем с интервалом 50 мс ты тестировали вероятность возникновения антидромного ТД в ответ на стимуляцию аксона в str.orience(Рис 3.4.4а). Поскольку AMPA, NMDA, ГАМКА, ГАМКBи mGluR группы III рецепторы были блокированы, мы предположили, что возможные эффекты высокочастотной стимуляции возбуждающих терминалей будут опосредованы каинатными рецепторами. В 7 интернейронах мы обнаружили значительное увеличение вероятности возникновения антидромного ТД после стимуляции возбуждающих терминалей (p<0,01 по сравнению с контрольными значениями), которое подавлялось при аппликации NBQX, антагониста каинатных рецепторов (100 μМ; p=0,41 по сравнению с контрольными значениями) (Рис. 3.4.4б,в).
Таким образом, мы показали, что активация аксональных каинатных рецепторов может происходить благодаря синаптически высвобождаемому глутамату. Поскольку не существует доказательств наличия аксо-аксональных синапсов в интернейронах поля СА1 гиппокампа, то этот глутамат, по всей видимости, диффундирует от удаленных возбуждающих синапсов и достигает каинатных рецепторов на интернейронах.
3.4.5 Последствия аксональной деполяризации, вызываемой каинатными рецепторами, для гамКергической передачи
В проделанных экспериментах с высокочастотной стимуляцией глутаматергических терминалей нам не удалось показать, что синаптически высвобождаемый глутамат способен вызывать спонтанные токи действия в дистальных участках аксонов. Вероятно, это связано с ограничениями метода исследования гетеросинаптической модуляции in vitro, описанными ранее. Однако, если такой феномен имеет место in vivo, то он может представлять собой абсолютно новый механизм интеграции возбуждающей передачи в гиппокампе. Другими словами, если спонтанные потенциалы действия начинают возникать в аксонах интернейронов, когда внеклеточная концентрация глутамата достигает определенного уровня, то это может лежать в основе гомеостатического механизма, усиливающего торможение в гиппокампе. Однако, эти интернейроны дожны иннервировать пирамидные клетки, тогда как в данной работе мы продемонстрировали, что каинат усиливает торможение и самих интернейронов. Тем не менее, действие каината на спонтанные ТПСТ в пирамидных клетках довольно хорошо исследовано, значительное увеличение в их частоте продемонстрировано несколькими различными лабораториями. Эти данные могут быть объяснены возникновением спонтанных потенциалов действия в дистальном аксоне интернейронов, иннервирующих пирамидные клетки. Другим объяснением является то, что деполяризация в этих клетках возникает за счет активации каинатных рецепторов в соматодендритном компартменте и потенциал действия генерируется в аксонном холмике. Действие каината на спонтанные ТПСТ в интернейронах было изучено гораздо меньше. Незадолго, до публикации наших данных появилась работа Cossart с соавторами, в которой был показан эффект каината на частоту потенциал действия независимых миниатюрных ТПСТ в интернейронах (Cossart et al. 2001b). Это свидетельствует в пользу того, что каинат может, при определенных условиях, влиять непосредственно на высвобождение ГАМК. В наших экспериментах мы не обнаружили этого эффекта на миниатюрные ТПСТ у морских свинок, хотя смогли его воспроизвести при аппликации 1 М (но не 250 нМ) каината на срезах гиппокампа крыс (Рис. 3.4.5). Вероятно, каинат, прежду всего, деполяризует аксоны, но эта деполяризация, при достижении ей определенного уровня, может электротонически распространиться в ГАМКергические терминали, приводя к “прямому” эффекту на высвобождение нейротрансмиттера.
а1
а2
а3
б1
б2
б3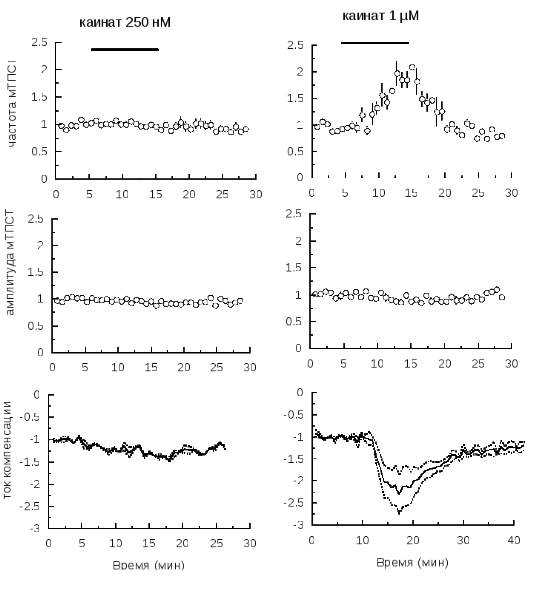
Рис. 3.4.5 Аппликация 1 μМ, но не 250 нМ, каината повышает частоту миниатюрных ТПСТ в интернейронах срезов гиппокампа крыс
а, Аппликация каината 250 нМ не вызывала значительных изменений ни в частоте (а1), ни амплитуде (а2) миниатюрных ТПСТ (спонтанных ТПСТ, регистрируемых в присутствии тетродотоксина) в интернейронах str.radiatum поля СА1 срезов гиппокампа крыс, При этом не происходило изменений в и токе компенсации (а3).б, Аппликация 1 μМ каината приводила к увеличению частоты (б1), но не амплитуды (б2) миниатюрных ТПСТ, а также увеличению тока компенсации (б3).
Для того чтобы определить роль каинатных рецепторов в модуляции ГАМКергической передачи между интернейронами мы исследовали действие каината на спонтанные ТПСТ, многие из которых отражают генерацию спонтанных потенциалов действия в пресинаптических нейронах. Каинат в концентрациях 250 нМ или 1 М значительно увеличивал как частотуспонтанных ТПСТ, регистрируемых в интернейронах, так и их амплитуду.
Существует несколько различных объяснений причинам, вызывающим увеличение одновременно в частоте и амплитуде сТПСТ в интернейронах под действием каината. Например, возможность существования специфической популяции пресинаптических интернейронов, чувствительных к каинату. Другим обяснением может быть облегчение распространения потенциалов действия в местах деления аксонов в пресинаптических интернейронах. Не останавливаясь на неопределенности механизмов, лежащих в основе этого феномена, важно отметить, что увеличение амплитуды сТПСТ под действием каината характерно только для интернейронов и не было показано для пирамидных клеток.
Таким образом, действие каината на нейроны гиппокампа обладает клеткоспецифичностью, подобной той, которая наблюдается в действии агонистов mGluR группы III. Мы показали, что деполяризация пресинаптических аксонов за счет каинатных рецепторов может объяснять увеличение спонтанных ТПСТ. Однако, почему каинат вызывает различные изменения этих токов в интернейронах и пирамидных клетках осталось неясным. Возможно, что различие определяется зависимостью распространения каинатных рецепторов по клеточной мембране в различных пресинаптических интернейронах. Не исключено, что интернейроны, в которых мы регистрировали ТПСТ, представляют собой гомогенную группу из всего разнообразия интернейронов гиппокампа (Freund and Buzsaki 1996; Freund and Gulyas 1997). Таким образом, мы не можем сказать имеют ли эти интернейроны связи с пирамидными клетками или же только с другими интернейронами. С другой стороны, в предыдущих работах не удалось показать определенной корреляции между морфологией интернейронов и действием на них каината (Cossart et al. 1998; Cossart et al. 2001b), что свидетельствует против выборочной модуляции возбудимости нейронов каинатными рецепторами.
