
- •Научные консультанты:
- •Сокращения и глоссарий
- •Введение
- •Обзор литературы
- •1.1 Торможение в гиппокампе
- •1.1.1 ГамКергическая синаптическая передача
- •1.1.2 ГамКергические рецепторы
- •1.1.3 Разнообразие форм торможения
- •1.1.4 Механизмы и функциональное значение тонического торможения
- •1.2 Взаимодействие между глутамат и гамКергической системами
- •1.2.1 Гетеросинаптические взаимодействия
- •1.2.2 Критерии гетеросинаптической депрессии
- •1.2.3 Метаботропные рецепторы группы III в гиппокампе
- •1.2.4 Каинатные рецепторы в гиппокампе
- •1.3 Механизмы фокального эпилептогенеза
- •1.3.1 Исследования эпилептогенеза
- •1.3.2 Критерии развития эпилептиформной активности
- •1.3.3 Возбуждающие механизмы в эпилептогенезе
- •1.3.4 Тормозные механизмы в эпилептогенезе
- •1.4 Постановка цели и задач исследования
- •2. Материалы и методы
- •2.1 Срезы гиппокампа
- •2.1.1 Приготовление и растворы
- •2.1.2 Рабочая установка для поддержания срезов и манипуляторы
- •2.1.3 Идентификация клеток с помощью световой микроскопии
- •2.2 Регистрация и анализ полевых потенциалов
- •2.3 Записи и анализ токов (потенциалов) в режиме фиксации потенциала (тока) с одиночных нейронов
- •2.3.1 Электроды и внутриклеточные растворы
- •2.3.2 Проведение регистраций и сохранение данных
- •2.3.2 Анализ спонтанных и вызванных ответов в режиме фиксации потенциала
- •2.4 Записи и анализ ответов на ионтофоретические аппликации
- •2.5 Записи и анализ токов с outside-out patch
- •2.5.1 Приготовление outside-out patch
- •2.5.2 Система быстрой аппликации веществ
- •2.5.3 Определение биофизических свойств рецепторов с использованием анализа токов, полученных с outside-out пейчей
- •2.6 Модели эпилептогенеза in vivo
- •2.6.1 Электрический киндлинг
- •2.6.2 Модель аудиогенной судорожной активности. Аудиогенный киндлинг
- •2.7 Использованные вещества
- •2.8 Статистический анализ
- •3 Результаты исследованИй и их обсуждение
- •3.1 Нетипичные фармакологические свойства гамКергических рецепторов в гиппокампальных интернейронах
- •3.1.1 Различная чувствительность ионотропных гамКергических рецепторов к пикротоксину в интернейронах и пирамидных клетках
- •3.1.2 Ионные каналы ионотропных гамКергических рецепторов в интернейронах и пирамидных клетках имеют различную проводимость
- •3.1.3 Ионотропные гамКергические рецепторы как в интернейронах, так и пирамидных клетках чувствительны к агонисту гамкс рецепторов
- •3.1.4 Пентобарбитал по-разному модулирует гамКергические токи, вызываемые аппликацией caca (50 м)
- •3.1.5 Тпст в интернейронах, регистрируемые в присутствии 100 м пикротоксина, обладают повышенной чувствительностью к антагонисту гамкс рецепторов
- •3.1.6 Токи, опосредованные гамКергическими рецепторами, в присутствии 100 м пикротоксина возникают за счет характерной Cl-/hco3- ионой проводимости
- •3.1.7 Эффект аллостерических модуляторов гамка рецепторов на устойчивые к пикротоксину токи, опосредованные гамКергическими рецепторами
- •3.1.8 Сравнение эффективности антагонистов гамка и гамкс рецепторов на устойчивые к пикротоксину токи, опосредованные гамКергическими рецепторами
- •3.1.9 Интернейроны содержат рецепторы, обладающие нетипичными фармакологическими свойствами
- •3.1.10 Нетипичные гамКергические рецепторы и традиционные типы рецепторов (гамка и гамкс)
- •3.1.11 Возможная субъединичная композиция нетипичных гамКергических рецепторов в интернейронах
- •Заключение
- •3.2 Регуляция возбудимости нейронов гиппокампа за счет гамКергического тонического торможения
- •3.2.1 Базовый тонический гамКергический ток специфичен для интернейронов, но не пирамидных клеток
- •3.2.2 Увеличение внеклеточной концентрации гамк ведет к возникновению тонического тока в пирамидных клетках и повышению в интернейронах
- •3.2.3 Температурная зависимость тонического гамКергического тока и фазических спонтанных тпст
- •3.2.4 Возможная роль тонического торможения в эпилептогенезе
- •3.2.5 Заключение
- •3.3 Модуляция гамКергической передачи в гиппокампе метаботропными рецепторами
- •3.3.1 L-ap4 подавляет и тормозные, и возбуждающие синаптические токи в интернейронах
- •Демонстрирующих отсутствие метаботропных рецепторов группы III на терминалях коллатералей Шаффера, оканчивающихся на пирамидных клетках са1.
- •3.3.2 Синаптически высвобождаемый глутамат снижает тпст
- •3.3.3 Глутамат опосредует гетеросинаптическую депрессию тпст
- •3.3.4 Изменения в эффективности обратного захвата глутамата влияет на гетеросинаптическую депрессию
- •3.3.5 Метаботропные рецепторы группы III опосредуют гетеросинаптическую депрессию по двум различным механизмам
- •3.3.6 Метаботропные рецепторы группы III модулируют частоту спонтанных тпст
- •3.3.7 Возможные молекулярные механизмы депрессии тпст при активации mGluR группы III
- •3.3.8 Последствия активации mGluR группы III для общей возбудимости нейрональной сети поля са1
- •3.3.9 Гетеросинаптическая депрессия, опосредованная метаботропными гамкb рецепторами
- •3.3.10 Заключение
- •3.4 Каинатные рецепторы модулируют гамКергическое торможение в гиппокампальных интернейронах
- •3.4.1 Каинат увеличивает частоту и амплитуду спонтанных тпст в интернейронах
- •3.4.2 Каинат увеличивает вероятность генерации антидромных потенциалов действия в интернейронах
- •3.4.3 Каинат вызывает спонтанные аксональные потенциалы действия
- •3.4.4 Спилловер глутамата активирует аксональные каинатные рецепторы
- •3.4.5 Последствия аксональной деполяризации, вызываемой каинатными рецепторами, для гамКергической передачи
- •3.4.6 Каинат усиливает вызванные тпст в интернейронах
- •3.4.7 Каинат приводит к увеличению гамКергического тонического тока
- •3.4.8 Последствия усиления гамКергической передачи в интернейронах, вызываемой каинатными рецепторами, для возбудимости нейрональной сети
- •3.4.9 Заключение
- •3.5 Оказывают ли метаботропные рецепторы группы III и каинатные рецепторы противоположное действие на гамКергическую передачу?
- •3.6 Механизмы развития пачечной активности в гиппокампе
- •3.6.1 Кратковременные увеличения внеклеточной концентрации калия создают долговременное снижение порога развития пачечных разрядов в поле са1 гиппокампа
- •3.6.2 Развитие пачечных разрядов в поле са1 гиппокампа не зависит от активности нейронов поля са3
- •3.6.3 Окклюзия развития пачечных разрядов в поле са1 в ответ на кратковременные увеличения внеклеточной концентрации калия в моделях эпилептогенеза in vivo
- •3.6.4 Является ли пачечная активность в поле са1 гиппокампа эпилептиформной?
- •3.6.5 Способность пирамидных нейронов поля са1 генерировать пачечные разряды сопровождается повышением возбудимости этих клеток
- •3.6.6 Роль nmda рецепторов и l-типа кальциевых каналов в повышение возбудимости пирамидных клеток и генерации пачечных разрядов
- •3.6.7 Заключение
- •Заключение
- •Клеткоспецифичность гамКергического торможения в гиппокампе
- •Клеткоспецифичность модуляции гамКергического торможения в гиппокампе
- •Возбудимость и торможение в эпилептогенезе
- •Эффектов веществ влияющих на гамКергические механизмы, описанные в данной диссертационной работе, представлена втаблице 4.1 (см также Рис. 4.1). Выводы
- •Список рисунков
- •Список литературы
3.2.5 Заключение
Таким образом, в данном разделе работы было показано:
1.В интернейронах str.radiatum, но не пирамидных клетках поля СА1 гиппокампа, при нормальных условиях помимо фазического торможения (ГАМКергических ТПСТ) существует пикротоксин-чувствительный ГАМКергический тонический ток.
2. Увеличение внеклеточной концентрации ГАМК при блокаде ее обратного захвата приводит к возникновению тонического тока как в интернейронах, так и в пирамидных клетках.
3. ГАМКергический тонический ток в интернейронах при нормальных условиях фармакологически отличается от ГАМКергического тонического тока, связанного с повышением внеклеточной концентрации ГАМК.
4. Повышение температуры приводит к увеличению частоты спонтанных ТПСТ (фазических токов). При этом сохраняется клеточная специфичность тонической проводимости для интернейронов, но не пирамидных клеток.
Результаты, полученные в данном разделе работы, являются первым детальным описанием тонического торможения в различных нейронах гиппокампа. Показана клеточная специфичность (интернейрон/пирамидная клетка) и фармакологическое различие типов тонического тока. Эти данные могут быть использованы для селективного изменения возбудимости определенных групп клеток и поиска эффективных антиэпилептических препаратов.
3.3 Модуляция гамКергической передачи в гиппокампе метаботропными рецепторами
Мы произвели регистрацию синаптических токов в интернейронах str.radiatum и пирамидных клетках поля СА1 с помощью пейчкламповских электродов (whole-cell patch pipettes). Приблизительно 25% интернейронов были биполярными клетками, остальные три- и мультиполярными. Мы не обнаружили принципиальных различий в ответах этих типов интернейронов на аппликацию L-AP4 (агонист метаботропных рецепторов группы III) или электрическую стимуляцию пресинаптических терминалей. По этой причине полученные данные были объединены вместе.
3.3.1 L-ap4 подавляет и тормозные, и возбуждающие синаптические токи в интернейронах
Моносинаптические ТПСТ регистрировались при комнатной температуре в ответ на внеклеточную стимуляцию в stratum radiatum в присутствии высоких концентраций антагониста NMDA рецепторов (APV, 50 М) и антагониста AMPA/каинатных рецепторов (NBQX, 10М). Аппликация L-AP4 (агонист метаботропных рецепторов группыIII, 50М) производила обратимое снижение ТПСТ до 4712 % (среднеестандартная ошибка среднего) от контрольных значений (Рис. 3.3.1а; p=0,01; n=5). Неожиданным оказалось то, что эта депрессия была практически идентичной по величине снижению ВПСТ в ответ на аппликацию L-AP4. ВПСТ регистрировались в отдельной группе экспериментов, в которых мы не добавляли NBQX, а заменили его пикротоксином (100М) и бикукуллином (10 µМ), чтобы блокировать ГАМКАрецепторы (Рис. 3.3.1б). В этом случае L-AP4 подавило ВПСТ до 5311 % от контроля (p=0,01, n=5).
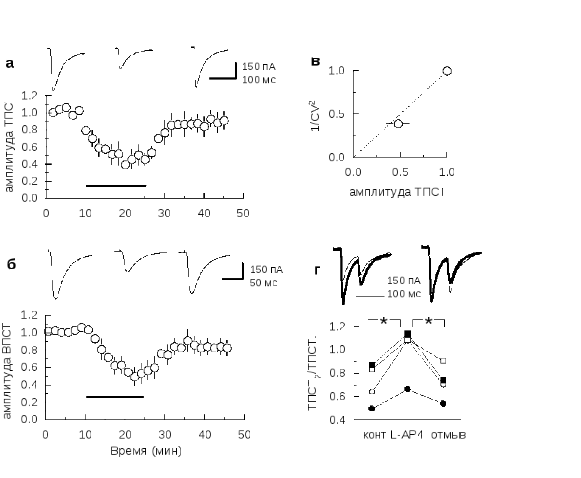
Рис. 3.3.1 L-AP4, агонист метаботропных рецепторов группы III, подавляет моносинаптические ТПСТ и ВПСТ в интернейронах в равной степени
а, Амплитуда ТПСТ (среднее ± С.О.С.), нормированная к средней амплитуде до аппликации L-AP4 (50 μМ) (n=5). Оригинальные записи над графиком получены до, во время и после аппликации L-AP4 с одного нейрона (усреднение по 30 последовательным регистрациям).б, Амплитуда ВПСТ, полученная таким же образом в отдельных сериях экспериментов (n=5).в, Депрессия ТПСТ сопровождалась снижением статистического параметра 1/CV2, что указывает на снижение квантового содержимого (quantal content). Статистический параметр 1/CV2был нормирован к базовым значениям в каждой клетке и усреднен во всех экспериментах. Затем был построен график отношения этого параметра к средней амплитуде ТПСТ, нормированной таким же образом. Диагональная линия показывает траэкторию изменений ожидаемую из распределения Пуассона при снижении квантового параметра высвобожденияm.г, Депрессия, вызываемая L-AP4, сопровождается обратимым изменением коэффициэнта парной депресии, что указывает на пресинаптический сайт действия этого агониста. Оригинальные записи над граффиком получены усреднением 10 последовательных регистраций в одной эксперименте. Жирные линии наложившиеся друг на друга контроль и отмывка, тонкая линия – ТПСТ при аппликации L-AP4. Записи справа теже, что на левой панели, но нормированные к амплитуде первого ТПСТ, чтобы оценить снижение парной депресии. *: p<0,05.
Снижение средней амплитуды ТПСТ сопровождалось снижением статистического параметра 1/CV2(эквивалентного среднее арифметическое2/дисперсия), который изменяется с изменением квантового состава выброса медиатора (Edwards et al. 1989) Было доказано, что его использование позволяет грубо оценить выброс медиатора в гиппокампальных синапсах (Manabe et al. 1993). Полученное изменение 1/CV2в наших экспериментах было пропорционально изменению средней амплитуды (Рис. 3.3.1в). Это свидетельствует в пользу того, что эффект L-AP4 может быть связан с пресинаптическим снижением вероятности выброса нейропередатчика. Для получения дополнительных доказательств пресинаптического эфекта активации метаботропных рецепторов группыIII, мы проверили, какой эффект L-AP4 оказывает на коэффициент парной депрессии ТПСТ. Для этого мы использовали два стимула с интервалом 50 мс. В подтверждение данных, полученных с использованием параметра 1/CV2, коэффициент парной депресии также менялся при аппликацииL-AP4 (Рис. 3.3.1г). Таким образом, мы показали, что ГАМКергические терминали содержат метаботропные рецепторы глутамата, активация которых пресинаптически модулирует выброс ГАМК.
В противоположность значительной депрессии ТПСТ и ВПСТ, регистрируемых в интернейронах, моносинаптические ТПСТ в пирамидных нейронах снижались только до 83 6 % от контроля (Рис. 3.3.2а; p=0,01; n=7). Это снижение было достоверно меньше, чем наблюдаемое в интернейронах (p<0,04; непарный t тест). Кроме того, мы не обнаружили эффекта L-AP4 на полевые ВПСП, записываемые в присутствии пикротоксина и APV вstr.radiatum(Рис. 3.3.2б). Это указывает на то, что и возбуждающая синаптическая передача в пирамидных клетках не чувствительна к активации метаботропных рецепторов группыIII. Эти данные согласуются с результатами предыдущих исследований (Scanziani et al. 1998; Shigemoto et al. 1996),

Рис. 3.3.2 L-AP4 сравнительно неэффективно в снижении ВПСТ и ТПСТ в пирамидных нейронах
а, Нормированная к базовым значениям амплитуда ТПСТ, зарегистрированых в пирамидных нейронах поля СА1, (n=7). Аппликация L-AP4 (50 μМ) приводила к небольшой, но статистически значимой их депрессии. Оргигинальные записи получены до, во время и после аппликации L-AP4 с одного нейрона.б, Наклон полевых ВПСП, полученных в str.radiatum поля СА1 (n=7). Аппликация L-AP4 не приводила к статистически значимому эффекту. Оригинальные записи полученны в одном эксперименте.
