
- •Научные консультанты:
- •Сокращения и глоссарий
- •Введение
- •Обзор литературы
- •1.1 Торможение в гиппокампе
- •1.1.1 ГамКергическая синаптическая передача
- •1.1.2 ГамКергические рецепторы
- •1.1.3 Разнообразие форм торможения
- •1.1.4 Механизмы и функциональное значение тонического торможения
- •1.2 Взаимодействие между глутамат и гамКергической системами
- •1.2.1 Гетеросинаптические взаимодействия
- •1.2.2 Критерии гетеросинаптической депрессии
- •1.2.3 Метаботропные рецепторы группы III в гиппокампе
- •1.2.4 Каинатные рецепторы в гиппокампе
- •1.3 Механизмы фокального эпилептогенеза
- •1.3.1 Исследования эпилептогенеза
- •1.3.2 Критерии развития эпилептиформной активности
- •1.3.3 Возбуждающие механизмы в эпилептогенезе
- •1.3.4 Тормозные механизмы в эпилептогенезе
- •1.4 Постановка цели и задач исследования
- •2. Материалы и методы
- •2.1 Срезы гиппокампа
- •2.1.1 Приготовление и растворы
- •2.1.2 Рабочая установка для поддержания срезов и манипуляторы
- •2.1.3 Идентификация клеток с помощью световой микроскопии
- •2.2 Регистрация и анализ полевых потенциалов
- •2.3 Записи и анализ токов (потенциалов) в режиме фиксации потенциала (тока) с одиночных нейронов
- •2.3.1 Электроды и внутриклеточные растворы
- •2.3.2 Проведение регистраций и сохранение данных
- •2.3.2 Анализ спонтанных и вызванных ответов в режиме фиксации потенциала
- •2.4 Записи и анализ ответов на ионтофоретические аппликации
- •2.5 Записи и анализ токов с outside-out patch
- •2.5.1 Приготовление outside-out patch
- •2.5.2 Система быстрой аппликации веществ
- •2.5.3 Определение биофизических свойств рецепторов с использованием анализа токов, полученных с outside-out пейчей
- •2.6 Модели эпилептогенеза in vivo
- •2.6.1 Электрический киндлинг
- •2.6.2 Модель аудиогенной судорожной активности. Аудиогенный киндлинг
- •2.7 Использованные вещества
- •2.8 Статистический анализ
- •3 Результаты исследованИй и их обсуждение
- •3.1 Нетипичные фармакологические свойства гамКергических рецепторов в гиппокампальных интернейронах
- •3.1.1 Различная чувствительность ионотропных гамКергических рецепторов к пикротоксину в интернейронах и пирамидных клетках
- •3.1.2 Ионные каналы ионотропных гамКергических рецепторов в интернейронах и пирамидных клетках имеют различную проводимость
- •3.1.3 Ионотропные гамКергические рецепторы как в интернейронах, так и пирамидных клетках чувствительны к агонисту гамкс рецепторов
- •3.1.4 Пентобарбитал по-разному модулирует гамКергические токи, вызываемые аппликацией caca (50 м)
- •3.1.5 Тпст в интернейронах, регистрируемые в присутствии 100 м пикротоксина, обладают повышенной чувствительностью к антагонисту гамкс рецепторов
- •3.1.6 Токи, опосредованные гамКергическими рецепторами, в присутствии 100 м пикротоксина возникают за счет характерной Cl-/hco3- ионой проводимости
- •3.1.7 Эффект аллостерических модуляторов гамка рецепторов на устойчивые к пикротоксину токи, опосредованные гамКергическими рецепторами
- •3.1.8 Сравнение эффективности антагонистов гамка и гамкс рецепторов на устойчивые к пикротоксину токи, опосредованные гамКергическими рецепторами
- •3.1.9 Интернейроны содержат рецепторы, обладающие нетипичными фармакологическими свойствами
- •3.1.10 Нетипичные гамКергические рецепторы и традиционные типы рецепторов (гамка и гамкс)
- •3.1.11 Возможная субъединичная композиция нетипичных гамКергических рецепторов в интернейронах
- •Заключение
- •3.2 Регуляция возбудимости нейронов гиппокампа за счет гамКергического тонического торможения
- •3.2.1 Базовый тонический гамКергический ток специфичен для интернейронов, но не пирамидных клеток
- •3.2.2 Увеличение внеклеточной концентрации гамк ведет к возникновению тонического тока в пирамидных клетках и повышению в интернейронах
- •3.2.3 Температурная зависимость тонического гамКергического тока и фазических спонтанных тпст
- •3.2.4 Возможная роль тонического торможения в эпилептогенезе
- •3.2.5 Заключение
- •3.3 Модуляция гамКергической передачи в гиппокампе метаботропными рецепторами
- •3.3.1 L-ap4 подавляет и тормозные, и возбуждающие синаптические токи в интернейронах
- •Демонстрирующих отсутствие метаботропных рецепторов группы III на терминалях коллатералей Шаффера, оканчивающихся на пирамидных клетках са1.
- •3.3.2 Синаптически высвобождаемый глутамат снижает тпст
- •3.3.3 Глутамат опосредует гетеросинаптическую депрессию тпст
- •3.3.4 Изменения в эффективности обратного захвата глутамата влияет на гетеросинаптическую депрессию
- •3.3.5 Метаботропные рецепторы группы III опосредуют гетеросинаптическую депрессию по двум различным механизмам
- •3.3.6 Метаботропные рецепторы группы III модулируют частоту спонтанных тпст
- •3.3.7 Возможные молекулярные механизмы депрессии тпст при активации mGluR группы III
- •3.3.8 Последствия активации mGluR группы III для общей возбудимости нейрональной сети поля са1
- •3.3.9 Гетеросинаптическая депрессия, опосредованная метаботропными гамкb рецепторами
- •3.3.10 Заключение
- •3.4 Каинатные рецепторы модулируют гамКергическое торможение в гиппокампальных интернейронах
- •3.4.1 Каинат увеличивает частоту и амплитуду спонтанных тпст в интернейронах
- •3.4.2 Каинат увеличивает вероятность генерации антидромных потенциалов действия в интернейронах
- •3.4.3 Каинат вызывает спонтанные аксональные потенциалы действия
- •3.4.4 Спилловер глутамата активирует аксональные каинатные рецепторы
- •3.4.5 Последствия аксональной деполяризации, вызываемой каинатными рецепторами, для гамКергической передачи
- •3.4.6 Каинат усиливает вызванные тпст в интернейронах
- •3.4.7 Каинат приводит к увеличению гамКергического тонического тока
- •3.4.8 Последствия усиления гамКергической передачи в интернейронах, вызываемой каинатными рецепторами, для возбудимости нейрональной сети
- •3.4.9 Заключение
- •3.5 Оказывают ли метаботропные рецепторы группы III и каинатные рецепторы противоположное действие на гамКергическую передачу?
- •3.6 Механизмы развития пачечной активности в гиппокампе
- •3.6.1 Кратковременные увеличения внеклеточной концентрации калия создают долговременное снижение порога развития пачечных разрядов в поле са1 гиппокампа
- •3.6.2 Развитие пачечных разрядов в поле са1 гиппокампа не зависит от активности нейронов поля са3
- •3.6.3 Окклюзия развития пачечных разрядов в поле са1 в ответ на кратковременные увеличения внеклеточной концентрации калия в моделях эпилептогенеза in vivo
- •3.6.4 Является ли пачечная активность в поле са1 гиппокампа эпилептиформной?
- •3.6.5 Способность пирамидных нейронов поля са1 генерировать пачечные разряды сопровождается повышением возбудимости этих клеток
- •3.6.6 Роль nmda рецепторов и l-типа кальциевых каналов в повышение возбудимости пирамидных клеток и генерации пачечных разрядов
- •3.6.7 Заключение
- •Заключение
- •Клеткоспецифичность гамКергического торможения в гиппокампе
- •Клеткоспецифичность модуляции гамКергического торможения в гиппокампе
- •Возбудимость и торможение в эпилептогенезе
- •Эффектов веществ влияющих на гамКергические механизмы, описанные в данной диссертационной работе, представлена втаблице 4.1 (см также Рис. 4.1). Выводы
- •Список рисунков
- •Список литературы
2.8 Статистический анализ
Экспериментальные данные каждой серии (n≥4) были усреднены и представлены в виде средняя ± стандартная ошибка средней. Достоверность различий данных оценивалась с использованием парного или непарного t‑теста и однофакторного дисперсионного анализа (ANOVA). Различия считались достоверными при P<0,05. Аппроксимирующие кривые на графиках рассчитывались по методу наименьших квадратов.
3 Результаты исследованИй и их обсуждение
3.1 Нетипичные фармакологические свойства гамКергических рецепторов в гиппокампальных интернейронах
3.1.1 Различная чувствительность ионотропных гамКергических рецепторов к пикротоксину в интернейронах и пирамидных клетках
Добавление неконкурентного антагониста ионотропных ГАМКергических рецепторов, пикротоксина (PTX), приводило к подавлению ТПСТ как в интернейронах str.radiatum, так и в пирамидных нейронах поля СА1 срезов гиппокампа (Рис.3.1.1 а,б). Однако, чувствительность ТПСТ, регистрируемых в двух популяциях клеток, к этому веществу значительно отличалась. Так использование 100 μМ пикротоксина (концентрация традиционно используемая для подавления ГАМКАрецептор опосредованных ТПСТ) практически полностью подавляло ТПСТ в пирамидных клетках, тогда как в интернейронах все еще регистрировался значительный ток (16 ± 5 % от базовых значений ТПСТ; p<0,01; n=7). Интересно, что аппроксимация по уравнению Хилла кривых концентрация PTX -ингибирование ТПСТ приводила к получению одинакового коэффициента Хилла для обоих типов клеток (0,9), но разному IC50(9 μМ для пирамидных клеток и 26 μМ для интернейронов; Рис.3.1.1в).
Пикротоксин представляет собой рацемическую смесь пикротина и более активного пикротоксинина, который, как предполагается, блокирует ионный канал ГАМКергических рецепторов (Gurley et al. 1995; Newland and Cull-Candy 1992). Хотя известно, что эффект пикротоксина может зависеть от активности рецепторов, нам не удалось обнаружить, что остаточный ТПСТ в интернейронах снижался со временем в присутствии 100 μМ пикротоксина. Таким образом, различная чувствительность ТПСТ
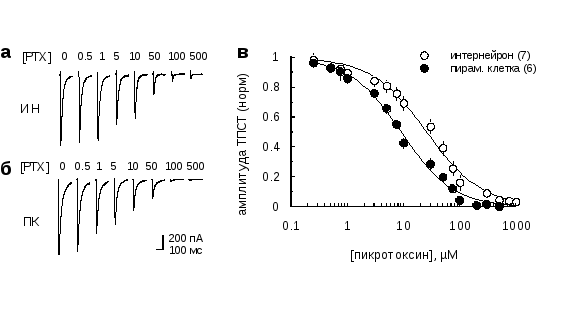
Рис. 3.1.1 ТПСТ в интернейронах менее чувствительны к пикротоксину, чем в пирамидных клетках
а, Оригинальные записи, полученные
с одного интернейрона в присутствии
D-APV (50 μM), NBQX (20 μM), CGP52432 (5M),
каждая усреднена по 10 последовательным
ТПСТ. Пикротоксин подавлял ТПСТ
концентрационно-зависимым образом.
Однако, при концентрации пикротоксина
100 µМ все еще наблюдался значительный
ток. б, оригинальные записи полученные
с одной пирамидной клетки, каждая
усреднена по 10 последовательным ТПСТ.
Пикротоксин, как и в интернейронах,
подавлял ТПСТ в пирамидных клетках
концентрационно-зависимым образом.
Причем, аппликация 100 µМ пикротоксина
полностью подавляла ТПСТ.в,
Зависимости характеризующие доза-эффект
пикротоксина на амплитуду ТПСТ в
интернейронах ( ;
n=7) и пирамидных нейронах (
;
n=7) и пирамидных нейронах ( ;
n=6), построенные в полулогарифмических
координатах. ТПСТ нормированы к амплитуде
базового ТПСТ (в отсутствии пикротоксина).
Линии аппроксимации показывают
теоретические кривые, полученные по
уравнению Хилла. Коэффициент Хила был
одинаковым для обоих типов клеток (0,9),
тогда как IC50была 9 µМ для
интернейронов и 26 µМ для пирамидных
клеток. Разбросы указывают величину
±С.О.С.
;
n=6), построенные в полулогарифмических
координатах. ТПСТ нормированы к амплитуде
базового ТПСТ (в отсутствии пикротоксина).
Линии аппроксимации показывают
теоретические кривые, полученные по
уравнению Хилла. Коэффициент Хила был
одинаковым для обоих типов клеток (0,9),
тогда как IC50была 9 µМ для
интернейронов и 26 µМ для пирамидных
клеток. Разбросы указывают величину
±С.О.С.

в интернейронах и пирамидных нейронах к этому веществу не отражает различную занятость рецепторов эндогенным агонистом (Hajos et al. 2000). С другой стороны, этот результат может быть объяснен какими-то различиями в постсинаптических рецепторах. Таких различий может быть предложено несколько. Во-первых, если ГАМКергические рецепторы гомогенны в обоих типах клеток, то они могут состоять из различных субъединиц (Sperk et al. 1997; Thomson et al. 2000). Во вторых, рецепторы могут быть гетерогенны и, в этом случае, разница в чувствительности ТПСТ в этих типах клеток может объясняться разной пропорцией ГАМКергических рецепторов, слабо чувствительных к пикротоксину. И в третьих, при наличии одинаковых рецепторов в интернейронах и пирамидных клетках их активация может регулироваться разными внутриклеточными механизмами. Для ответа на этот вопрос мы провели разностороннее исследование биофизических и фармакологических свойств ГАМКергических рецепторов в интернейронах и пирамидных клетках.
