
- •Научные консультанты:
- •Сокращения и глоссарий
- •Введение
- •Обзор литературы
- •1.1 Торможение в гиппокампе
- •1.1.1 ГамКергическая синаптическая передача
- •1.1.2 ГамКергические рецепторы
- •1.1.3 Разнообразие форм торможения
- •1.1.4 Механизмы и функциональное значение тонического торможения
- •1.2 Взаимодействие между глутамат и гамКергической системами
- •1.2.1 Гетеросинаптические взаимодействия
- •1.2.2 Критерии гетеросинаптической депрессии
- •1.2.3 Метаботропные рецепторы группы III в гиппокампе
- •1.2.4 Каинатные рецепторы в гиппокампе
- •1.3 Механизмы фокального эпилептогенеза
- •1.3.1 Исследования эпилептогенеза
- •1.3.2 Критерии развития эпилептиформной активности
- •1.3.3 Возбуждающие механизмы в эпилептогенезе
- •1.3.4 Тормозные механизмы в эпилептогенезе
- •1.4 Постановка цели и задач исследования
- •2. Материалы и методы
- •2.1 Срезы гиппокампа
- •2.1.1 Приготовление и растворы
- •2.1.2 Рабочая установка для поддержания срезов и манипуляторы
- •2.1.3 Идентификация клеток с помощью световой микроскопии
- •2.2 Регистрация и анализ полевых потенциалов
- •2.3 Записи и анализ токов (потенциалов) в режиме фиксации потенциала (тока) с одиночных нейронов
- •2.3.1 Электроды и внутриклеточные растворы
- •2.3.2 Проведение регистраций и сохранение данных
- •2.3.2 Анализ спонтанных и вызванных ответов в режиме фиксации потенциала
- •2.4 Записи и анализ ответов на ионтофоретические аппликации
- •2.5 Записи и анализ токов с outside-out patch
- •2.5.1 Приготовление outside-out patch
- •2.5.2 Система быстрой аппликации веществ
- •2.5.3 Определение биофизических свойств рецепторов с использованием анализа токов, полученных с outside-out пейчей
- •2.6 Модели эпилептогенеза in vivo
- •2.6.1 Электрический киндлинг
- •2.6.2 Модель аудиогенной судорожной активности. Аудиогенный киндлинг
- •2.7 Использованные вещества
- •2.8 Статистический анализ
- •3 Результаты исследованИй и их обсуждение
- •3.1 Нетипичные фармакологические свойства гамКергических рецепторов в гиппокампальных интернейронах
- •3.1.1 Различная чувствительность ионотропных гамКергических рецепторов к пикротоксину в интернейронах и пирамидных клетках
- •3.1.2 Ионные каналы ионотропных гамКергических рецепторов в интернейронах и пирамидных клетках имеют различную проводимость
- •3.1.3 Ионотропные гамКергические рецепторы как в интернейронах, так и пирамидных клетках чувствительны к агонисту гамкс рецепторов
- •3.1.4 Пентобарбитал по-разному модулирует гамКергические токи, вызываемые аппликацией caca (50 м)
- •3.1.5 Тпст в интернейронах, регистрируемые в присутствии 100 м пикротоксина, обладают повышенной чувствительностью к антагонисту гамкс рецепторов
- •3.1.6 Токи, опосредованные гамКергическими рецепторами, в присутствии 100 м пикротоксина возникают за счет характерной Cl-/hco3- ионой проводимости
- •3.1.7 Эффект аллостерических модуляторов гамка рецепторов на устойчивые к пикротоксину токи, опосредованные гамКергическими рецепторами
- •3.1.8 Сравнение эффективности антагонистов гамка и гамкс рецепторов на устойчивые к пикротоксину токи, опосредованные гамКергическими рецепторами
- •3.1.9 Интернейроны содержат рецепторы, обладающие нетипичными фармакологическими свойствами
- •3.1.10 Нетипичные гамКергические рецепторы и традиционные типы рецепторов (гамка и гамкс)
- •3.1.11 Возможная субъединичная композиция нетипичных гамКергических рецепторов в интернейронах
- •Заключение
- •3.2 Регуляция возбудимости нейронов гиппокампа за счет гамКергического тонического торможения
- •3.2.1 Базовый тонический гамКергический ток специфичен для интернейронов, но не пирамидных клеток
- •3.2.2 Увеличение внеклеточной концентрации гамк ведет к возникновению тонического тока в пирамидных клетках и повышению в интернейронах
- •3.2.3 Температурная зависимость тонического гамКергического тока и фазических спонтанных тпст
- •3.2.4 Возможная роль тонического торможения в эпилептогенезе
- •3.2.5 Заключение
- •3.3 Модуляция гамКергической передачи в гиппокампе метаботропными рецепторами
- •3.3.1 L-ap4 подавляет и тормозные, и возбуждающие синаптические токи в интернейронах
- •Демонстрирующих отсутствие метаботропных рецепторов группы III на терминалях коллатералей Шаффера, оканчивающихся на пирамидных клетках са1.
- •3.3.2 Синаптически высвобождаемый глутамат снижает тпст
- •3.3.3 Глутамат опосредует гетеросинаптическую депрессию тпст
- •3.3.4 Изменения в эффективности обратного захвата глутамата влияет на гетеросинаптическую депрессию
- •3.3.5 Метаботропные рецепторы группы III опосредуют гетеросинаптическую депрессию по двум различным механизмам
- •3.3.6 Метаботропные рецепторы группы III модулируют частоту спонтанных тпст
- •3.3.7 Возможные молекулярные механизмы депрессии тпст при активации mGluR группы III
- •3.3.8 Последствия активации mGluR группы III для общей возбудимости нейрональной сети поля са1
- •3.3.9 Гетеросинаптическая депрессия, опосредованная метаботропными гамкb рецепторами
- •3.3.10 Заключение
- •3.4 Каинатные рецепторы модулируют гамКергическое торможение в гиппокампальных интернейронах
- •3.4.1 Каинат увеличивает частоту и амплитуду спонтанных тпст в интернейронах
- •3.4.2 Каинат увеличивает вероятность генерации антидромных потенциалов действия в интернейронах
- •3.4.3 Каинат вызывает спонтанные аксональные потенциалы действия
- •3.4.4 Спилловер глутамата активирует аксональные каинатные рецепторы
- •3.4.5 Последствия аксональной деполяризации, вызываемой каинатными рецепторами, для гамКергической передачи
- •3.4.6 Каинат усиливает вызванные тпст в интернейронах
- •3.4.7 Каинат приводит к увеличению гамКергического тонического тока
- •3.4.8 Последствия усиления гамКергической передачи в интернейронах, вызываемой каинатными рецепторами, для возбудимости нейрональной сети
- •3.4.9 Заключение
- •3.5 Оказывают ли метаботропные рецепторы группы III и каинатные рецепторы противоположное действие на гамКергическую передачу?
- •3.6 Механизмы развития пачечной активности в гиппокампе
- •3.6.1 Кратковременные увеличения внеклеточной концентрации калия создают долговременное снижение порога развития пачечных разрядов в поле са1 гиппокампа
- •3.6.2 Развитие пачечных разрядов в поле са1 гиппокампа не зависит от активности нейронов поля са3
- •3.6.3 Окклюзия развития пачечных разрядов в поле са1 в ответ на кратковременные увеличения внеклеточной концентрации калия в моделях эпилептогенеза in vivo
- •3.6.4 Является ли пачечная активность в поле са1 гиппокампа эпилептиформной?
- •3.6.5 Способность пирамидных нейронов поля са1 генерировать пачечные разряды сопровождается повышением возбудимости этих клеток
- •3.6.6 Роль nmda рецепторов и l-типа кальциевых каналов в повышение возбудимости пирамидных клеток и генерации пачечных разрядов
- •3.6.7 Заключение
- •Заключение
- •Клеткоспецифичность гамКергического торможения в гиппокампе
- •Клеткоспецифичность модуляции гамКергического торможения в гиппокампе
- •Возбудимость и торможение в эпилептогенезе
- •Эффектов веществ влияющих на гамКергические механизмы, описанные в данной диссертационной работе, представлена втаблице 4.1 (см также Рис. 4.1). Выводы
- •Список рисунков
- •Список литературы
2.5.3 Определение биофизических свойств рецепторов с использованием анализа токов, полученных с outside-out пейчей
Нестационарный дисперсионный анализ токов с outside-outпейчей в ответ на быструю аппликацию ГАМК производился, как было описано ранее (Jonas et al. 1993; Perrais and Ropert 1999; Sigworth 1980). Регистрировались как минимум 30 последовательных ответов со стабильной амплитудой (Рис. 2.7). Затем рассчитывался средний ток и дисперсия для каждой точки. Связь между этими параметрами основана на следующих соотношениях:
I(t)=NP(t)i, (1)
где I(t) – средний ток в данный момент времени,N– число каналов открытое при пиковой амплитуде тока,P(t) – вероятность открытого состояния канала в данный момент времени,i– средний ток одиночного канала
σ2ток- σ2шум=NP(t)(1-P(t))i2, (2)
значения параметров те же что и в (1), σ2ток- дисперсия тока, вызванного аппликацией ГАМК, в данной временной точке, σ2шум– дисперсия базового тока до
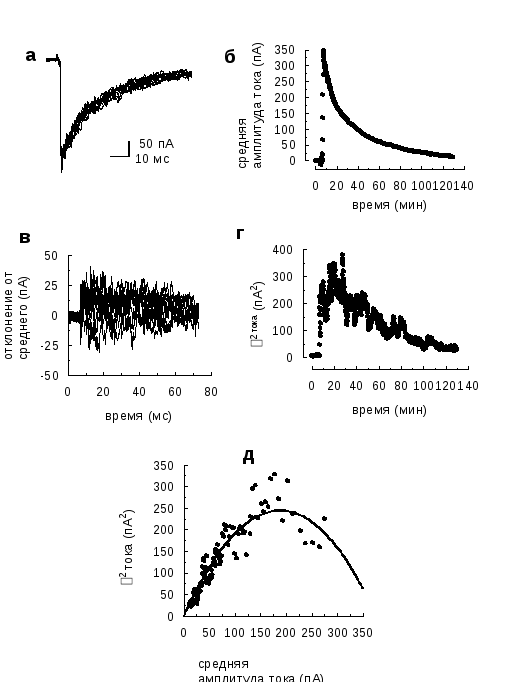
Рис. 2.7 Использование метода нестационарного дисперсионного анализа для определения биофизических параметров ГАМКергических рецепторов
а, Для анализа использовались данные с пейчей, в которых амплитуда ответов на быструю аппликацию была сравнительно стабильной (не наблюдалось тенденции к ее увеличению или уменьшению с течением времени). Ответы оцифровывались с частотой 10 кГц. Полученные токи усреднялись (б) и затем путем вычитания среднего определялась динамика отклонений индивидуальных ответов от среднего (в) После этого рассчитывалась дисперсия для каждой точки ответа, из которой вычиталась дисперсия шума (тока до аппликации агониста;г). Получив эти данные, мы строили зависимость дисперсии от средней амплитуды тока для каждой временной точки (д). Эта зависимость аппроксимировалась по методу наименьших квадратов с использованием уравнения σ2ток- σ2шум= iI-I2/NP, где σ2ток– дисперсия ГАМКергического тока, σ2шум– дисперсия базового тока перед стимуляцией I – средняя амплитуда тока. При этом мы получали параметры: i – средний ток одиночного канала и NPчисло каналов в пейче.
аппликации (вариабельность этого тока связана со спонтанным открыванием-закрыванием каналов).
Из (1) и (2) получается соотношение σ2ток- σ2шум=iI-I2/N, которое связывает амплитуду тока амплитуду тока с дисперсией. Таким образом, зависимость дисперсии от тока аппроксимировалась параболической кривой, полученной по данному уравнению. Из этой аппроксимации мы получали параметрыiиN. После чего рассчитывалась максимальная вероятность открытого состояния канала (Pотк) по уравнению:Pотк=1-(σ2пик- σ2шум)/iIпик, гдеIпики σ2пик– максимальная амплитуда тока и дисперсия в этой точке, соответственно.
2.6 Модели эпилептогенеза in vivo
2.6.1 Электрический киндлинг
Операционная техника
Опыты проводились на 9 крысах-самцах Вистар массой 270-350 граммов. В ходе предварительной операции 5 животным под нембуталовым наркозом (50 мг/кг, в/б) стереотаксически вживлялись 2 электрода в левый гиппокамп: рострально (монополярный электрод; AP=-1,8; ML= 1,5; DV=3,2) и каудально (парный электрод; AP=-3,6; ML=-3; DV=4). Для электрической стимуляции гиппокампа использовался ростральный электрод и один из электродов каудальной пары. Для регистрации послеразрядов (ПР) пирамидных нейронов использовался другой электрод каудальной пары. Индифферентный электрод (для регистрации) находился в назальных частях черепа.
Стимуляция
Внутримозговая электрическая стимуляция животных начиналась через неделю после операции. Был использован протокол (rapid alternate kindling), предложенный ранее Лотманом и Вильямсоном (Lothman and Williamson 1994). Электрической стимуляции подвергались 5 животных. Другие 4 служили в качестве контроля. Частота стимуляции была 50 Гц, длительность 10 секунд. Для стимуляции использовались прямоугольные импульсы тока длительностью 0,2 мсек. и интенсивностью, вызывающей электрические послеразряды (группу популяционных спайков длительностью не менее 10 секунд после окончания стимуляции). Обычно интенсивность тока варьировала в пределах 250-400 μА. В день давалось 12 таких стимулов с интервалом 30 минут. Эти стимулы давались через 1 сутки в течение 8 суток (всего 48 стимулов).
Критерием выработки определенной стадии киндлинга являлась длительность послеразрядов и поведенческие проявления, оцениваемые по шкале Рэйсина (Racine 1972):
1 стадия – "отряхивание мокрой собаки", жевание, подергивание лицевых мышц;
2 стадия – качание головой, судорожные подергивания мышц туловища;
3 стадия – клонус передних конечностей;
4 стадия - клонус передних конечностей и поднимание на задние лапы;
5 стадия - клонус передних конечностей, поднимание на задние лапы и потеря равновесия.
Срезы гиппокампа между ростральным и каудальным электродами выделялись через 24 часа после того, как животные достигали 4-5 стадий киндлинга (соответствующие электрографические и поведенческие реакции на 3 последовательных стимуляции).
