
- •Глава 18 патофизиология почек
- •18.1. Характеристика процессов, лежащих в основе работы почек
- •Часть III. Патофизиология органов и систем
- •18.2. Показатели экскреторной функции почек в норме
- •18.3. Неэкскреторные функциипочек
- •18.4. Определение размеровпочечного кровотока
- •Часть III. Патофизиология органов и систем
- •18.5. Нарушение клубочковой фильтрации
- •18.6. Нарушение функции канальцев
- •Часть III. Патофизиология органов и систем
- •18.7. Роль почек в регуляции обмена электролитов и его нарушениях
- •18.8. Роль почек в обмене воды и его нарушениях
- •Часть III. Патофизиология органов и систем
- •18.9. Роль почек в поддержании кислотно-основного равновесия и его нарушениях
- •Часть III. Патофизиология органов и систем
- •18.10. Ренальные и экстраренальные нарушения при заболеваниях почек
- •18.10.1. Ренальные нарушения
- •Часть III. Патофизиология органов и систем
- •Глава 18 / патофизиология почек
- •Часть III. Патофизиология органов и систем
- •Часть III. Патофизиология органов и систем
- •Глава 18 / патофизиология почек
- •Часть III. Патофизиология органов и систем
- •Глава 18 / патофизиология почек
- •Часть III. Патофизиология органов и систем
- •Часть III. Патофизиология органов и систем
- •18.13. Гломерулонефриты
- •Часть III. Патофизиология органов и систем
- •18.14. Пиелонефрит
- •18.15. Почечнокаменная болезнь (нефролитиаз)
- •Часть III. Патофизиология органов и систем
- •Глава 18 / патофизиология почек
- •Глава 19 патофизиология эндокринной системы
- •Часть III. Патофизиология органов и систем
- •Часть III. Патофизиология органов и систем
- •Часть III. Патофизиология органов и систем
- •Часть III. Патофизиология органов и систем
- •Глава 19 / патофизиология эндокринной системы
- •Часть III. Патофизиология органов и систем
- •Часть III. Патофизиология органов и систем
- •Часть III. Патофизиология органов и систем
- •Часть III. Патофизиология органов и систем
- •Часть III. Патофизиология органов и систем
- •Часть III. Патофизиология органов и систем
- •Глава 20 патофизиология нервной системы
- •Часть III. Патофизиология органов и систем
- •20.1.6. Инкубационный период
- •Часть III. Патофизиология органов и систем
- •20.2. Типовые патологические процессы в нервной системе
- •20.2.1. Дефицит торможения. Растормаживание
- •20.2.2. Экспериментальные и клинические проявления растормаживания
- •Часть III. Патофизиология органов и систем
- •Часть III. Патофизиология органов и систем
- •Часть III. Патофизиология органов и систем
- •Глава 20 / патофизиология нервной системы
- •Часть III. Патофизиология органов и систем
- •Часть III. Патофизиология органов и систем
- •20.4. Генераторы патологически усиленного возбуждения (гпув)
- •20.4.1. Понятие и общая характеристика
- •Часть III. Патофизиология органов и систем
- •Часть III. Патофизиология органов и систем
- •Глава 20 / патофизиология нервной системы
- •Часть III. Патофизиология органов и систем
- •Часть III. Патофизиология органов и систем
- •20.9.7. Принципы лечения патологической боли
- •Глава 20 / патофизиология нервной системы
- •Глава 21 патофизиология высшей нервной деятельности
- •1904 Г.
- •Часть III. Патофизиология органов и систем
- •21.1. Причины возникновения функциональной патологии
- •21.2. Проявления функциональной патологии внд
- •21.3. Механизмы возникновения патологии внд
- •Часть III. Патофизиология органов и систем
- •21.4. Типы внд
- •21.5. Информационная патология внд
- •Часть III. Патофизиология органов и систем
- •21.6. Саморегуляция поведения
- •Часть III. Патофизиология органов и систем
- •21.7. Посттравматическая патология внд
- •Часть III. Патофизиология органов и систем
- •Часть III. Патофизиология органов и систем
- •Часть III. Патофизиология органов и систем
- •Часть I. Общая нозология (Адо а.Д., Новицкий в.В.)Глава I. Общее учение о болезни 25
- •Глава 2. Болезнетворные факторы внешней среды (Адо а.Д., Новицкий в.В.) 42
- •Глава 3. Местные и общие реакции организма на повреждение 66
- •Глава 4. Роль наследственности, конституции и возраста в патологии 102
- •Глава 5. Реактивность и резистентность организма, их роль в патологии
- •Глава 6. Роль иммунной системы в патологии (Климов в.В.) 150
- •Глава 7. Аллергия (Порядин г.В.) 164
- •Глава 9. Воспаление (Клименко н.А.) 207
- •Глава 10. Лихорадка (Лаврова b.C.) 235
- •Глава 11. Патофизиология типовых нарушений обмена веществ 245
- •Глава 12. Патофизиология тканевого роста (Адо а.Д.) 358
- •Часть III. Патофизиология органов и систем
- •Глава 13. Патофизиология системы крови (Гольдберг е.Д., Новицкий в.В.) 404
- •Глава 14. Патофизиология сердечно-сосудистой системы (Лишманов ю.Б., Маслов л.Н.,Пирогова н.П.) 451
- •Глава 15. Патофизиология дыхания 503
- •Глава 16. Патофизиология пищеварения (Белобородова э.И.) 538
- •Глава 18. Патофизиология почек (Лаврова b.C.) 598
- •Глава 19. Патофизиология эндокринной системы 624
- •Глава 20. Патофизиология нервной системы (Крыжановский г.Н.) 654
- •Глава 21. Патофизиология высшей нервной деятельности (Хананашвили м.М.) 688
Часть III. Патофизиология органов и систем
Такая
возможность хорошо известна при лечении
экзогенными гормональными препаратами.
Установлено образование антител к
инсулину, СТГ, АКТГ у большинства
лечившихся людей, что в ряде случаев
сопровождается снижением лечебного
эффекта препарата. Возможно образование
аутоантител и к гормонам, образующимся
в самом организме;
б) изменения в активном центре или конфор-мации молекулы гормона в связи с мутацией изамещением в молекуле гормона одной аминокислоты на другую. Такие замещения обнаружены в активном центре инсулина. Можнопредположить такую возможность в отношениидругих гормонов, и в частности СТГ. Последнеепредположение вытекает из клинических наблюдений. Так, есть группа больных карликовостьос очень высокой концентрацией СТГ в плазмекрови, однако эффекта этот гормон на рост организма не оказывает. Гормон определяется им-мунологически, что свидетельствует о сохранности его антигенных свойств. Больные отвечаютувеличением роста на введение экзогенного СТГ,что указывает на наличие нормально функционирующих рецепторов к данному гормону. Сопоставление этих двух фактов дает основаниесделать заключение о недостаточной активности эндогенного СТГ;
в) нарушение превращения прогормона в гормон. Установлено, что белковые гормоны секре-тируются вначале как прогормоны в составе более крупных полипептидных цепей, которыезатем расщепляются. Так, например, плацентасекретирует АКТГ, липотропин и Р-эндорфин какобщую молекулу. В некоторых случаях у больных сахарным диабетом обнаружен инсулин, укоторого С-терминальный конец р-цепи связанс С-пептидом. В обычных условиях С-пептидсоединяет а- и Р-цепи инсулина и вся молекуланазывается проинсулином. Это одноцепочныйбелок с м. м. 10 000 Д, физиологически неактивный. В островках Лангерганса или даже напериферии от проинсулина в результате протео-лиза отщепляется С-пептид, и проинсулин превращается в активный инсулин. Нарушение отщепления С-пептида, очевидно, не дает инсулину возможности принять такую конформацию,в которой он наиболее активен.
Блокада гормонального рецептора
Очевидно, это довольно распространенный
механизм, приводящий к картине гормональной недостаточности. Сюда относятся все случаи, когда активный гормон не находит своего рецептора на клетке или в ней в связи с потерей рецептора, или в связи с фиксацией на его поверхности антагонистов, конформационными изменениями и другими факторами, препятствующими соединению с гормоном. Обычно концентрация гормона в таких случаях нормальна либо увеличена. Введение таким больным с лечебной целью гормонов не сопровождается соответствующим эффектом. Для получения некоторого эффекта нужно вводить большие дозы препарата. Описаны случаи вазопрессинрезистентных форм несахарного диабета, сопровождающиеся значительным увеличением содержания антидиуретического гормона в крови и отсутствием эффекта на его введение извне. В ряде случаев карликового роста концентрация СТГ в крови нормальна и больные не отвечают на экзогенный СТГ. Введение СТГ не стимулируют (как в норме) образование соматомедина, через который СТГ оказывает свое влияние на рост. При псев-догипопаратиреозе развивается синдром, сходный с гипопаратиреозом, сопровождащийся ги-покальциемией, гиперфосфатемией и даже развитием тетании. Такие больные не реагируют на введение экзогенного паратгормона. Аналогичные изменения выявлены и в отношении глю-кокортикоидных рецепторов. Обнаружена изо-форма ГР, которая не связывала гормон, поэтому не было влияния на экспрессию генов. В других случаях определялся укороченный в карбоксильном конце ГР, который также оказался функционально неполноценным. В Т-лимфоцитах стероид-резистентных больных бронхиальной астмой выявлялось обратимое цитокин-опосре-дованное снижение аффинности ГР к гормону, которое ассоциировалось с изменением функции этих клеток.
Нарушение пермиссивного действия глюкокортикоидов
Как указывалось выше, эффекты ряда гормонов «дистантного» действия, и в частности ка-техоламинов, реализуются на фоне физиологических концентраций кортизола. Эту роль кор-тизола называют пермиссивной. Поэтому снижение концентрации кортизола ведет к уменьшению, а иногда и к извращению эффекта кате-холаминов. Так, например, адреналин вызывает
633
гликогенолиз в печени и липолиз в жировой ткани в присутствии кортизола. Поэтому у ад-реналэктомированных животных значительно снижены оба эти эффекта адреналина. Вызываемый адреналином гликогенолиз является сложным и многозвеньевым процессом. Он начинается с соединения адреналина с р-адренергичес-ким рецептором на клеточной мембране. Это вызывает активацию аденилатциклазы и приводит к усилению образования циклического аде-нозинмонофосфата, который, в свою очередь, через ряд реакций приводит к активации фос-форилазы и гликогенолизу.
Механизм пермиссивного действия кортизола может реализоваться на разных уровнях в зависимости от характера стимулируемой обменной реакции и вида клеток. Он не влияет на связывание адреналина с его рецепторами на лейкоцитах, в том числе и на лимфоцитах, так как не обнаружено различий в их связывающей способности у больных бронхиальной астмой по сравнению со здоровыми. Однако число Р-адреноре-цепторов на клетках тканей дыхательных путей и лейкоцитах этих больных оказывалось сниженным. Лечение глюкокортикоидами увеличивало экспрессию этих рецепторов. В определенных случаях кортизол в физиологических концентрациях оказывает непосредственное активирующее влияние на аденилатциклазу, что ведет к увеличению концентрации цАМФ. В других случаях при нормальной или повышенной под влиянием катехоламинов концентрации цАМФ в отсутствие глюкокортикоидов оказывались блокированными последующие звенья процесса. В подобных случаях находили блокаду одной из
стадий активации фосфорилазы в связи с недостаточной мобилизацией ионов кальция. Увеличение концентрации этих ионов или добавление глюкокортикоидов восстанавливало ход процесса.
Нарушение метаболизма гормонов
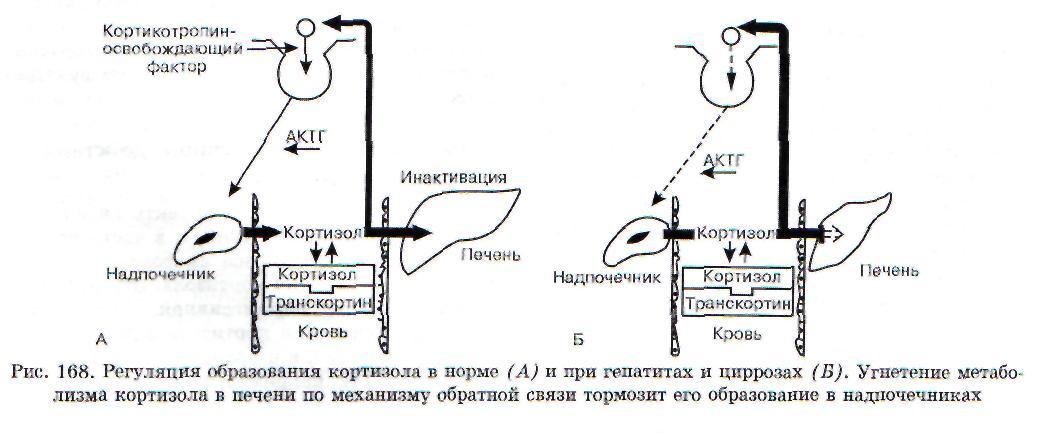
При гепатитах и циррозах печени метаболизм гормонов угнетается. Замедление метаболизма кортизола приводит к задержке его в организме. Это включает механизм обратной связи и угнетает функцию коры надпочечников, что приводит к некоторой их атрофии (рис. 168). Снижение инактивации эстрадиола в печени у мужчин вызывает включение механизма обратной связи, в результате чего угнетается образование гонадотропных гормонов в гипофизе и, как следствие, снижается функция тестикул, развивается импотенция. Одновременно при циррозах печени тестостерон легче превращается в эстрогены.
Таким образом, причины и механизмы нарушения функции желез внутренней секреции многообразны. Они могут действовать как изолированно, так и в различных комбинациях, приводя к сложному переплетению обменных функциональных и структурных нарушений.
19.1.4. Роль аутоаллергических (аутоиммунных) механизмов в развитии эндокринных нарушений
Все больше появляется данных о том, что наиболее частым механизмом нарушения функ-
634
ции
эндокринной системы является образование
аутоантител к различным ее компонентам.
Эти аутоантитела гетерогенны по своему
составу и свойствам и действуют на
различных участках эндокринной регуляции.
Описана группа
аутоантител, повреждающих клетки
желез внутренней секреции и приводящих
к развитию недостаточности той или иной
железы. Так,
известны аутоиммунные формы недостаточности
щитовидной, паращитовидных, надпочечных
желез. Аналогичным образом развивается
инсу-линзависимая (I
тип) форма сахарного диабета.
Наиболее ярко аутоаллергический механизм повреждения выявляется при тиреоидите Хасимото. Это заболевание щитовидной железы было описано Хасимото в 1912 г. Оно встречается преимущественно у женщин в возрасте за 50 лет и сопровождается снижением функции железы - гипотиреоидизмом и увеличением ее объема, т.е. развитием зоба. Строение железы резко изменено. Она инфильтрирована главным образом лимфоцитами, поэтому это заболевание иногда называют лимфоидным зобом. Инфильтрация носит диффузный и очаговый характер. Количество фолликулов постепенно уменьшается, и они заменяются соединительной тканью. Это приводит к постепенному снижению функции железы, иногда вплоть до развития миксе-цемы. В железе имеется как минимум три антигена (естественные или изолированные). Они находятся в тиреоглобулине, в коллоиде фолликулярного эпителия. Аутоантитела могут образовываться ко всем трем антигенам. Одновременно в повреждении участвует и аллергическая реакция замедленного типа.
Инсулинзависимый тип сахарного диабета часто сочетается с образованием аутоантител к островкам. Состав этих аутоантител различен. Можно обнаружить антитела к а- и Р-клеткам. Причем они могут быть направлены к рецепторам для глюкозы, к участкам мембраны, ответственным за Са2+-опосредованный экзоци-тоз глюкагона и/или инсулина. Это создает различные сочетания в нарушениях образования глюкагона и инсулина, что находит свое отражение в пестроте клинических проявлений диабета.
Действие другой группы аутоантител направлено против полипептидных гормонов.
Наибольшее внимание привлекает третья группа аутоантител, действие которых направ-
лено на рецепторы для гормонов на различных клетках-мишенях. Эти аутоантитела получили название антирецепторных. Рецептор представляет собой обычно сложный белок, состоящий из нескольких субъединиц, и выполняет, как правило, две функции: а) узнавания, в которой рецептор специфически связывает химический сигнал (гормон, медиатор, токсин, вирус), и б) передачи, в которой взаимодействие химического сигнала с рецептором трансформируется в определенный биохимический процесс. Антирецепторные антитела могут быть направлены к различным частям рецептора. Поэтому возможны различные последствия связывания аутоантител с рецепторами. Установлены следующие варианты:
1.Антитела блокируют место узнавания на рецепторе. Поэтому естественный или экзогенный гормон полностью или частично не может с ним связаться. Развивается клиника недостаточности данной железы, хотя гормон в крови есть. Выявляется резистентность к экзогенному гормону.
Антитела связываются с активным местом рецептора. Возникает имитация действия гормона, развивается клиника гиперфункции данной железы. По механизму обратной связи образование естественного гормона снижается.
Образование комплекса «антитело + рецептор» в зависимости от вида антител может приводить к активации комплемента и повреждению рецепторов.
Образовавшиеся комплексы «антитело + рецептор» собираются в одном месте на поверхности клетки (кэппинг - образование шапки), после чего в этом месте происходит впячивание части мембраны внутрь клетки с образованием фа-госомы, где происходит деградация комплексов. Взамен утраченных рецепторов клетка образует новые. При хроническом течении процесса может происходить истощение воспроизводящей функции клетки и на ее поверхности уменьшается число рецепторов к данному гормону.
Процесс поглощения, деградации и воспроизведения рецепторов происходит и в норме. Так поглощаются и разрушаются гормон-рецептор-ные комплексы. От избытка гормона клетка защищается, уменьшая образование рецепторов. Этот механизм, в частности, лежит в основе сни-
635
жения чувствительности клеток-мишеней к инсулину у людей, употребляющих избыточное количество пищи. Последнее ведет к усилению образования инсулина. В ответ на избыток инсулина клетки-мишени снижают число рецепторов. Развивается один из видов инсулиноре-зистентности. Он хорошо лечится ограничением приема пищи.
Характер функциональных нарушений будет определяться свойствами образовавшихся ауто-антител и их соотношением. Чаще идет образование аутоантител одновременно к различным субъединицам рецептора. Так, например, при диффузном токсическом зобе (базедова болезнь, Гревса болезнь) примерно у 95% нелеченых больных выявляются аутоантитела к рецептору для тиреотропного гормона (ТТГ). Они получили разные названия (длительно действующий стимулятор - lats; протектор длительно действующего стимулятора -lats-p; тиреоидстимулирующие антитела - tsa b; тиреотропинсвязывающий ингибитор tsI и др.).
636
Более детальные исследования показали, что одни из них направлены к гликопротеиновой субъединице (место узнавания сигнала), другие - к ганглиозидной субъединице (функция передачи сигнала). Все они в той или иной степени блокируют связывание ТТГ, но при этом одни стимулируют образование цАМФ, синтез и осво-
бождение Т3 и Т4, а другие - рост тиреоидных клеток без влияния на образование цАМФ. Отсюда первые приводят к развитию клиники ги-пертиреоидизма, а вторые - к развитию зоба с небольшим увеличением содержания в крови Т3 и Т,. По ходу развития заболевания количество антител разных видов обычно меняется. Поэтому изменяются функция щитовидной железы и клиника заболевания. Аналогичным образом дело обстоит с функцией других клеток-мишеней.
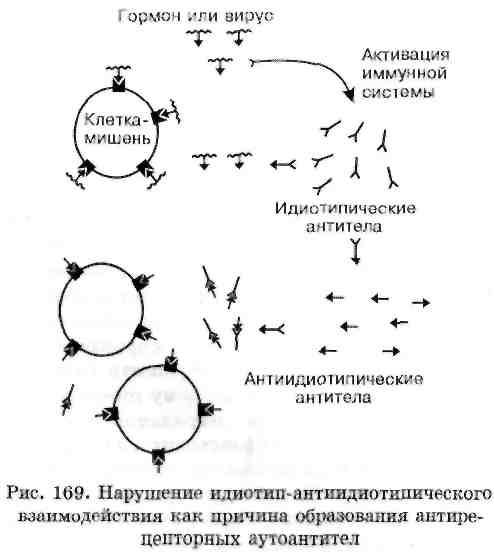
Возникает вопрос: почему вырабатываются аутоантитела к рецепторам клеток? Считают, что это связано с дисбалансом в механизмах идио-тип-антиидиотипического взаимодействия. Суть его сводится к тому (рис. 169), что на антигенную детерминанту гормона, которая может оказаться той частью, которой гормон связывается с рецептором клетки, образуются специфические антитела с уникальной конфигурацией на антигенсвязывающем конце. Эта специфическая, уникальная конфигурация получила название идиотипа. Идиотип является зеркальным отражением конфигурации антигенной детерминанты, поэтому и способен связываться с ней. Но сам идиотип, т.е. его конфигурация, является чужеродной для иммунной системы организма, и она начинает образовывать анти-антитела, специфичные к идиотипу и получившие название анти-идиотипических антител. Последние, являясь зеркальным отражением специфичности идиотипических антител, становятся по конфигурации аналогичными антигенной детерминанте гормона. Поэтому они могут связываться как с идиотипическими антителами, так и с гормональными рецепторами клетки-мишени.
Полипептидные гормоны имеют обычно несколько антигенных детерминант. Некоторые из них могут оказаться теми участками, через которые гормон связывается с местом узнавания или передачи сигнала на рецепторе. Поэтому обычно образуются различные виды аутоантител со специфичностью к различным участкам рецептора со всеми вытекающими отсюда последствиями.
У подавляющего числа людей антирецептор-ные антитела не обнаруживаются, так как в физиологических условиях к собственным гормонам имеется иммунологическая толерантность и иммунная реакция на них не включается. Что же должно произойти, чтобы этот механизм включился? Во-первых, должны быть какие-то
