
- •Механизм:
- •Нитриты
- •Гидразиды
- •3) Из сл.Эфиров
- •Дикарбоновые кислоты
- •Ненасыщенные дикарбоновые кислоты
- •Ароматические дикарбоновые кислоты
- •Сульфоновые кислоты
- •Ароматические (фенолокислоты)
- •Производные солициловой кислоты
- •1) Произ-ые по –cooh:
- •2) Ппроизв-ые по –oh:
- •Оксокислоты
- •Алкилирование
- •Природные α-аминокислоты
- •Специфич.Св-ва аминокислот.
- •Пептиды и белки
- •С троение пептидной группы
- •Химический метод синтеза пептидов(классич)
- •Твердофазный синтез пептидов (тфсп)
- •Важнейшие пентозы:
- •Важнейшие гeксозы:
- •Стереоизомерия
- •Таутомерия
- •Конформации моносахаридов.
- •Конформация галактоперонозы
- •Химические св-ва моносахаридов.
- •Качественные реакции обнаружения гексоз., и пентоз.,
- •Другие представители моносахаридов.
- •Аминосахара
- •Дисахариды
- •Химические св-ва:
- •Полисахариды
- •Крахмал
- •Аминопектин
- •Декстраны
- •Пособы получения:
- •Галогенирование
- •Специфич.Реакции
- •Пятичленные гетероциклы с 2-мя гетероатомами
- •Имидазол. Получение:
- •Важнейшие производные:
- •Производные пиразола.
- •3(5)-Оксипиразол пиразолон-3(5)
- •Синтез антипирина
- •Синтез амидо из антипирина
- •Хинолин
- •Производные хинолина
- •Производные пиримидина
- •Синтез барбитуровой к-ты.
- •Оксазины
- •Тиазины
- •Производные фенотиазина
- •Мочевая к-та.
- •Метилированные ксантины
- •Птеридин
- •Аллоксазин изоаллоксазин.
- •Алкалоиды
- •**Морфин
- •** Кокаин
- •Нуклеиновые ( азотистые основания)
- •Нуклеозиды:
- •Нуклеотиды
- •2 Цепи в этой спирали антипараллельны, т.Е.Их 5’ и 3’-межнуклеотидные фосфодиэфир.Мостики параллельны противоположно.
- •Коферментные нуклеотиды
- •2)Флавиновые ( фмн и фад)
- •Терпены
- •Циклические
- •Производные камфана :
- •Стероидные гормоны (половые г.И г.Коры надпочечников)
- •Желчные кислоты
- •Стерины
- •Омыляемые липиды
- •Простые липиды
- •Обзорная лекция
- •Задачи:
Пособы получения:
** циклизация 1,4 – дикарбонильных соединении.






 P2S5
R R
P2S5
R R


 СH2-CH2
S
СH2-CH2
S
R




 -C
C-R CH-CH
-C
C-R CH-CH




 O O R-C
C-R NH3
R R
O O R-C
C-R NH3
R R

 OH
OH N
OH
OH N
H





 H2SO4,
to
R
H2SO4,
to
R
 O
O
** взаимные превращения (цикл реак.Юрьева)







 H2O
H2O
N NH3 O
H



 H2O
Al2O3
H2S
H2O
Al2O3
H2S
NH3 t=450o H2O






S
Специфические способы получения:
**нагрев.аммонильной соли слизевой кислоты.
П
 иррол
иррол










 HO-CH-CH-OH
to
HO-CH-CH-OH
to




 HC CH COONH4
-H2O
N
HC CH COONH4
-H2O
N
H
 4NOOH
OH OH - CO2
H
4NOOH
OH OH - CO2
H
-NH3
** перегонка сукцин имида с Zn-ой пылью.






 H2C
CH2
H2C
CH2
O

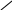

 =
=O Zn
=
=O Zn
NH N
H
*


 *
ацетилен + NH3
*
ацетилен + NH3
H
 CaCH+NH3
300o-400o
CaCH+NH3
300o-400o
Al2O3 N
H




*
 *
HCaCH+2HC=O
to
[HOCH2–CaC–CH2OH]+
–NH3,
to
*
HCaCH+2HC=O
to
[HOCH2–CaC–CH2OH]+
–NH3,
to
H N
H
Фуран
** сухая перегонка слизевой к-ты.


 HO-CH-CH-OH
HO-CH-CH-OH
H








 OOC-CH
CH –COONH HOOC - - COOH
- COOH to
OOC-CH
CH –COONH HOOC - - COOH
- COOH to
OH OH O O -CO2
Дегидрослизевая пирослиз.
К-та к-та.
** нагревание альдопентоз с водоотним.св-ми.












 HO-CH-CH-OH
-C=O [O] -COOH
to =
HO-CH-CH-OH
-C=O [O] -COOH
to =


 HCH CH C=O O H
O -CO2
O
HCH CH C=O O H
O -CO2
O
OH OH H
Гиофен
** Парафазная циклизация бутана с серой
С



 4H10
+ HS 700oC
4H10
+ HS 700oC
-3H2S S
* *
по Чичибабину
*
по Чичибабину
2HC aCH+H2S 400o-450oC
 H2O3
S
H2O3
S
** 2CH3C=O + H2S 300o
 H Al2O3
S
H Al2O3
S
Химические свойства:
** кислотно-основные
Т.к.неподел.пара е- гетероатомов втянуты в общи секстед, поэтому гетероциклы не проявляют основных св-в.
Пиррол и фуран ацидофобные в кисл.среде теряют ароматичность и поляризуются с обр.смол.
+










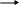







 .. +H+
H H
полимер-ия
.. +H+
H H
полимер-ия
Х X H X+ H
Х=0; NH
Пиррол облад.слаб.кисл.св-ами реагирует с сильн.основ.с Me, MeOH и др.







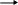 N + KOH
(тв) N пирролат
калия
N + KOH
(тв) N пирролат
калия
H -H2O K
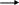 N + NaNH2
N-
пирролнатрии
N + NaNH2
N-
пирролнатрии
H -NH3 Na+
N +CH3MgBr N- пирролмагний бромид
 H -CH4
MgBr +
H -CH4
MgBr +
** реак.электрофильного замещ.
Яв-сь П-избыт.ароматич.системами они легче чем бензол вступают в реак. SЕ
По активности они располаг. в ряд:
Пиррол> фуран > тиофен
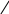

 (B) 4 3(B)
реак. SЕ идут
преимущественно в полож. α(2)
(B) 4 3(B)
реак. SЕ идут
преимущественно в полож. α(2)

(

 α)5
(б-)2(α)
α)5
(б-)2(α)
..
Х
1
