
- •Механизм:
- •Нитриты
- •Гидразиды
- •3) Из сл.Эфиров
- •Дикарбоновые кислоты
- •Ненасыщенные дикарбоновые кислоты
- •Ароматические дикарбоновые кислоты
- •Сульфоновые кислоты
- •Ароматические (фенолокислоты)
- •Производные солициловой кислоты
- •1) Произ-ые по –cooh:
- •2) Ппроизв-ые по –oh:
- •Оксокислоты
- •Алкилирование
- •Природные α-аминокислоты
- •Специфич.Св-ва аминокислот.
- •Пептиды и белки
- •С троение пептидной группы
- •Химический метод синтеза пептидов(классич)
- •Твердофазный синтез пептидов (тфсп)
- •Важнейшие пентозы:
- •Важнейшие гeксозы:
- •Стереоизомерия
- •Таутомерия
- •Конформации моносахаридов.
- •Конформация галактоперонозы
- •Химические св-ва моносахаридов.
- •Качественные реакции обнаружения гексоз., и пентоз.,
- •Другие представители моносахаридов.
- •Аминосахара
- •Дисахариды
- •Химические св-ва:
- •Полисахариды
- •Крахмал
- •Аминопектин
- •Декстраны
- •Пособы получения:
- •Галогенирование
- •Специфич.Реакции
- •Пятичленные гетероциклы с 2-мя гетероатомами
- •Имидазол. Получение:
- •Важнейшие производные:
- •Производные пиразола.
- •3(5)-Оксипиразол пиразолон-3(5)
- •Синтез антипирина
- •Синтез амидо из антипирина
- •Хинолин
- •Производные хинолина
- •Производные пиримидина
- •Синтез барбитуровой к-ты.
- •Оксазины
- •Тиазины
- •Производные фенотиазина
- •Мочевая к-та.
- •Метилированные ксантины
- •Птеридин
- •Аллоксазин изоаллоксазин.
- •Алкалоиды
- •**Морфин
- •** Кокаин
- •Нуклеиновые ( азотистые основания)
- •Нуклеозиды:
- •Нуклеотиды
- •2 Цепи в этой спирали антипараллельны, т.Е.Их 5’ и 3’-межнуклеотидные фосфодиэфир.Мостики параллельны противоположно.
- •Коферментные нуклеотиды
- •2)Флавиновые ( фмн и фад)
- •Терпены
- •Циклические
- •Производные камфана :
- •Стероидные гормоны (половые г.И г.Коры надпочечников)
- •Желчные кислоты
- •Стерины
- •Омыляемые липиды
- •Простые липиды
- •Обзорная лекция
- •Задачи:
Важнейшие пентозы:
 O O
O
O O
O


 C C
C
C C
C
 H H
H
H H
H
 H-C-OH H-C-H
H-C-OH
H-C-OH H-C-H
H-C-OH
H-C-OH H-C-OH HO-C-H
H-C-OH H-C-OH H-C-OH
CH2OH CH2OH CH2OH
Д-рибоза 2-дезокси-Д-рибоза Д-ксилоза
 O
O
C CH2OH

 H C=O
H C=O
H -C-OH H-C-OH
H O-C-H
H-C-OH
O-C-H
H-C-OH
H O-C-H CH2OH
CH2OH
Li-арабиноза Д-рибулоза
Важнейшие гeксозы:
 O O
O
O O
O
1C C C


 H H
H
H H
H
H
 2-C-OH
HO2-C-H
H-C-OH
2-C-OH
HO2-C-H
H-C-OH
H O3-C-H HO3-C-H HO3-C-H
H -C-OH H-C-OH HO4-C-H
H -C-OH
H-C-OH H-C-OH
-C-OH
H-C-OH H-C-OH
CH2OH CH2OH CH2OH
Д-глюкоза д-манноза д-галактоза
CH2OH
C=O
H O-C-H
H-C-OH
H-C-OH
CH2OH
Д-фруктоза
Стереоизомерия
Все молекулы моносахаридов содерж.хиральные (ассим) атомы С
Альдотриозы-1
Альдотетрозы-2
Альдопентозы-3
Альдогексозы-4
Китозы с тем же числом углер.атомов содержат на 1 хиральный атом меньше.
Число стереоизомеров опр-ся N=2n
Если n=4, то N=16
Относительная конфигурация, т.е. принадл. к Д или Li-ряду опред-ся путем сравнения конфигурации у последнего ассим.атома С (последнего по счету) с конфигурацией хирального центра в
Д или Li-глицерин альдегиде, предложенным Розновым за стандарт.
 O O
O
O O
O



 C C
C
C C
C
H H H
H -C-OH H-C*-OH HO-C*-H O

 CH2OH
HO-C*-H
H-C*-OH
C
CH2OH
HO-C*-H
H-C*-OH
C
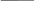 H-C*-OH
HO-C*-H
H
H-C*-OH
HO-C*-H
H
 H-C*-OH
‘ HO-C*-H
HO-C-H
H-C*-OH
‘ HO-C*-H
HO-C-H
CH2OH CH2OH CH2OH
Д-глицерин Д-глюкоза Li-глюкоза Li –глицериновый альдегид
альдегид
Д-глюкоза Li-глюкоза

Энантиомеры
Большинство моносахаридов относятся к Д-ряду.
При наличии в молекуле 2-х хиральных центров, сущ-ет диастереомеры, α –ые отп.конфиг.у одного хирального центра.
Химия углеродов диастереомера наз-ся эпимерами
(Д-глюкоза и Д-монноза)
