
- •Учебник подготовлен в рамках Инновационной образовательной программы
- •ISBN 978-5-7262-0821-3
- •5.1. Однокомпонентные диаграммы фазового равновесия,
- •5.2.1. Диаграмма с полной взаимной растворимостью
- •5.2.4. Диаграммы с наличием трехфазного равновесия
- •5.2.5. Диаграммы с эвтектическим и эвтектоидным
- •5.2.6. Диаграммы с монотектическим и монотектоидным
- •5.2.8. Диаграммы с перитектическим и перитектоидным
- •7.1. Физико-химические основы взаимодействия
- •7.1.4. Роль термодинамики и химической кинетики
- •7.2.3. Пленки на металлах как продукты химической
- •7.2.9. Формирование защитных жаростойких пленок
- •7.2.10. Влияние внешних и внутренних факторов
- •7.3.3. Механизм электрохимической коррозии. Работа
- •7.3.4. Гетерогенность поверхности и микрогальванические
- •7.3.7. Термодинамика процессов электрохимической
- •7.4.3. Влияние примесей в жидких металлах
- •7.4.4. Основные пути снижения взаимодействия
- •конструкционных материалов с жидкометаллическими
- •7.5. Защита от коррозии на стадии проектирования и разработки
- •Предисловие к тому 2
- •Глава 4. ТЕРМОДИНАМИКА В МАТЕРИАЛОВЕДЕНИИ
- •Введение.
- •4.1. Основные понятия термодинамики
- •4.2. Метод термодинамических потенциалов
- •4.3. Прикладная термохимия
- •4.4. Фазовые равновесия
- •4.5. Термодинамика растворов
- •4.6. Физическая химия неидеальных растворов
- •4.7. Термодинамическая теория диаграмм состояния
- •Список использованной литературы
- •Глава 5. ДИАГРАММЫ ФАЗОВОГО РАВНОВЕСИЯ
- •Введение
- •5.2.2. Диаграмма с расслоением твердого раствора
- •5.2.3. Диаграмма с наличием упорядочения
- •5.2.4. Диаграммы с наличием трехфазного равновесия
- •5.2.7. Диаграмма с метатектическим равновесием
- •5.2.9. Диаграмма с синтектическим равновесием
- •5.2.10. Диаграммы с промежуточными фазами
- •5.3. Диаграмма железо – углерод
- •5.4. Анализ сложных диаграмм фазового равновесия
- •Контрольные вопросы
- •Список использованной литературы
- •6.4. Закономерности сегрегации примесей
- •Контрольные вопросы
- •Список использованной литературы
- •Глава 7. СОВМЕСТИМОСТЬ И КОРРОЗИЯ МАТЕРИАЛОВ
- •7.1.1. Совместимость материалов со средой
- •7.1.2. Коррозия. Основные понятия и определения
- •7.1.3. Коррозионные проблемы
- •7.1.5. Классификация процессов коррозии
- •7.2. Химическая коррозия металлов
- •7.2.1. Химическая газовая коррозия
- •7.2.4. Состав и структура оксидов. Эпитаксия
- •7.2.5. Толщина и защитные свойства пленок
- •7.2.7. Механизм химической газовой коррозии
- •7.2.8. Оксидные пленки на поверхности железа
- •7.2.11. Химическая коррозия в газовых теплоносителях
- •7.3. Электрохимическая коррозия
- •7.3.1. Основные признаки и причины
- •7.3.2. Электролиты
- •7.3.6. Электродные потенциалы
- •7.3.8. Диаграммы Пурбе
- •7.3.9. Кинетика электрохимических процессов коррозии
- •7.3.10. Электрохимическая защита
- •7.4. Коррозия в жидкометаллических средах
- •7.4.1. Типы процессов
- •7.4.2. Растворение твердого металла в жидком
- •7.5. Защита от коррозии на стадии проектирования
- •7.5.1. Коррозия и вопросы конструирования
- •7.5.2. Выбор материалов и их совместимость
- •7.5.3. Выбор рациональной формы элементов
- •7.5.4. Учет влияния механических нагрузок
- •7.5.5. Рациональные способы сборки конструкций
- •Контрольные вопросы
- •Список использованной литературы
5.2.2. Диаграмма с расслоением твердого раствора
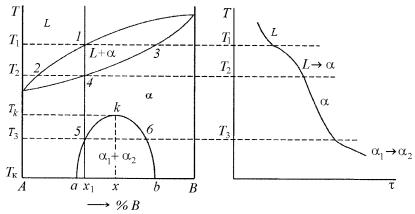
Иногда наблюдается неограниченная растворимость компонентов в жидком и твердом состояниях при высоких температурах и разрыв этой растворимости при низких температурах, т.е. имеется ограниченная взаимная растворимость компонентов А и В ниже какой-то определенной температуры Tк (рис. 5.15).
Кривая akb, показывающая ограниченную взаимную растворимость в этой системе называется кривой расслоения или бинодальной кривой. При температурах выше этой кривой, т.е. в однофазной α-области, все сплавы представляют собой ненасыщенные растворы замещения на основе компонентов А и В. Ниже этой области в двухфазной области α1 + α2 все сплавы состоят из двух фаз α1 и α2, каждая из которых – это насыщенный твердый раствор на основе компонента А или В. Твердые α1- и α2-растворы имеют одну и ту же кристаллическую решетку и отличаются один от другого только химическим составом.
Рис. 5.15. Диаграмма фазового равновесия с расслоением твердого раствора
Кривая ak показывает, какие максимальные количества компонента В могут растворяться в компоненте А, т.е. состав насыщенного α1-твердого раствора. Кривая bk показывает, какие максимальные количества компонента А могут растворяться в компоненте В, т.е. состав насыщенного твердого α2-раствора. Состав α1-твердого
248
раствора изображается кривой ak, а α2-твердого раствора bk. Из диаграммы фазового равновесия в соответствии с наклоном кривых ak и bk следует, что взаимная растворимость компонентов А и В в твердом состоянии уменьшается с понижением температуры. Точку максимума k на бинодальной кривой akb называют критической точкой. В сплаве х, отвечающем по составу этой точке, при температуре Tk составы α1- и α2-растворов, из которых он состоит при более низких температурах, совпадают друг с другом.
Зависимость изобарно-изотермического потенциала твердой фазы от состава при температурах ниже Tk, показывающая термодинамический стимул расслоения α-твердого раствора была приведена на рис. 5.10.
Рассмотрим фазовые превращения, протекающие в различных сплавах при охлаждении при переходе через бинодальную кривую akb (рис. 5.15). Очевидно, что попадая на эту кривую, кристаллы α- твердого раствора одного состава становятся насыщенными относительно кристаллов того же твердого раствора другого состава, и при понижении температуры из одного твердого раствора выделяется другой твердый раствор. Например, в сплавах участка a–k при охлаждении ниже кривой ak из α1-твердого раствора, богатого компонентом А, выделяются кристаллы α2-раствора, богатого компонентом В, что записывается как α1 → α2 . В сплавах участка b–k при температурах ниже кривой kb из α2-раствора выделяются кристаллы α1-твердого раствора, или в краткой записи α2 → α1. Таким образом, в сплавах участка a–b в твердом состоянии происходит образование кристаллов одного твердого раствора из другого твердо-
го раствора, что называется вторичной кристаллизацией.
Рассмотрим фазовые превращения при охлаждении в одном из сплавов, например, сплаве х1. В интервале температур T1–T2 происходит кристаллизация данного сплава с выделением кристаллов α- твердого раствора. Ниже этой температуры в интервале температур T2–T3 происходит охлаждение сплава, состоящего из α-твердого раствора. Как только температура сплава х понизится до T3, кристаллы α- (или теперь уже α1-) твердого раствора окажутся насыщенными относительно кристаллов α2-раствора. При охлаждении ниже этой температуры из α1-твердого раствора должны выделять-
249
ся вторичные кристаллы α2-раствора, богатые компонентом В. Состав первых α2- кристаллов определится точкой 6 на кривой kb. При понижении температуры состав α1-кристаллов изменяется по кривой ak от точки 5 к точке a, а состав выделяющихся из них α2- кристаллов – по кривой bk от точки 6 к точке b.
В соответствии с правилом отрезков за счет уменьшения количества α1-кристаллов в сплаве х увеличится количество вторичных α2-кристаллов, что легко рассчитывается количественно по правилу отрезков при любой температуре ниже T3. Бинодальная кривая akb (или кривая расслоения твердого раствора) всегда располагается ниже кривой солидуса и не может ее пересекать. Если бинодальная кривая пересекает кривую солидуса, то в равновесии с двумя твердыми растворами оказывается жидкая фаза и появляется трехфазное равновесие, которое будет рассмотрено ниже.
5.2.3. Диаграмма с наличием упорядочения
Разрыв непрерывной растворимости компонентов А и В в твердом состоянии возможен также при образовании в ряде сплавов упорядоченных α′-твердых растворов. Физическая сущность упорядочения и физические основы перехода из неупорядоченного твердого раствора в упорядоченный и наоборот рассматриваются в п. 4.9.1. Поэтому здесь будет приведена только графическая интерпретация этих переходов применительно к диаграммам фазового равновесия.
На рис. 5.16 приведена диаграмма фазового равновесия с упорядоченными твердыми растворами. Многие твердые растворы замещения при низких температурах упорядочены, а при высоких температурах (выше точки Курнакова Тк) они разупорядочены. При медленном охлаждении в них происходит атомное перераспределение, в результате которого атомы различных компонентов занимают определенное положение в решетке. Низкотемпературное распределение атомов называется сверхструктурой.
В решетке неупорядоченного твердого раствора все кристаллографические плоскости одного типа статистически одинаковы. В упорядоченном растворе часть плоскостей одного типа обогащена
250
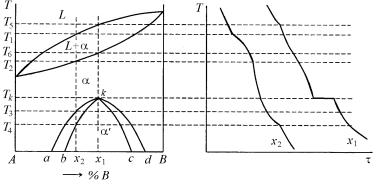
атомами одного из компонентов или состоит только из атомов одного компонента. Эти плоскости обогащения чередуются через одну, две или в другой кратности и поэтому на рентгенограмме упорядоченного твердого раствора появляются, кроме обычных отражений, зависящих от симметрии решетки в целом, как и в неупорядоченном растворе, еще дополнительно отражения от плоскостей обогащения. Эти отражения называются сверхструктурными линиями. Температуру перехода Tk неупорядоченного α-твердого раствора стехиометрического состава х1 в упорядоченный α′-твердый раствор при охлаждении называют точкой Курнакова, так как он впервые вместе с русскими учеными Заседателевым и Жемчужным обнаружил упорядоченные фазы в системе Cu–Au.
Рис. 5.16. Диаграмма фазового равновесия с упорядоченными твердыми растворами
Кривая akd называется кривой начала упорядочения. Иногда точку k называют точкой Кюри упорядочения.
Всплаве х1 при температуре Tk в равновесии оказываются неупорядоченный α и упорядоченный α′-растворы состава точки k.
При охлаждении сплава х1 превращение α → α′ совершается скачкообразно при постоянной температуре Tk.
Всплавах участков b–х1 и х1–c превращение α → α′ совершается
винтервале температур между кривыми akd и bkc. В двухфазных областях α + α′ между этими кривыми сплавы состоят из двух фаз: неупорядоченного α-раствора и упорядоченного α′-раствора разных составов, между которыми имеются межфазные границы. Переход
251
