
- •Передмова
- •3. Зміст навчання.
- •Заняття №1 класифікація та номенклатура органічних сполук актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод)
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод)
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод)
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Короткі методичні вказівки до роботи на практичному занятті
- •Заняття № 5. Алкани та циклоалкани Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод)
- •1. План опису механізму реакцій радикального заміщення
- •2. Інструкція з виконання лабораторних дослідів Хімічні властивості алканів та циклоалканів
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття № 6 ненасичені вуглеводні: алкени, алкіни, алкадієни Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод)
- •1. План опису механізму реакцій електрофільного приєднання
- •2. Інструкція з виконання лабораторних дослідів Хімічні властивості ненасичених вуглеводнів
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Тест 10
- •Тест 11
- •Тест 12
- •Короткі методичні вказівки до проведення практичного заняття
- •Заняття №7 моноядерні арени. Реакції електрофільного заміщення в аренах і правила орієнтації замісників актуальність теми
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод)
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття № 8
- •Багатоядерні арени
- •З конденсованими іІзольованими ядрами
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод)
- •1. Інструкція з виконання лабораторних дослідів Хімічні властивості багатоядерних аренів
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття № 9 галогенопохідні вуглеводнів. Реакції нуклеофільного заміщення та елімінування актуальність теми
- •Цілі навчання
- •Орієнтовна основа дії (оод)
- •1. План опису механізму реакцій нуклеофільного заміщення
- •2. Інструкція з виконання лабораторних дослідів Хімічні властивості галогенпохідних вуглеводнів
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Короткі методичні вказівки до проведення практичного заняття
- •Заняття №10 нітросполуки. Аміни. Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод)
- •Завдання для перевірки досягнення конкретних цілей навчання Тест 1
- •Заняття № 11 діазо- та азосполуки. Теорія колірності актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Діазо- та азосполуки
- •Азосполуки
- •Орієнтовна основа дії (оод) Інструкція з виконання лабораторних дослідів Хімічні властивості діазо- та азосполук
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття №12 cпирти. Аміноспирти. Етери актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод) Інструкція з виконання лабораторних дослідів Хімічні властивості спиртів, аміноспиртів та етерів
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття №13 Феноли. Амінофеноли Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод) Інструкція з виконання лабораторних дослідів Хімічні властивості фенолів та амінофенолів
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття №14 Аліфатичні альдегіди та Аліфатичні кетони Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод) Інструкція з виконання лабораторних дослідів Хімічні властивості аліфатичних альдегідів та кетонів
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття №15 Ароматичні альдегіди та кетони Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод) Інструкція з виконання лабораторних дослідів Хімічні властивості ароматичних альдегідів та кетонів
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття №16 Монокарбонові кислоти Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод) Інструкція з виконання лабораторних дослідів Хімічні властивості монокарбонових кислот
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття №17 Дикарбонові кислоти Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод)
- •1. Алгоритм складання синтезу за участю малонового естеру
- •2. Інструкція з виконання лабораторних дослідів Хімічні властивості дикарбонових кислот
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття №18 Функціональні похідні карбонових кислот Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод) Інструкція з виконання лабораторних дослідів Хімічні властивості функціональних похідних карбонових кислот
- •Завдання для перевірки досягнення конкретних цілей навчання Тест 1
- •Заняття №19 гетероФункціональні карбоновІ кислотИ. Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод) Інструкція з виконання лабораторних дослідів Хімічні властивості гетерофункціональних карбонових кислот
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття №20 похідні вугільної кислоти Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод) Інструкція з виконання лабораторних дослідів Хімічні властивості вугільної кислоти
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття № 21 Колоквіум : «Вуглеводні та їх функціональні похідні» Цілі навчання
- •Зміст навчання
- •Заняття №22 Підсумковий модульний контроль
Граф логічної структури
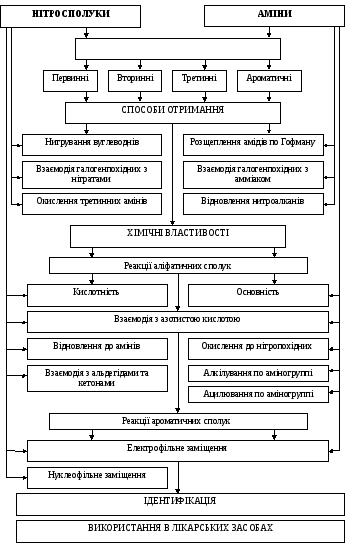
Джерела інформації
Обов'язкова література:
Органічна хімія. Підручник для вищих фармацевтичних закладів освіти. У 2 кн. / В.П. Черних, Б.С.Зіменковський, І.С.Гріценко,- Харків; Основа, 1997.- Кн. 2,- с.187-229.
Черных В.П., Лекции по органической химии- Харків; Золоті сторінки, 2005 с.164-190.
Общий практикум по органической химии / В.П. Черних и др. - Харків: Изд-во НФАУ; Золотые страницы, 2002.-с.213-229.
Сборник тестов по органической химии/ под. ред. В.П.Черных. – Харків 2005.С. 157-170.
Лекція з органічної хімії за темою: Нітросполуки. Аміни
Додаткова література:
Моррисон Р., Бойд Р. Органическая химия. Пер с англ. - М.: Мир, 1974.
Степаненко Б.Н. Курс органической химии. В 2-х ч. - М.: Высшая школа, 1981.
Некрасов В.В. Руководство к малому практикуму по органической химии. - М.: Химия, 1975.
Орієнтовна основа дії (оод)
1. Алгоритм написання реакцій нітросполук з азотистою кислотою
Первинні
1. Алгоритм написання реакцій амінів з азотистою кислотою



3. Інструкція з виконання лабораторних дослідів
Хімічні властивості нітросполук та амінів
Принцип методу:нітросполуки та аміни мають в своєму складі атом гідрогену, але до нітросполук він входить в максимально окисленій, а до складу амінів в максимально відновленій формі. Це приводить до протилежності в кислотно-основних та окисно-відновних властивостях. До того ж протилежні знаки мезомерних ефектів приводять до протилежного впливу цих груп в якості замісників на ароматичні системи. Об’єднуючим реагентом для ідентифікації цих сполук є азотиста кислота, з якою, як нітросполуки, так і аміни реагують по різному в залежності від їх будови.
Ціль:за допомогою характерних реакцій практично довести хімічні властивості представників класів нітросполук та амінів.
Обладнання та реактиви: штатив з пробирками, склянки 25 мл, пальник, універсальний індикаторний папір, газетний папір, фільтрувальний папір, льодова суміш, нітробензол, конц. HCl, 10 %-ний р-н HCl, 10 %-ний р-н H2SO4, 5 %-ний р-н NaNO2, 30 %-ний р-н NaNO2, гранульований Zn, 5%-ний р-н NaOH, 10 %-ний р-н K2Cr2O7, 25 %-ний водн. р-н метиламіну, анілін, етиламін, 5 %-ний р-н CuSO4, 1 %-ний р-н FeCl3, лужний розчин -нафтолу, хлороформ, етанол, бромна вода, насичений розчин кальцію гипохлорит-хлориду, 2 %-ного розчину калію хлорату.
Методика виконання:
Опит 24. Відновлення ароматичних нітросполук
Відновлення нітроаренів в кислому середовищі. У пробірку поміщають 1 краплю нітробензолу, додають 3 краплі концентрованої хлоридної кислоти і шматочок (2x2 мм) гранульованого цинку. Вміст пробірки постійно струшують і спостерігають виділення бульбашок газу – водню.
Нітробензол повинен добре перемішуватися бульбашками газу. Якщо виділення бульбашок газу сповільнюється, вміст пробірки злегка підігрівають в полум'ї пальника. Реакцію проводять до повного розчинення цинку, іноді доцільно додати додатково 1-2 краплі 10 %-ного розчину хлоридної кислоти:
Вільну основу аніліну виділяють при підлуговуванні 5%-ним розчином натрію гідроксиду.
Опит 25. Основність амінів
А.На універсальний індикаторний папір наносять окремо по 1 краплі 25 %-ного водного розчину метиламіну і аніліну і порівнюють їх основність.
Аліфатичні аміни на відміну від ароматичних проявляють більш виражені основні властивості.
Б.В пробірку поміщають 10 крапель 5 %-ного розчину купруму (II) сульфату і додають по каплях 25 %-ний розчин метиламіну. Спостерігають утворення блакитного осаду купруму (II) гідроксиду, який потім розчиняється, інтенсивно забарвлюючи розчин у фіолетовий колір:
В.В пробірку поміщають 2 краплі 25 %-ного розчину метиламіну і 2 краплі 1 %-ного розчину ферруму (III) хлориду. Спостерігають утворення осаду бурого кольору :
Опит 26. Розчинність аніліну і його солей у воді
У пробірку поміщають 1 краплю аніліну і 3 краплі води. При енергійному струшуванні пробірки спостерігають помутніння рідини – утворення емульсії анілін-вода. Суміш розбавляють рівною кількістю води і повторно струшують пробірку. Емульсія зберігається, що свідчить про погану розчинність аніліну у воді.
Вміст пробірки ділять на дві частини. До однієї з них додають 1-2 краплі 10 %-ного розчину хлоридної кислоти. Розчин стає прозорим в результаті утворення добре розчинної у воді солі - анілінія хлориду.
Водний розчин анілінія хлориду, що утворився, зберігають для наступних дослідів.
До іншої частини розчину додають 1-2 краплі 10 %-ного розчину сульфатної кислоти. При струшуванні пробірки спостерігають випадіння кристалічного осаду важкорозчинної у воді сірнокислої солі аніліну.
Опит 27. Взаємодія амінів з азотистою кислотою
Реакції первинних амінів: а) дезамінування первинних аліфатичних амінів. У пробірку поміщають 6 крапель етиламіну, 3 краплі концентрованої хлоридної кислоти і 5 крапель 5 %-ного розчину натрію нітриту. Спостерігають виділення пухирків газу – азоту.
Негорючість газу, що виділився, підтверджують, підносячи лучину, що горить, до отвору пробірки. Наявність спирту в пробірці після проведення досвіду доводять йодоформною пробою (див. опит 47).
б) діазотування первинних ароматичних амінів. У пробірку поміщають 4 краплі аніліну, 2-3 мл води і 20 крапель концентрованої хлоридної кислоти. Пробірку занурюють в склянку з льодом, охолоджують до 0-5 oC і при струшуванні додають 5 крапель 30 %-ного розчину натрію нітриту. Первинні ароматичні аміни під дією азотистої кислоти перетворюються на солі діазонію, утворення яких можна підтвердити наступною реакцією азосполучення.
Отриманий розчин солі діазонію підливають в пробірку, що містить 2 мл лужного розчину -нафтолу. Спостерігають утворення оранжево-червоного осаду азобарвника.
Опит 28. Изонітрильна проба
У пробірку поміщають 1 краплю аніліну, 2-3 краплі 10 %-ного розчину натрію гідроксиду, 2 краплі хлороформу і 10 крапель етанолу. При повільному нагріванні суміші до початку кипіння появляється характерний, неприємний запах ізонітрилу (пробірку з-під тяги не виносити!).
Перш ніж вилити розчин у банку для зливу хімічні реактивів, отриманий ізонітрил необхідно гідролізувати. У пробирку додають 1 мл 10 %-ного розчину сульфатної кислоти і кип’ятять суміш до зникнення характерного запаху.
Опит 30. Лігнінова проба
На шматочки газетного і фільтрувального паперу з допомогою скляної палички наносять по 1 краплі хлоридної солі аніліну, отриманої в опиті 26. Забарвлення фільтрувального паперу, що складається з практично чистої целюлози, не змінюється. На газетному папері, що містить, окрім целюлози, лігнін, з'являється жовто-помаранчева пляма.
Опит 31. Бромування аніліну
У пробірку поміщають 1 краплю аніліну і 5-6 крапель води. Вміст пробірки енергійно струшують і до отриманого розчину по каплях додають бромну воду. Спостерігають знебарвлення жовто-бурого забарвлення бромної води і виділення білого осаду 2,4,6-триброманіліну.
Опит 32. Окислення аніліну
На предметне скло на відстані 2см один від одного наносять 3 краплі хлоридної солі аніліну, отриманої в опиті 26.
До першої краплі додають 1 краплю 10 %-ного розчину калію дихромату і 1 краплю 10 %-ного розчину сульфатної кислоти. Спостерігають перехід забарвлення від темно-зеленого до темно-синього, а потім - чорного.
До другої краплі додають 1 краплю насиченого розчину кальцію гипохлорит-хлориду. Спостерігають перехід від темно-фіолетового до темно-синього забарвлення.
До третьої краплі додають 1 краплю 2 %-ного розчину калію хлорату. Спостерігають появу пурпурово-фіолетового забарвлення.
Хід роботи:
Підготуйте робоче місце.
Виконайте опити згідно методики.
Запишіть рівняння реакцій, що відбуваються.
Зробіть висновок щодо досягнення цілі дослідження.
Приберіть за собою робоче місце.
