
- •Передмова
- •3. Зміст навчання.
- •Заняття №1 класифікація та номенклатура органічних сполук актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод)
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод)
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод)
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Короткі методичні вказівки до роботи на практичному занятті
- •Заняття № 5. Алкани та циклоалкани Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод)
- •1. План опису механізму реакцій радикального заміщення
- •2. Інструкція з виконання лабораторних дослідів Хімічні властивості алканів та циклоалканів
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття № 6 ненасичені вуглеводні: алкени, алкіни, алкадієни Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод)
- •1. План опису механізму реакцій електрофільного приєднання
- •2. Інструкція з виконання лабораторних дослідів Хімічні властивості ненасичених вуглеводнів
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Тест 10
- •Тест 11
- •Тест 12
- •Короткі методичні вказівки до проведення практичного заняття
- •Заняття №7 моноядерні арени. Реакції електрофільного заміщення в аренах і правила орієнтації замісників актуальність теми
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод)
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття № 8
- •Багатоядерні арени
- •З конденсованими іІзольованими ядрами
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод)
- •1. Інструкція з виконання лабораторних дослідів Хімічні властивості багатоядерних аренів
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття № 9 галогенопохідні вуглеводнів. Реакції нуклеофільного заміщення та елімінування актуальність теми
- •Цілі навчання
- •Орієнтовна основа дії (оод)
- •1. План опису механізму реакцій нуклеофільного заміщення
- •2. Інструкція з виконання лабораторних дослідів Хімічні властивості галогенпохідних вуглеводнів
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Короткі методичні вказівки до проведення практичного заняття
- •Заняття №10 нітросполуки. Аміни. Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод)
- •Завдання для перевірки досягнення конкретних цілей навчання Тест 1
- •Заняття № 11 діазо- та азосполуки. Теорія колірності актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Діазо- та азосполуки
- •Азосполуки
- •Орієнтовна основа дії (оод) Інструкція з виконання лабораторних дослідів Хімічні властивості діазо- та азосполук
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття №12 cпирти. Аміноспирти. Етери актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод) Інструкція з виконання лабораторних дослідів Хімічні властивості спиртів, аміноспиртів та етерів
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття №13 Феноли. Амінофеноли Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод) Інструкція з виконання лабораторних дослідів Хімічні властивості фенолів та амінофенолів
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття №14 Аліфатичні альдегіди та Аліфатичні кетони Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод) Інструкція з виконання лабораторних дослідів Хімічні властивості аліфатичних альдегідів та кетонів
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття №15 Ароматичні альдегіди та кетони Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод) Інструкція з виконання лабораторних дослідів Хімічні властивості ароматичних альдегідів та кетонів
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття №16 Монокарбонові кислоти Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод) Інструкція з виконання лабораторних дослідів Хімічні властивості монокарбонових кислот
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття №17 Дикарбонові кислоти Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод)
- •1. Алгоритм складання синтезу за участю малонового естеру
- •2. Інструкція з виконання лабораторних дослідів Хімічні властивості дикарбонових кислот
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття №18 Функціональні похідні карбонових кислот Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод) Інструкція з виконання лабораторних дослідів Хімічні властивості функціональних похідних карбонових кислот
- •Завдання для перевірки досягнення конкретних цілей навчання Тест 1
- •Заняття №19 гетероФункціональні карбоновІ кислотИ. Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод) Інструкція з виконання лабораторних дослідів Хімічні властивості гетерофункціональних карбонових кислот
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття №20 похідні вугільної кислоти Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод) Інструкція з виконання лабораторних дослідів Хімічні властивості вугільної кислоти
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття № 21 Колоквіум : «Вуглеводні та їх функціональні похідні» Цілі навчання
- •Зміст навчання
- •Заняття №22 Підсумковий модульний контроль
Зміст навчання
Основні теоретичні питання:
Електронна будова бензолу. Ароматичні властивості. Загальні критерії ароматичності.
Номенклатура та ізомерія моноядерних аренів.
Способи отримання моноядерних аренів:
Фізичні й хімічні властивості:
реакції електрофільного заміщення (SE).Механізми нітрування, сульфування, галогенування, алкілування, ацилювання. Роль каталізатора;
реакції приєднання та окислення ;
галогенування гомологів бензолу за участю бокового ланцюга.
Вплив замісників у бензольному кільці на напрям та швидкість реакцій електрофільного заміщення.
Узгоджена та неузгоджена орієнтація в дизаміщених бензолу.
Ідентифікація моноядерних аренів.
Окремі представникі. Використання.
Граф логічної структури
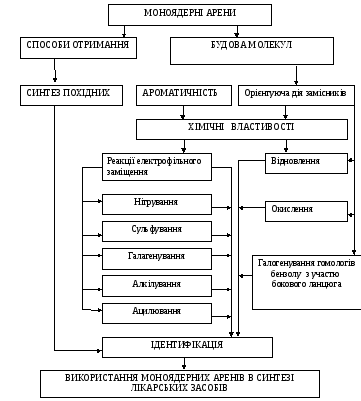
Джерела інформації
Обов'язкова література:
Органічна хімія. Підручник для вищих фармацевтичних закладів освіти. У 2 кн. / В.П. Черних, Б.С.Зіменковський, І.С.Гріценко,- Харків; Основа, 1997.- Кн.2,-с.88-117.
Черных В.П., Лекции по органической химии- Харків; Золоті сторінки, 2005 с.123-200.
Общий практикум по органической химии / В.П. Черних и др..- Харків: Изд-во НФАУ; Золотые страницы, 2002.-с.190-198.
Сборник тестов по органической химии/ Под ред. В.П.Черных. – Харків 2005.-с. 109-142.
Лекція з органічної хімії за темою: ”Вуглеводні. Поняття про ароматичні вуглеводні. Моноядерні арени. Правила орієнтації”.
Додаткова література:
Моррисон Р., Бойд Р. Органическая химия. Пер.с англ. - М.: Мир, 1974.
Степаненко Б.Н. Курс органической химии. В 2-х ч. - М.: Высшая школа, 1981.
Некрасов В.В. Руководство к малому практикуму по органической химии. - М.:Химия, 1975.
Орієнтовна основа дії (оод)
1. Алгоритм виявлення ознак ароматичності органічних сполук

2. План опису механізму реакцій електрофільного заміщення

3. Інструкція з виконання лабораторних дослідів
Хімічні властивості одноядерних аренів
Принцип методу:особливості хімічних властивостей бензолу та його гомологів витікають з особливостей будови, тобто наявності ароматичної структури. Для сполук цього класу характерні реакції електрофільного заміщення.
Ціль:за допомогою характерних реакцій практично довести хімічні властивості представників класу ароматичних вуглеводнів.
Обладнання та реактиви: штатив з пробирками, пробкa з газовідвідною трубкою, предметне скло, скляна паличка, піпетки, лакмусовий папір, пальник, повітряний холодильник, водяна лазня, 1 %-ний р-н KMnO4, конц. H2SO4, 5 %-ний р-н H2SO4, конц. HNO3, толуол, бензол, п-диметилбензол.
Методика виконання:
Опит 7. Нітрування ароматичних вуглеводнів
У суху пробірку поміщають 3 краплі концентрованої сульфатної кислоти, 2 краплі концентрованої нітратної кислоти і 2 краплі толуолу. Вміст пробірки нагрівають в полум'ї пальника, а потім виливають в пробірку з 10 каплями води. Наявність продуктів нітрування встановлюють по характерному запаху, що нагадує запах гіркого мигдалю.
Опит 8. Сульфування бензолу і його гомологів
У три сухі пробірки окремо поміщають по 10 крапель бензолу, толуолу і п-ксилолу (п-диметилбензолу), а потім підливають по 1 мл концентрованої сульфатної кислоти. Пробірки закривають пробками з повітряними холодильниками і нагрівають на водяній лазні (60-80 °С) при частому і енергійному струшуванні. Спостерігають поступове зникнення емульсії в пробірках і утворення гомогенних розчинів. Після охолодження реакційної маси вміст пробірок виливають в склянки з холодною водою. Спостерігають відсутність органічного шару над водою, що свідчить про повне сульфування вуглеводнів (сульфокислоти добре розчинні у воді).
Опит 10. Окислення бокових ланцюгів гомологів бензолу
У пробірку поміщають 1 краплю 1 %-ного розчину калію перманганату, 5 крапель води, 1 краплю 5 %-ного розчину сірчаної кислоти і 1 краплю толуолу. Вміст пробірки енергійно струшують нагрівають в полум'ї пальника. Спостерігають знебарвлення рожево-фіолетового забарвлення розчину, що пояснюється окисленням бокового ланцюгу в молекулі толуолу.
Хід роботи:
Підготуйте робоче місце.
Виконайте опити згідно методики.
Запишіть рівняння реакцій, що відбуваються.
Зробіть висновок щодо досягнення цілі дослідження.
Приберіть за собою робоче місце.
