
- •Передмова
- •3. Зміст навчання.
- •Заняття №1 класифікація та номенклатура органічних сполук актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод)
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод)
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод)
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Короткі методичні вказівки до роботи на практичному занятті
- •Заняття № 5. Алкани та циклоалкани Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод)
- •1. План опису механізму реакцій радикального заміщення
- •2. Інструкція з виконання лабораторних дослідів Хімічні властивості алканів та циклоалканів
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття № 6 ненасичені вуглеводні: алкени, алкіни, алкадієни Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод)
- •1. План опису механізму реакцій електрофільного приєднання
- •2. Інструкція з виконання лабораторних дослідів Хімічні властивості ненасичених вуглеводнів
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Тест 10
- •Тест 11
- •Тест 12
- •Короткі методичні вказівки до проведення практичного заняття
- •Заняття №7 моноядерні арени. Реакції електрофільного заміщення в аренах і правила орієнтації замісників актуальність теми
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод)
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття № 8
- •Багатоядерні арени
- •З конденсованими іІзольованими ядрами
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод)
- •1. Інструкція з виконання лабораторних дослідів Хімічні властивості багатоядерних аренів
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття № 9 галогенопохідні вуглеводнів. Реакції нуклеофільного заміщення та елімінування актуальність теми
- •Цілі навчання
- •Орієнтовна основа дії (оод)
- •1. План опису механізму реакцій нуклеофільного заміщення
- •2. Інструкція з виконання лабораторних дослідів Хімічні властивості галогенпохідних вуглеводнів
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Короткі методичні вказівки до проведення практичного заняття
- •Заняття №10 нітросполуки. Аміни. Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод)
- •Завдання для перевірки досягнення конкретних цілей навчання Тест 1
- •Заняття № 11 діазо- та азосполуки. Теорія колірності актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Діазо- та азосполуки
- •Азосполуки
- •Орієнтовна основа дії (оод) Інструкція з виконання лабораторних дослідів Хімічні властивості діазо- та азосполук
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття №12 cпирти. Аміноспирти. Етери актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод) Інструкція з виконання лабораторних дослідів Хімічні властивості спиртів, аміноспиртів та етерів
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття №13 Феноли. Амінофеноли Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод) Інструкція з виконання лабораторних дослідів Хімічні властивості фенолів та амінофенолів
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття №14 Аліфатичні альдегіди та Аліфатичні кетони Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод) Інструкція з виконання лабораторних дослідів Хімічні властивості аліфатичних альдегідів та кетонів
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття №15 Ароматичні альдегіди та кетони Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод) Інструкція з виконання лабораторних дослідів Хімічні властивості ароматичних альдегідів та кетонів
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття №16 Монокарбонові кислоти Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод) Інструкція з виконання лабораторних дослідів Хімічні властивості монокарбонових кислот
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття №17 Дикарбонові кислоти Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод)
- •1. Алгоритм складання синтезу за участю малонового естеру
- •2. Інструкція з виконання лабораторних дослідів Хімічні властивості дикарбонових кислот
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття №18 Функціональні похідні карбонових кислот Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод) Інструкція з виконання лабораторних дослідів Хімічні властивості функціональних похідних карбонових кислот
- •Завдання для перевірки досягнення конкретних цілей навчання Тест 1
- •Заняття №19 гетероФункціональні карбоновІ кислотИ. Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод) Інструкція з виконання лабораторних дослідів Хімічні властивості гетерофункціональних карбонових кислот
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття №20 похідні вугільної кислоти Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Граф логічної структури
- •Орієнтовна основа дії (оод) Інструкція з виконання лабораторних дослідів Хімічні властивості вугільної кислоти
- •Завдання для перевірки досягнення конкретних цілей навчання
- •Заняття № 21 Колоквіум : «Вуглеводні та їх функціональні похідні» Цілі навчання
- •Зміст навчання
- •Заняття №22 Підсумковий модульний контроль
Орієнтовна основа дії (оод)
1. План опису механізму реакцій нуклеофільного заміщення
Утворення
нестійкого перехідного стану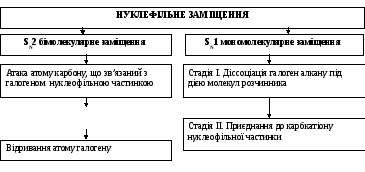
2. Інструкція з виконання лабораторних дослідів Хімічні властивості галогенпохідних вуглеводнів
Принцип методу:наявність атому галогену в вуглеводні створює умови для проведення подібних реакцій ідентифікації для всіх речовин цього класу. Хімічні властивості галогенпохідних вуглеводнів значно відрізняються в залежності відбудови вуглецевого залишку.
Ціль:за допомогою характерних реакцій практично довести хімічні властивості представників класу галогенпохідних вуглеводнів
Обладнання та реактиви: штатив з пробирками, чистий та технічний хлороформ, хлорбензен, бензилхлориду, 10 %-ний р-н KI, 5 %-ний р-н NaOH, 5 %-ного р-н HNO3, крохмальний клейстер, 4 %-ний спиртовий р-н AgNO3, 1 %-ний р-н AgNO3.
Методика виконання:
Опит 17. Визначення доброякісності хлороформу
Хлороформ під дією світла і кисню повітря поступово окислюється з утворенням хлороводню і отруйного фосгену, який при подальшому окисленні розкладається до карбон (IV) оксиду і вільного хлору.
Паралельно для порівняння проводять досліди з очищеним хлороформом.
Для відкриття хлороводню в пробірку поміщають 2 краплі технічного хлороформу, додають 3 краплі води і 2 краплі 1 %-ного розчину срібла нітрату. У пробірці з технічним хлороформом спостерігають появу муті білого кольору.
Для відкриття хлору в пробірку поміщають 3 краплі технічного хлороформу, додають 5 крапель води і 1 краплю 10 %-ного розчину калію йодиду. Вміст пробірки перемішують і за наявності вільного хлору в розчині спостерігають забарвлення нижнього хлороформного шару в рожевий колір.
Відсутність рожевого забарвлення свідчить про те, що розчин не містить йоду, а отже, і домішок хлору. Якщо забарвлення розчину слабке і з'являється сумнів в наявності йоду, додають 1 краплю крохмального клейстеру. Спостерігають появу фіолетового забарвлення розчину.
Опит 18. Гідроліз сполук, що містять галогени в ароматичному ядрі і боковому ланцюзі
У одну пробірку поміщають 2 краплі хлорбензену, в іншу - 2 краплі бензилхлориду і додають по 6-8 крапель 5 %-ного раствора натрію гідроксиду. Вміст пробірок нагрівають до кипіння і додають по 2 краплі 1 %-ного розчину срібла нітрату. У пробірці з бензилхлоридом спостерігають появу білого осаду :
У пробірці з хлорбензеном видимих змін не спостерігають.
Опит 19. Проба Бельштейна
Аналізовану пробу наносять на кінець заздалегідь прожареного мідного дроту і нагрівають в полум'ї пальника, що не світиться. За наявності в пробі галогенів полум'я пальника забарвлюється в зелений колір.
Опит 21. Відщеплення галогену під дією спиртового розчину срібла нітрату
Опит проводять паралельно з різними галогенпохідними вуглеводнів, заздалегідь промитими водою для усунення можливих домішок.
У суху пробірку поміщають 1 мл 4 %-ного спиртового розчину срібла нітрату і 1 краплю досліджуваної сполуки. Якщо впродовж 1-2 хв не виділяється осад срібла галогеніду, то вміст пробірки нагрівають до кипіння. Осади срібла галогенідів, на відміну від інших можливих сполук, не розчиняються при додаванні 2-3 крапель 5 %-ного розчину азотної кислоти.
Хід роботи:
Підготуйте робоче місце.
Виконайте опити згідно методики.
Запишіть рівняння реакцій, що відбуваються.
Зробіть висновок щодо досягнення цілі дослідження.
Приберіть за собою робоче місце.
