
- •Коллектив авторов
- •Глава 1. Строение и функции
- •Глава 8. Химический пилинг. -
- •Глава 1
- •1.1. Эпидермис
- •1.3. Гиподерма
- •1.4. Иннервация кожи
- •1.7. Иммунная система кожи
- •Глава 2 старение кожи
- •2.1. Естественное старение кожи
- •2.2. Фотостарение кожи
- •2.3. Методы профилактики старения кожи
- •Глава 3
- •3.2. Основы для наружных средств
- •3.3. Лекарственные формы
- •3.4. Специфические наружные средства
- •Глава 4
- •4.1. Компоненты косметических средств для ухода за кожей
- •4.2. Косметические средства для личной гигиены
- •4.4. Кремы
- •4.5. Декоративная косметика
- •4.6. Камуфлирование дефектов на коже
- •Глава 5
- •5.8. Другие
- •Глава 6
- •Глава 7
- •8.2. Поверхностный химический пилинг
- •8.3. Средний химический пилинг
- •Глава 9
- •Глава 10
- •10.1. Краткий обзор
- •Глава 11 угри (acne)
- •11.3. Тактика лечения
- •11.6. Амбулаторное лечение
- •11.7. Косметические средства
- •Глава 12
- •12.1. Розовые угри (rosacea)
- •12.3. Периоральный дерматит
- •Глава 13 рубцы
- •13.2. Факторы, влияющие на формирование рубца
- •13.3. Клинические варианты рубцов
- •13.4. Лечение келоидных и гипертрофических рубцов
- •Глава 14
- •14.3. Клинические проявления и диагностика впч-инфекции
- •Глава 15 болезни ногтей
- •15.5. Лечение ониходистрофий
- •Глава 16 опухоли кожи
- •16.1. Классификации опухолей кожи
1.7. Иммунная система кожи
В связи с тем что этот раздел является чрезвычайно объемным и сложным, мы посчитали целесообразным рас- сказать о роли иммунной системы ко- жи лишь в том объеме, который соч- ли необходимым для дерматокосмето- логов.
Кожу с ее многочисленными кро- веносными, лимфатическими сосуда- ми, региональными лимфатическими узлами, циркулирующими лимфоцита-
ми и другими иммунными клетка- ми многие рассматривают как само- стоятельную иммунологическую еди- ницу.
Клеточные компоненты иммунной системы кожи. Т-лимфоциты могут циркулировать в нормальной коже, где они, вероятно, и созревают. Сущест- вуют различные типы Т-клеток: Т-хел- перы, облегчающие иммунные реак- ции, Т-клетки, участвующие в реак- циях замедленной чувствительности (специфические сенсибилизаторы), ци- тотоксические Т-клетки и Т-супрессо- ры, влияющие на другие лимфоциты [66].
Поверхностные рецепторы, обнару- живающиеся с помощью монокло- нальных антител на мембранах клеток, помогают определить подтипы лимфо- цитов. Т-хелперы часто имеют CD4- рецептор, а Т-супрессоры — CD8-pe- цепторы, хотя и не всегда. Кроме того,
3*
35
на поверхности Т-клеток располагает- ся большое количество поверхностных рецепторов. Среди них выделяют многочисленные Т-клеточные рецеп- торы, которые отвечают за распозна- вание специфического антигенного пептида, связанного с главным ком- плексом тканевой гистосовместимости (МНС). В-лимфоцитов в здоровой ко- же не обнаруживают, но нередко вы- являют при ряде заболеваний.
Другими клеточными компонента- ми иммунной системы кожи являются тканевые базофилы, эпителиоциты, гистиоциты и клетки Лангерганса, строение и функции которых рассмат- ривались выше [65].
Иммуногенетические компоненты. Тканевые индивидуальные антигены находятся в МНС, локализованном у человека на HLA-гене, расположен- ном на 6-й хромосоме. МНС II клас- са — антигены, в основном HLA-DR, экспрессированы на В-лимфоцитах, клетках Лангерганса, некоторых Т-клет- ках, макрофагах и эпителиоцитах. Они жизненно важны для иммунного рас- познавания, а также при транспланта- ции [73].
Кроме того, появление определен- ных HLA-генов связано с повышенной вероятностью возникновения ряда за- болеваний, часть которых имеет ауто- иммунную природу (табл. 1.2).
Функциональные компоненты иммун- ной системы кожи. Цитокины — водо- растворимые молекулы, синтезируют-
Таблица 1.2. Примеры заболеваний кожи, ассоциированных с HLA-антиге- нами
|
Заболевание |
HLA-антиге- ны |
Частота, % |
|
Псориаз |
В13, Bw37, Cw23 |
21 (6) 4(2) 70 (23) |
|
Болезнь Рейтера |
В27 |
78 (8) |
|
Герпетиформ- ный дерматит |
В8 |
77 (25) |
Примечание. В скобках — показатель у здо- ровых людей.
Таблица 1.3. Некоторые цитокины, син- тезируемые в коже [14]
|
Цитокины |
Источник |
Действие |
|
у-Интер- ферон |
Т-клетки, натураль- ные кил- леры |
HLA-DR и ICAM- 1-экспрессия, дифференциров- ка В-клеток |
|
ИЛ-1 |
Клетки Лангерган-са, Т-клет- ки, макро- фаги, эпи- телиоциты |
Активация Т-кле- ток и макрофагов, пролиферация В-клеток |
|
ИЛ-2 |
Активиро- ванные Т-клетки |
Высвобождение Т-клеточных ци- токинов, проли- ферация В-клеток |
|
ИЛ-3 |
Т-клетки |
Универсальный специфический фактор роста |
ся множеством клеток кожи: Т-клет- ками, клетками Лангерганса, эпите- лиоцитами, фибробластами, эндотели- альными клетками и макрофагами и способствуют взаимодействию между ними (табл. 1.3) [14, 64, 70, 75]. Т-клеточные цитокины разделяют- ся на Th-1-цитокины — прототипы Y-интерферона и Th-2-цитокины, включающие ИЛ-4, -5, -10. Сущест- вует гипотеза, что развитие псориаза и аллергического контактного дерма- тита во многом связано с нарушением Th-1-цитокинов, в то время как про- тотипом Th-2-опосредованных дерма- тозов является атопический дерматит [74].
Эйкозаноиды представляют собой неспецифические воспалительные ме- диаторы (например, простагландины, тромбоксаны и лейкотриены) и син- тезируются из арахидоновой кислоты тканевыми базофилами, макрофагами и эпителиоцитами.
Активация комплемента может про- ходить по классическому или альтер- нативному пути и приводит к различ- ным молекулярным эффектам: опсо- низации, лизису, дегрануляции тка- невых базофилов, сокращению глад-
36
кой мускулатуры и хемотаксису ней- трофилов и макрофагов.
Молекулы адгезии, особенно ICAM-1, поверхностные молекулы мембран клетки, обнаруживаются в лимфоцитах и иногда в эндотелиаль- ных клетках и эпителиоцитах. Взаи- модействуя с антигенами, они способ- ствуют присоединению к Т-лимфоци- там [69].
При воспалительных процессах в коже и аутоиммунных дерматозах от- мечают различные нарушения в им- мунных клетках и продукции цитоки- нов. Корректируя эти патологические реакции, в перспективе можно будет добиться полного излечения или дли- тельных ремиссий при многих заболе- ваниях кожи, тем более что уже сейчас исследования способов регуляции им- мунного ответа привели к созданию средств, влияющих на механизм пред- ставления антигенов, молекулы адге- зии и цитокины [75]. Интересно от- метить, что наряду с системными иммуномодулирующими препаратами появились аналогичные, но наружного действия. Один из них, имиквимод, лишенный системных побочных эф- фектов, с успехом применяется при заболеваниях, ассоциированных с ви- русом папилломы человека, актини- ческом кератозе, базально-клеточном раке и даже при меланоме [63]. Другие наружные препараты, подавляющие активацию Т-клеток, такролимус и пимекролимус, оказались эффектив- ными у больных атопическим дерма- титом.
Аллергические реакции на коже. Тер- мин "аллергия" используется в тех случаях, когда иммунная реакция не соответствует силе воздействия аллер- гена и приводит к повреждению ткани. В коже отмечаются все основные типы аллергических реакций.
При аллергической реакции немед- ленного типа (I тип) IgE связываются с поверхностью тучных клеток с по- мощью Fc-рецепторов (рис. 1.16).
При контакте с антигеном (напри- мер, содержащимся в пище или пыли) молекулы IgE прикрепляются к тка-

Рис. 1.16. Реакция немедленного типа. 1 — антиген; 2 — IgE; 3 — Fc-рецептор; 4 — гранулы тканевых базофилов; 5 — выделен- ные медиаторы воспаления.

Рис. 1.17. Цитотоксическая реакция, опос- редованная антителами. I — цитотоксический эффект; II — активация комплемента; III — комплементзависимый лизис. 1 — Fc-рецептор; 2 — Т-киллерный лимфоцит; 3 и 5 — IgG; 4 — антиген; 6 — клетки-мишени базальной мембраны.
невым базофилам, вызывая их дегра- нуляцию. Последнюю могут вызывать не только IgE, но и другие факторы. Этот процесс происходит с высвобож-
37
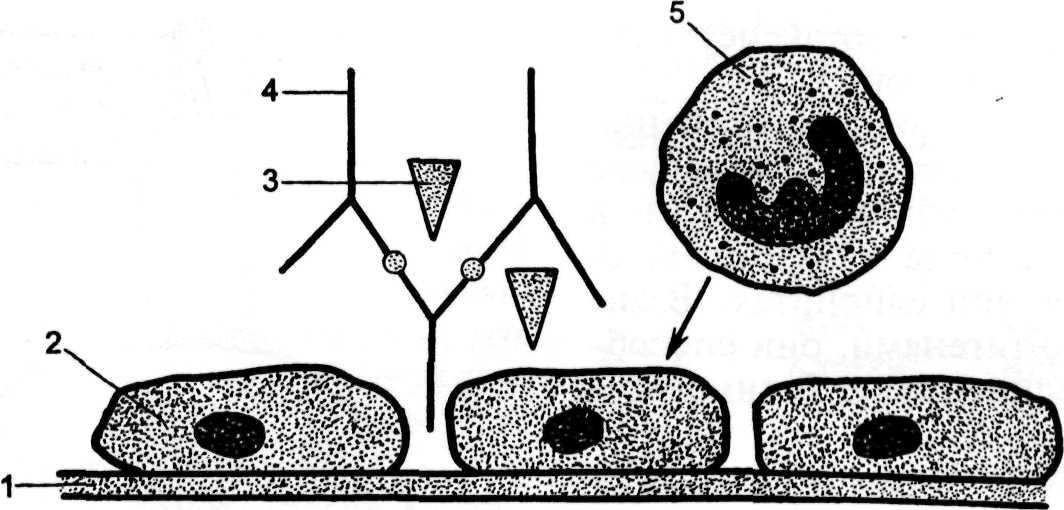
1 — базальная мембрана; 2 — эндотелиальная клетка; 3 — активация комплемента; 4 — ком- плекс IgG — антиген; 5 — хемоаттрактанты полиморфно-ядерных лейкоцитов.

1 — рецепторы; 2 — HLA-DR; 3 — антиген; 4 — клетка Лангерганса; 5 — макрофаг; 6 — сенси- билизированный Т-лимфоцит.
дением воспалительных медиаторов типа гистамина, простагландинов и лейкотриенов. В результате на коже появляется уртикарная сыпь, а при массированном высвобождении ги- стамина — анафилаксия. Несмотря на то что реакция немедленного типа длится несколько минут, в нее часто вовлекаются реакции замедленного типа.
В основе цитотоксических реакций,
опосредованных антителами (II тип), лежит выработка антител против анти- генов клеток-мишеней или отдельных структур кожи, индуцируемая цито- токсическим действием Т-киллерных клеток или активацией комплемента (рис. 1.17). Например, IgG-антитела при пузырчатке, направленные против поверхностных антигенов эпителио- цитов, приводят к активации энзимов, аттракции эффекторных клеток и ли-
38
зису эпителиоцитов. В результате об- разуются внутриэпидермальные пузы- ри. Другим примером гиперчувстви- тельности являются гемолитическая анемия и реакции на переливание не- совместимой крови.
Аллергические реакции, при кото- рых иммунные комплексы формиру- ются и откладываются на стенках мел- ких сосудов, относят к III типу. Эти комплексы индуцируют активацию комплемента, агрегацию тромбоцитов и выход лизосомальных ферментов из полиморфно-ядерных лейкоцитов, что приводит к повреждению сосудов (рис. 1.18). Такой тип реакций наблюдают при системной красной волчанке, дер- матомиозите и инфекционном эндо- кардите [67].
Во время клеточно-опосредованной аллергической реакции IV типа спе- цифически сенсибилизированные Т- лимфоциты вступают в повторный контакт с антигеном, представленным на поверхности антигенпрезентирую- щих клеток (рис. 1.19).
При этом высвобожденные цитоки- ны индуцируют активацию Т-кле- ток и усиливают реакцию за счет учас- тия других Т-клеток и макрофагов. В результате этого процесса в течение 48—72 ч происходит значительное по- вреждение ткани. Примерами реакций IV типа являются контактный аллер- гический дерматит, лепра, туберкулез и реакция на внутрикожное введение туберкулина.
ТЕСТЫ
1.Укажите функцию, не свойственную коже:
а)всасывание;
б)выделение;
в)барьерная;
г)образование токсинов; ^\
д)органа чувств.
2.Из перечисленных структур в состав дермоэпидермального соединения не входят:
а)наружная клеточная мембрана базальных эпителиоцитов;
б)светлая пластинка;
в)базальная пластинка;
г)фиброретикулярная пластинка;
д)кератиносомы.
3.Укажите, какие клетки не определя- ют в эпидермисе:
а)эпителиоциты;
б)клетки Меркеля;
в)клетки Лангерганса;
г)фибробласты;
д)меланоциты.
4.Укажите слой эпидермиса, в котором образуются тельца Одланда:
а)базальный; г) блестящий;
б)шиповатый; д) роговой.
в)зернистый;
5.Из перечисленных факторов тормо- зит деление эпителиоцитов и способ-ствует их дифференцировке:
а)эпидермальный фактор роста;
б)трансформирующий фактор ро- ста а;
в)трансформирующий фактор ро- ста Р;
г)фактор роста фибробластов;
д)все перечисленные.
6.Ключевой аминокислотой в синтезе меланина является:
а)тирозин;г) гистидин;
б)аланин;д) фенилаланин.
в)метионин;
7.Укажите, какие клетки не определя- ют в дерме:
а)гистиоциты;
б)фибробласты;
в)эпителиоциты;
г)тканевые базофилы;
д)макрофаги.
8.Из перечисленных компонентов в состав межклеточного матрикса дер- мы не входят:
а)основное вещество дермы;
б)адгезивные белки;
в)фибробласты;
г)коллагеновые волокна;
д)эластиновые волокна.
9.Укажите, какие волокна отсутствуют в дерме:
а)коллагеновые; :
б)эластические;
в)ретикулярные;
г)гиалиновые;■ , ■
д)нервные.
10. Укажите стадию развития волос, на которой наблюдается их выпаде- ние:
а)анагенная; в) телогенная.
б)катагенная;
39
11. Из перечисленных желез в коже от- сутствуют:
а)одноклеточные;
б)эккринные;
в)апокринные;
г)голокринные;
д)эндокринные.
12.На тактильное воздействие отвечают:
а)ноцирецепторы;
б)терморецепторы;
в)колбы Краузе;
г)тельца Фатера—Пачини;
д)тельца Мейсснера.
13.Какова основная функция гломус- ных телец:
а)сенсорная;
б)осязательная;
в) усиление тока крови в коже;
г) иммунная;
д) фотозащита. ....-.,.
Правильные ответы: 1г; 2д; Зг; 46; 5в; 6а; 7в; 8в; 9г; Юв; Па; 12д; 13в.
СПИСОК ЛИТЕРАТУРЫ
Строение и функции эпидермиса
Гетлинг З.М. Ультраструкгура эпидер- миса и его барьерная функция // Эс- тетическая медицина. — 2002. — Т. 1, № 3. - С. 208-214.
Мордовцев В.Н., Цветкова Г.М. Пато- логия кожи. — М.: Медицина, 1993.
Asselineau D., Bernard В.А., Bailly С, Darmon M. Retinoic acid improves epi- dermal morphogenesis // Develop. Biol. —
1989. - Vol. 133. - P. 322-325.
Barrandon Y., Green H. Three clonal types of keratinocytes with different capacities for multiplication // Proc. Nat. Acad. Sci. USA. - 1987. - Vol. 84. - P. 2302- 2306.
Bikle D.D. l,25(OH)2D3-modulated cal- cium induced keratinocyte differentiati- on // J. Invest. Dermatol. Symp. Proc. — 1995.-Vol. l.-P. 22-27.
Braun-Falco O., Plewig G., Wolff H.H. Dermatology. — Berlin: Springer, 2000.
Briggaman R.A. Epidermal-dermal junction structure, composition, function and dis- ease relationships // Progr. Dermatol. —
1990. - Vol. 24. - P. 1.
8. Dale B.A. Filaggrins. Cellular and Molecu- lar Biology of Intermediate Filments / Ed. R.W. Goldman, P.M. Steinert. — New York: Plenum, 1990. - P. 393.
9. DiPerslo СМ., Hodivala-Dilke KM., Jaenisch R. et al. Integrin is required for normal development of the epidermal basement membrane // J. Cell Biol. — 1997. - Vol. 137. - P. 729-742.
Feingold K.R. The regulation and role of epidermal lipid synthesis // Adv. Lipid Res. — 1991. — Vol. 24. — P. 57—82.
Fine J.D., McGrath J., Eady R.A. Inherited epidermolysis bullosa comes into the new millennium: A revised classification system based on current knowledge of pathoge- netic mechanisms and clinical laboratory, and epidemiologic findings of large, well- defined patient cohorts // J. Amer. Acad. Dermatol. - 2000. - Vol. 43. - P. 135— 137.
Freinkel R.K., Woodley D.T. The biology of the skin. — New York: Parthenon Pub- lishing Group, 2001.
Fuchs E., Cleveland D. A structural scattfolding of intermediate filaments in health and disease // Science. — 1998. — Vol. 279.-P. 514-519.
Gawkrodger D.J. An illustrated colour text dermatology. — New York: Churchill Liv- ingstone, 1997.
Goldsmith L. Physiology, biochemistry, and molecular biology of the skin. — New York: Oxford University Press, 1991.
Heisig M., Lieckfeldt R., Wittum G. et al. Non steady-state descriptions of drug per- meation through stratum corneum. I. The biphasic brick-and-mortar model // Phar- maceutical Res. — 1996. — Vol. 13. — P. 421-426.
Hohl D. Cornified cell envelope // Derma- tologica. — 1990. — Vol. 180.— P. 201— 211.
Holbrook K.A. Biologic structure and function: perspective on morphologic approaches to the study of the gra- nular layer keratinocyte // J. Invest. Dermatol. - 1989. - Vol. 94. - P. 84s- 104s.
Holick M.F., Chen M.L., Kong X.F., Sa- nan D.K. Clinical uses for calciotropic hormones 1,25-dihydroxyvitamin D3 and parathyroid hormone-related peptide in dermatology: a new perspective // J. Invest. Dermatol. Symp. Proc. — 1996. — Vol. 1. — P. 1-9.
Hynes R.O. Integrins: versality, modula- tion, and signaling in cell adhesion // Cell. - 1992. - Vol. 69. - P. 11-25.
McCall C.A, Cohen J.J. Programmed cell death in terminally differentiating kerati- nocytes: role of endogenous endonuclea- se // J. Invest. Dermatol. — 1991. —Vol. 97.-P. 111-114.
40
Milisavljevic V., Freedberg I.M., Blumen- berg M. Close linkage of the two keratin gene clusters in human genome // Genomics. - 1996. - Vol. 34. - P. 134— 138.
Moll I., Gillardon S.F., Waltering S. et al. Differences of bcl-2 protein expression between Merkel cells and Merkel cell carcinomas // J. Cutan. Pathol. — 1996.-Vol. 23.-P. 109-117.
Rothnagel J.A., Dominey A.M., Dempsey L.D. et al. Mutations in the rod domain of keratins 1 and 10 in epidermolytic hyperkeratoses // Science. — 1992. — Vol. 257.-P. 1128—1130.
Ruoslahti E. Integrals // J. Clin. In- vest. - 1991. — Vol. 87. — P.I—5.
Sakuntabhai A. Mutations in ATP2A2, encoding Сгг+ pump, cause Darier dise- ase // Nature Genet. — 1999. —Vol. 21. — P. 271—277.
Sato J., Denda M., Nacanishi J. et al. Cholesterol sulfate inhibits proteases that are involved in desquamation of stratum corneum // J. Invest. Dermatol. — 1998. — Vol. 111.-P. 189-193.
Smack D.P., Korge B.P., James W.D. Kera- tin and keratinization // J. Amer. Acad. Dermatol. — 1994. — Vol. 30. — P. 85— 102.
Sun T.T., Eicher R., Schemer A. Classi- fication, expression, and possible me- chanisms of evoluation of mammalian epithelial keratins: a unifuing model / In: A. Levine, W. Topp, G.N. Vande- Woude et al., eds. The Cancer Cell. — New York: Cold Spring Harbor, 1984. — P. 169.
Widelitz R.B., Jiang T.X., Noveen A. et al. Molecular histology in skin ap- pendage morphogenesis // Micros- copy Res. Tech. — 1997. — Vol. 38. — P. 452-465.
Wrone-Smith Т., Mitra R.S., Thompson C.B. et al. Keratinocytesderived from pso- riatic plaques are resistant to apoptosis compared with normal skin // Amer. J. Pathol. - 1997. - Vol. 151. - P. 1321 — 1329.
Пигментация кожи
Fulton J.E. Utilizing the ultraviolet (UV detect) camera to enhance the appearan- ce of photodamage and other skin condi- tions // Dermatol. Surg. — 1997. — Vol. 23. - P. 163—169.
McLeod S.D., Ranson M., Mason R.S. Effects of estrogens on human melanocy-
tes in vitro // J. Steroid. Biochem. — 1994.-Vol. 49.-P. 9-14.
Mishima Y. Molecular and biologic control of melagenesis through tyrosinase genes and intrinsic and extrinsic regulatory fac- tor // Pigment. Cell Res. — 1994. — Vol. 7. - P. 376-387.
Nordlund JJ. The pigmentary system: an explanded perspective // Ann. Dermatol. Venereol. — 1994. — Vol. 100. — P. 191S— 195S.
Thody A.J., Smith A.G. Hormones and skin pigmentation in the mammal // Int. J. Dermatol. - 1977. - Vol. 16. - P. 657— 664.
Thody A.J., Higgins E.H., Wakamatzu K. et al. Pheomelanin as well as eumelanin is present in human epidermis // J. In- vest. Dermatol. — 1991. — Vol. 97.— P. 340-344. ..-: ; .
Строение и функции дермы
Bayreuther К., Francz P.I., Gogol J., Kon- termanr K. Terminal differentiation, aging, apoptosis and spontaneous transformation in fibroblast stem cell systems in vivo and in vitro // Ann. NY Acad. Sci. — 1992. — Vol. 663. - P. 167-179.
Callen J.P., Tuffanelli D.L., Provost T.T. Collagen-vascular diseases: An update. // J. Amer. Acad. Dermatol. — 1993. — Vol. 28. - P. 477.
Cerio R., Griffiths C.E., Cooper CD. et al. Characterization of factor ХШа positi- ve dermal dendritic cells in normal and inflamed skin // Brit. J. Der- matol. - 1989. - Vol. 12. - P. 421— 431.
Harrop A.R., Ghahary A., Scott P.G. et al. Regulation of collagen synthesis and mRNA expression in normal and hyper- trophic scar fibroblasts in vitro by inter- feron-gamma // J. Surg. Res. — 1995. — Vol. 58. - P. 471-477.
Headington J.T., Cerio R. Dendritic cells and dermis // Amer. J. Dermapatol. — 1990. - Vol. 12. - P. 217-220.
lozzo R. V. Matrix proteoglycans: from mo- lecular designs to cellular function // Ann. Rev. Biochem. — 1998. — Vol. 67. - P. 609-652.
Kadler K.E., Holmes D.F., Trotter J.A., Chapman J.A. Collagen fibril formation // Biochem. J. — 1996. — Vol. 316. — P. 1— 11.
Lasser A. The mononuclear phagocytic system: a review // Hum. Pathol. — 1985.-Vol. 14.-P. 108-126.
.41
Latijnhouwers M., Bergers M, Ропес М. et al. Human epidermal keratinocytes are a source of tenascin-C during wound hea- ling // J. Invest. Dermatol. — 1997. — Vol. 108. - P. 776-783.
Longaker M.T., Adzick N.S., Hall J.L. et al. Studies in fetal wound healing, VII. Fetal wound healing may be modulated by hyaluronic acid stimulating activity in amniotic fluid // J. Pediatr. Surg. — 1990. — Vol. 25. — P. 430—433.
Morgan M.B., Truitt C.A., Taira J. et al. Fibronectin and the extracellular matrix in the perforating disorders of the skin // Amer. J. Dermapatol. — 1998. — Vol. 20. — P. 147-154.
Naukkarinen A., Jarvikallio A., Lakkakorpi J. et al. Quantitative histochemical analysis of mast cells and sensory nerves in pso- riatic skin // J. Pathol. — 1996. — Vol. 180. - P. 200-205.
Paige D.G., Lake B.D., Bailey AJ. et al. Restrictive dermatopathy: a disorder of fibroblasts // Brit. J. Dermatol. — 1992. — Vol. 127. - P. 630-634.
Smith L.T. Patterns of type VI colla- gen compared to types I, III, and V collagen in human embryonic and fetal skin and in fetal skin-derived cell cultures // Matrix Biol. - 1994. - Vol. 14. - P. 159— 170.
Tanaka Y., Kimata K., Adams D .H, Eto S. Modulation of cytokine function by heparan sulfate proteoglycans: sophistica- ted models for the regulation of cellu- lar responses to cytokines // Proc. Assoc. Amer. Phys. — 1998. — Vol. 110. — P. 118— 125.
Uitto J. Understanding premature skin aging // New Engl. J. Med. — 1997. — Vol. 337. - P. 1463-1465.
Zhang M.C., He L., Giro M. et al. Cutis laxa arising from frameshift mutations in exon 30 of elastin gene (ELN) // J. Biol. Chem. - 1999. - Vol. 274. - P. 981 — 986.
Придатки кожи
Dawber R. Diseases of Hair and Scalp. — Oxford: Blackwell Science, 1997.
Lavker R., Sun T.T. Epidermal stem cells // J. Invest. Dermatol. — 1983. — Vol. 81. —P. 121—127.
Sato K., Kang W.H., Saga W. et al. Biology of sweat glands and their disorders. I. Normal sweat gland function // J. Amer. Acad. Dermatol. — 1989. — Vol. 20. — P. 537-563.
58. Scher R.K., Daniel C.R. Nails: Therapy, Diagnosis, Surgery 2nd ed / Philadelphia: W.B. Saunders Co, 1997.
Иннервация кожи j
Lynn B. Cutaneous sensation // Physiol- ogy, Biochemistry, and Molecular Biology of the Skin / Ed. L.A. Goldsmith. — New York: Oxford University Press, 1991. — P. 779-815.
Munger B.L., Ide C. The structure and function of cutaneous sensory receptors // Arch. Histol. Cytol.-1988.-Vol. 51.- P. 1-34.
Кровеносная и лимфатическая система кожи
Braverman I.M. Ultrastructure and organi- zation of the cutaneous microvasculare in normal and pathologic states [Review] // J. Invest. Dermatol. — 1989. — Vol. 93 (Suppl.). - P. 2S-9S.
Ruan T. Cutaneous circulation // Physi- ology, Biochemistry, and Molecular Bio- logy of the Skin / Ed. L.A. Gold- smith. — New York: Oxford University Press, 1991. - P. 1019-1083.
Иммунная система кожи
Arani I., Tyring S.K., Trofatter K.F. En- hancement of the treatment of external genital warts treated with topical imi- quimod cream 5 % // Antiviral Res. — 1999.-Vol. 43.-P. 55-63.
Baggiolini M. Chemokines and leukocyte traffic // Nature. — 1998. — Vol. 392. - P. 565-568.
Barratt-Boys S.M., Watkins S.C., Finn O.J. In vivo migration of dendritic cells differ- entiated in vitro // J. Immunol. — 1997. - Vol. 158. - P. 4543-4547.
Bos J.D. Skin immune system / Ed. J.D. Bos. — Boca Ration: CRC Press, 1995.
Callen J.P., Tuffanelli D.L., Provost T.T. Collagen-vascular diseases: An update // J. Amer. Acad. Dermatol. — 1993. — Vol. 28. - P. 477.
Cruz PD., Bergstersser P.R. Antigen processing and presentation by epider- mal Langerhans cells: induction of im- munity or unresponsiveness // Derma- tol. Clin. — 1990. — Vol. 8. — P. 633— 647.
Dahl M.V. Clinical immunodermatolo-
42
gy / Ed. M.V. Dahl. — St. Louis: Mosby, 1996.
Dinarello C.A. The biological prop- erties of interleukin-1 // Europ. Cytokine Network. - 1994. - Vol. 5. - P.517- 531.
Enk A.H., Katz S.I. Contact sensitivity as a model for T-cell activation in skin // J. Invest. Dermatol. — 1995.—Vol. 105. — P. 80S-83S.
Kripke M.L., Munn C.G., Jeevan A. et al. Evidence that cutaneous antigen-pre- senting cells migrate to regional lymph nodes during contact sensitization //
J. Immunol. - 1990. - Vol. 145 — P. 2833-2838.
Nickolof B.J. Dermal immune system. — Boca Raton, FL: CRC Press, 1993.
Sauder D.N. Cutaneous immunobiology // Ann. Dermatol. Venereol. — 2002. — Vol. 129.— P. Is274.
Schall T.J. The Cytokines Handbook / Ed. A.W. Thomson. - London: Academic Press Ltd, 1994. - P. 419-460.
Udey M.C. Cadherins and Langerhans cell immunobiology // Clin. Exp. Immu- nol. - 1997. - Vol. 107 (Suppl. 1). - P. 6-8.
