
- •Коллектив авторов
- •Глава 1. Строение и функции
- •Глава 8. Химический пилинг. -
- •Глава 1
- •1.1. Эпидермис
- •1.3. Гиподерма
- •1.4. Иннервация кожи
- •1.7. Иммунная система кожи
- •Глава 2 старение кожи
- •2.1. Естественное старение кожи
- •2.2. Фотостарение кожи
- •2.3. Методы профилактики старения кожи
- •Глава 3
- •3.2. Основы для наружных средств
- •3.3. Лекарственные формы
- •3.4. Специфические наружные средства
- •Глава 4
- •4.1. Компоненты косметических средств для ухода за кожей
- •4.2. Косметические средства для личной гигиены
- •4.4. Кремы
- •4.5. Декоративная косметика
- •4.6. Камуфлирование дефектов на коже
- •Глава 5
- •5.8. Другие
- •Глава 6
- •Глава 7
- •8.2. Поверхностный химический пилинг
- •8.3. Средний химический пилинг
- •Глава 9
- •Глава 10
- •10.1. Краткий обзор
- •Глава 11 угри (acne)
- •11.3. Тактика лечения
- •11.6. Амбулаторное лечение
- •11.7. Косметические средства
- •Глава 12
- •12.1. Розовые угри (rosacea)
- •12.3. Периоральный дерматит
- •Глава 13 рубцы
- •13.2. Факторы, влияющие на формирование рубца
- •13.3. Клинические варианты рубцов
- •13.4. Лечение келоидных и гипертрофических рубцов
- •Глава 14
- •14.3. Клинические проявления и диагностика впч-инфекции
- •Глава 15 болезни ногтей
- •15.5. Лечение ониходистрофий
- •Глава 16 опухоли кожи
- •16.1. Классификации опухолей кожи
Глава 1
СТРОЕНИЕ И ФУНКЦИИ КОЖИ
С .Н.
Ахтямов, З.М. Гетлинг, Ю.С. Бутов
.Н.
Ахтямов, З.М. Гетлинг, Ю.С. Бутов
Кожа — метаболически активный ор- ган, площадь которого составляет 1,8 м2, масса — приблизительно 16% от массы тела. Кожа выполняет мно- жество функций:
является барьером для микроорга- низмов;
защищает от механических повреж- дений;
предотвращает потерю жидкостей из организма;
уменьшает воздействие УФ-излуче- ния;
участвует в терморегуляции;
выполняет сенсорные функции;
обеспечивает синтез витамина D;
осуществляет иммунный надзор;
выполняет дыхательную функцию;
принимает участие в обмене ве- ществ.
Кожный покров состоит из эпидер- миса, дермы и подкожной клетчатки. На рис. 1.1 показано 2 типа кожи: слева — утолщенная, без волос (на ла- донях и подошвах); справа — более тонкая, с волосяными фолликулами.
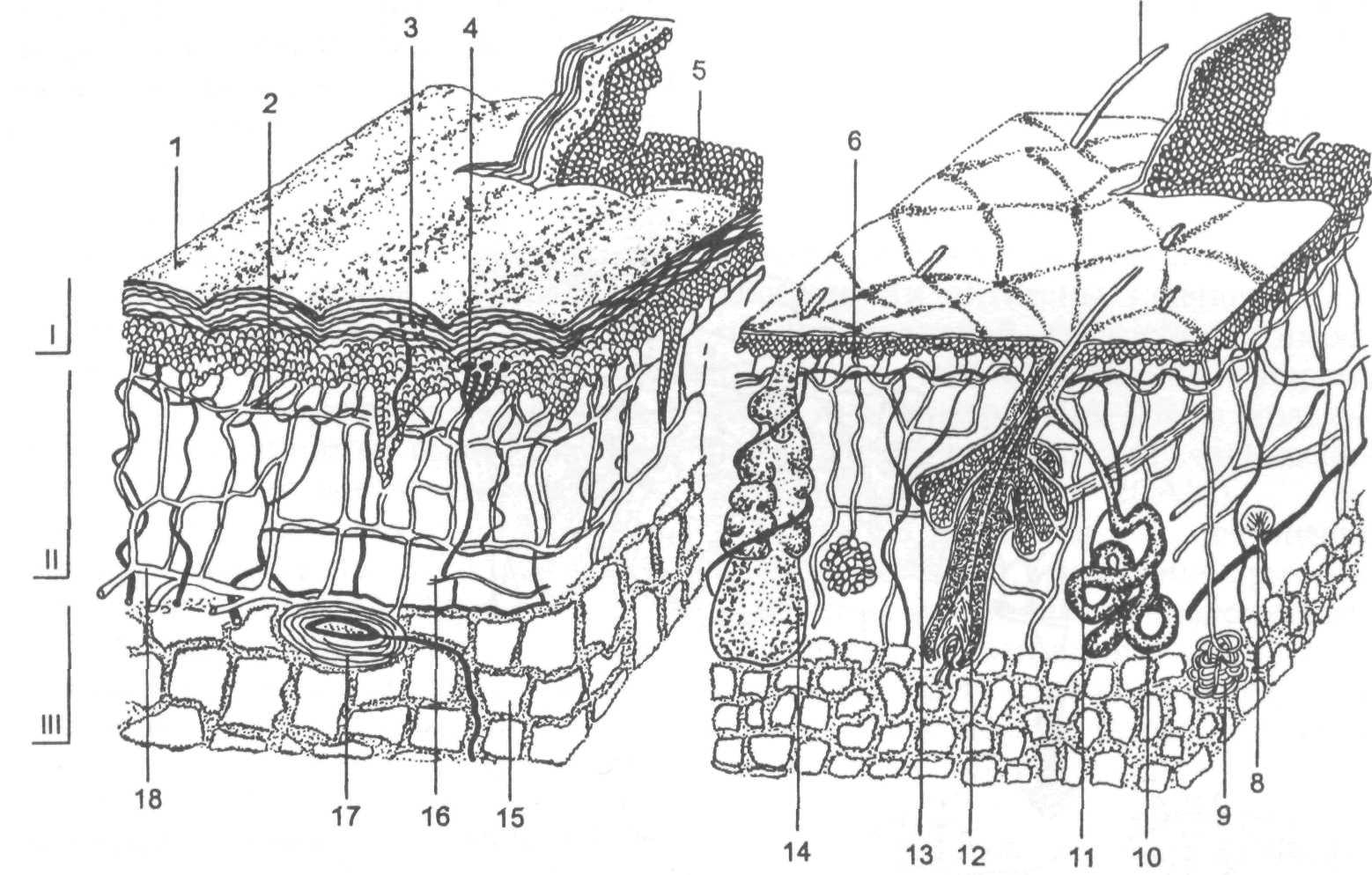
Рис. 1.1. Структура кожи.
1 — эпидермис; II — дерма; III — гиподерма. 1 — проток потовой железы; 2 — поверхностная артериовенозная сеть; 3 — свободные нервные окончания; 4 — диски Меркеля; 5 — дермальные сосочки; 6 — выводной проток эккринной железы; 7 — стержень волоса; 8 — тельце Руффини; 9 — секреторный отдел эккринной железы; 10 — апокринная железа; 11 — мышца, поднимаю- щая волос; 12 —волосяной фолликул; 13, 14 — сальная железа; 15 — подкожная клетчатка; 16 — нервные клетки; 17 — тельце Пачини; 18 — глубокая артериовенозная сеть.
1.1. Эпидермис
Эпидермис — наружный слой кожи, представлен непрерывно возобновля- ющимися эпителиальными клетками — эпителиоцитами (кератиноцитами), которые постоянно находятся в про- цессе дифференцировки, начиная с нижнего, слабо дифференцированно- го базального слоя, в направлении к верхнему роговому слою. Эпидермис состоит из нескольких типов клеток, имеющих различное эмбриональное происхождение, — эпителиоцитов, ме- ланоцитов, внутриэпидермальных мак- рофагов (клеток Лангерганса), клеток Меркеля и разделен на пять слоев (рис. 1.2): базальный, шиповатый, зернистый, блестящий и роговой, ко- торые отражают разные стадии диф- ференцировки эпителиальных эле- ментов.
Поддержание клеточного гомеоста- за в эпидермисе в целом зависит от соотношения образующихся и погиба- ющих клеток. На этот процесс влияет множество факторов: уровень взаимо-
действий эпителиоцитов с другими клетками эпидермиса; качество адге- зии эпителиоцитов друг с другом и базальной мембраной; различные за- болевания кожи, возраст и пол чело- века, климатические условия и т.д. [1].
Эпидермис не имеет строго опреде- ленной толщины, на разных участках тела она значительно варьирует: в об- ласти ладоней составляет около 0,1 мм, на подошвах — от 0,8 до 1,4 мм, на других участках тела — в среднем ме- нее 1 мм.
Эпителиоциты — основной тип кле- ток эпидермиса. Они составляют при- близительно 90—95 % клеточной мас- сы эпидермиса, их строение и функ- ции изменяются в зависимости от их расположения в эпидермисе и степени дифференцировки. Основной струк- турной единицей эпителиоцитов явля- ются тонофиламенты диаметром 8— 10 нм и их пучки (тонофибриллы) диаметром 25 нм. Вместе с микротру- бочками тонофиламенты формируют цитоскелет, поддерживающий струк- турную целостность клетки.
 Рис.
1.2. Поперечное сечение эпидермиса.
I
— базальный слой; II
— шиповатый слой;
III
— зернистый слой; IV
— роговой слой (1 —
меланоцит,
2 — клетка Лангерганса). Ниже
(показано
стрелкой) дермоэпидермальное со-
единение,
состоящее из полудесмосом (3),
светлой
(4), базальной (5) и фиброретикуляр-
ной
(6) пластинок, коллагеновых волокон
типа
I
(7), крепящих фибрилл (8), крепящих
протеинов
(9), десмосом (10).
Рис.
1.2. Поперечное сечение эпидермиса.
I
— базальный слой; II
— шиповатый слой;
III
— зернистый слой; IV
— роговой слой (1 —
меланоцит,
2 — клетка Лангерганса). Ниже
(показано
стрелкой) дермоэпидермальное со-
единение,
состоящее из полудесмосом (3),
светлой
(4), базальной (5) и фиброретикуляр-
ной
(6) пластинок, коллагеновых волокон
типа
I
(7), крепящих фибрилл (8), крепящих
протеинов
(9), десмосом (10).
12

— цитоплазма; II — плазма- тическая мембрана; III — свет- лая пластинка; IV — базальная пластинка; V — дермальный матрикс. 1 — тонофиламенты;
— буллезный пемфигоидный антиген-1 (ВР230); 3 — бул- лезный пемфигоидный анти- ген-2 (ВР180); 4 — интегрины; 5 — унцеин; 6 — тонкие фила- менты; 7 — коллагеновые во- локна IV типа; 8 — ламинин-6; 9 — ламинин-7; 10 — ретику- линовые фибриллы; 11 — эластические волокна; 12 — диски прикрепления; 13 — кол- лагеновые волокна типа VII; 14 — крепящие фибриллы.
Одна из основных фун- кций эпителиоцитов — синтез кератина. Напри- мер, роговой слой на 65 % состоит из керати- на, остальная его масса — растворимые белки (10 %), аминокислоты (10 %), липиды (10 %) и различные компонен- ты мембран клеток (5 %). Идентифи- цировано около 30 видов полипепти- дов кератина. В целом их разделяют на кислотные (К10—К20) и основ- ные/нейтральные (К1—К9) [24, 29, 31]. Генетическое картирование пока- зало, что большинство генов, ответст- венных за кислотные кератины, нахо- дится в хромосоме 17ql2—ql3, за ос- новные/нейтральные кератины — в хромосоме 12qll— ql3 [22].
Кератины — облигатные гетеропо- лимеры, состоят из молекул кислот- ного и основного а-кератина, пред- ставленного в виде свернутой спирали. Ковалентные связи, соединяющие мо- лекулы цистина, обеспечивают проч- ность кератина. Характер сборки спе- цифических пар кератинов зависит от типа клетки и ткани, состояния диф- ференцировки и наличия заболеваний кожи [28J.
Эпителиоциты выполняют важные иммунные функции: они способны
синтезировать провоспалительные ци- токины, в частности интерлейкин-1 (ИЛ-1), и могут экспрессировать на поверхности антигены главного ком- плекса тканевой гистосовместимос- ти — major histocompatibility complex, МНС (например, HLA-DR) и молеку- лы межклеточной адгезии — intercellu- lar adhesion molecules (ICAM).
Дермоэпидермальное соединение (ДЭС) — граница между эпидермисом и дермой, механически поддерживает эпидермис и выполняет барьерную функцию. ДЭС также участвует в транспорте веществ и газообмене меж- ду эпидермисом и дермой.
В состав ДЭС входят клеточная мембрана базальных эпителиоцитов с полудесмосомами, светлая пластинка (lamina lucida), базальная пластинка (lamina densa) и фиброретикулярная пластинка (см. рис. 1.2; рис. 1.3) [7, 8, 11, 12].
Вдоль клеточной мембраны через небольшие интервалы определяются
13
образования, имеющие ту же структу- ру, что и десмосомы, но с вдвое мень- шим числом слоев, в связи с чем получившие название "полудесмосо- мы". Главные компоненты полудесмо- сом: плектин, буллезный пемфигоид- ный антиген-1 (ВР230), участвующий в прикреплении тонофиламентов, бул- лезный пемфигоидный антиген-2 (ВР180), специфические рецепторы — интегрины (а6(34 и аЗр4) и коллаген типа VII. К полудесмосомам прикреп- ляются пучки тонофиламентов базаль- ных эпителиоцитов.
Светлая пластинка располагается непосредственно под клеточной мем- браной базальных эпителиоцитов. В состав светлой пластинки входят гликопротеины, играющие важную роль в адгезии между базальными клетками и базальной пластинкой, а также несколько типов уникальных белков, включая ламинины и менее известные крепящие филаментассоци- ированные белки унцеины. Эти белки обладают высокой биологической ак- тивностью и участвуют в сборке ба- зальной мембраны.
Базальная пластинка имеет фибрил- лярное строение и располагается не- посредственно под светлой пластин- кой. Она состоит из коллагеновых во- локон типа IV и гепарансульфата (пер- лекана). Тонкие крепящие фибриллы базальной пластинки пересекают свет- лую пластинку, направляясь к клеточ- ной мембране базальных эпителиоци- тов в зоне полудесмосом.
Зона, расположенная под базальной пластинкой, называется фиброретику- лярной пластинкой. Она состоит из коллагеновых, ретикулиновых и кре- пящих фибрилл. Последние присоеди- нены к базальной пластинке и закан- чиваются в дисках прикрепления в дерме. Особый интерес к фиброрети- кулярной пластинке связан с насы- щенностью ее структурами, перенося- щими рецепторы для синтеза факто- ров роста эпидермиса, и наличием множества молекул, обладающих адге- зивными свойствами (например, те- наскин). Применение технологии по-
ли- и моноклональных антител позво- лило идентифицировать несколько особых белков и протеогликанов, на- ходящихся только в ДЭС (например, кератины К5 и К14).
Базальный слой. Эпителиоциты, расположенные на базальной мембра- не, являются зародышевыми клетка- ми. Кроме того, в базальном слое присутствуют меланоциты и клетки Меркеля.
Базальные клетки располагаются на базальной мембране и имеют цилинд- рическую форму и вертикальную ори- ентацию. Их ядра овальной формы, интенсивно окрашиваются гематокси- лином и богаты хроматином. В цито- плазме базальных клеток обнаружива- ются многочисленные органеллы: ми- тохондрии, комплекс Гольджи, рибо- сомы, полирибосомы, лизосомы, центриоли, эндоплазматическая сеть, тонофиламенты, образующие цитоске- лет, и различные включения (гранулы меланина, капли жира). Наличие большого количества рибосом обус- ловлено пролиферацией базальных клеток и синтезом тонофиламентов.
Соединение базальных клеток меж- ду собой осуществляется посредством десмосом, располагающихся в местах контактов двух соседних клеток, через определенные интервалы. Эта связь играет большую роль в структурной целостности эпидермиса и обеспечи- вает регулирование эпителиоцитов — их пролиферацию, миграцию и диф- ференцировку. Кроме того, десмосомы распределяют структурные напряже- ния по всему эпидермису и помогают сохранять между соседними клетками расстояние, равное 20 нм. Десмосомы имеют семислойное строение и обра- зованы двумя "дисками прикрепле- ния", разделенными электронно-про- зрачной зоной. Десмосомы на 76 % состоят из белков, 14 % составляют углеводы и 10%—липиды, главным образом холестерин и фосфолипиды, структурно и функционально связан- ные с компонентами ДЭС.
Часть базальных клеток находится в покое, а другая — в процессе деле-
14
ния, их пролиферативный потенциал характеризуется определенной гетеро- генностью. По способности к образо- ванию клонов различают 3 типа кле- ток. Клетки первого типа — ростко- вые, долгоживущие клетки — состав- ляют примерно 10 % от общего коли- чества базальных эпителиоцитов. Они имеют наиболее высокий потенциал к образованию клонов и делятся, про- дуцируя одну дочернюю клетку, кото- рая в дальнейшем будет подвергаться дифференцировке. Материнские, рост- ковые клетки при этом по-прежнему остаются в базальном слое, а дочер- ние — транзитамплифицированные клет- ки второго типа — подвергаются огра- ниченному числу делений в базальном и первом супрабазальном слое. Третий тип — постмитотические дифферен- цирующиеся базальные клетки [4].
Высокая митотическая активность ростковых клеток иногда делает их мишенью для различных нежелатель- ных воздействий, например УФ-излу- чения, и может привести к образова- нию опухолей на коже.
Базальные эпителиоциты активно синтезируют ряд компонентов ДЭС, включая ламинин и фибронектин. На поверхности базальных клеток также обнаруживается большое количество интегринов, которые присоединяются к ДЭС и внеклеточным матричным протеиновым лигандам. Разработаны две гипотезы, объясняющие функци- онирование интегринов. Согласно первой гипотезе, интегрины участвуют в образовании цитоскелета и могут изменять как форму, так и архитекто- нику клетки, согласно второй — явля- ются истинными рецепторами, спо- собными стимулировать биохимичес- кие процессы в пределах самой клетки [9, 15]. Так или иначе интегрины обес- печивают взаимодействие между клет- ками, а также между клетками и вне- клеточным матриксом и регулируются факторами роста [20, 25].
Шиповатый слой состоит из 3—8 рядов клеток, которые более диффе- ренцированны, чем базальные клетки. Непосредственно над базальным сло-
ем они имеют полигональную форму, а в верхней части шиповатого слоя становятся уплощенными. Клетки ши- поватого слоя, как и базальные, кон- тактируют друг с другом посредством десмосом, количество которых здесь больше, что придает ему большую прочность.
Ультраструктурно шиповатые клет- ки похожи на базальные, но отлича- ются от них более развитой системой тонофиламентов, меньшим содержа- нием органелл и отсутствием пигмента.
В верхней части шиповатого слоя появляются пластинчатые гранулы (ламеллярные гранулы, тельца Одлан- да, кератиносомы), располагающиеся на периферии клеток, иногда соеди- няющиеся с плазматической мембра- ной либо выходящие в межклеточные пространства. Эти органеллы содержат липиды, фосфолипиды, свободные стеролы, церамиды и гликозилцерами- ды. Кроме того, в пластинчатых гра- нулах обнаруживается большое коли- чество гидролитических ферментов, таких как кислая фосфатаза, нуклео- зиддифосфатаза, фосфолипазы, арил- сульфатаза, неспецифическая эстераза. Свое содержимое гранулы выделяют в межклеточное пространство, форми- руя эпидермальный липидный барьер [6, 10].
Шиповатые клетки состоят из боль- шого количества тонофибрилл, распо- лагающихся по всей цитоплазме и прикрепленных к десмосомам. В этих клетках синтезируются кератины К1 — К10 — маркеры дифференцировки эпителиоцитов. В гиперпролифериру- ющем эпидермисе (например, при псориазе, заживлении ран) синтез К1 и К10 ослаблен, а Кб и К16, наоборот, усиливается [13].
В шиповатом слое находятся внут- риэпидермальные макрофаги — клет- ки Лангерганса.
Зернистый слой представлен не- сколькими рядами уплощенных и ори- ентированных горизонтально эпители- оцитов. Клетки зернистого слоя также соединяются десмосомами, ультра- структура которых аналогична таковой
15
 нижележащих
слоев, но на границе с
роговым слоем
они теряют межкле-
точный
контактный слой. Зернистые
клетки
определяются по характерным
цитоплазматическим
базофильным ке-
ратогиалиновым
гранулам. Гранулы
кератогиалина тесно
связаны с пучка-
ми тонофиламентов и
состоят в ос-
новном
из электронно-плотного белка
профилаггрина
[18]. Во время превра-
щения
зернистой клетки в роговую
происходит
трансформация предшест-
венника
профилаггрина в олигомер-
ную,
а затем в мономерную филаг-
гриновую
субъединицу. Филаггрин
служит
матричным белком, способст-
вующим
агрегации кератиновых фила-
ментов
и образованию дисульфидных
связей
[8]. В зернистом слое обнару-
живается
и другой белок — лорикрин,
который
в основном характерен для
клеточных
мембран эпителиоцитов.
нижележащих
слоев, но на границе с
роговым слоем
они теряют межкле-
точный
контактный слой. Зернистые
клетки
определяются по характерным
цитоплазматическим
базофильным ке-
ратогиалиновым
гранулам. Гранулы
кератогиалина тесно
связаны с пучка-
ми тонофиламентов и
состоят в ос-
новном
из электронно-плотного белка
профилаггрина
[18]. Во время превра-
щения
зернистой клетки в роговую
происходит
трансформация предшест-
венника
профилаггрина в олигомер-
ную,
а затем в мономерную филаг-
гриновую
субъединицу. Филаггрин
служит
матричным белком, способст-
вующим
агрегации кератиновых фила-
ментов
и образованию дисульфидных
связей
[8]. В зернистом слое обнару-
живается
и другой белок — лорикрин,
который
в основном характерен для
клеточных
мембран эпителиоцитов.
Несмотря на то что пластинчатые гранулы впервые появляются в цито- плазме клеток верхнего отдела шипо- ватого слоя, наибольшее их количест- во приходится на участок, располо- женный между зернистым и орого- вевающими слоями эпидермиса. Ли- пиды, высвобождающиеся из гранул, заполняют межклеточные промежутки рогового слоя, обеспечивая его барьер- ные свойства.
В зернистых клетках находятся и другие маркеры кератинизации: инво- люкрин, кератолинин, лорикрин, мел- кие пролинобогащенные протеины (корнифин, SPR1, SPR2), элафин, фи- лаггринсвязывающие пептиды и эн- воплакин.
Блестящий слой хорошо определяет- ся только на ладонях и подошвах и состоит из плотно расположенных уд- линенных и уплощенных клеток, ли- шенных ядер. В этом слое эпителио- циты продолжают синтезировать и мо- дифицировать белки и ферменты, уча- ствующие не только в кератинизации, но и в запрограммированном разру- шении клеток. В результате происхо- дит разрушение большинства структур зернистых клеток, включая их ядра. Такая форма деструкции морфологи-
16
чески и биохимически соответствует j апоптозной форме гибели клеток [21]. ' В межклеточном пространстве пере- ходного слоя наблюдается аккумуля- ция липидов и полисахаридов, участ- вующих в образовании водонепрони- цаемых оболочек роговых чешуек.
Роговой слой. Последний этап жиз- недеятельности эпителиоцитов прохо- j дит в роговом слое, где они превра- ' щаются в полигональные ороговевшие клетки, не содержащие ядер. Такие эпителиоциты получили название "ро- говые чешуйки". Роговой слой защи- щает кожу от потери воды и проник- новения веществ извне, а также от механических воздействий [1, 2, 17].
Этот слой представлен рядами ро- говых чешуек и более выражен в об- ласти ладоней и подошв, на других участках тела он значительно тоньше. Толщина рогового слоя также зависит от пола, возраста и наличия заболева- ний кожи. Друг от друга чешуйки отделены межклеточными промежут- ками, в которых видны десмосомы, имеющие вид уплотненных образова- ний. Трансформация десмосом, начи- нающаяся на границе зернистого и рогового слоев, происходит под дей- ствием ферментов, выделяющихся из пластинчатых гранул.
Барьерная функция рогового слоя обеспечивается двухкомпонентной системой, работающей по принципу модели "кирпичной кладки", где роль кирпичей выполняют насыщенные протеином роговые чешуйки, а рас- твора — внеклеточный липидный мат- рикс [16]. В роговых чешуйках опре- деляются структурные протеины двух типов: богатый гистидином основной протеин филаггрин, участвующий в образовании кератина, и протеин обо- лочки инволюкрин. Кроме того, рого- вые чешуйки содержат большое коли- чество высокомолекулярных керати- нов, находящихся в электронно- плотном, богатом филаггрином мат- риксе. Расположенные вертикальными колоннами роговые чешуйки поддер- живают целостность рогового слоя в условиях постоянной десквамации.
Поскольку роговые чешуйки двигают- ся к поверхности кожи, их структура, состав и функции постоянно изменя- ются. Так, вблизи клеточной стенки роговой чешуйки появляется краевая зона, состоящая из ш-гидроксицера- мидов, происходит постепенное изме- нение десмосом, а межклеточные про- межутки заполняются липидами, обес- печивающими барьерную функцию и десквамацию эпидермиса.
Клетки, расположенные в глубокой части рогового слоя, образуют ком- пактный слой, утолщенный, с плотно расположенными в нем роговыми че- шуйками. Клетки компактного слоя отличаются большим разнообразием сцепления с соседними роговыми че- шуйками, расположенными латераль- но, сверху и снизу от них. При распаде филаггрина в этом слое образуются различные субстанции (прежде всего свободные аминокислоты), которые способны присоединять воду. Эти суб- станции получили название "нату- ральный увлажняющий фактор". За счет них роговой слой способен по- глощать воду в количестве, в 3 раза превышающем его собственный объ- ем. При высыхании рогового слоя, т. е. когда содержание воды снижается бо- лее чем на 10 %, его эластичность значительно уменьшается.
Роговые чешуйки, расположенные в верхней части рогового слоя, менее сцеплены друг с другом, так как их десмосомы подвергаются протеолити- ческой деградации. В этом участке под действием холестеринсульфатазы про- исходит дальнейшая трансформация липидов, которая во многом опреде- ляет способность эпидермиса к гидра- тации и десквамации клеток [27]. Дефицит холестеринсульфатазы при- водит к замедлению десквамации оро- говевших клеток и гиперкератозу. Вследствие присущей верхнему отделу рогового слоя способности к физио- логическому отшелушиванию внешних слоев клеток его называют разобщен- ным слоем.
Важность физиологических функ- ций и структур рогового слоя стано-
вится наиболее отчетливой при ряде заболеваний с вовлечением рогового слоя. Так, при псориазе обнаружива- ются не полностью ороговевшие клет- ки с сохранившимися ядрами (пара- кератоз). Такой феномен, возможно, объясняется дефектами апоптоза и со- провождается нарушением барьерной функции рогового слоя и гиперпроли- ферацией эпителиоцитов [31]. При ре- цессивном Х-связанном ихтиозе инги- бирование протеаз холестеринсульфа- том приводит к замедлению дегра- дации десмосом и, таким образом, способствует ретенционному гиперке- ратозу.
Барьерные функции кожи обеспе- чиваются не только уникальным стро- ением рогового слоя, но и значением рН на его поверхности от нейтраль- ного до кислого. Известно, что кислая среда является неблагоприятной для развития патогенной микрофлоры. Она формируется в результате воздей- ствия в основном кожного сала, пота и жизнедеятельности микроорганиз- мов на поверхности кожи.
Таким образом, роговой слой сохра- няет некоторые важные метаболичес- кие функции и не должен рассматри- ваться в качестве инертного слоя. Сви- детельством этому является и тот факт, что любые нарушения рогового слоя (например, при его удалении) приводят к повышению пролифера- тивной активности нижележащих сло- ев, что способствует восстанавлению барьерной функции.
В целом, подводя итоги, можно ут- верждать, что эпидермис — единая функциональная и анатомическая структура кожи. Условное разделение эпидермиса на несколько слоев отра- жает прежде всего процесс дифферен- цировки эпителиоцитов, который про- текает в 4 этапа. На рис. 1.4 показан процесс созревания базальных клеток до роговых чешуек. Малодифференци- рованные клетки в базальном слое делятся непрерывно, при этом часть этих клеток остается на месте, а другая продвигается вверх и подвергается дифференцировке. В шиповатом слое
17

Механизмы регулирования пролифе- рации и дифференцировки эпителиоци- тов. Важнейшая структура, регулирую- щая функции эпителиоцитов, — дер- ма — тесно связана с эпидермисом. Другие регуляторы — факторы роста — не только влияют на образование, про- лиферацию и дифференцировку эпи- телиоцитов, но и в большой мере про- граммируют их гибель [29]. Они
Рис. 1.4. Этапы созревания (дифференцировки) эпите- лиоцитов.
I — базальный слой; II — ши- поватый слой; III — зернис- тый слой; IV — роговой слой. 1 — кератогиалиновые гранулы; 2 — пластинчатые гранулы; 3 — пучки тонофи- ламентов; 4 — эндоплазма™ - ческая сеть; 5 — ядро; 6 — ми- тохондрии.
включают эпидермаль- ный фактор роста (ЭФР), трансформирующий фак- тор роста а (ТФР-а И (3 (ТФР-(3), фактор роста кератиноцитов (ФРК). ЭФР и его рецептор в эпителиоцитах осущест- вляют контроль за меха- низмом деления клетки. В случае присоединения ЭФР к рецептору послед- ний димеризуется и через тирозинкиназный меха- низм инициирует фос- форилирование, которое воздействует на ядро и стимулирует дифферен- цировку и деление клет- ки. ЭФР, ТФР-а и ФРК действуют как митогены для эпителиоцитов, ТФР- (3, наоборот, подавляет синтез ДНК и митозы в эпителиоцитах, способствуя их дифференцировке.
Синтезируемые эпителиоцитами цитокины, такие как интерлейкины (ИЛ-1, -6, -8) и колониестимулирую- щий фактор для гранулоцитарно-мо- ноцитарной клетки-предшественницы (ГМ-КСФ), наблюдаются в нормаль- ном эпидермисе. При воспалительных процессах, заживлении ран количество цитокинов увеличивается, они высво- бождаются из поврежденных клеток и, присоединяясь к соответствующим ре- цепторам на соседних клетках, акти- вируют их деление и пролиферацию. Следует отметить, что факторы роста, цитокины и нейропептиды в эпидер- мисе работают по принципу взаимо-
18
действия "клетка — клетка" и "клет- ка — матрикс".
Другие регулирующие субстанции включают рецепторы стероид-тирео- идной группы и их лиганды. Напри- мер, разнообразные биологические эф- фекты ретиноидов заключаются преж- де всего в активации или угнетении различных сетов, ответственных за пролиферацию и дифференцировку ге- нов через взаимодействие с рецепто- рами для ретинойной кислоты и ре- тинойные Х-рецепторы. Такое взаимо- действие имеет дозозависимый харак- тер [3].
Для поддержания эпидермального гомеостаза необходимо участие вита- мина D3. Активная форма витамина D3—1,25 (OH)2D3 — действует через его рецептор, который образует гете- родимеры с ретинойными Х-рецепто- рами, уменьшая пролиферацию эпи- телиоцитов и стимулируя их диффе- ренцировку [5]. Поэтому, подобно ретиноидам, витамин D3 и его синте- тические аналоги применяются при лечении ряда пролиферативных забо- леваний кожи [19].
Другой важный элемент, регули- рующий жизнедеятельность эпителио- цитов, — кальций. Изучение влияния концентрации кальция in vitro пока- зывает, что низкий уровень кальция в коже способствует пролиферации эпи- телиоцитов, а высокий служит триг- герным механизмом для дифференци- ровки клеток. Поэтому его присутст- вие необходимо для прохождения эпителиоцитом нормального клеточ- ного цикла и выполнения связанных с ним функций, таких как формиро- вание десмосом и трансглютаминаз- ных сшивок [26].
Кинетические исследования пока- зывают, что в среднем деление базаль- ных клеток происходит каждые 200— 400 ч. В результате дифференцирова- ния клетка приблизительно за 14 дней достигает рогового слоя и находится там в течение последующих 14 дней. Продолжительность жизненного цик- ла клетки значительно сокращается при заболеваниях кожи, сопровожда-
ющихся нарушением кератинизации, например при псориазе.
Меланоциты — клетки, определяю- щие пигментацию кожи. Кроме эпите- лиоцитов, в базальном слое находятся меланоциты, составляющие 5—10 % от общего количества клеток эпидермиса [35]. Меланоциты — отростчатые пиг- ментсинтезирующие клетки, защи- щающие от солнечной радиации. По разным оценкам, каждый меланоцит находится в контакте примерно с 36 эпителиоцитами, образуя "эпидермо- меланоцитную единицу". На поверх- ности меланоцитов десмосом нет.
В цитоплазме меланоцитов содер- жатся митохондрии, эндоплазматичес- кая сеть, пластинчатый комплекс, ри- босомы и фибриллы, которые распо- лагаются диффузно. Эти фибриллы обладают сократительной способнос- тью, участвуя в высвобождении мела- нина из клетки.
Процесс синтеза меланина в мела- ноцитах происходит в удлиненных, окруженных мембраной структурах — премеланосомах, которые в дальней- шем, уплотняясь, образуют меланосо- мы, располагающиеся изолированно. Следует отметить, что способность синтезировать меланин присуща всем меланоцитам. При этом только мела- ноциты, находящиеся в коже и в во- лосяных фолликулах, способны транс- портировать меланин в соседние клет- ки. Этот процесс происходит путем фагоцитоза меланосом эпителиоцита- ми базального слоя, в которых мела- носомы располагаются в цитоплазме и группируются в комплексы, образуя защитный слой (рис. 1.5). В эпидер- мисе меланоциты распределяются до- вольно равномерно, образуя своеоб- разный защитный экран от УФ-излу- чения. Меланин действует как энер- гетический трансформатор, ловушка свободных радикалов и абсорбент УФ- излучения, дающего канцерогенный эффект [32].
На количество и распределение ме- ланоцитов влияет множество факто- ров: область тела, пол, возраст, расо- вая принадлежность и др. Например,
19

Рис. 1.5. Транспорт меланина из мелано- цитов в эпителиоциты. 1 — комплекс меланосом; 2 — ядро меланоци- та; 3 — меланоцит; 4 — эпителиоцит.
на лице и в области гениталий они обнаруживаются в наибольшем коли- честве — примерно 1100 — 1300 мела- ноцитов на 1 см2. УФ-излучение, глав- ным образом УФВ (280—320 нм), так- же индуцирует пигментацию кожи как за счет непосредственного фотоокис- ления меланина, так и путем стиму- лирования синтеза меланина.
Процесс синтеза меланина схема- тично представляется следующим об- разом. Ключевой аминокислотой в синтезе меланина является тирозин.
В меланосомах тирозин под действием тирозиназы трансформируется в диок- сифенилаланин (ДОФА) и затем окис- ляется до дофахинона (рис. 1.6). Ти- розиназа — фермент, содержащий медь, закодирована в хромосоме Ilql4-21 [34].
На уровне дофахинона процесс про- должается по двум направлениям. В первом случае часть его превраща- ется в бициклические продукты, вклю- чая лейкодофахром (циклодофа), до- фахром, 5,6-дигидроксииндол и ин- дол-5,6-хинон. При таутомеразной реакции образуются схожие молекулы, но с добавлением к ним карбоксили- рованной кислоты. Эти продукты полимеризации образуют эумеланин, придающий коже коричневый или черный цвет. Во втором случае при присоединении к дофахинону глута- тиона или цистеина посредством ре- акций полимеризации образуются фе- омеланины и трихромы, окрашиваю- щие кожу соответственно в желтый, красный и насыщенный красный цвет [37].
Таким образом, в коже человека
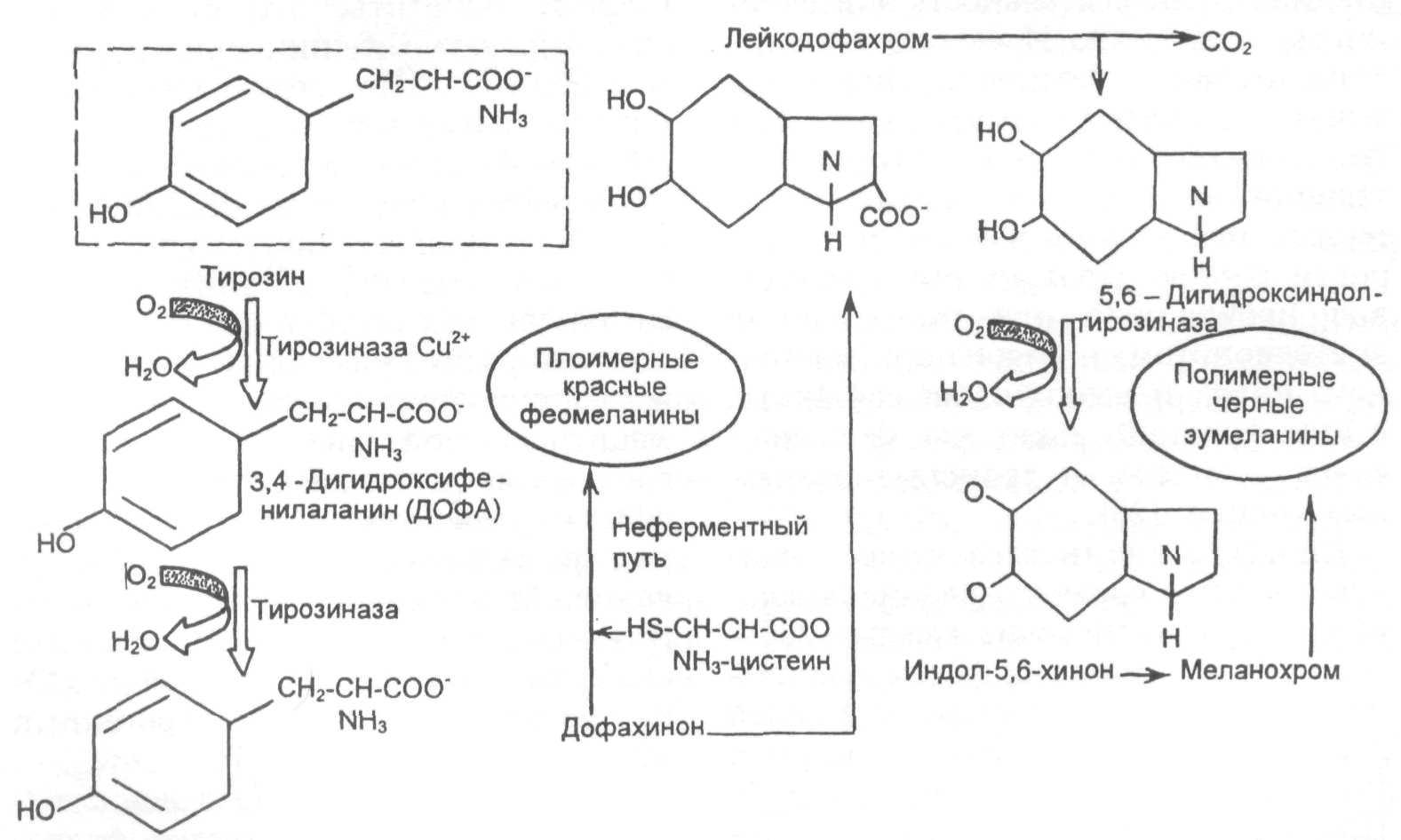
Рис. 1.6. Биосинтез меланина. 20
Таблица 1.1. Шкала оценки пигментации
|
Тип кожи |
Цвет кожи |
Цвет глаз |
Ожого- вая реак- ция кожи на солнце |
Способ- ность кожи к загару |
Ответ кожи на УФ-излучение |
Вероят- ность раз- вития ра- ка кожи |
|
I |
Белый (фарфо- ровый) |
Голубой, серый |
Всегда ожог |
Отсутству- ет |
Рано появляется множество весну- шек; резкое сни- жение содержания меланина в коже |
Очень высокая |
|
II |
Белый (жем- чужный) |
Зеленый |
Всегда ожог |
Редко |
Веснушки; умерен- ное снижение со- держания мелани- на в коже |
Высокая |
|
III |
Коричневатый (смуглый) |
Светло- карий |
Иногда ожог |
Появляет- ся быстро |
Множество весну- шек и/или гипер- |
Умерен- ная |
|
|
|
|
|
|
пигментация |
|
|
IV |
Оливковый |
Карий |
Ожог |
Появляет- |
Гиперпигментация |
Низкая |
|
|
|
|
крайне редко |
ся быстро |
(может быть в виде пятен, но веснуш- ки не появляются) |
|
|
V |
Темно-корич- невый с крас- новатым от- тенком |
Темно- карий |
Может развиться легкая эритема |
Темно- коричне- вый |
Однородная гипер- пигментация (без образования пя- тен) |
Практи- чески от- сутствует |
|
VI |
Черный |
Черный |
Ожога не бывает |
Черный |
Однородная пиг- ментация |
То же |
синтезируется 3 типа меланина: эуме- ланины, феомеланины и трихромы. Эумеланины придают волосам темный цвет, а феомеланины и трихромы встре- чаются в основном в светлых и рыжих волосах. Чаще всего меланины пред- ставлены комбинацией эу- и феоме- ланинов. Вариации пигментации кожи у людей разных рас завися"" главным образом от цвета, количества, размера и распределения меланосом, а не от количества меланоцитов. Так, эпите- лиоциты темнокожих людей могут со- держать 400 меланосом, в то время как у светлокожих их только 100.
Кроме указанных факторов, влия- ющих на степень пигментации, суще- ствуют и другие, главным образом свя- занные с регулированием синтеза меланина. К ним относятся мелано- цитстимулирующий гормон (МСГ), гормоны гипофиза (адренокортико- тропный гормон — АКТГ и р-липо- тропин), эстрогены и др. [33, 36].
В химическом отношении между МСГ и АКТГ имеется определенное сход- ство. Пигментацию также стимулиру- ют различные факторы роста, обра- зующиеся в эпителиоцитах в ответ на УФ-излучение, например свободные ра- дикалы. Другим сильным стимулятором являются мелкие фрагменты ДНК, осо- бенно тимидин и динуклеотиды, высво- бождающиеся во время репарации ДНК. Пигментация кожи имеет важное значение в дерматокосметологии, на- пример существует определенная связь пигментации с образованием келоид- ный рубцов после абразии кожи (ме- ханическая, лазерная, химическая), от ее выраженности зависит склонность кожи к тем или иным новообразова- ниям, индуцированным УФ-излучени- ем. Это послужило Т.Фитцпатрику ос- нованием предложить шкалу типов ко- жи в зависимости от степени ее пиг- ментации. Позднее она была усовер- шенствована J.Fulton [32] (табл. 1.1).
21
В базальном слое располагаются также клетки Меркеля, являющиеся механорецепторами. Они характеризу- ются наличием в их цитоплазме ней- рофиламентов и гранул с плотным центром, окруженных мембраной и похожих на нейросекреторные грану- лы. Эти клетки тесно связаны с тер- минальными окончаниями кожных нервов и, возможно, играют роль сен- соров [23].
Внутриэпидермальные макрофаги (клетки Лангерганса) располагаются в шиповатом слое, имеют отростчатую форму и составляют 2—8 % от общего количества эпидермальных клеток. На поверхности этих клеток, как и у ме- ланоцитов, отсутствуют десмосомы. В цитоплазме клеток Лангерганса об- наруживаются хорошо развитые орга- неллы: многочисленные митохондрии, эндоплазматическая сеть, пластинча- тый комплекс, рибосомы, лизосомы и специфичные гранулы Бирбека. Тоно- филаменты отсутствуют.
Внутриэпидермальные макрофаги — внешние стражи клеточной иммунной системы, отвечащие за распознавание, процессинг и представление раствори- мых антигенов и гаптенов к сенсиби- лизированным Т-лимфоцитам [68, 72]. Предположение об иммунной функ- ции клеток Лангерганса впервые было сделано на основании исследований, показавших, что в коже, подвержен- ной воздействию контактных аллерге- нов, вокруг внутриэпидермальных макрофагов образуются лимфоцитар- ные инфильтраты [71]. Клетки Лан- герганса примыкают к эпителиоцитам посредством Е-рецепторов и имеют на своей поверхности рецепторы для Fc- фрагмента иммуноглобулина G (Ig G) и для компонента комплемента СЗ. Клетки Лангерганса экспрессируют множество молекул, которые влияют на их созревание: CD4, CD45, CD40, CD80, CD86, HLA-DR и ICAM-1 [76].
Т-лимфоциты и клетки Лангерганса взаимодействуют друг с другом с по- мощью адгезионных молекул и ICAM- 1. При контакте с антигенами клетка Лангерганса подвергает их переработ-
ке в цитоплазме и затем экспрессирует на поверхность клетки, соединяясь с главным комплексом гистосовмести- мости (МНС). Взаимодействие ком- плекса "МНС—антиген" с Т-лимфо- цитом вместе с высвобождением ци- токинов из клеток Лангерганса приво- дит к активации Т-лимфоцитов [66, 68, 73].
1.2. Дерма
Дерма — основной компонент соеди- нительной ткани кожи, обеспечиваю- щий ее гибкость, эластичность и прочность. Она защищает организм от механических повреждений, участвует в терморегуляции, содержит большое количество нервов и сосудов. Дерма, как уже отмечалось, теснейшим обра- зом связана с эпидермисом, участвуя в образовании и функционировании ДЭС и репаративных процессах. На разных участках тела толщина дермы сильно варьирует: например, на веках она очень тонкая (0,6 мм), а в области спины, на ладонях и подошвах — толстая (3 мм и более).
Дерму образуют два слоя: верхний сосочковый и нижний сетчатый. Кро- ме различий в положении, они разли- чаются по степени организации соеди- нительной ткани, количеству волок- нистых образований, клеток, нервных волокон и сосудов. Границей между сосочковым и сетчатым слоем дермы является субпапиллярное сплетение, расположенное в горизонтальной плос- кости.
Сосочковый слой. Каркас этого слоя образуют тонкие коллагеновые и ок- ситалановые эластические волокна. Зрелые эластические волокна, как правило, отсутствуют. Они обнаружи- ваются в основном при ряде наслед- ственных заболеваний соединительной ткани (например, при доминантно на- следственной форме синдрома Элер- са — Данлоса), у людей пожилого воз- раста или при длительном интенсив- ном воздействии УФ-излучения [12]. Развитая сеть коллагеновых и эласти-
22
ческих волокон образуется благодаря их синтезу большим количеством фиб- робластов, имеющих высокую степень метаболической активности.
Структурные характеристики основ- ного вещества в сосочковом слое дер- мы позволяют коже легко приспосаб- ливаться к механическим воздействи- ям, например к растяжению.
Соединительная ткань, имеющая такие же, как и в сосочковом слое, организацию и состав, окружает воло- сяные фолликулы и сосуды. Эта зона соединительной ткани называется ад- вентицием.
Сетчатый слой дермы образован в основном коллагеновыми волокнами большого диаметра, сплетенными в крупные пучки. Зрелые эластические волокна переплетаются с пучками кол- лагеновых волокон, придавая дерме упругость и эластичность. В здоровой коже размер эластических волокон и пучков коллагеновых волокон в сетча- том слое увеличивается по мере их приближения к гиподерме.
Условно сетчатый слой разделяется на верхнюю и нижнюю зоны, что характеризует прежде всего степень различий в размере и характере фиб- розной соединительной ткани. В верх- ней зоне сетчатого слоя дермы опре- деляются в основном коллагеновые волокна и пучки, а также горизонталь- но ориентированные элауниновые эластические волокна. Эта область на- сыщена фибробластами и другими со- единительнотканными клетками, а в случае воспаления — лейкоцитами и лимфоцитами. Верхняя зона имеет более слабые механические свойства по сравнению с глубокой нижней зо- ной сетчатого слоя дермы и, вероятно, поэтому склонна к развитию различ- ных патологических процессов, на- пример к потере эластических воло- кон.
В целом дерма состоит из клеток и сложного межклеточного вещества — экстрацеллюлярного матрикса.
Клетки дермы. Самая высокая кон- центрация клеток в дерме находится в сосочковом слое и вокруг кровенос-
ных сосудов. Кроме того, они обнару- живаются между пучками коллагено- вых волокон в сетчатом слое.
Основной тип клеток дермы — фиб- робласты — мезенхимальные клетки, ответственные за синтез и распад во- локнистых и множества других раство- римых соединений межклеточного матрикса. Один и тот же фибробласт способен одновременно синтезировать несколько типов белковых субстан- ций, например коллаген и эластин. Популяция фибробластов в коже ха- рактеризуется большим разнообрази- ем. Даже в пределах однородной ткани можно обнаружить фенотипически разные виды фибробластов. Незрелые клетки, начиная с ростковых, после- довательно дифференцируются и до- стигают зрелых форм. Фазы покоя и пролиферации фибробластов зависят от множества иммунных медиаторов (ИЛ-la, 1р и 8) и других цитокинов. В конце этого длительного процесса фибробласты подвергаются дегенера- ции или трансформации [38, 50].
В дерме также содержатся гистио- циты — клетки, имеющие звездчатую, дендритную или, реже, веретенообраз- ную форму. Как правило, они распо- лагаются в большом количестве в со- сочковом и верхнем отделе сетчатого слоя дермы, вблизи субпапиллярного сосудистого сплетения и в подкожной жировой клетчатке. Гистиоциты явля- ются иммунокомпетентными клетка- ми, функционирующими как эффек- торные клетки афферентного звена иммунного ответа. Вероятно, гистио- циты могут стать клетками-мишенями при развитии различных доброкачест- венных фиброзных новообразований кожи (дерматофибромы, фиброксан- томы и др.) [40]. При воспалительных заболеваниях, например при псориазе и экземе, количество этих клеток уве- личивается, они активируются, вызы- вая экспрессию различных маркеров воспаления, например ICAM-1. В то же время в случае злокачественных фиброзных неоплазий и доброкачест- венных фибропролиферативных забо- леваний (келоидные рубцы, склеро-
23
дермия) количество гистиоцитов умень- шается или они вообще отсутствуют [40, 42].
Другой тип гистиоцитов — макро- фаги — имеет костномозговое проис- хождение. При проникновении в кро- вяное русло они превращаются в мо- ноциты и затем мигрируют в дерму, где подвергаются дифференцировке. Макрофаги являются активными фа- гоцитами, участвуют в обработке и представлении антигена к иммуноком- петентым лимфоцитам, оказывают бактерицидное и тумороцидное дейст- вие за счет продукции лизоцима, пере- кисей и супероксида, синтезируют различные факторы роста, цитокины и другие иммуномодуляторные моле- кулы и гемопоэтины, вовлекаются в процесс коагуляции, атерогенеза, за- живления ран и ремоделирования тка- ней [45].
Тканевые базофилы дермы пред- ставляют собой клетки, предшествен- ники которых находятся в костном мозге (CD34+) и распределяются по всей соединительной ткани. Их наи- большая концентрация наблюдается в сосочковом слое дермы, около ДЭС, вокруг кровеносных сосудов, нервных волокон и придатков кожи, в подкож- ной клетчатке. Тканевые базофилы синтезируют множество медиаторов и во время активации являются первич- ными эффекторами аллергических ре- акций. Они также участвуют в проти- воопухолевом иммунном надзоре и при появлении опухолевых клеток вы- свобождают фактор некроза опухоли а (ФНО-а) — субстанцию, обладаю- щую цитотоксической активностью. Кроме того, тканевые базофилы игра- ют большую роль в противопаразитар- ной защите, стимулируют хемотаксис, активацию и пролиферацию эозино- филов, усиливают фагоцитоз, изменя- ют тонус и проходимость сосудов, сти- мулируют репарацию соединительной ткани и ангиогенез [49]. В цитоплазме тканевых базофилов находятся мета- хроматические гранулы, содержащие гепарин и гистамин. В здоровой коже их обнаруживается относительно ма-
ло, но их количество может увеличи- ваться при некоторых дерматозах, осо- бенно зудящих (мастоцитоз, атопичес- кий дерматит, экзема, красный плос- кий лишай и т.д.).
Межклеточный матрикс состоит из 3 компонентов: основного вещества, адгезивных белков и волокнистых структур (коллагеновые, эластические и ретикулярные волокна). Он выпол- няет разнообразные функции: обеспе- чивает механические контакты между клетками, образует прочные структу- ры, формирует пути миграции клеток, вдоль которых они могут перемещать- ся.
Основное вещество дермы построено таким образом, что позволяет клеткам свободно перемещаться и регулирует деформацию кожи. Оно представляет собой гелеобразную аморфную суб- станцию, состоящую из гликозамино- гликанов (ГАГ), протеогликанов (ПТГ), гликопротеинов (ГП), растворимого коллагена, ферментов и продуктов их распада.
ГАГ являются линейными полиме- рами, состоящими из повторяющихся дисахаридов и обеспечивающими дер- ме необходимую вязкость и гидрата- цию. Они способны связать воду в количестве, до 1000 раз превышающем их собственный объем. Поэтому на- сыщенность дермы ГАГ в молодом возрасте во многом обеспечивает глад- кую, без морщин кожу. Повышение уровня ГАГ также наблюдается при заживлении ран на коже, когда миг- рация клеток является одной из ос- новных составляющих процесса репа- рации [47]. По мере старения дермы в ее основном веществе начинают пре- обладать сульфатированные ГАГ, а уро- вень гиалуроновой кислоты, одного из важнейших представителей ГАГ, начи- нает снижаться.
ГАГ в виде высокомолекулярных полимеров с белковой сердцевиной, к которой присоединена гиалуроновая кислота (гиалуронат), называют про- теогликанами. По форме они напоми- нают ершик для мытья бутылок (рис. 1.7). Необычно крупные молекулы
24

Слева — протеогликан агрегирован с центральной нитью гиалуронана, справа — детальный вид
протеогликанового мономера с белковой сердцевиной. 1 и 7 — гиалуронан; 2 — гликозамино-
гликан; 3 — белковая сердцевина; 4 — олигосахаридная связь; 5 — мономер протеогликана; 6 —
гликопротеин.
ПТГ преобладают в общем объеме ос- новного вещества дермы. Их основная роль заключается в связывании фак- торов роста и цитокинов и в облегче- нии взаимодействия клеток с волок- нистыми структурами внеклеточного матрикса. Благодаря этим свойствам ПТГ могут влиять на пролиферацию, дифференцировку, репарацию и мор- фогенез кожи. Основные ПТГ в дерме (компоненты ДЭС) — хондроитин- сульфат и дерматансульфат (бигликан, декорин, верзикан), гепаран, гепаран- сульфат (перлекан, синдекан) и хонд- роитин-6-сульфат [43, 52].
Адгезивные белки. Наиболее важны- ми адгезивными белками являются фибронектин, ламинин, тромбоспон- дин, витронектин и тенаскин. Эти по- лифункциональные белки-ГП способ- ны связывать различные составные компоненты межклеточного матрикса. Кроме того, адгезивные белки обеспе- чивают фиксацию клеток в межкле- точном матриксе за счет взаимодейст-
вия с мембранными рецепторами — интегринами. В результате их присо- единения к клеткам, коллагеновым и эластическим волокнам, другим ГП адгезивные белки участвуют в процес- се гомеостаза дермы, способствуя ад- гезии, миграции, созреванию и диф- ференцировке клеток и других дер- мальных компонентов.
Фибронектин — нерастворимый, ни- тевидный ГП — синтезируется в коже как эпителиальными, так и мезенхи- мальными клетками. Он находится в коллагеновых и эластических волок- нах, определяется в ДЭС и на поверх- ности клеток, обеспечивая их адгезию с основным веществом дермы. Фиб- ронектин также связывает тромбоциты с коллагеном, обнаруживается в фиб- рин-фибриногеновых комплексах и играет большую роль в организации основного вещества дермы. Такая осо- бенность фибронектина придает ему свойство "молекулярного клея". По- вышение уровня фибронектина в
25
плазме крови и коже может свидетель- ствовать о заболеваниях, связанных с повышенной проницаемостью кожи [481.
Витронектин присутствует в дерме повсюду, где обнаруживаются эласти- ческие волокна, за исключением ок- ситалановых.
Тенаскин — крупный гексамерный ГП основного вещества. Минималь- ные количества тенаскина присутству- ют в дерме в ограниченном простран- стве между ДЭС и кровеносными со- судами, окруженными гладкомышеч- ными волокнами. Кроме того, тенас- кин обнаруживают в области мышц, поднимающих волосы, и в потовых железах. Количество тенаскина в со- сочковом слое дермы резко возрастает при гиперпролиферации эпидермиса. Основным источником тенаскина, ве- роятно, являются эпителиоциты [46].
Волокнистые структуры дермы. Коллагеновые волокна — основной ком- понент дермы — составляют прибли- зительно 75 % сухой массы кожи и обеспечивают ее прочность и эластич- ность. В настоящее время идентифи- цировано более 20 генетически раз- личных типов коллагена [39, 44]. Эти молекулы состоят из трех полипептид- ных цепей разных типов (а-спиралей), скрученных в виде правой тройной спирали. В свою очередь полипептид- ные цепи построены из часто повто- ряющихся фрагментов, имеющих ха- рактерную последовательность GLY— X—Y. Каждым третьим аминокислот- ным остатком является глицин (GLY), положение X занимает пролин, a Y — как пролин, так и гидроксипролин. Присутствие в полипептидной цепи остатков гидроксиаминокислот явля- ется характерной особенностью кол- лагена. На одном из концов молекула коллагена сшита поперечными связя- ми, количество которых возрастает по мере старения организма.
Молекулы коллагенов обладают способностью спонтанно агрегировать с образованием более сложных струк- тур, микрофибрилл и фибрилл. Боль- шинство коллагенов образует фибрил-
26
лы цилиндрической формы диаметром 20—50 нм с характерными поперечны- ми полосами, повторяющимися через каждые 64—67 нм.
Формирование коллагеновых воло- кон происходит с участием фибро- бластов и включает две последователь- ные стадии: внутри- и внеклеточную. На внутриклеточной стадии предше- ственник коллагена (препропептид) синтезируется на рибосомах фибро- бластов и подвергается модификации в эндоплазматическом ретикулуме и аппарате Гольджи, что приводит к об- разованию растворимого проколлаге- на. Прежде чем появиться в межкле- точном пространстве, молекула про- коллагена проходит этапы модифика- ции и сборки, т.е. полипептидные цепи скручиваются в тройную спи- раль. На внеклеточной стадии прокол- лаген выходит из клетки и в результате ступенчатой сборки образует микро- фибриллы. Последние подвергаются конденсации с образованием внутри- и межмолекулярных поперечных свя- зей, в результате чего фибриллы кол- лагена приобретают окончательную структуру, становятся нерастворимы- ми, прочными на разрыв и высокоу- стойчивыми к действию протеиназ (рис. 1.8) [41]. В синтезе коллагена также участвуют молекулы аскорбино- вой кислоты, меди, двухвалентного железа и кислорода. Сборка фибрилл в коллагеновые волокна осуществля- ется с помощью ГАГ, располагающих- ся на их поверхности.
Вне клетки аминокислотные и кар- боксильные остатки коллагена утили- зируются с помощью коллагеновых металлопротеиназ.
В дерме взрослого человека интерс- тициальный фибриллярный коллаген (типов I, III и V) является самой большой фракцией коллагена: при- близительно 80—90 % составляет кол- лаген типа I и 8—12 % — коллаген ти- па III.
Коллаген типа I в большом коли- честве обнаруживается в сетчатом слое, а коллаген типа III — преиму- щественно в сосочковом слое дермы.
Рис.
1.8. Синтез коллагена.
1
— выработка гликозаминогликанов
в
комплексе
Гольджи; 2 — синтез поли-
пептидов
(проколлагена) в рибосомах;
3
— сборка проколлагеновой молекулы
из
трех проколлагеновых цепочек; 4
—
агрегация
в коллагеновые фибриллы.

Эластические волокна составляют 1—3 % дермы и формируют обширнуюсеть от ДЭС до гиподермы. Эласти- ческие волокна также обнаруживаются в стенках сосудов кожи и оболочках волосяных фолликулов. Сеть из элас- тических волокон обеспечивает коже растяжимость и эластичность. В отли- чие от коллагена, синтезируемого только фибробластами, эластические волокна продуцируются также и глад- комышечными клетками.
Эластические волокна состоят из двух основных компонентов — эласти-
на и фибриллинов. Эластины пред- ставляют собой белки-полимеры с по- перечными сшивками, а фибрилли- ны — гликопротеины.
Процесс эластогенеза начинается с синтеза микрофибрилл. Затем микро- фибриллярный каркас покрывается эластином. Волокна, покрытые рас- творимым эластином, называются ок- ситалановыми. Гибкие окситалановые волокна интегрируют клетки, приспо- собленные к деформациям кожи. Эти волокна идут перпендикулярно ДЭС к области, расположенной между сосо- чковым и сетчатым слоями дермы, где они сливаются с горизонтальной се- тью элауниновых эластических воло- кон.
Элауниновые волокна содержат не- большое количество нерастворимого эластина. Они также трансформиру- ются в сеть зрелых эластических во- локон, которые находятся повсюду в сетчатом слое. Формирование эласти- ческих волокон в дерме происходит очень медленно, но может ускоряться под воздействием УФ-излучения и при воспалении.
Количество и структура эластичес- ких волокон также изменяются с воз- растом и при многих генодерматозах [53]. Интересно отметить, что дефекты в кодировании генов эластических во- локон не всегда являются причиной заболеваний эластической соедини- тельной ткани. Например, cuds laxa —
27
заболевание, характеризующееся об- висанием кожи на сгибательных участ- ках конечностей, может быть следст- вием патологии гена, ответственного за развитие синдрома Менкеса. При этом синдроме определяют дефект транспортировки меди, что воздейст- вует на фермент лизилоксидазу, уча- ствующую в сшивках коллагена и эластина [54].
Ретикулярные волокна (аргирофиль- ные волокна) располагаются в основ- ном на границе эпидермиса и дермы, вокруг сосудов, сальных и потовых желез и волосяных фолликулов. Эти волокна по составу аналогичны кол- лагеновым фибриллам, но имеют меньший диаметр. Наибольшее коли- чество ретикулярных волокон обнару- живают в заживающих ранах, когда происходит усиленное образование коллагена в фибробластах.
