
- •Патологическая физиология
- •Глава 1. Общее учение о болезни 92
- •Глава 6. Патологическая физиология периферического (органного) кровообращения 695
- •Глава 12. Патологическая физиология 1237
- •.Краткие сведения об истории патологической физиологии
- •Экспериментально-физиологическое, физико-химическое направление
- •.Часть первая общая нозология
- •Глава 1. Общее учение о болезни
- •1.1. Здоровье и болезнь
- •1.1.1. Норма и здоровье
- •1.1.2. Определение сущности болезни
- •1.1.3. Патологическая реакция, патологический процесс, патологическое состояние
- •1.2. Общие вопросы учения об этиологии болезней
- •1.3. Общие вопросы учения о патогенезе болезней
- •1.4. Исходы болезни
- •На повреждение
- •2.1. Общая патология клетки
- •2.1.1. Повреждение клеток в патологии
- •2.1.2. Нарушение функций клеточных структур
- •Кусочки ткани Выделенные митохондрии
- •Время переживания органа при 24°с (мин)
- •2.1.3. Механизмы нарушения барьерной функции биологических мембран
- •СюТоксическое действие
- •Токсическое действие
- •2.1.4. Другие причины нарушения барьерных свойств липидного слоя мембран
- •Глава 1. Общее учение о болезни 92
- •Глава 6. Патологическая физиология периферического (органного) кровообращения 705
- •Глава 12. Патологическая физиология 1247
- •2.1.5. Нарушение электрической стабильности липидного слоя
- •2.2. Общие реакции организма на повреждение
- •2.2.1. Общий адаптационный синдром (стресс)
- •2.2.2. Активация протеолитических систем плазмы крови
- •I Фактор Хагемана Калликреин j I Прекалликреин
- •2.2.4. Кома
- •2.2.5. Ответ острой фазы
- •2.2.5.2. Главные медиаторы ответа острой фазы
- •3.1. Реактивность организма
- •3.2. Виды реактивности
- •3.5. Резистентность
- •3.6. Факторы, влияющие на реактивность
- •3.7. Роль наследственности
- •Гидрооксифенил виноградная кислота
- •Фенилпиро- виноградная кислота
- •Гомоге нти зи н о вая кислота
- •Гомогентизиноксидаза (алкаптонурия)
- •4.1. Основные представления о строении
- •4.2. Общая стратегия иммунной защиты
- •4.3. Иммунодефицитные состояния
- •4.3.1. Первичные иммунодефициты
- •4.3.2. Вторичные иммунодефициты
- •4.4. Аутоиммунные процессы
- •4.5. Лимфопролиферативные процессы
- •5.1. Взаимоотношение аллергии и иммунитета
- •5.3. Специфические аллергические реакции
- •5.3.1. Аллергические реакции I типа (анафилактические)
- •5.3.2. Аллергические реакции II типа
- •5.3.3. Аллергические реакции III типа
- •5.3.4. Аллергические реакции IV типа
- •Характеристика повышенной чувствительности немедленного и замедленного типов
- •5.4. Атопия. Атонические и псевдоатопические заболевания
- •5.4.1. Механизмы развития
- •5.4.2. Механизмы обратимой обструкции дыхательных путей
- •5.5. Псевдоаллергия
- •5.5.1. Гистаминовый тип псевдоаллергии
- •5.5.2. Нарушение активации системы комплемента
- •5.5.3. Нарушения метаболизма арахидоновой кислоты
- •Глава 6. Патологическая физиология периферического (органного) кровообращения и микроциркуляции
- •Состояние кровотока в микрососудах при артериальной гиперемии, ишемии, капиллярном стазе и венозном застое крови,
- •Признаки расстройства периферического кровообращения (в.В. Воронин, модификация г.И. Мчедлишвили)
- •6.1. Артериальная гиперемия
- •6.3. Нарушение реологических свойств крови, вызывающее стаз в микрососудах
- •6.4. Венозный застой крови
- •Превалирование резорбция вал фильтрацией я оды а микрооо- суддк мозга
- •6.6. Кровоизлияние в мозг
- •7.1. Нарушение микроциркуляции
- •7.2. Воспалительные экссудаты
- •7.3. Эмиграция лейкоцитов периферической крови
- •7.4. Фагоцитоз
- •7.5. Специализированные функции нейтрофилов, моноцитов
- •7.6. Медиаторы воспаления
- •7.7. Исходы воспаления
- •8.1. Этиология
- •8.3. Функция органов и систем
- •9.1. Нарушение обмена белков
- •9.1.1. Нарушение расщепления и всасывания белков
- •9.1.4. Патология межуточного обмена белков (нарушение обмена аминокислот)
- •9.1.5. Изменение скорости распада белка
- •9.1.6. Патология конечного этапа обмена белков
- •9.2. Нарушение обмена липидов
- •9.2.1. Нарушение транспорта липидов и перехода их в ткани
- •9.2.2. Роль нарушений липидного обмена в патогенезе атеросклероза
- •9.2.3. Жировая инфильтрация и жировая дистрофия
- •9.3. Нарушение обмена углеводов
- •9.3.3. Нарушение регуляции углеводного обмена
- •9.4. Нарушение водного баланса
- •9.4.1. Основы регуляции водного баланса
- •9.4.2. Формы нарушения водного баланса
- •9.4.2.1. Увеличение объема внеклеточной жидкости (гиперволемия)
- •9.4.2.2. Уменьшение объема внеклеточной жидкости (гиповолемия)
- •9.5. Нарушение электролитного баланса
- •Организма человека
- •9.5.1. Нарушение баланса натрия
- •9.5.2. Нарушение баланса калия
- •9.5.3. Нарушение баланса кальция
- •9.5.4. Нарушение баланса фосфатов
- •9.5.5. Нарушение баланса магния
- •9.6. Нарушение кислотно-основного баланса
- •9.6.1. Основы регуляции кислотно-основного баланса
- •0A* й к * 5 сз" 5 неш Лшкжы Анионы КаикшыКат ионы
- •9.6.2. Основные показатели коб
- •9.6.3. Формы нарушения кислотно-основного баланса
- •9.6.3.1. Респираторный ацидоз
- •9.6.3.2. Метаболический ацидоз
- •9.6.3.3. Респираторный алкалоз
- •9.6.3.4. Метаболический алкалоз
- •9.6.3.5. Смешанные нарушения кислотно-основного баланса
- •10.2. Компенсаторно-приспособительные реакции при гипоксии
- •10.3. Нарушение обмена веществ
- •10.4. Коррекция гипоксии: необходим избыток или недостаток кислорода?
- •11.1. Механизмы клеточного деления
- •11 »2. Патофизиология клеточного деления
- •11.2.1. Активация онкогенов
- •11.2.2. Инактивация генов-супрессоров
- •11.2.3. Нарушение апоптоза
- •11.2.4. Нарушение механизмов репарации днк
- •11.3. Опухолевый рост
- •11.3.2. Этиология опухолей
- •11.3.3. Свойства опухолевых клеток in vitro
- •11.3.4. Межклеточная кооперация
- •11.3.5. Свойства злокачественных опухолей
- •11.3.6. Взаимоотношения опухоли и организма
- •11.3.7. Механизмы резистентности опухолей к терапевтическим воздействиям
- •.Часть третья нарушение функций органов и систем
- •Глава 12. Патологическая физиология нервной системы
- •12.1. Общие реакции нервной системы на повреждение
- •12.2. Нарушение функции нервной системы,
- •12.3. Метаболические энцефалопатии
- •12.4. Повреждение мозга,
- •12.5. Расстройства функций нервной системы, обусловленные повреждением миелина
- •12.6. Нарушение нервных механизмов управления движениями
- •12.6.1. Расстройства движений,
- •12.6.1.1. Болезни моторных единиц
- •12.6.1.2. Расстройства движений
- •12.6.1.3. Нарушение движений при повреждении мозжечка
- •12.6.1.4. Нарушение движений
- •13.1. Нарушение механизмов регуляции артериального давления
- •13.2. Расстройства функций мочевого пузыря
- •13.5. Вегетативные расстройства,
- •15.1. Нарушение центральных механизмов регуляции
- •15.2. Патологические процессы в железах
- •15.3. Периферические (внежелезистые) механизмы нарушения активности гормонов
- •15.4. Роль аутоаллергических (аутоиммунных) механизмов в развитии эндокринных нарушений
- •1]ДиОТипиЧесИиЕ ahtuteaa
- •16.1. Нарушение функций гипофиза
- •16.1.1. Недостаточность функции гипофиза
- •16.1.2. Гиперфункция передней доли гипофиза
- •16.2. Нарушение функций надпочечников
- •16.2.1. Кортикостероидная недостаточность
- •16.2.2. Гиперкортикостероидизм
- •16.2.3. Гиперфункция мозгового слоя надпочечников
- •16.3. Нарушение функций щитовидной железы
- •16.3.1. Гипертиреоз
- •16.3.2. Гипотиреоз
- •16.4. Нарушение функций околощитовидных желез
- •16.5. Нарушение функций половых желез
- •17.1. Краткие сведения
- •17.2. Атеросклероз
- •17.2.1. Теории происхождения
- •17.2.2. Регресс атеросклероза
- •17.3. Нарушение коронарного кровотока
- •17.3.1. Ишемия миокарда
- •17.3.2. Оглушенный и бездействующий миокард
- •17.4.Артериальная гипертензия
- •Гипертоническая болезнь!
- •17.4.1. Патогенез гипертонической болезни
- •17.4.2. Вторичная артериальная гипертензия
- •17.6. Механизмы развития сердечной недостаточности
- •17.6.2. Диастолическая форма сердечной недостаточности
- •17.7. Механизмы развития аритмий
- •17.7.1. Нарушение образования импульсов
- •17,7,2, Риэнтри
- •17.7.3. Нарушение проводимости
- •Внешнего дыхания
- •18.1. Определение понятия «дыхательная недостаточность»
- •18.2. Оценка функций внешнего дыхания придыхательной недостаточности
- •18.3. Патофизиологические варианты дыхательной недостаточности
- •18.3.1. Центрогенная дыхательная недостаточность
- •18.3.2. Нервно-мышечная дыхательная недостаточность
- •18.3.3. «Каркасная» дыхательная недостаточность
- •18.3.4. Механизмы дыхательной недостаточности при патологии дыхательных путей
- •18.3.5. Паренхиматозная дыхательная недостаточность
- •18.4. Показатели газового состава крови при дыхательной недостаточности
- •18.4.1. Гипоксемическая (I типа) дыхательная недостаточность
- •18.4.2. Гиперкапнически-гипоксемический (вентиляционный) тип дыхательной недостаточности
- •19.1. Основы регуляции клеточного цикла
- •19.2. Патология красной крови
- •19.2.1. Анемии
- •19.2.2. Эритроцитозы
- •19.4. Патология белой крови
- •19.4.1. Лейкоцитопении
- •19.4.2. Лейкоцитоз
- •19.5. Лейкозы (гемобластозы, лейкемии)
- •20.1. Факторы, свертывающие кровь
- •VIll/vWf I
- •20.2. Геморрагические синдромы
- •20.4. Синдром диссеминированного
- •20.5. Методы оценки нарушений системы гемокоагуляции
- •21.1. Нарушение лимфообразования
- •Глава 1. Общее учение о болезни 92
- •Глава 6. Патологическая физиология периферического (органного) кровообращения 705
- •Глава 12. Патологическая физиология 1247
- •21.2. Недостаточность транспорта лимфы
- •21.3. Нарушение свертывания лимфы
- •21.4. Роль лимфатической системы в развитии отека
- •21.5. Функции лимфатической системы при развитии воспаления
- •22.1. Нарушение функций пищевода
- •22.2. Нарушение функций желудка
- •22.2.1. Нарушения секреции соляной кислоты и пепсина
- •22.2.2. Нарушение слизеобразующей функции желудка
- •22.2.3. Патофизиологические механизмы язвенной болезни
- •22.2.4. Нарушение двигательной функции желудка
- •22.3. Патофизиологические механизмы болей в животе
- •22.4. Нарушение экзокринной функции поджелудочной железы
- •22.4.1. Патофизиологические механизмы развития острого панкреатита
- •22.4.2. Патофизиологические механизмы развития хронического панкреатита
- •22.5. Нарушение функций кишечника
- •22.5.1. Нарушение переваривания и всасывания в кишечнике
- •22.5.2. Нарушения двигательной функции кишечника
- •23.1. Печеночно-клеточная недостаточность
- •23.2. Патофизиологические механизмы синдрома портальной гипертензии
- •23.3. Патофизиологические механизмы желтухи
- •24.1. Нарушение клубочковой фильтрации
- •24.2. Нарушение функций канальцев
- •24.3. Изменение состава мочи
- •24.4. Нефротический синдром
- •24.5. Острая почечная недостаточность
- •24.6. Хроническая почечная недостаточность
- •24.7. Мочекаменная болезнь
5.4. Атопия. Атонические и псевдоатопические заболевания
5.4.1. Механизмы развития
Установлено, что у людей имеются заболевания, сходные с анафилактическими реакциями, воспроизводимыми в эксперименте у животных. Однако по ряду признаков они отличаются от анафилаксии, и чтобы подчеркнуть отличие этой группы заболеваний A.F. Coca и R.A. Cooke в 1923 г. обозначили их термином «атопия» (от греч. atopia — странность, необычность).
К группе классических атопических болезней относят круглогодичный атопический ринит, поллиноз (от англ. pollen — пыльца), атопичес- кую форму бронхиальной астмы и атопический дерматит. Близки с этой группой по механизму развития определенные острые аллергические реакции на лекарства и пищевые продукты.
К признакам, характеризующим атопию (табл 5.3) относятся естественное возникновение, наследственная предрасположенность, возможность повреждения любой системы организма в отличие от анафилаксии, при которой всегда имеется определенный шоковый орган в пределах одного вида животных. При реакциях обоих видов повреждение тканей вызывается аллергическими механизмами первого типа. Однако в последнее время стало ясно, что атопия отличается от анафилакси
и
еще одним важным признаком — в ее развитии большую роль играют неспецифические (неиммунные) механизмы. Таким образом, атопия это более широкий феномен, чем анафилаксия, поэтому нельзя сводить ато- пию только к повреждению, связанному с развитием аллергических механизмов первого типа.
|
Таблица 5.3 Показатель |
Анафилаксия |
Атопия |
|
* Условия воспроизведения Роль наследственности Шоковый орган Участвующие механизмы:
|
Искусственное Незначительная Один в пределах вида I тип аллергических реакций Незначительное влияние |
Естественное Выраженная Любой I тип аллергических реакций Выраженное влияние |
Наследственная предрасположенность — важнейший признак ато- пии. В настоящее время обсуждается возможность участия в ее развитии около 20 генов, для многих генов определены их локализация и связь с тем или иным признаком атопии. Их обнаружили на хромосомах 4, 5,6,7, 11, 13, 14. W. Cookson (1996) условно разделил их наследующие классы:
класс — гены, в общем предрасполагающие к развитию атопии (вклю
чение lgE-опосредованного воспаления) и увеличению общего IgE;
класс — гены, влияющие на специфический lgE-ответ;
класс — гены, влияющие на бронхиальную гиперреактивность незави
симо от атопии;
класс — гены, определяющие развитие воспаления, не связанные с IgE-
ответом.
Таким образом, основу развития атопии составляет тот набор генов, который передается по наследству. Однако эта наследственная предрасположенность не создает фенотипа атопии, а является лишь способствующим условием. Реализация этой предрасположенности в клинические проявления атопии (атопический фенотип) происходит только при воздействии соответствующих факторов окружающей среды. Таковыми факторами для каждого индивидуума служат «свои» аллергены.
Уже упоминалось, что в развитии атопии принимают участие группы механизмов: специфические (иммунные) и неспецифические (неиммунные). Все изменения в организме, связанные с включением этих механизмов, в большей или меньшей степени возможны при всех классических атопических заболеваниях.
Различия
между анафилаксией и атопией
дифференцировки нулевых Т-хелперных клеток (Тх-0). При обычном ответе на антиген Тх0 дифференцируется главным образом в ТХ1, которые секретируют ИЛ-2 (интерлейкин-2), у-интерферон (у-ИФ) и ряд других медиаторов, что активирует развитие клеточного механизма иммунитета (схема 5.1)
.
Тх2
секреция ИЛ-4, ИЛ-5, ИЛ-10, ИЛ-13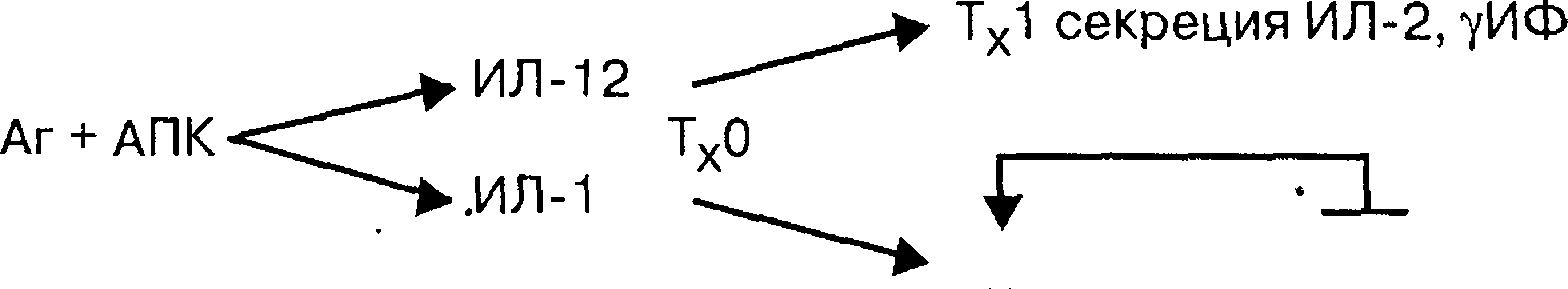
Схема 5.1. Пути дифференцировки ТхО-клеток и роль некоторых интерлейкинов. Аг — антиген; АПК — Аг-представляющая клетка, ИЛ — интерлейкин, Тх — Т-хелперная
клетка.
У людей, предрасположенных к развитию атонических реакций, имеется сдвиг дифференцировки Тх0 в сторону преимущественного образования Тх2-клеток. Последние секретируют главным образом ИЛ-4, ИЛ-5, ИЛ-3, ИЛ-10 и ряд других медиаторов. Эти медиаторы, особенно ИЛ-4, переключают в В-лимфоцитах синтез антител с G-класса на Е-класс. Между Тх1- и Тх2-зависимыми ответами имеется конкуренция. При преобладании Тх2-зависимого ответа угнетается ТХ1-зависимый ответ и наоборот. В связи с этим при атопических заболеваниях выявляют угнетение клеточного и в определенной степени гуморального звеньев иммунитета, что в далеко зашедших случаях приводит к развитию инфекционных процессов в виде пиодермии, хронического отита, гайморита, бронхита и др.
У здоровых людей содержание общего IgE в плазме крови варьирует от 0 до 40—60 ед/мл (1 Международная единица = 2,4 нг). Оно наименьшее при рождении, затем увеличивается и к 10—12-летнему возрасту стабилизируется. При атопических заболеваниях в 80—85 % случаев концентрация общего IgE повышается до 100—120 ед/мл и более и может достигать нескольких тысяч единиц. Общим он называется потому, что в его состав входят как lgE-антитела к определенному аллергену, так и молекулы IgE, которые неспецифичны к данному аллергену. Одновременно с увеличением общего IgE возрастает, как правило, и специфический IgE. Однако в ряде случаев при атопических заболеваниях вместе с повышением уровня общего IgE или без такового в сыворотке крови обнаруживали lgG4, который, как и IgE, может фиксироваться набазофилах и выполнять роль реагинов.
Образовавшиеся под влиянием аллергена lgE-антитела и молекулы неспецифического IgE фиксируются на клетках через Fc- рецепторы. Различают два вида этих рецепторов. Первый вид — классические высокоаффинные рецепторы (FceRI), которые находятся на тучных клетках и базофилах. Считают, что на одном базофиле может фик
сироваться от 30x103 до 400x103 молекул IgE. Большая их часть приходится на молекулы неспецифического IgE; концентрация специфического IgE, как правило, меньше. Второй тип рецепторов — низкоаффинные (FceRII). Они находятся на макрофагах, эозинофилах и тромбоцитах и не имеют перекрестной специфичности с первым видом рецепторов. Афинность этих рецепторов, как и число несущих их клеток, может возрастать. Это ведет к тому, что начальный механизм развития аллергической реакции немедленного типа (ранняя фаза в первые 15—20 мин) может иметь продолжение в виде отсроченной фазы (через 4—8 ч), характеризующейся развитием воспаления. В развитии отсроченной фазы большую роль играет накопление в месте начальной реакции клеток, участвующих в воспалении. Это главным образом эозинофилы, а также нейтрофилы, макрофаги и лимфоциты. На их поверхности через рецепторы второго типа фиксируется специфический IgE. С ним соединяется соответствующий аллерген, в результате эти клетки высвобождают ряд медиаторов, обладающих провоспалительной активностью (катионные белки, активные формы кислорода и др.). Поздняя фаза аллергических реакций немедленного типа у больных бронхиальной астмой проявляется повышением чувствительности и реактивности бронхов к различным неспецифическим раздражителям (холодный воздух, острые и резкие запахи и др.) и сопровождается бронхиальной обструкцией. У лиц, перенесших анафилактический шок, он может повториться (через несколько часов после того, как пациент был выведен из этого состояния). У15—20 % больных атопией общий IgE находится в пределах нормы или ее верхней границы. Кроме атопических заболеваний, уровень IgE может повышаться при респираторных вирусных заболеваниях, некоторых первичных имму- нодефицитах, заболеваниях печени.
Патохимическая стадия реакции I типа начинается после связывания аллергена с lgE-антителами, как циркулирующими, так и фиксиро1 ванными на клетках (аллерген образует мостики между фиксированными на клетках lgE-антителами).
Активация тучных и базофильных клеток приводит к высвобождению различных медиаторов, что морфологически определяется как их дегра- нуляция. Процесс высвобождения медиаторов требует энергетического обеспечения, поэтому блокада энергообразования блокирует и выброс медиаторов.
Из тучных клеток и базофильных лейкоцитов выделены различные медиаторы, причем некоторые из них находятся в клетках в готовом виде. Одни из них легко секретируются из имеющегося «запаса» (гистамин, серотонин, различные эозинофильные хемотаксические факторы), другие труднее высвобождаются из клетки, так как входят в состав матрикса гранул (гепарин, арилсульфатаза А, галактозидаза, хемотрипсин, супе- роксиддисмутаза и др.). Ряд медиаторов предварительно не депонируется. Они образуются после стимуляции клетки (лейкотриены, тромбо- цитактивирующие факторы и др.). Эти медиаторы, обозначаемые как первичные, действуют на сосуды и клетки-мишени опосредованно, включая в развитие аллергической реакции эозинофилы, тромбоциты и другие клетки. В результате к месту активации тучных клеток мигрируют эозинофильные и нейтрофильные гранулоциты, которые в свою очередь также начинают выделять медиаторы, обозначаемые как вторичные — фосфолипаза Д, арилсульфатаза В, гистаминаза (диаминооксидаза), лей- котриены и др.
Накапливающиеся медиаторы оказывают патогенное действие на клетки, что приводит к развитию патофизиологической стадии.
Неспецифические механизмы:
нарушения равновесия влияний симпатической и парасимпатической иннервации систем организма, менее выраженные при рините и наиболее резко — при атопическом дерматите.
При всех трех классических атопических заболеваниях увеличена хо- линергическая реактивность, что проявляется более резким сужением зрачка на закапывание в глаза холиномиметиков по сравнению с таковым у здоровых лиц. При сочетании астмы с дерматитом усилено спонтанное и стимулированное холиномиметиками потоотделение. При ато- пической астме, кроме того, повышен холинергический тонус бронхов, что проявляется либо приступом астмы, либо повышением реактивности и чувствительности бронхов при проведении провокационных тестов с холиномиметиками.
При атопии p-2-адренергическая реактивность снижена. A. Szen- tivahyi (1968) выдвинул даже Р-адренергическую теорию атопических нарушений при бронхиальной астме и развития атопии вообще. Сниженная Р2-адренореактивность проявляется меньшей степенью гликогенолиза, липолиза, повышения пульсового давления и образования цАМФ в лейкоцитах при добавлении адреналина или изопротеринола по сравнению с таковой у здоровых лиц.
Одновременно усиливается а-адренореактивность, что не выявляют при ринитах; ее можно обнаружить при астме и особенно резкое увеличение при атопическом дерматите. У последних отмечается выраженная вазоконстрикция в виде белого дермографизма, бледного цвета кожи лица и снижения температуры кожи пальцев;
повышенная способность тучных клеток и базофилов высвобождать медиаторы как спонтанно, так и в ответ на различные неиммунологические стимулы. Установлено, что базофилы больных атопическим ринитом и/или астмой, атопическим дерматитом более легко, чем лейкоциты здоровых людей, высвобождают гистамин в ответ на различные неиммунологические (неспецифические) стимулы (метахолин, Кон-А, кальциевые ионофоры, полимиксин-В и др.). Более того, у этих больных возможно спонтанное выделение гистамина базофилами. Аналогичными свойствами обладают тучные клетки из бронхоальвеолярного смыва у больных ато- пической астмой. Этот эффект связывают с повышенной активностью в клетках фосфодиэстеразы цАМФ и снижением концентрации последнего. Угнетение фосфодиэстеразы в этих клетках приводило к повышению уровня цАМФ и нормализации высвобождения гистамина
;
3) известно, что атопия сопровождается различной степенью эозино- филии и инфильтрацией слизистых оболочек и секретов дыхательных путей и желудочно-кишечного тракта.
Особенности
реактивности людей трех конституциональных
типов
|
Таблица 5.4 Признаки |
Тип конституции | ||
|
атопический |
псевдоатопический |
неатопический | |
|
Механизмы |
Специфические и |
Только или |
Нет |
|
развития атопии |
неспецифические |
главным образом |
|
|
|
|
неспецифические |
|
|
Преобладание |
Нет |
Есть |
Есть |
|
ТХ1-зависимой |
|
|
|
|
реакции |
|
|
|
|
Преобладание |
Есть |
Нет |
Нет |
|
Тх2-зависимой |
|
|
|
|
реакции |
|
|
|
|
Исходно сущест |
Есть |
Есть |
Нет |
|
вующая неспеци |
|
|
|
|
фическая гиперре |
|
|
|
|
активность тканей |
|
|
|
У лиц атопической конституции поступление аллергена сопровождается развитием типичных атопических заболеваний (поллиноз, круглогодичный атопический ринит, атопический вариант бронхиальной астмы и др.). Лица с псевдоатопической конституцией, имеющие главным образом неспецифические механизмы из атопического генотипа, не реагируют на аллергены; причинными факторами у них становятся ирританты (раздражающие вещества) и псевдоаллергены (например, нестероидны
е
противовоспалительные препараты, физическая нагрузка и др.). Проявления псевдоатопических заболеваний сходны с таковыми при истинных атопических заболеваниях, хотя они не имеют в своем патогенезе IgE- опосредованных иммунных механизмов, поэтому общий IgE у таких лиц в норме и не удается найти аллергена.
Объектом атопической альтерации может быть любая система организма. Развитие повреждения той или иной системы организма определяется не только его общими свойствами, или конституцией, но и особенностями реактивности того или иного «шокового» органа (системы организма). Именно это, наряду с природой аллергена и путями его поступления и, определяет локализацию процесса и появление определенного атопического заболевания.
Особенности реактивности «шокового» органа определяются многими влияниями на его функционирование. Из них наибольшую роль играет сдвиг в балансе влияний парасимпатического и симпатического отделов нервной системы на данный орган. Обычно это проявляется в какой-либо одной системе организма. Так, белый дермографизм выявляют только при атопическом дерматите, но его, как правило, не бывает при атопическом рините или астме. При астме повышена холинореактив- ность дыхательных путей, но она не проявляется при атопическом дерматите, сопровождающемся поражением только кожи.
