
- •Патологическая физиология
- •Глава 1. Общее учение о болезни 92
- •Глава 6. Патологическая физиология периферического (органного) кровообращения 695
- •Глава 12. Патологическая физиология 1237
- •.Краткие сведения об истории патологической физиологии
- •Экспериментально-физиологическое, физико-химическое направление
- •.Часть первая общая нозология
- •Глава 1. Общее учение о болезни
- •1.1. Здоровье и болезнь
- •1.1.1. Норма и здоровье
- •1.1.2. Определение сущности болезни
- •1.1.3. Патологическая реакция, патологический процесс, патологическое состояние
- •1.2. Общие вопросы учения об этиологии болезней
- •1.3. Общие вопросы учения о патогенезе болезней
- •1.4. Исходы болезни
- •На повреждение
- •2.1. Общая патология клетки
- •2.1.1. Повреждение клеток в патологии
- •2.1.2. Нарушение функций клеточных структур
- •Кусочки ткани Выделенные митохондрии
- •Время переживания органа при 24°с (мин)
- •2.1.3. Механизмы нарушения барьерной функции биологических мембран
- •СюТоксическое действие
- •Токсическое действие
- •2.1.4. Другие причины нарушения барьерных свойств липидного слоя мембран
- •Глава 1. Общее учение о болезни 92
- •Глава 6. Патологическая физиология периферического (органного) кровообращения 705
- •Глава 12. Патологическая физиология 1247
- •2.1.5. Нарушение электрической стабильности липидного слоя
- •2.2. Общие реакции организма на повреждение
- •2.2.1. Общий адаптационный синдром (стресс)
- •2.2.2. Активация протеолитических систем плазмы крови
- •I Фактор Хагемана Калликреин j I Прекалликреин
- •2.2.4. Кома
- •2.2.5. Ответ острой фазы
- •2.2.5.2. Главные медиаторы ответа острой фазы
- •3.1. Реактивность организма
- •3.2. Виды реактивности
- •3.5. Резистентность
- •3.6. Факторы, влияющие на реактивность
- •3.7. Роль наследственности
- •Гидрооксифенил виноградная кислота
- •Фенилпиро- виноградная кислота
- •Гомоге нти зи н о вая кислота
- •Гомогентизиноксидаза (алкаптонурия)
- •4.1. Основные представления о строении
- •4.2. Общая стратегия иммунной защиты
- •4.3. Иммунодефицитные состояния
- •4.3.1. Первичные иммунодефициты
- •4.3.2. Вторичные иммунодефициты
- •4.4. Аутоиммунные процессы
- •4.5. Лимфопролиферативные процессы
- •5.1. Взаимоотношение аллергии и иммунитета
- •5.3. Специфические аллергические реакции
- •5.3.1. Аллергические реакции I типа (анафилактические)
- •5.3.2. Аллергические реакции II типа
- •5.3.3. Аллергические реакции III типа
- •5.3.4. Аллергические реакции IV типа
- •Характеристика повышенной чувствительности немедленного и замедленного типов
- •5.4. Атопия. Атонические и псевдоатопические заболевания
- •5.4.1. Механизмы развития
- •5.4.2. Механизмы обратимой обструкции дыхательных путей
- •5.5. Псевдоаллергия
- •5.5.1. Гистаминовый тип псевдоаллергии
- •5.5.2. Нарушение активации системы комплемента
- •5.5.3. Нарушения метаболизма арахидоновой кислоты
- •Глава 6. Патологическая физиология периферического (органного) кровообращения и микроциркуляции
- •Состояние кровотока в микрососудах при артериальной гиперемии, ишемии, капиллярном стазе и венозном застое крови,
- •Признаки расстройства периферического кровообращения (в.В. Воронин, модификация г.И. Мчедлишвили)
- •6.1. Артериальная гиперемия
- •6.3. Нарушение реологических свойств крови, вызывающее стаз в микрососудах
- •6.4. Венозный застой крови
- •Превалирование резорбция вал фильтрацией я оды а микрооо- суддк мозга
- •6.6. Кровоизлияние в мозг
- •7.1. Нарушение микроциркуляции
- •7.2. Воспалительные экссудаты
- •7.3. Эмиграция лейкоцитов периферической крови
- •7.4. Фагоцитоз
- •7.5. Специализированные функции нейтрофилов, моноцитов
- •7.6. Медиаторы воспаления
- •7.7. Исходы воспаления
- •8.1. Этиология
- •8.3. Функция органов и систем
- •9.1. Нарушение обмена белков
- •9.1.1. Нарушение расщепления и всасывания белков
- •9.1.4. Патология межуточного обмена белков (нарушение обмена аминокислот)
- •9.1.5. Изменение скорости распада белка
- •9.1.6. Патология конечного этапа обмена белков
- •9.2. Нарушение обмена липидов
- •9.2.1. Нарушение транспорта липидов и перехода их в ткани
- •9.2.2. Роль нарушений липидного обмена в патогенезе атеросклероза
- •9.2.3. Жировая инфильтрация и жировая дистрофия
- •9.3. Нарушение обмена углеводов
- •9.3.3. Нарушение регуляции углеводного обмена
- •9.4. Нарушение водного баланса
- •9.4.1. Основы регуляции водного баланса
- •9.4.2. Формы нарушения водного баланса
- •9.4.2.1. Увеличение объема внеклеточной жидкости (гиперволемия)
- •9.4.2.2. Уменьшение объема внеклеточной жидкости (гиповолемия)
- •9.5. Нарушение электролитного баланса
- •Организма человека
- •9.5.1. Нарушение баланса натрия
- •9.5.2. Нарушение баланса калия
- •9.5.3. Нарушение баланса кальция
- •9.5.4. Нарушение баланса фосфатов
- •9.5.5. Нарушение баланса магния
- •9.6. Нарушение кислотно-основного баланса
- •9.6.1. Основы регуляции кислотно-основного баланса
- •0A* й к * 5 сз" 5 неш Лшкжы Анионы КаикшыКат ионы
- •9.6.2. Основные показатели коб
- •9.6.3. Формы нарушения кислотно-основного баланса
- •9.6.3.1. Респираторный ацидоз
- •9.6.3.2. Метаболический ацидоз
- •9.6.3.3. Респираторный алкалоз
- •9.6.3.4. Метаболический алкалоз
- •9.6.3.5. Смешанные нарушения кислотно-основного баланса
- •10.2. Компенсаторно-приспособительные реакции при гипоксии
- •10.3. Нарушение обмена веществ
- •10.4. Коррекция гипоксии: необходим избыток или недостаток кислорода?
- •11.1. Механизмы клеточного деления
- •11 »2. Патофизиология клеточного деления
- •11.2.1. Активация онкогенов
- •11.2.2. Инактивация генов-супрессоров
- •11.2.3. Нарушение апоптоза
- •11.2.4. Нарушение механизмов репарации днк
- •11.3. Опухолевый рост
- •11.3.2. Этиология опухолей
- •11.3.3. Свойства опухолевых клеток in vitro
- •11.3.4. Межклеточная кооперация
- •11.3.5. Свойства злокачественных опухолей
- •11.3.6. Взаимоотношения опухоли и организма
- •11.3.7. Механизмы резистентности опухолей к терапевтическим воздействиям
- •.Часть третья нарушение функций органов и систем
- •Глава 12. Патологическая физиология нервной системы
- •12.1. Общие реакции нервной системы на повреждение
- •12.2. Нарушение функции нервной системы,
- •12.3. Метаболические энцефалопатии
- •12.4. Повреждение мозга,
- •12.5. Расстройства функций нервной системы, обусловленные повреждением миелина
- •12.6. Нарушение нервных механизмов управления движениями
- •12.6.1. Расстройства движений,
- •12.6.1.1. Болезни моторных единиц
- •12.6.1.2. Расстройства движений
- •12.6.1.3. Нарушение движений при повреждении мозжечка
- •12.6.1.4. Нарушение движений
- •13.1. Нарушение механизмов регуляции артериального давления
- •13.2. Расстройства функций мочевого пузыря
- •13.5. Вегетативные расстройства,
- •15.1. Нарушение центральных механизмов регуляции
- •15.2. Патологические процессы в железах
- •15.3. Периферические (внежелезистые) механизмы нарушения активности гормонов
- •15.4. Роль аутоаллергических (аутоиммунных) механизмов в развитии эндокринных нарушений
- •1]ДиОТипиЧесИиЕ ahtuteaa
- •16.1. Нарушение функций гипофиза
- •16.1.1. Недостаточность функции гипофиза
- •16.1.2. Гиперфункция передней доли гипофиза
- •16.2. Нарушение функций надпочечников
- •16.2.1. Кортикостероидная недостаточность
- •16.2.2. Гиперкортикостероидизм
- •16.2.3. Гиперфункция мозгового слоя надпочечников
- •16.3. Нарушение функций щитовидной железы
- •16.3.1. Гипертиреоз
- •16.3.2. Гипотиреоз
- •16.4. Нарушение функций околощитовидных желез
- •16.5. Нарушение функций половых желез
- •17.1. Краткие сведения
- •17.2. Атеросклероз
- •17.2.1. Теории происхождения
- •17.2.2. Регресс атеросклероза
- •17.3. Нарушение коронарного кровотока
- •17.3.1. Ишемия миокарда
- •17.3.2. Оглушенный и бездействующий миокард
- •17.4.Артериальная гипертензия
- •Гипертоническая болезнь!
- •17.4.1. Патогенез гипертонической болезни
- •17.4.2. Вторичная артериальная гипертензия
- •17.6. Механизмы развития сердечной недостаточности
- •17.6.2. Диастолическая форма сердечной недостаточности
- •17.7. Механизмы развития аритмий
- •17.7.1. Нарушение образования импульсов
- •17,7,2, Риэнтри
- •17.7.3. Нарушение проводимости
- •Внешнего дыхания
- •18.1. Определение понятия «дыхательная недостаточность»
- •18.2. Оценка функций внешнего дыхания придыхательной недостаточности
- •18.3. Патофизиологические варианты дыхательной недостаточности
- •18.3.1. Центрогенная дыхательная недостаточность
- •18.3.2. Нервно-мышечная дыхательная недостаточность
- •18.3.3. «Каркасная» дыхательная недостаточность
- •18.3.4. Механизмы дыхательной недостаточности при патологии дыхательных путей
- •18.3.5. Паренхиматозная дыхательная недостаточность
- •18.4. Показатели газового состава крови при дыхательной недостаточности
- •18.4.1. Гипоксемическая (I типа) дыхательная недостаточность
- •18.4.2. Гиперкапнически-гипоксемический (вентиляционный) тип дыхательной недостаточности
- •19.1. Основы регуляции клеточного цикла
- •19.2. Патология красной крови
- •19.2.1. Анемии
- •19.2.2. Эритроцитозы
- •19.4. Патология белой крови
- •19.4.1. Лейкоцитопении
- •19.4.2. Лейкоцитоз
- •19.5. Лейкозы (гемобластозы, лейкемии)
- •20.1. Факторы, свертывающие кровь
- •VIll/vWf I
- •20.2. Геморрагические синдромы
- •20.4. Синдром диссеминированного
- •20.5. Методы оценки нарушений системы гемокоагуляции
- •21.1. Нарушение лимфообразования
- •Глава 1. Общее учение о болезни 92
- •Глава 6. Патологическая физиология периферического (органного) кровообращения 705
- •Глава 12. Патологическая физиология 1247
- •21.2. Недостаточность транспорта лимфы
- •21.3. Нарушение свертывания лимфы
- •21.4. Роль лимфатической системы в развитии отека
- •21.5. Функции лимфатической системы при развитии воспаления
- •22.1. Нарушение функций пищевода
- •22.2. Нарушение функций желудка
- •22.2.1. Нарушения секреции соляной кислоты и пепсина
- •22.2.2. Нарушение слизеобразующей функции желудка
- •22.2.3. Патофизиологические механизмы язвенной болезни
- •22.2.4. Нарушение двигательной функции желудка
- •22.3. Патофизиологические механизмы болей в животе
- •22.4. Нарушение экзокринной функции поджелудочной железы
- •22.4.1. Патофизиологические механизмы развития острого панкреатита
- •22.4.2. Патофизиологические механизмы развития хронического панкреатита
- •22.5. Нарушение функций кишечника
- •22.5.1. Нарушение переваривания и всасывания в кишечнике
- •22.5.2. Нарушения двигательной функции кишечника
- •23.1. Печеночно-клеточная недостаточность
- •23.2. Патофизиологические механизмы синдрома портальной гипертензии
- •23.3. Патофизиологические механизмы желтухи
- •24.1. Нарушение клубочковой фильтрации
- •24.2. Нарушение функций канальцев
- •24.3. Изменение состава мочи
- •24.4. Нефротический синдром
- •24.5. Острая почечная недостаточность
- •24.6. Хроническая почечная недостаточность
- •24.7. Мочекаменная болезнь
2.1.5. Нарушение электрической стабильности липидного слоя
Явление электрического пробоя мембран. Явление электрического пробоя мембран изучалось многими авторами на искусственных мембранах и отдельных клетках. Мембраны обладают определенным
сопротивлением (R) электрическому току (I), которое при небольшой разности потенциалов (U) между двумя сторонами мембраны является постоянной величиной. Иными словами, для мембраны соблюдается закон Ома:
I = U/R .
Это означает, что зависимость между напряжением на мембране (и) и током через мембрану (I) линейная. Однако такая зависимость сохраняется при сравнительно небольших величинахи — обычно не выше 200— 300 мВ. При определенной критической разности потенциалов на мембране, называемой «потенциалом пробоя» (U*), происходит резкое возрастание тока. При постоянном мембранном потенциале, если он превышает критическое значение, ток самопроизвольно нарастает во времени до полного разрушения мембраны. Это явление называется электрическим пробоем мембраны.
В основе этого явления лежит самопроизвольное зарождение дефектов в липидном бислое вследствие теплового движения фосфолипид- ных молекул. При отсутствии разности потенциалов на мембране размеры спонтанно образовавшихся пор не увеличиваются, так как этот процесс сопровождается ростом площади раздела фаз липид — вода и требует преодоления очень значительных сил поверхностного натяжения на границе раздела фаз. Более того, под действием сил поверхностного натяжения спонтанно образовавшийся дефект (пора) сразу же затягивается, и мембрана остается целой. Увеличение разности потенциалов на мембране уменьшает энергию, необходимую для образования и роста поры. При критической разности потенциалов U* рост спонтанно образовавшихся пор становится самопроизвольным, ток через мембрану резко возрастает, а если разность потенциалов поддерживать, мембрана будет полностью разрушена.
Для патологии клетки является чрезвычайно важным то обстоятельство, что электрическая прочность мембран, мерой которой служит потенциал пробоя, снижается под действием повреждающих факторов. Как уже говорилось, основными причинами нарушения барьерных свойств мембран в патологии являются перекисное окисление липидов, действие мембранных фосфолипаз, механическое растяжение мембран или адсорбция на них некоторых белков. Изучение влияния этих действующих факторов на электрическую прочность мембран показало, что все они снижают потенциал пробоя мембран.
Пробой мембран собственным мембранным потенциалом («самопробой»). Электрический пробой мембраны может наблюдаться не только под действием напряжения, подаваемого на мембрану от внешнего источника, но и под действием собственного мембранного потенциала, т.е. разности потенциалов, возникающей на мембране в результате диффузии ионов. Разумеется, этого не происходит в нормально функционирующих неповрежденных клетках, потому что потенциалы пробоя мембран U* выше, чем разности потенциалов, существующие на клеточных и внутриклеточных мембранах (U* > U)
.
При повреждении мембранных структур потенциал пробоя U* снижается и может сложиться ситуация U* < U, когда мембрана будет «пробиваться» собственным мембранным потенциалом. К чему это приводит в условиях живой клетки? Предположим, клетку облучают ультрафиолетовыми лучами, под влиянием которых в липидных мембранах активируется перекисное окисление. В неповрежденных митохондриях потенциал на мембране равен 175 мВ, а потенциал пробоя составляет около 200 мВ. В процессе активации перекисного окисления липидов потенциал пробоя начинает постепенно снижаться,,и как только он достигает значения 175 мВ, мембрана митохондрий «пробивается» собственным мембранным потенциалом. То же происходит и при активации фосфолипаз: снижение потенциала пробоя до величины, равной существующему на мембране потенциалу, приводит к электрическому пробою мембраны и потере ею барьерных свойств. В опытах с эритроцитами и митохондриями было показано, что и осмотическое растяжение мембраны, и добавление чужеродных белков могут снизить потенциал пробоя мембран настолько, что мембраны начинают «пробиваться» собственным мембранным потенциалом.
Рис.
2.9.
Снижение электрической прочности
мембран (потенциала пробоя)
Время,
мин
при
действии повреждающих воздействиях.
1 — перекисное окисление липидов,
вызванное УФ облучением; 2 — действие
фосфоли пазы А2; 3 — адсорбция поликатиона
(белок протамин-сульфат); 4 — растяжение
мемб
раны,
вызванное разностью гидростатического
давления (АР).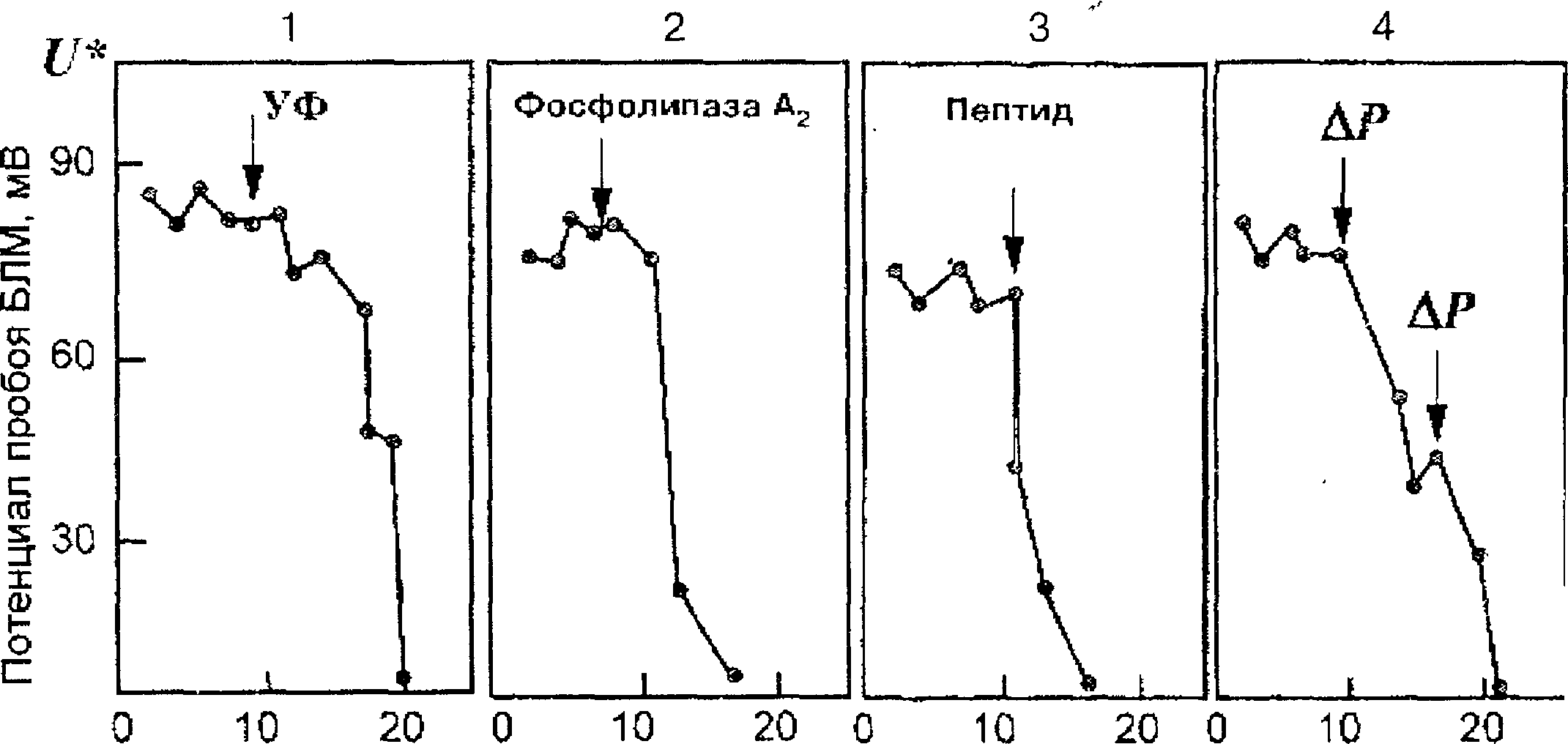
го пробоя дает четкий ответ на этот вопрос. Самопроизвольному росту пор, случайно зародившихся в липидном бислое, препятствуют силы поверхностного натяжения на границе раздела фаз липидный слой мембраны — окружающий водный раствор. Нужно приложить довольно большую разность потенциала к мембране, чтобы преодолеть эти силы и вызвать рост поры. Теперь становится понятно, что вещества, снижающие поверхностное натяжение (детергенты), должны облегчать самопроизвольный рост пор и снижать величину критического потенциала, который нужно приложить к мембране, чтобы вызвать электрический пробой. Это и наблюдается в действительности. Продукты перекисного окисления липидов, так же как и продукты гидролиза фосфолипидов фосфо- липазами (лизолецитины), и многие белки снижают поверхностное натяжение на границах раздела фаз. Именно поэтому они снижают потенциал пробоя мембран, т.е. уменьшают их электрическую прочность (см. рис. 2.9). Механическое растяжение мембраны (ДР на рис. 2.9) действует сходно, так как противодействует силам поверхностного натяжения. Таким образом, электрический пробой мембран оказывается универсальным механизмом нарушения барьерной функции мембран в патологии.
Повышение электрической прочности мембран. Известны два способа, с помощью которых живые клетки повышают свою электрическую прочность: асимметричный поверхностный потенциал и наличие холестерина. Поверхностный потенциал возникает на мембране в случае появления на поверхности липидного слоя заряженных химических группировок, таких, например, как карбоксил или фосфат. Непосредственно на липидный бислой действует потенциал, равный разности между потенциалом в водной среде, омывающей мембрану, и поверхностным потенциалом. За счет неодинакового заряда на поверхностях мембраны реальная разность потенциалов, приложенная к липидному бислою, может быть больше или меньше трансмембранной разности потенциалов. В большинстве биологических мембран заряды распределены таким образом, что разность потенциалов на липидном бислое меньше разности потенциалов между водными растворами, омывающими мембрану. Это повышает реальную электрическую прочность мембраны и снижает вероятность ее самопробоя.
Второй фактор, повышающий электрическую прочность мембран, — это холестерин. Было показано, что включение молекул холестерина в фосфолипидный бислой весьма заметно увеличивает электрическую прочность мембран, т.е. повышает потенциал пробоя. Особенно заметно действие холестерина на поврежденные мембраны. Защитные свойства холестерина против электрического пробоя мембраны можно объяснить его влиянием на вязкость липидного бислоя. Известно, что введение холестерина в фосфолипидный бислой может повысить вязкость последнего в 2—3 раза, что приводит к замедлению образования и роста дефектов (пор) в липидном бислое мембран. Какуже говорилось, именно образование и увеличение дефектов в липидном слое под действием приложенного электрического поля лежат в основе явления электрического пробоя.
Нарушение структурных (матричных) свойств липидного бислоя. Наиболее изучены три характеристики липидного слоя мембран, от которых зависят его свойства как жидкой фазы (матрицы), обеспечивающей функционирование мембранных белков и рецепторов: поверхностный заряд, вязкость и площадь липидного слоя. Все эги характеристики изучаются с помощью флюоресцентных и спиновых зондов.
Перекисное окисление липидов и действие мембранных фосфоли- паз приводят к накоплению в липидной фазе мембран жирных кислот, которые придают мембране при нейтральных рН отрицательный заряд. Увеличение отрицательных зарядов на поверхности мембраны облегчает связывание с мембраной положительно заряженных ионов и белковых молекул, несущих положительные заряды, и, наоборот, уменьшает взаимодействие мембран с другими отрицательно заряженными молекулами или мембранами. Связывая больше Са2", мембраны с большим числом отрицательных зарядов на поверхности становятся более доступны для действия фосфолипаз, но зато хуже связывают ионы Fe2f, которые ускоряют пероксидацию липидов.
Вместе с тем при перекисном окислении липидов увеличивается вязкость липидного слоя мембран. Значительное увеличение вязкости происходит при увеличении содержания в мембранах холестерина. Возрастание вязкости приводит кторможению встроенных в мембраны ферментов, таких, как Na+—К+—АТФаза и Са2+—АТФаза. Это в свою очередь изменяет ионный баланс клетки и может привести к нарушениям метаболизма. Одна из теорий происхождения атеросклероза заключается в том, что увеличение содержания холестерина в крови больных или активация перекисного окисления липидов сопровождается возрастанием вязкости мембран клеток сосудистой стенки, в частности плазматической мембраны мышечных клеток. Это приводит к нарушению работы кальциевой помпы и увеличению концентрации кальция в цитоплазме гладкомы- шечных клеток. В итоге усиливается клеточное деление и развивается ате- росклеротическая бляшка.
С помощью флюоресцентных зондов было показано, что при перекисном окислении уменьшаются площадь поверхности липидного слоя мембран, а также площадь, занимаемая фосфолипидами на поверхности липопротеидов плазмы крови. Это связано с окислением части жирно- кислотных цепей фосфолипидов и выходом их в водную фазу. Одним из результатов такого явления оказывается увеличение относительной концентрации холестерина в липидном монослое на поверхности липопротеидов, подвергнутых перекисному окислению. Липопротеиды низкой плотности (ЛНП) в результате этого переносят еще больше холестерина в клеточные мембраны сосудистой стенки, чем неокисленные ЛНП, и их атерогенность возрастает. Липопротеиды высокой плотности (ЛВП), в норме акцептирующие холестерин с мембран клеток и обладающие анти- атерогенным действием, в результате перекисного окисления полностью теряют способность акцептировать холестерин. Возрастание атероген- ных (холестериндонорных) свойств ЛНП и утрата антиатерогенных (хо- лестеринакцепторных) свойств ЛВП несомненно относятся к числу причин, объясняющих тот факт, что перекисное окисление липидов в сосудистой стенке способствует развитию атеросклероза.
