
- •Патологическая физиология
- •Глава 1. Общее учение о болезни 92
- •Глава 6. Патологическая физиология периферического (органного) кровообращения 695
- •Глава 12. Патологическая физиология 1237
- •.Краткие сведения об истории патологической физиологии
- •Экспериментально-физиологическое, физико-химическое направление
- •.Часть первая общая нозология
- •Глава 1. Общее учение о болезни
- •1.1. Здоровье и болезнь
- •1.1.1. Норма и здоровье
- •1.1.2. Определение сущности болезни
- •1.1.3. Патологическая реакция, патологический процесс, патологическое состояние
- •1.2. Общие вопросы учения об этиологии болезней
- •1.3. Общие вопросы учения о патогенезе болезней
- •1.4. Исходы болезни
- •На повреждение
- •2.1. Общая патология клетки
- •2.1.1. Повреждение клеток в патологии
- •2.1.2. Нарушение функций клеточных структур
- •Кусочки ткани Выделенные митохондрии
- •Время переживания органа при 24°с (мин)
- •2.1.3. Механизмы нарушения барьерной функции биологических мембран
- •СюТоксическое действие
- •Токсическое действие
- •2.1.4. Другие причины нарушения барьерных свойств липидного слоя мембран
- •Глава 1. Общее учение о болезни 92
- •Глава 6. Патологическая физиология периферического (органного) кровообращения 705
- •Глава 12. Патологическая физиология 1247
- •2.1.5. Нарушение электрической стабильности липидного слоя
- •2.2. Общие реакции организма на повреждение
- •2.2.1. Общий адаптационный синдром (стресс)
- •2.2.2. Активация протеолитических систем плазмы крови
- •I Фактор Хагемана Калликреин j I Прекалликреин
- •2.2.4. Кома
- •2.2.5. Ответ острой фазы
- •2.2.5.2. Главные медиаторы ответа острой фазы
- •3.1. Реактивность организма
- •3.2. Виды реактивности
- •3.5. Резистентность
- •3.6. Факторы, влияющие на реактивность
- •3.7. Роль наследственности
- •Гидрооксифенил виноградная кислота
- •Фенилпиро- виноградная кислота
- •Гомоге нти зи н о вая кислота
- •Гомогентизиноксидаза (алкаптонурия)
- •4.1. Основные представления о строении
- •4.2. Общая стратегия иммунной защиты
- •4.3. Иммунодефицитные состояния
- •4.3.1. Первичные иммунодефициты
- •4.3.2. Вторичные иммунодефициты
- •4.4. Аутоиммунные процессы
- •4.5. Лимфопролиферативные процессы
- •5.1. Взаимоотношение аллергии и иммунитета
- •5.3. Специфические аллергические реакции
- •5.3.1. Аллергические реакции I типа (анафилактические)
- •5.3.2. Аллергические реакции II типа
- •5.3.3. Аллергические реакции III типа
- •5.3.4. Аллергические реакции IV типа
- •Характеристика повышенной чувствительности немедленного и замедленного типов
- •5.4. Атопия. Атонические и псевдоатопические заболевания
- •5.4.1. Механизмы развития
- •5.4.2. Механизмы обратимой обструкции дыхательных путей
- •5.5. Псевдоаллергия
- •5.5.1. Гистаминовый тип псевдоаллергии
- •5.5.2. Нарушение активации системы комплемента
- •5.5.3. Нарушения метаболизма арахидоновой кислоты
- •Глава 6. Патологическая физиология периферического (органного) кровообращения и микроциркуляции
- •Состояние кровотока в микрососудах при артериальной гиперемии, ишемии, капиллярном стазе и венозном застое крови,
- •Признаки расстройства периферического кровообращения (в.В. Воронин, модификация г.И. Мчедлишвили)
- •6.1. Артериальная гиперемия
- •6.3. Нарушение реологических свойств крови, вызывающее стаз в микрососудах
- •6.4. Венозный застой крови
- •Превалирование резорбция вал фильтрацией я оды а микрооо- суддк мозга
- •6.6. Кровоизлияние в мозг
- •7.1. Нарушение микроциркуляции
- •7.2. Воспалительные экссудаты
- •7.3. Эмиграция лейкоцитов периферической крови
- •7.4. Фагоцитоз
- •7.5. Специализированные функции нейтрофилов, моноцитов
- •7.6. Медиаторы воспаления
- •7.7. Исходы воспаления
- •8.1. Этиология
- •8.3. Функция органов и систем
- •9.1. Нарушение обмена белков
- •9.1.1. Нарушение расщепления и всасывания белков
- •9.1.4. Патология межуточного обмена белков (нарушение обмена аминокислот)
- •9.1.5. Изменение скорости распада белка
- •9.1.6. Патология конечного этапа обмена белков
- •9.2. Нарушение обмена липидов
- •9.2.1. Нарушение транспорта липидов и перехода их в ткани
- •9.2.2. Роль нарушений липидного обмена в патогенезе атеросклероза
- •9.2.3. Жировая инфильтрация и жировая дистрофия
- •9.3. Нарушение обмена углеводов
- •9.3.3. Нарушение регуляции углеводного обмена
- •9.4. Нарушение водного баланса
- •9.4.1. Основы регуляции водного баланса
- •9.4.2. Формы нарушения водного баланса
- •9.4.2.1. Увеличение объема внеклеточной жидкости (гиперволемия)
- •9.4.2.2. Уменьшение объема внеклеточной жидкости (гиповолемия)
- •9.5. Нарушение электролитного баланса
- •Организма человека
- •9.5.1. Нарушение баланса натрия
- •9.5.2. Нарушение баланса калия
- •9.5.3. Нарушение баланса кальция
- •9.5.4. Нарушение баланса фосфатов
- •9.5.5. Нарушение баланса магния
- •9.6. Нарушение кислотно-основного баланса
- •9.6.1. Основы регуляции кислотно-основного баланса
- •0A* й к * 5 сз" 5 неш Лшкжы Анионы КаикшыКат ионы
- •9.6.2. Основные показатели коб
- •9.6.3. Формы нарушения кислотно-основного баланса
- •9.6.3.1. Респираторный ацидоз
- •9.6.3.2. Метаболический ацидоз
- •9.6.3.3. Респираторный алкалоз
- •9.6.3.4. Метаболический алкалоз
- •9.6.3.5. Смешанные нарушения кислотно-основного баланса
- •10.2. Компенсаторно-приспособительные реакции при гипоксии
- •10.3. Нарушение обмена веществ
- •10.4. Коррекция гипоксии: необходим избыток или недостаток кислорода?
- •11.1. Механизмы клеточного деления
- •11 »2. Патофизиология клеточного деления
- •11.2.1. Активация онкогенов
- •11.2.2. Инактивация генов-супрессоров
- •11.2.3. Нарушение апоптоза
- •11.2.4. Нарушение механизмов репарации днк
- •11.3. Опухолевый рост
- •11.3.2. Этиология опухолей
- •11.3.3. Свойства опухолевых клеток in vitro
- •11.3.4. Межклеточная кооперация
- •11.3.5. Свойства злокачественных опухолей
- •11.3.6. Взаимоотношения опухоли и организма
- •11.3.7. Механизмы резистентности опухолей к терапевтическим воздействиям
- •.Часть третья нарушение функций органов и систем
- •Глава 12. Патологическая физиология нервной системы
- •12.1. Общие реакции нервной системы на повреждение
- •12.2. Нарушение функции нервной системы,
- •12.3. Метаболические энцефалопатии
- •12.4. Повреждение мозга,
- •12.5. Расстройства функций нервной системы, обусловленные повреждением миелина
- •12.6. Нарушение нервных механизмов управления движениями
- •12.6.1. Расстройства движений,
- •12.6.1.1. Болезни моторных единиц
- •12.6.1.2. Расстройства движений
- •12.6.1.3. Нарушение движений при повреждении мозжечка
- •12.6.1.4. Нарушение движений
- •13.1. Нарушение механизмов регуляции артериального давления
- •13.2. Расстройства функций мочевого пузыря
- •13.5. Вегетативные расстройства,
- •15.1. Нарушение центральных механизмов регуляции
- •15.2. Патологические процессы в железах
- •15.3. Периферические (внежелезистые) механизмы нарушения активности гормонов
- •15.4. Роль аутоаллергических (аутоиммунных) механизмов в развитии эндокринных нарушений
- •1]ДиОТипиЧесИиЕ ahtuteaa
- •16.1. Нарушение функций гипофиза
- •16.1.1. Недостаточность функции гипофиза
- •16.1.2. Гиперфункция передней доли гипофиза
- •16.2. Нарушение функций надпочечников
- •16.2.1. Кортикостероидная недостаточность
- •16.2.2. Гиперкортикостероидизм
- •16.2.3. Гиперфункция мозгового слоя надпочечников
- •16.3. Нарушение функций щитовидной железы
- •16.3.1. Гипертиреоз
- •16.3.2. Гипотиреоз
- •16.4. Нарушение функций околощитовидных желез
- •16.5. Нарушение функций половых желез
- •17.1. Краткие сведения
- •17.2. Атеросклероз
- •17.2.1. Теории происхождения
- •17.2.2. Регресс атеросклероза
- •17.3. Нарушение коронарного кровотока
- •17.3.1. Ишемия миокарда
- •17.3.2. Оглушенный и бездействующий миокард
- •17.4.Артериальная гипертензия
- •Гипертоническая болезнь!
- •17.4.1. Патогенез гипертонической болезни
- •17.4.2. Вторичная артериальная гипертензия
- •17.6. Механизмы развития сердечной недостаточности
- •17.6.2. Диастолическая форма сердечной недостаточности
- •17.7. Механизмы развития аритмий
- •17.7.1. Нарушение образования импульсов
- •17,7,2, Риэнтри
- •17.7.3. Нарушение проводимости
- •Внешнего дыхания
- •18.1. Определение понятия «дыхательная недостаточность»
- •18.2. Оценка функций внешнего дыхания придыхательной недостаточности
- •18.3. Патофизиологические варианты дыхательной недостаточности
- •18.3.1. Центрогенная дыхательная недостаточность
- •18.3.2. Нервно-мышечная дыхательная недостаточность
- •18.3.3. «Каркасная» дыхательная недостаточность
- •18.3.4. Механизмы дыхательной недостаточности при патологии дыхательных путей
- •18.3.5. Паренхиматозная дыхательная недостаточность
- •18.4. Показатели газового состава крови при дыхательной недостаточности
- •18.4.1. Гипоксемическая (I типа) дыхательная недостаточность
- •18.4.2. Гиперкапнически-гипоксемический (вентиляционный) тип дыхательной недостаточности
- •19.1. Основы регуляции клеточного цикла
- •19.2. Патология красной крови
- •19.2.1. Анемии
- •19.2.2. Эритроцитозы
- •19.4. Патология белой крови
- •19.4.1. Лейкоцитопении
- •19.4.2. Лейкоцитоз
- •19.5. Лейкозы (гемобластозы, лейкемии)
- •20.1. Факторы, свертывающие кровь
- •VIll/vWf I
- •20.2. Геморрагические синдромы
- •20.4. Синдром диссеминированного
- •20.5. Методы оценки нарушений системы гемокоагуляции
- •21.1. Нарушение лимфообразования
- •Глава 1. Общее учение о болезни 92
- •Глава 6. Патологическая физиология периферического (органного) кровообращения 705
- •Глава 12. Патологическая физиология 1247
- •21.2. Недостаточность транспорта лимфы
- •21.3. Нарушение свертывания лимфы
- •21.4. Роль лимфатической системы в развитии отека
- •21.5. Функции лимфатической системы при развитии воспаления
- •22.1. Нарушение функций пищевода
- •22.2. Нарушение функций желудка
- •22.2.1. Нарушения секреции соляной кислоты и пепсина
- •22.2.2. Нарушение слизеобразующей функции желудка
- •22.2.3. Патофизиологические механизмы язвенной болезни
- •22.2.4. Нарушение двигательной функции желудка
- •22.3. Патофизиологические механизмы болей в животе
- •22.4. Нарушение экзокринной функции поджелудочной железы
- •22.4.1. Патофизиологические механизмы развития острого панкреатита
- •22.4.2. Патофизиологические механизмы развития хронического панкреатита
- •22.5. Нарушение функций кишечника
- •22.5.1. Нарушение переваривания и всасывания в кишечнике
- •22.5.2. Нарушения двигательной функции кишечника
- •23.1. Печеночно-клеточная недостаточность
- •23.2. Патофизиологические механизмы синдрома портальной гипертензии
- •23.3. Патофизиологические механизмы желтухи
- •24.1. Нарушение клубочковой фильтрации
- •24.2. Нарушение функций канальцев
- •24.3. Изменение состава мочи
- •24.4. Нефротический синдром
- •24.5. Острая почечная недостаточность
- •24.6. Хроническая почечная недостаточность
- •24.7. Мочекаменная болезнь
2.2.2. Активация протеолитических систем плазмы крови
Протеолитические системы широко представлены в организме. К ним относятся системы комплемента, калликреин-кининовая, фибрино- литическая, свертывания крови. Все они играют определенную роль в физиологических процессах, а также участвуют в развитии некоторых компенсаторных приспособительных реакций организма при действии на него различных повреждающих факторов. И только в случаях, когда активация этих систем становится неоптимальной данным конкретным условиям, они превращаются в патогенный фактор, обусловливающий развитие патологического процесса. В данном разделе будет показано значение калликреин-кининовой системы и системы комплемента.
Роль калликреин-кининовой системы. Активация этой системы приводит к образованию кининов (сх. 2.1). Кинины — группа биологически активных нейровазоактивных полипептидов. Наиболее изученной является калликреин-кининовая система плазмы крови и один из кининов — нонапептид брадикинин.
Физиологическое значение кининов основано на том, что они ока-
' г
зывают непосредственное влияние на тонус и проницаемость сосудистой стенки, вызывая расширение прекапиллярных сосудов и увеличивая
Запуск
процесса свертывания
кроны
ДктивиРовАиный
фактор
Хагемана

X/
Ловреждающце аоздЕистаия |
ДШВАЦиЯ - угнетенце -
Фрагменты
КШШМОГЕН
=i-K|/IIUH
Kaaaukpeuh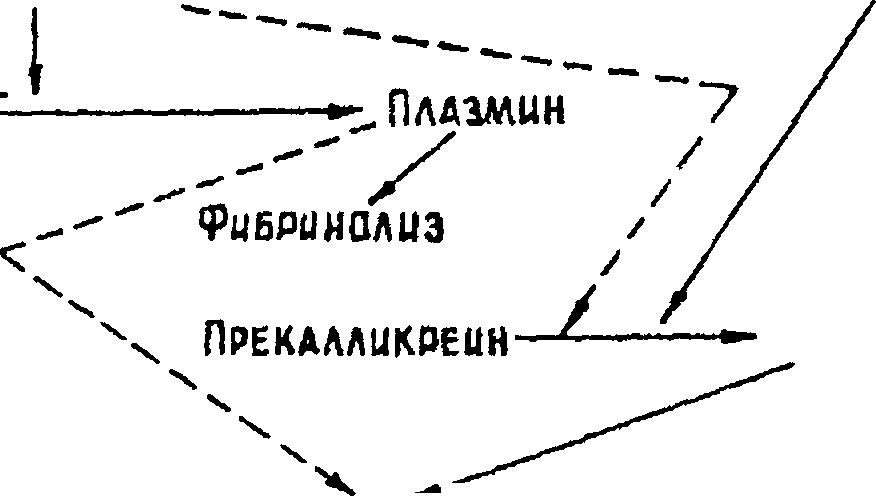
Неактивные
продукт
ы
Кимиидзы
Схема 2 1. Активация калликреин-кининовой систем
ыпроницаемость капилляров. В связи с этим кинины играют особую роль в органах, периодически экскретирующих значительные количества жидкости (слюнные железы, поджелудочная железа, потовые железы, желудок, кишечник).
Активация калликреин-кининовой системы происходит при действии на организм различных повреждающих факторов, нарушающих целость клеток и тканей и приводящих, как правило, к активации фактора Хагема- на. Это— травмы, токсины, облучение, накопление продуктов обмена веществ (например, кристаллов мочекислого натрия), ишемия и др. Обычно в результате местных повреждающих воздействий развивается воспаление. В его развитии определенную роль играет увеличение содержания кининов, которые через изменение сосудистой реакции оказывают влияние на интенсивность и характер воспаления, а также участвуют в формировании чувства боли. Участвуют кинины и в развитии общих реакций организма на повреждение, причем главным образом в формировании компенсаторно-приспособительных механизмов, и только в случаях неадекватного их образования кинины могут стать патогенетическим фактором различных расстройств.
Одно из таких компенсаторно-приспособительных влияний выявляется в генерализованном действии на гемодинамику. При определенной концентрации кинины уменьшают периферическое сопротивление сосудов малого и большого круга кровообращения, что увеличивает возврат крови к сердцу, а это, в свою очередь, увеличивает ударный объем обоих желудочков сердца. Этот механизм может включаться при срочных или длительных адаптивных реакциях организма в условиях действия на него различных факторов в виде эмоциональных или физических нагрузок, тепла, гипоксии и др. При острой ишемии и инфаркте миокарда компенсаторная роль увеличенного образования кининов сводится к расширению сосудов миокарда и увеличению сердечного выброса, а также к развитию гипотензии, что облегчает работу сердца и вызывает перераспределение крови. Неадекватность активации калликреин-кининовой системы может стать патогенетическим фактором развития фатальной гипотензии, шока, болевого эффекта (кардиогенный шок).
Кинины принимают участие в развитии реакций при аллергической альтерации тканей. Аллергическое воспаление, как и обычное, также сопровождается увеличением концентрации кининов. Их обнаруживают в экссудате суставов при ревматоидном артрите, причем иногда в довольно значительной концентрации. Отмечают их увеличение в крови и цереброспинальной жидкости у собак с экспериментальным аллергическим энцефаломиелитом, в миокарде и плазме крови кроликов с экспериментальным аллергическим миокардитом.
Установлено 10—15-кратное увеличение содержания кининов в крови больных людей во время обострения бронхиальной астмы. Очевидно, кинины играют определенную роль в развитии бронхоспазма, так как обладают способностью вызывать при определенной концентрации спазм гладкой мускулатуры бронхиол. Сокращение гладкомышечных клеток пои взаимодействии кининов с рецепторами клетки приводит к активации кальциевых каналов и поступлению кальция в цитоплазму, где он и стимулирует процесс сокращения. Это действие усиливается на фоне снижения активности (3-адренергических рецепторов, а последнее, как правило, выявляется у больных бронхиальной астмой. Поэтому может сложиться и такая ситуация, когда концентрация кининов, недостаточная для того, чтобы вызвать бронхоспазм у здорового человека, будет вызывать его у больного, имеющего сниженную активность (3-адренергических рецепторов.
Активация калликреин-кининовой системы обнаружена при шоках различной этиологии, ревматизме, нефритах, артритах, карциноидном и демпинг-синдромах, атеросклерозе, гипертонической болезни и других заболеваниях. Соотношение защитного и патогенного компонентов в каждом конкретном случае различно. Применяя ингибиторы протеолиза, можно ограничить активность калликреин-кининовой системы и тем самым в той или иной мере ограничить выраженность соответствующих симптомов и интенсивность развития патологического процесса.
Роль системы комплемента. Комплемент— система функционально связанных сывороточных белков, активация которых приводит к образованию биологически активных веществ, участвующих в осуществлении защитных реакций организма. Комплемент обозначают буквой «С», а его компоненты — соответствующей цифрой. При обозначении активированного компонента над цифрой ставится черточка: С1, С2 и т.д. Различают два пути активации комплемента: классический и альтернативный.
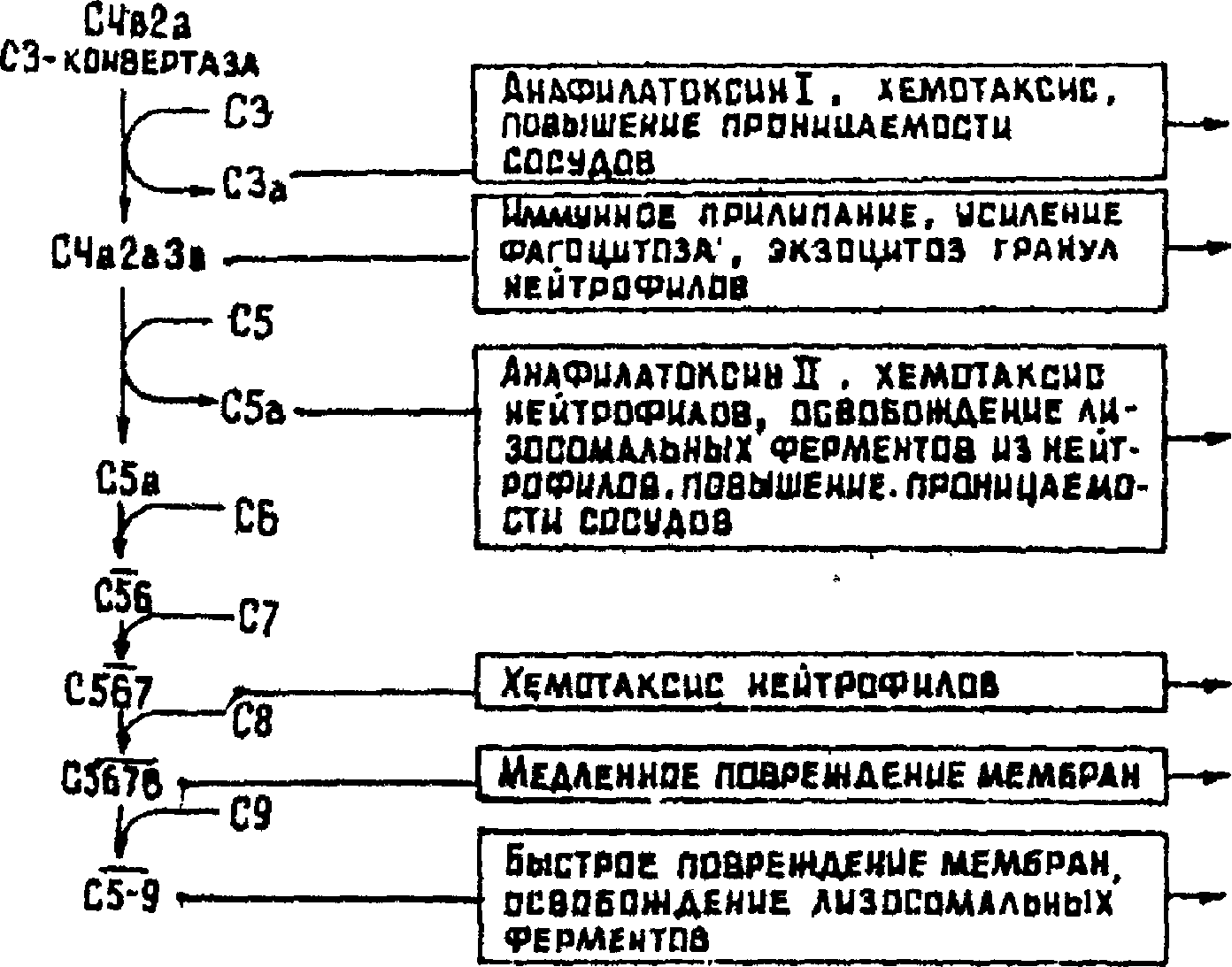
Классический путь активируется комплексом Аг + Ат (схема 2.2). Как видно из схемы, в процессе активации происходит расщепление ряда компонентов С с образованием активных продуктов. Некоторые из них уходят из цепи активации, другие объединяются. Конечным этапом активации является образование комплекса С5—9, оказывающего цито- токсическое действие на клетки-мишени (клетки тканей, микробы с фиксированными на них антителами). Если проанализировать эффекты различных компонентов С, то окажется, что все они участвуют в развитии того или иного компонента воспалительной реакции. Поэтому сложилось представление, что биологический смысл активации С заключается в подключении к иммунной (специфической) реакции неспецифических механизмов защиты — фагоцитоза, воспаления, при помощи которых образовавшийся комплекс фиксируется и фагоцитируется.
Альтернативный путь активации С является важнейшим механизмом противоинфекционной защиты и активируется бактериальными полисахаридами. Он включается быстро и без участия иммунных механизмов. В отличие от классического пути активация начинается с расщепления СЗ с участием ряда дополнительных факторов. Процессы активации комплемента контролируются ингибиторами различных звеньев этой системы. Наиболее изучены С1- и СЗ-ингибиторы. С1-ингибитор эстеразы блокирует спонтанную активацию С1. Кроме того, он ограничивает активность калликреин-кининовой и фибринолитической систем.Cf<* + Clr + Cfs
т
♦АГ![]()
CI
U—СЧ
CI
Ut
C2
C2a![]()
ТШШНЙОЕГ nOUAUnAHUE ИЕМХРйЛиЗДЦиЯ aUPUCDB
ХКинияппадойядл шивност
ь
VU zs
UI
U
а
Схема 2.2. Классический путь активации комплемента и биологические эффекты продуктов его активации. Процесс начинается с присоединения к антителу комплекса Ciq, а затем Clr. Последний приобретает протеазную активность и расщепляет Cls, в результате чего он превращается в активную эстеразу. Происходит активация первого компонента — С1. В свою очередь С1 вызывает расщепление С4 и С2 Из фрагментов С4в + С2а образуется активный компонент С4в2а, являющийся конвертазой третьего компонента — СЗ-конвертазы. Она расщепляет СЗ на два фрагмента: СЗа и СЗв. Последний компонент совместно с С4в2а принимает участие в активации последующих компонентов комплемента.
.
Плазмин
Фн6ряно~
