
- •Биохимия животных Электронный дидактический комплекс (эдк)
- •Физическая химия вода
- •Активная реакция водных растворов
- •Ионное произведение воды. Водородный показатель
- •Методы определения рН среды
- •Роль активной реакции среды в биологических процессах
- •Буферные pacтворы, состав, механизм действия
- •Буферная емкость
- •Биологическое значение буферных систем
- •Коллоидная химия
- •Классификация дисперсных систем
- •Поверхностные явления
- •Адсорбция
- •Коллоидные растворы (золи) Методы получения
- •Строение коллоидных частиц
- •Коагуляция. Седиментация. Пептизация
- •Молекулярно-кинетические свойства коллоидных растворов
- •Осмотическое давление
- •Биологическое значение явления осмоса
- •Механизмы, участвующие в сохранении изоосмии:
- •Оптические свойства коллоидных систем
- •Растворы высокомолекулярных соединений
- •Свободная и связанная вода в коллоидных pacтвopax
- •Свойства растворов вмс
- •Денатурация
- •2. Белки; биологическая роль Аминокислоты
- •Содержание белков в организме и тканях
- •Методы выделения белков
- •Методы фракционирования и очистки белков
- •Физико-химические свойства белков
- •Аминокислоты
- •Ациклические аминокислоты
- •Структура белковой молекулы
- •Классификация белков
- •Химия сложных белков
- •3. Нуклеиновые кислоты
- •Нуклеотиды и нуклеозиды
- •Структура днк
- •Рибонуклеиновые кислоты
- •4. Ферменты
- •Биосинтез и клеточная локализация ферментов
- •Химическая природа ферментов
- •Строение ферментов
- •Активный центр фермента
- •Регуляция активности ферментов
- •Механизм действия ферментов
- •Основные свойства ферментов
- •2. Зависимость активности ферментов от рН среды.
- •Факторы, определяющие активность ферментов
- •Активирование и ингибирование ферментов
- •Типы ингибирования
- •Классификация и номенклатура ферментов
- •Применение ферментов.
- •Использование иммобилизованных ферментов для производства биологических соединений
- •Иммуноферментный анализ и его использование в ветеринарии
- •5. Химия витаминов
- •Классификация и номенклатура витаминов
- •I. Жирорастворимые витамины
- •II. Витамины, растворимые в воде
- •Витамин d, антирахитический, кальциферол
- •Витамин e, антистерильный, токоферолы
- •Витамин к, антигеморрагический (филлохинон)
- •Витамин q (убихинон)
- •Водорастворимые витамины
- •Витамин b1, антиневритный, тиамин
- •Витамин b2, рибофлавин
- •Витамин b3, пантотеновая кислота
- •Витамин b5, pp, никотинамид, ниацин, антипеллагрический
- •Витамин b6, адермин, пиридоксол
- •Витамин b12, кобаламин, антианемический
- •Фолиевая кислота
- •Витамин с (аскорбиновая кислота)
- •Биотин, витамин h
- •6. Гормоны
- •Гормоны гипофиза
- •Поджелудочная железа
- •Гормоны щитовидной железы
- •Гормоны надпочечников
- •Гормоны коры надпочечников
- •Гормоны половых желез
- •Гормоны тимуса (вилочковой железы)
- •Гормоны местного действия
- •7. Обмен веществ и энергии
- •Основные этапы обмена веществ
- •Биологическое окисление
- •Окислительное фосфорилирование
- •Токсичность кислорода
- •8. Химия и обмен углеводов
- •Моносахариды
- •Производные моносахаридов.
- •Полисахариды (гликаны)
- •Гетерополисахариды (гетерогликаны)
- •Обмен углеводов
- •Катаболизм глюкозы
- •Гликогенолиз
- •Биосинтез углеводов
- •Биосинтез гликогена (гликогенез)
- •Регуляция углеводного обмена.
- •9. Химия и обмен липидов
- •Химическое строение нейтральных жиров
- •Жирные кислоты.
- •Нейтральные гликолипиды
- •Фосфолипиды (фосфатиды)
- •Сфинголипиды
- •Двойной липидный слой мембран
- •Обмен липидов
- •Переваривание липидов в желудочно-кишечном тракте
- •Промежуточный обмен липидов
- •Энергетический баланс β-окисления жирных кислот
- •Метаболизм ацетил-коэнзима а
- •Пути образования кетоновых тел
- •Биосинтез липидов
- •Метаболизм стеринов и стеридов
- •Липосомы
- •10. Обмен белков
- •Биологическая ценность белков
- •Нормы белка в питании животных
- •Белковые резервы организма
- •Обмен простых белков
- •Переваривание белков в желудочно-кишечном тракте моногастричных животных
- •Переваривание белков в кишечнике.
- •Особенности переваривания белков у жвачных животных
- •Дезаминирование аминокислот
- •Трансаминирование – непрямой путь дезаминирования аминокислот
- •Декарбоксилирование аминокислот
- •Окислительное расщепление аминокислот
- •Особенности обмена отдельных аминокислот
- •11. Биосинтез белка
- •Генетический код
- •Этапы синтеза белка
- •Мультиферментный механизм синтеза белка
- •12.Обмен нуклеиновых кислот Переваривание нуклеиновых кислот в желудочно-кишечном тракте
- •Промежуточный обмен нуклеиновых кислот Распад нуклеиновых кислот в тканях
- •Пиримидиновые основания
- •Биосинтез нуклеиновых кислот
- •Рекомбинантные молекулы и проблемы генной инженерии
- •Клонирование животных
- •Метод молекулярной гибридизации
- •Принцип метода
- •Способы гибридизации
- •Метод блоттинга по Саузерну
- •Полимеразная цепная реакция (пцр)
- •Необходимые приборы и реактивы
- •13. Обмен воды и солей
- •Вода, ее содержание и роль в организме
- •Потребность животного организма в минеральных веществах, их поступление и выделение
- •Микроэлементы
- •14. Биохимия крови
- •Физико-химические свойства крови
- •Буферные системы крови
- •Плазма крови и ее химический состав
- •Белки плазмы и сыворотки крови
- •Небелковые азотистые вещества крови
- •Форменные элементы крови
- •15. Биохимия мышечной ткани
- •Механизм сокращения мышцы
- •Азотистые экстрактивные вещества мышц
- •Минеральные вещества
- •Окоченение мышц
- •16. Биохимия молока и молокообразования
- •17. Биохимия почек и мочи
- •Патологические компоненты мочи
- •Особенности мочи птиц
- •18. Биохимия кожи и шерсти
- •19. Биохимия яйца
- •Биосинтез компонентов яйца
- •Предметный указатель
- •Приложения
- •Рекомендуемая литература
- •Тесты для проверки биохимических
- •Глава 8. Химия обмена углеводов
- •24. Сложноэфирные связи в молекулах триацилглицеролов подвергаются ферментативному гидролизу при участии:
- •Глава 11. Синтез белка
- •Глава 12. Обмен нуклеиновых кислот
- •Глава 13. Биохимия почек и мочи
Особенности переваривания белков у жвачных животных
Как известно, у жвачных животных желудок 4-х камерный, состоит из рубца, сетки, книжки, сычуга. Сычуг является собственным желудком, где вырабатывается сок, содержащий HCl, реннин, пепсин. Рубец, сетка, книжка – в них происходит основное превращение белков и других азотистых веществ корма под действием микрофлоры и простейших. Рубцовая микрофлора имеет сбалансированный характер. Общее количество бактерий в рубце составляет 109-1010 клеток в 1 г содержимого, или в рубцовом содержимом находится 1,5-2,0 кг бактерий. Это огромное количество. Под действием бактериальных ферментов растительные и животные белки в рубце расщепляются до пептидов, аминокислот и свободного аммиака. Одновременно идет синтез бактериального белка за счет размножения микробов.
Кроме бактерий в рубце значительное место занимают простейшие, их количество в 1 мл составляет 105-106. На долю инфузории приходится 1/20 массы рубцовой жидкости у крупного рогатого скота, а их азот занимает 10-12 % общего азота кормовой смеси преджелудков. Инфузории размножаются быстро, за сутки меняется 4-5 поколений и ежесуточное их переваривание в сычуге и кишечнике достигает 70 % всех простейших рубца.
Простейшие синтезируют незаменимые аминокислоты, обеспечивающие животное полноценным белком. Это имеет существенное значение для животного. Простейшие содержат больше незаменимых аминокислот, особенно лизина, чем бактерии. Таким образом, в организме жвачных бактерии – главный поставщик ферментов, гидролизирующих белки до аминокислот.
Бактерии и инфузории систематически поступают в сычуг и перевариваются. Часть аминокислот под действием ферментов бактерий подвергаются гидролитическому дезаминированию:
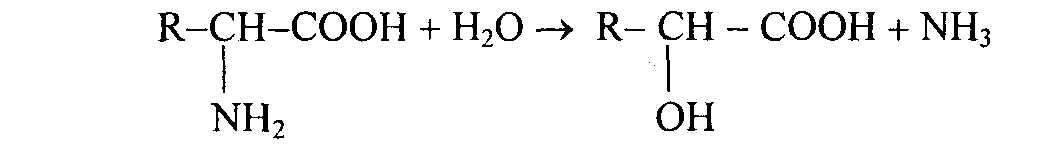
Или происходит восстановительное дезаминирование с участием НАДН2:
![]()
В результате процессов дезаминирования аминокислот в рубце накапливается большое количество аммиака. Оптимальным для бактерий и инфузорий является значение рН 5,5-7,0. После дезаминирования кислотные остатки превращаются в CO2 и летучие жирные кислоты. Микрофлора рубца способна расщеплять не только белковые молекулы, но и небелковые азотистые вещества. Известно, что вместе с растительными кормами до 10-30 % азота может быть, в виде небелкового азота (аминокислоты, амиды и т.д.). Эти продукты гидролизуются до аммиака и жирных кислот. Таким же процессам гидролиза подвергаются пуриновые и пиримидиновые основания: аденин, гуанин, ксантин, мочевая кислота и гуанидин, которые расщепляются с образованием NH3, CO2 и уксусной кислоты.
Мочевина (диамид угольной кислоты) может попадать в рубец с кормом или слюной (куда попадает из крови в результате обезвреживания аммиака в печени в орнитиновом цикле), а также в виде подкормки (карбамид-мочевина). При недостаточности азотистых веществ в корме мочевина начинает усиленно поступать в рубцовое содержимое путем выделения стенкой рубца из крови.
В рубце под влиянием бактериальных ферментов уреазы мочевина гидролизуется с образованием аммиака, CO2, H2O:
![]()
Аммиак частично всасывается в кровь и превращается в печени в мочевину, далее выделяется почками. Частично используется бактериями для синтеза аминокислот:
Бактерии могут синтезировать все аминокислоты заменимые и незаменимые, о чем уже указывалось выше.
Для практики животноводства важно использование карбамида для пополнения азота рациона жвачных, при этом следует учесть, что гидролиз мочевины идет в 4 раза быстрее, чем усвоение бактериями освободившегося аммиака, поэтому в корм добавляют мочевину малыми порциями, в брикетированном виде, в виде добавок к силосу (добавляют при силосовании) и т.д. За сутки коровы могут использовать 60-150 г мочевины, овцы 10-15 г. Это позволяет заменить 20-30 % перевариваемого протеина корма.
Распад белков в тканях и его биологическое значение
Аминокислоты всасываются в кровь, доставляются в печень, где частично дезаминируются, декарбоксилируются или подвергаются трансаминированию. Кроме того, происходит постоянно обновление белков собственного тела – распад (в лизосомах) и синтез de novo. Обновление аминокислот в белках ткани идет очень интенсивно. Так, белки печени обновляются наполовину за 8-12 суток, плазмы крови – за 18-45 суток. У крупного рогатого скота при выращивании на мясо за сутки синтезируется 120-200 г белка, у лактирующей коровы с молоком выделяется 600-1200 г новых белков. Распад тканевых белков – аутолиз происходит под действием ферментов – тканевых протеаз – катепсинов.
Третьим источником свободных аминокислот (1-ый из кишечника, 2-ой - аутолиз) в клетках организма является их синтез. В растениях синтезируется очень большой набор аминокислот (свыше 20), а в животном организме синтезируются только заменимые аминокислоты путем восстановительного аминирования кетокислот и трансаминирования.
Восстановительное аминирование кетокислот является обратным процессом окислительного дезаминирования аминокислот (глутаминовая, аспарагиновая и др.). Ресинтез происходит в 2 этапа:

Таким образом, в первую фазу реакции из кетокислоты и аммиака образуются иминокислоты, во вторую – иминокислота восстанавливается за счет водорода восстановленной формы НАД или НАДФ, то есть НАД•H2, НАДФ•Н2 – в аминокислоту. Этот путь синтеза аминокислот в организме животных ограничен, он ярче выражен у растений и микробов (бактерий).
Наиболее выраженный путь биосинтеза аминокислот в организме – путь переаминирования (трансаминирования). Он открыт в 1937 году Браунштейном A.E. и Крицманом М.Г. Было установлено, что из глутаминовой и пировиноградной кислот могут образоваться α-кетоглутаровая кислота и аланин без промежуточного выделения аммиака.

Эту реакцию называют трансаминированием, при этом происходит перенос аминогруппы с аминокислоты на кетокислоту. Донором аминогруппы является аминокислота, акцептором – кетокислота. Все природные аминокислоты подвержены ферментативному переаминированию. Наиболее активно эта реакция происходит между глутаминовой кислотой и щавелевоуксусной.
Между аспарагиновой кислотой и α-кетоглутаровой (в печени и мышечной ткани) реакция происходит с участием трансфераз (трансаминаз); коферментом является фосфо- пиридоксаль (витамин B6).
Аминогруппа через основание Шиффа переходит на фосфопиридоксаль, в результате синтезируется фоофопиридоксамин и соответствующая кетокислота. Фосфопиридоксамин реагирует с новой кетокислотой, образуя новую аминокислоту с освобождением фосфопирид оксаля. Процесс образования промежуточного продукта можно представить следующим образом:
Процесс образования промежуточного продукта можно представить следующим образом:

Переаминирование играет очень важную роль при синтезе в тканях необходимых аминокислот.
Таким образом, фонд свободных аминокислот клеток формируется за счет:
1) поступления из органов пищеварения;
2) распада белков;
3) синтеза заменимых аминокислот в реакциях трансаминирования, восстановительного аминирования кетокислот.
