
- •Биохимия животных Электронный дидактический комплекс (эдк)
- •Физическая химия вода
- •Активная реакция водных растворов
- •Ионное произведение воды. Водородный показатель
- •Методы определения рН среды
- •Роль активной реакции среды в биологических процессах
- •Буферные pacтворы, состав, механизм действия
- •Буферная емкость
- •Биологическое значение буферных систем
- •Коллоидная химия
- •Классификация дисперсных систем
- •Поверхностные явления
- •Адсорбция
- •Коллоидные растворы (золи) Методы получения
- •Строение коллоидных частиц
- •Коагуляция. Седиментация. Пептизация
- •Молекулярно-кинетические свойства коллоидных растворов
- •Осмотическое давление
- •Биологическое значение явления осмоса
- •Механизмы, участвующие в сохранении изоосмии:
- •Оптические свойства коллоидных систем
- •Растворы высокомолекулярных соединений
- •Свободная и связанная вода в коллоидных pacтвopax
- •Свойства растворов вмс
- •Денатурация
- •2. Белки; биологическая роль Аминокислоты
- •Содержание белков в организме и тканях
- •Методы выделения белков
- •Методы фракционирования и очистки белков
- •Физико-химические свойства белков
- •Аминокислоты
- •Ациклические аминокислоты
- •Структура белковой молекулы
- •Классификация белков
- •Химия сложных белков
- •3. Нуклеиновые кислоты
- •Нуклеотиды и нуклеозиды
- •Структура днк
- •Рибонуклеиновые кислоты
- •4. Ферменты
- •Биосинтез и клеточная локализация ферментов
- •Химическая природа ферментов
- •Строение ферментов
- •Активный центр фермента
- •Регуляция активности ферментов
- •Механизм действия ферментов
- •Основные свойства ферментов
- •2. Зависимость активности ферментов от рН среды.
- •Факторы, определяющие активность ферментов
- •Активирование и ингибирование ферментов
- •Типы ингибирования
- •Классификация и номенклатура ферментов
- •Применение ферментов.
- •Использование иммобилизованных ферментов для производства биологических соединений
- •Иммуноферментный анализ и его использование в ветеринарии
- •5. Химия витаминов
- •Классификация и номенклатура витаминов
- •I. Жирорастворимые витамины
- •II. Витамины, растворимые в воде
- •Витамин d, антирахитический, кальциферол
- •Витамин e, антистерильный, токоферолы
- •Витамин к, антигеморрагический (филлохинон)
- •Витамин q (убихинон)
- •Водорастворимые витамины
- •Витамин b1, антиневритный, тиамин
- •Витамин b2, рибофлавин
- •Витамин b3, пантотеновая кислота
- •Витамин b5, pp, никотинамид, ниацин, антипеллагрический
- •Витамин b6, адермин, пиридоксол
- •Витамин b12, кобаламин, антианемический
- •Фолиевая кислота
- •Витамин с (аскорбиновая кислота)
- •Биотин, витамин h
- •6. Гормоны
- •Гормоны гипофиза
- •Поджелудочная железа
- •Гормоны щитовидной железы
- •Гормоны надпочечников
- •Гормоны коры надпочечников
- •Гормоны половых желез
- •Гормоны тимуса (вилочковой железы)
- •Гормоны местного действия
- •7. Обмен веществ и энергии
- •Основные этапы обмена веществ
- •Биологическое окисление
- •Окислительное фосфорилирование
- •Токсичность кислорода
- •8. Химия и обмен углеводов
- •Моносахариды
- •Производные моносахаридов.
- •Полисахариды (гликаны)
- •Гетерополисахариды (гетерогликаны)
- •Обмен углеводов
- •Катаболизм глюкозы
- •Гликогенолиз
- •Биосинтез углеводов
- •Биосинтез гликогена (гликогенез)
- •Регуляция углеводного обмена.
- •9. Химия и обмен липидов
- •Химическое строение нейтральных жиров
- •Жирные кислоты.
- •Нейтральные гликолипиды
- •Фосфолипиды (фосфатиды)
- •Сфинголипиды
- •Двойной липидный слой мембран
- •Обмен липидов
- •Переваривание липидов в желудочно-кишечном тракте
- •Промежуточный обмен липидов
- •Энергетический баланс β-окисления жирных кислот
- •Метаболизм ацетил-коэнзима а
- •Пути образования кетоновых тел
- •Биосинтез липидов
- •Метаболизм стеринов и стеридов
- •Липосомы
- •10. Обмен белков
- •Биологическая ценность белков
- •Нормы белка в питании животных
- •Белковые резервы организма
- •Обмен простых белков
- •Переваривание белков в желудочно-кишечном тракте моногастричных животных
- •Переваривание белков в кишечнике.
- •Особенности переваривания белков у жвачных животных
- •Дезаминирование аминокислот
- •Трансаминирование – непрямой путь дезаминирования аминокислот
- •Декарбоксилирование аминокислот
- •Окислительное расщепление аминокислот
- •Особенности обмена отдельных аминокислот
- •11. Биосинтез белка
- •Генетический код
- •Этапы синтеза белка
- •Мультиферментный механизм синтеза белка
- •12.Обмен нуклеиновых кислот Переваривание нуклеиновых кислот в желудочно-кишечном тракте
- •Промежуточный обмен нуклеиновых кислот Распад нуклеиновых кислот в тканях
- •Пиримидиновые основания
- •Биосинтез нуклеиновых кислот
- •Рекомбинантные молекулы и проблемы генной инженерии
- •Клонирование животных
- •Метод молекулярной гибридизации
- •Принцип метода
- •Способы гибридизации
- •Метод блоттинга по Саузерну
- •Полимеразная цепная реакция (пцр)
- •Необходимые приборы и реактивы
- •13. Обмен воды и солей
- •Вода, ее содержание и роль в организме
- •Потребность животного организма в минеральных веществах, их поступление и выделение
- •Микроэлементы
- •14. Биохимия крови
- •Физико-химические свойства крови
- •Буферные системы крови
- •Плазма крови и ее химический состав
- •Белки плазмы и сыворотки крови
- •Небелковые азотистые вещества крови
- •Форменные элементы крови
- •15. Биохимия мышечной ткани
- •Механизм сокращения мышцы
- •Азотистые экстрактивные вещества мышц
- •Минеральные вещества
- •Окоченение мышц
- •16. Биохимия молока и молокообразования
- •17. Биохимия почек и мочи
- •Патологические компоненты мочи
- •Особенности мочи птиц
- •18. Биохимия кожи и шерсти
- •19. Биохимия яйца
- •Биосинтез компонентов яйца
- •Предметный указатель
- •Приложения
- •Рекомендуемая литература
- •Тесты для проверки биохимических
- •Глава 8. Химия обмена углеводов
- •24. Сложноэфирные связи в молекулах триацилглицеролов подвергаются ферментативному гидролизу при участии:
- •Глава 11. Синтез белка
- •Глава 12. Обмен нуклеиновых кислот
- •Глава 13. Биохимия почек и мочи
Плазма крови и ее химический состав
После удаления из крови форменных элементов остается плазма. В обычных условиях, вне организма, плазма свертывается. После удаления из плазмы фибриногена остается сыворотка крови. Для предотвращения свертывания крови добавляют стабилизаторы (соль лимонной или щавелевой кислоты, гепарин).
Плазма составляет около 55-60% объема крови. В ее составе 90-96% воды, 4-10% сухих веществ, в т. ч. органические вещества: белковые – альбумины, глобулины, фибриноген, ферменты; небелковые – пептиды, аминокислоты, мочевина, мочевая кислота, аллантоин, креатинин, билирубин, амиды, минеральные вещества (около 1%), гормоны, витамины; безазотистые вещества – глюкоза, молочная кислота, жирные кислоты, глицерин, триглицериды, холестерин, промежуточные продукты их обмена.
Минеральные вещества плазмы: NaCl, KCl, CaCl2, MgCl2, NaHCO3, CaCO3, K2HPO4, Na2SO4, Са3(РО4)2. Кроме того, в небольших количествах содержатся ионы железа, меди, йода, цинка, кобальта, марганца и т.д.
Минеральные вещества могут находиться в ионо- и молекулярно-дисперсном состоянии, а также могут входить в состав сложных органических соединений. Считают, что в обменных процессах наиболее активны минеральные вещества, связанные с белками крови.
Содержание ионов (катионов и анионов) в плазме крови, мг% у лошади составляет следующие величины:
|
катионы |
анионы |
|
Na+ - 340 мг% K+- 24 Ca2+ - 14 Mg2+-3,5 |
Cl- - 330 HCO3- - 200 HPO42- - 3,0 |
Роль солей щелочных и щелочноземельных металлов в крови разнообразна. Они участвуют в создании осмотического давления, состояния изотонии с внутриклеточным содержимым различных тканей. Отдельные ионы имеют специфические функции. Ионы Na+ повышают набухание тканей и увеличивают их проницаемость. Ионы Са++ действуют противоположно: уплотняют протоплазму клетки, уменьшают ее проницаемость. Ионы Mg++ вызывают анестезию. Катионы крови влияют на активность многих ферментов.
Содержание кальция и фосфора изменяется при рахите, остеомаляции, тетании и других нарушениях минерального обмена.
Железо сосредоточено в эритроцитах. В плазме – в составе трансферрина. Железо депонируется в виде ферритина. Избыток железа откладывается в форме гемосидерина в клетках ретикулоэндотелиальной системы.
Белки плазмы и сыворотки крови
Плазма содержит 2,5-8,0% белка, в том числе фибриногена – 0,5%. У разных видов животных содержание белка в плазме составляет следующие величины, в %: куры – 5,2; кролики – 7,1; коровы – 7,5; лошади – 7,8; свиньи – 7,4.
Содержание белка в сыворотке крови колеблется в зависимости от возраста, пола, продуктивности. Снижение содержания белка – гипопротеинемия наблюдается при белковом голодании, при приеме больших количеств жидкости, нарушении функции почек, печени, неполноценном белковом питании, повышенном распаде белков. При сильных поносах и рвоте концентрация белков в крови повышается (гиперпротеинемия). При электрофорезе в полиакриламидном геле белки крови можно разделить до 30 и более фракций.
Альбумины имеют повышенную электрофоретическую подвижность, хорошо растворимы в воде, на 98% состоят из аминокислот. Изоэлектрическая точка при рН 4,9; М.м. 65000-70000 Да; период полураспада 3,7 суток. В крови 30-55% белков – альбумины.
Синтезируются в основном в клетках печени. Они участвуют в регуляции водно-солевого обмена между кровью и тканями. Альбумины можно рассматривать как аминокислотный резерв организма. Кроме того, они адсорбируют аминокислоты и в таком виде транспортируют их в ткани.
Альбумины могут образовывать различные комплексы с металлами, гормонами, витаминами, токсинами, осуществляя их транспорт в организме. В этих комплексах многие биологически активные вещества теряют свою активность или, наоборот, усиливают, т.е. альбумины регулируют влияние их на метаболические процессы. Выступают в виде буферных веществ, поддерживая рН.
Глобулины. Различают α, β, γ-глобулины.
α-Глобулины при электрофорезе продвигаются за альбуминами, разделяются на несколько фракций (α1, α2, α3 -глобулины). М.м. 160000 - 200000. Изоэлектрическая точка при рН 4,7-5,2. Их функция – белки-переносчики, (легко соединяются с липидами, углеводами, витаминами, желчными пигментами). В их составе 25-35% углеводов. Сюда относится гаптоглобулин – переносчик железа, церулоплазмин – переносчик меди. Церулоплазмин, относящийся к α2-гликопротеидам плазмы крови, играет главную роль в обмене медьсодержащих энзимов. Во фракции α-глобулинов находятся также белки, участвующие в свертывании крови.
β-Глобулины. Молекулярная масса 90000-1,Зх106 Да. Изоэлектрическая точка рН 4,4. Образуют комплексы с липидами. К этой группе относится трансферрин. В этой фракции находится белок проконвертин, участвующий в превращении протромбина в тромбин.
γ-Глобулины. Наименее подвижная фракция с высокой М.м., выполняют защитные функции. В их составе белки-антитела, обеспечивающие защиту против инфекционных болезней.
Иммунные белки – иммуноглобулины (Ig). Содержание иммуноглобулинов резко увеличивается при иммунизации, хронических заболеваниях. Иммуноглобулины синтезируются в лимфоидной ткани селезенки, лимфоузлов, костного мозга и т.д. против чужеродных белков (антигенов). Их молекулярная масса составляет до Ix106 Да и более. Состоят из двух тяжелых полипептидных цепей (H-Heavy, Мм 50-75 кДа) и двух легких цепей L (Light, Мм 23 кДа), соединенных дисульфидными мостиками, (рис. 14.1.). Н-цепи имеют ≈ 700, а L-цепи ≈ 200 аминокислотных остатков. В пептидных цепях различают вариабельные (v) и постоянные константные (с) области. В результате различных сочетаний отдельных участков иммуноглобулинов может образовываться большое число индивидуальных иммуноглобулинов - до 107 .
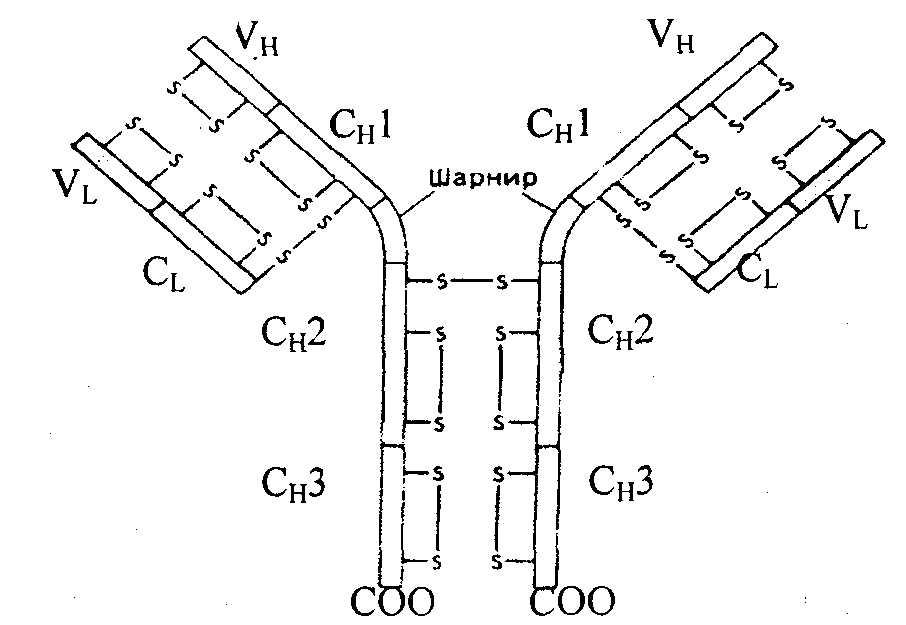
Рис. 14.1. Структура молекулы иммуноглобулина.
Две легкие и две тяжелые цепи удерживаются вместе дисульфидными связями. Каждая из легких и тяжелых цепей имеет на своем N- конце вариабельный yчасток (VL или VH). B состав легких цепей входит один константный участок (CL); у тяжелых цепей константная часть состоит из четырех доменов (СН1, СН2, СнЗ и шарнирный участок).
Различают иммуноглобулины классов IgG, M, A, D, E. Они различаются по молекулярной массе, по скорости седиментации, концентрации в сыворотке крови и т.д.
В сыворотке крови содержатся и другие белки. Например, C-реактивный белок появляется при воспалительных процессах и некрозах. Пропердин и интерферон – защитные белки. Интерферон является универсальным противовирусным белком. Фибриноген и протромбин принимают участие в процессе свертывания крови. В небольших количествах в сыворотки крови содержатся гормоны и ферменты. Металлопротеиды – целый ряд белков крови способных связывать различные металлы, образуя комплексные соединения: церулоплазмин – М.м. 150 кДа, 8 атомов Cu++ , трансферрин, гаптоглобин и другие.
