
- •Биохимия животных Электронный дидактический комплекс (эдк)
- •Физическая химия вода
- •Активная реакция водных растворов
- •Ионное произведение воды. Водородный показатель
- •Методы определения рН среды
- •Роль активной реакции среды в биологических процессах
- •Буферные pacтворы, состав, механизм действия
- •Буферная емкость
- •Биологическое значение буферных систем
- •Коллоидная химия
- •Классификация дисперсных систем
- •Поверхностные явления
- •Адсорбция
- •Коллоидные растворы (золи) Методы получения
- •Строение коллоидных частиц
- •Коагуляция. Седиментация. Пептизация
- •Молекулярно-кинетические свойства коллоидных растворов
- •Осмотическое давление
- •Биологическое значение явления осмоса
- •Механизмы, участвующие в сохранении изоосмии:
- •Оптические свойства коллоидных систем
- •Растворы высокомолекулярных соединений
- •Свободная и связанная вода в коллоидных pacтвopax
- •Свойства растворов вмс
- •Денатурация
- •2. Белки; биологическая роль Аминокислоты
- •Содержание белков в организме и тканях
- •Методы выделения белков
- •Методы фракционирования и очистки белков
- •Физико-химические свойства белков
- •Аминокислоты
- •Ациклические аминокислоты
- •Структура белковой молекулы
- •Классификация белков
- •Химия сложных белков
- •3. Нуклеиновые кислоты
- •Нуклеотиды и нуклеозиды
- •Структура днк
- •Рибонуклеиновые кислоты
- •4. Ферменты
- •Биосинтез и клеточная локализация ферментов
- •Химическая природа ферментов
- •Строение ферментов
- •Активный центр фермента
- •Регуляция активности ферментов
- •Механизм действия ферментов
- •Основные свойства ферментов
- •2. Зависимость активности ферментов от рН среды.
- •Факторы, определяющие активность ферментов
- •Активирование и ингибирование ферментов
- •Типы ингибирования
- •Классификация и номенклатура ферментов
- •Применение ферментов.
- •Использование иммобилизованных ферментов для производства биологических соединений
- •Иммуноферментный анализ и его использование в ветеринарии
- •5. Химия витаминов
- •Классификация и номенклатура витаминов
- •I. Жирорастворимые витамины
- •II. Витамины, растворимые в воде
- •Витамин d, антирахитический, кальциферол
- •Витамин e, антистерильный, токоферолы
- •Витамин к, антигеморрагический (филлохинон)
- •Витамин q (убихинон)
- •Водорастворимые витамины
- •Витамин b1, антиневритный, тиамин
- •Витамин b2, рибофлавин
- •Витамин b3, пантотеновая кислота
- •Витамин b5, pp, никотинамид, ниацин, антипеллагрический
- •Витамин b6, адермин, пиридоксол
- •Витамин b12, кобаламин, антианемический
- •Фолиевая кислота
- •Витамин с (аскорбиновая кислота)
- •Биотин, витамин h
- •6. Гормоны
- •Гормоны гипофиза
- •Поджелудочная железа
- •Гормоны щитовидной железы
- •Гормоны надпочечников
- •Гормоны коры надпочечников
- •Гормоны половых желез
- •Гормоны тимуса (вилочковой железы)
- •Гормоны местного действия
- •7. Обмен веществ и энергии
- •Основные этапы обмена веществ
- •Биологическое окисление
- •Окислительное фосфорилирование
- •Токсичность кислорода
- •8. Химия и обмен углеводов
- •Моносахариды
- •Производные моносахаридов.
- •Полисахариды (гликаны)
- •Гетерополисахариды (гетерогликаны)
- •Обмен углеводов
- •Катаболизм глюкозы
- •Гликогенолиз
- •Биосинтез углеводов
- •Биосинтез гликогена (гликогенез)
- •Регуляция углеводного обмена.
- •9. Химия и обмен липидов
- •Химическое строение нейтральных жиров
- •Жирные кислоты.
- •Нейтральные гликолипиды
- •Фосфолипиды (фосфатиды)
- •Сфинголипиды
- •Двойной липидный слой мембран
- •Обмен липидов
- •Переваривание липидов в желудочно-кишечном тракте
- •Промежуточный обмен липидов
- •Энергетический баланс β-окисления жирных кислот
- •Метаболизм ацетил-коэнзима а
- •Пути образования кетоновых тел
- •Биосинтез липидов
- •Метаболизм стеринов и стеридов
- •Липосомы
- •10. Обмен белков
- •Биологическая ценность белков
- •Нормы белка в питании животных
- •Белковые резервы организма
- •Обмен простых белков
- •Переваривание белков в желудочно-кишечном тракте моногастричных животных
- •Переваривание белков в кишечнике.
- •Особенности переваривания белков у жвачных животных
- •Дезаминирование аминокислот
- •Трансаминирование – непрямой путь дезаминирования аминокислот
- •Декарбоксилирование аминокислот
- •Окислительное расщепление аминокислот
- •Особенности обмена отдельных аминокислот
- •11. Биосинтез белка
- •Генетический код
- •Этапы синтеза белка
- •Мультиферментный механизм синтеза белка
- •12.Обмен нуклеиновых кислот Переваривание нуклеиновых кислот в желудочно-кишечном тракте
- •Промежуточный обмен нуклеиновых кислот Распад нуклеиновых кислот в тканях
- •Пиримидиновые основания
- •Биосинтез нуклеиновых кислот
- •Рекомбинантные молекулы и проблемы генной инженерии
- •Клонирование животных
- •Метод молекулярной гибридизации
- •Принцип метода
- •Способы гибридизации
- •Метод блоттинга по Саузерну
- •Полимеразная цепная реакция (пцр)
- •Необходимые приборы и реактивы
- •13. Обмен воды и солей
- •Вода, ее содержание и роль в организме
- •Потребность животного организма в минеральных веществах, их поступление и выделение
- •Микроэлементы
- •14. Биохимия крови
- •Физико-химические свойства крови
- •Буферные системы крови
- •Плазма крови и ее химический состав
- •Белки плазмы и сыворотки крови
- •Небелковые азотистые вещества крови
- •Форменные элементы крови
- •15. Биохимия мышечной ткани
- •Механизм сокращения мышцы
- •Азотистые экстрактивные вещества мышц
- •Минеральные вещества
- •Окоченение мышц
- •16. Биохимия молока и молокообразования
- •17. Биохимия почек и мочи
- •Патологические компоненты мочи
- •Особенности мочи птиц
- •18. Биохимия кожи и шерсти
- •19. Биохимия яйца
- •Биосинтез компонентов яйца
- •Предметный указатель
- •Приложения
- •Рекомендуемая литература
- •Тесты для проверки биохимических
- •Глава 8. Химия обмена углеводов
- •24. Сложноэфирные связи в молекулах триацилглицеролов подвергаются ферментативному гидролизу при участии:
- •Глава 11. Синтез белка
- •Глава 12. Обмен нуклеиновых кислот
- •Глава 13. Биохимия почек и мочи
Поджелудочная железа
α и β- клетки островков (лат. insula – остров) Лангерганса вырабатывают, соответственно, глюкагон и инсулин – гормоны противоположного действия.
Инсулин был первым белком, первичная структура которого раскрыта в 1953 году Сэнджером, а в 1963 году синтезирован, в т.ч. у нас в стране. Инсулин – простой белок с М.м. 6000 Да, молекула содержит 51 аминокислотный остаток, построена из двух пептидных цепей. Пептидные цепи соединены между собой двумя дисульфидными связями. Цепь А-глициновая имеет 21 аминокислотный остаток, а цепь В-фенилаланиновая – 30 аминокислотных остатков. Инсулин синтезируется в виде предшественников (проинсулин, состоит из 84 аминокислотных остатков), избирательное выщепление С-пептида (33 аминокислотных остатка) приводит к образованию инсулина.
Инсулин влияет на сахарный обмен. Чем больше сахара в крови, тем больше инсулина; стимулирует процесс превращения глюкозы в гликоген в мышцах и печени и образование жира из углеводов. Ускоряет окисление глюкозы в мышцах и других тканях.
Недостаток инсулина в организме приводит к развитию сахарного диабета: когда концентрация инсулина падает ниже определенного уровня, содержание глюкозы в крови возрастает из-за подавления механизмов поглощения ее из крови и утилизации в тканях, при этом наблюдается выделение сахара с мочой. При недостатке инсулина усиливается окисление жиров, что ведет к образованию кетоновых тел (в избыточном количестве) ацетоуксусной кислоты, ацетона, β-оксимасляной кислоты.
Инсулин для лечебных целей получают из тканей животных или же с помощью методов генной инженерии. Этот гормон широко применяется при сахарном диабете.
Глюкагон – повышает содержание глюкозы в крови путем стимуляции гликогенолиза в печени, действуя при этом как антагонист инсулина.
Глюкагон – одноцепочечный полипептид, состоящий из 29 аминокислотных остатков, М.м. 4200 Да. Глюкагон вызывает Ускорение распада гликогена и торможение его синтеза, результатом является гликогенолиз – распад гликогена до глюкозы в печени. Кроме того, он способствует образованию глюкозы из промежуточных продуктов обмена белков и жиров (глюконеогенез).
Гормоны щитовидной железы
Щитовидная железа находится в области гортани, состоит из 2-х долей, вес у крупного рогатого скота – 20 г, овец – 5 г, свиней – 12-30 г. В щитовидной железе вырабатываются гормоны тироксин и трийодтиронин – йодсодержащие производные тирозина.
Фолликулы щитовидной железы заполнены белком (коллоидом), содержащим йодтиреоглобулин – высокомолекулярный гликопротеид. Его молекулярная масса 670000 Да, константа седиментации 195 S, содержит 0,5-1,0 % йода, 8-10% углевода гетерополисахарида. При гидролизе йодтиреоглобулина выделяется L-тироксин. Его можно рассматривать как производное L-тиронина -3,5, 3 ,5 -тетрайодтиронина:
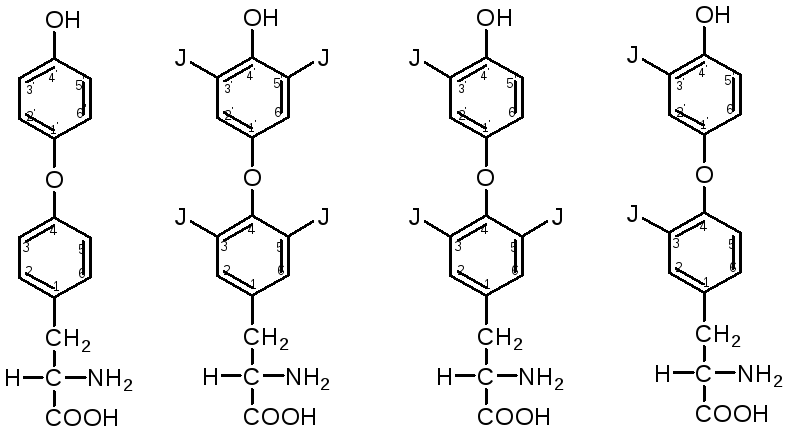
|
L-тиронин (Т) |
L-тироксин, Т4 (3,5,3',5',-тетра- йодтиронин) |
3,5,3'-L-трийод- тиронин (Т3) |
L-3,3-дийод- тиронин (Т2) |
Кроме тироксина имеется небольшое количество трийодтиронина, биологическая активность которого в 5-10 раз больше тироксина. Моно- и дийодтирозин – содержатся в небольших количествах и обладают слабой гормональной активностью. Биосинтез гормонов щитовидной железы хорошо изучен с помощью меченого йода J131. Из щитовидной железы они поступают в кровь, причем различают в крови связанный с белками и свободный гормоны. Разрушение их происходит в печени и почках.
Биосинтез тиреоидных гормонов регулируется, главным образом, тиреотропным гормоном передней доли гипофиза.
Действие тиреоидных гормонов – многообразное, они влияют на рост, развитие организма, дифференцировку клеток, уровень метаболизма в тканях. Они повышают поглощение кислорода и теплопродукцию, усиливают обмен углеводов, белков, жиров.
Гипофункция щитовидной железы ведет к глубоким нарушениям обмена веществ, снижает основной обмен, снижается температура тела. Недостаток гормона в период развития ведет к замедлению роста, повреждению центральной нервной системы, к кретинизму.
Атрофия в зрелом возрасте ведет к микседеме (слизистый отек) с понижением обмена, отложением жира и задержкой воды в организме. Явление гипофункции щитовидной железы может быть и как следствие недостаточного содержания йода в кормах.
Гипофункция щитовидной железы, связанная с недостаточным содержанием йода в кормах, воде отмечается в эндемических по йоду местностях Российской Федерации – Марийской, Мордовской, Удмуртской, Татарской Республиках. Характеризуется увеличением щитовидной железы (особенно у новорожденных), мертворождаемостью, рождением молодняка без шерсти, снижением продуктивности животных. Для лечения и профилактики применяется йодированная соль.
Гиперфункция щитовидной железы – гипертериоидизм -характеризуется резким повышением основного обмена, у человека развивается заболевание – базедова болезнь (тахикардия, пучеглазие, зоб), развивается общее истощение организма, а также психические расстройства
Тиреокальцитонин (кальцитонин) – гормон щитовидной железы синтезируется в особых клетках, так называемых парафолликулярных или С-клетках, представляет собой пептид из 32 аминокислотных остатков, вызывает задержку кальция в костной ткани. Способствует переходу кальция из крови в костную ткань, поддерживает постоянный уровень в крови не только кальция, но и фосфора.
Гормон паращитовидных желез – паратгормон, по химической природе является белком с Мм 9000 Да, состоит из 84 аминокислотных остатков, регулирует обмен кальция и фосфора, мобилизует кальций из костей, является антагонистом кальцитонина по отношению к кальцию.
Удаление околощитовидных желез вызывает у животных титанические судороги на фоне резкого падения концентрации кальция в плазме крови. Введение солей кальция предупреждает гибель животных.
