
- •Биохимия животных Электронный дидактический комплекс (эдк)
- •Физическая химия вода
- •Активная реакция водных растворов
- •Ионное произведение воды. Водородный показатель
- •Методы определения рН среды
- •Роль активной реакции среды в биологических процессах
- •Буферные pacтворы, состав, механизм действия
- •Буферная емкость
- •Биологическое значение буферных систем
- •Коллоидная химия
- •Классификация дисперсных систем
- •Поверхностные явления
- •Адсорбция
- •Коллоидные растворы (золи) Методы получения
- •Строение коллоидных частиц
- •Коагуляция. Седиментация. Пептизация
- •Молекулярно-кинетические свойства коллоидных растворов
- •Осмотическое давление
- •Биологическое значение явления осмоса
- •Механизмы, участвующие в сохранении изоосмии:
- •Оптические свойства коллоидных систем
- •Растворы высокомолекулярных соединений
- •Свободная и связанная вода в коллоидных pacтвopax
- •Свойства растворов вмс
- •Денатурация
- •2. Белки; биологическая роль Аминокислоты
- •Содержание белков в организме и тканях
- •Методы выделения белков
- •Методы фракционирования и очистки белков
- •Физико-химические свойства белков
- •Аминокислоты
- •Ациклические аминокислоты
- •Структура белковой молекулы
- •Классификация белков
- •Химия сложных белков
- •3. Нуклеиновые кислоты
- •Нуклеотиды и нуклеозиды
- •Структура днк
- •Рибонуклеиновые кислоты
- •4. Ферменты
- •Биосинтез и клеточная локализация ферментов
- •Химическая природа ферментов
- •Строение ферментов
- •Активный центр фермента
- •Регуляция активности ферментов
- •Механизм действия ферментов
- •Основные свойства ферментов
- •2. Зависимость активности ферментов от рН среды.
- •Факторы, определяющие активность ферментов
- •Активирование и ингибирование ферментов
- •Типы ингибирования
- •Классификация и номенклатура ферментов
- •Применение ферментов.
- •Использование иммобилизованных ферментов для производства биологических соединений
- •Иммуноферментный анализ и его использование в ветеринарии
- •5. Химия витаминов
- •Классификация и номенклатура витаминов
- •I. Жирорастворимые витамины
- •II. Витамины, растворимые в воде
- •Витамин d, антирахитический, кальциферол
- •Витамин e, антистерильный, токоферолы
- •Витамин к, антигеморрагический (филлохинон)
- •Витамин q (убихинон)
- •Водорастворимые витамины
- •Витамин b1, антиневритный, тиамин
- •Витамин b2, рибофлавин
- •Витамин b3, пантотеновая кислота
- •Витамин b5, pp, никотинамид, ниацин, антипеллагрический
- •Витамин b6, адермин, пиридоксол
- •Витамин b12, кобаламин, антианемический
- •Фолиевая кислота
- •Витамин с (аскорбиновая кислота)
- •Биотин, витамин h
- •6. Гормоны
- •Гормоны гипофиза
- •Поджелудочная железа
- •Гормоны щитовидной железы
- •Гормоны надпочечников
- •Гормоны коры надпочечников
- •Гормоны половых желез
- •Гормоны тимуса (вилочковой железы)
- •Гормоны местного действия
- •7. Обмен веществ и энергии
- •Основные этапы обмена веществ
- •Биологическое окисление
- •Окислительное фосфорилирование
- •Токсичность кислорода
- •8. Химия и обмен углеводов
- •Моносахариды
- •Производные моносахаридов.
- •Полисахариды (гликаны)
- •Гетерополисахариды (гетерогликаны)
- •Обмен углеводов
- •Катаболизм глюкозы
- •Гликогенолиз
- •Биосинтез углеводов
- •Биосинтез гликогена (гликогенез)
- •Регуляция углеводного обмена.
- •9. Химия и обмен липидов
- •Химическое строение нейтральных жиров
- •Жирные кислоты.
- •Нейтральные гликолипиды
- •Фосфолипиды (фосфатиды)
- •Сфинголипиды
- •Двойной липидный слой мембран
- •Обмен липидов
- •Переваривание липидов в желудочно-кишечном тракте
- •Промежуточный обмен липидов
- •Энергетический баланс β-окисления жирных кислот
- •Метаболизм ацетил-коэнзима а
- •Пути образования кетоновых тел
- •Биосинтез липидов
- •Метаболизм стеринов и стеридов
- •Липосомы
- •10. Обмен белков
- •Биологическая ценность белков
- •Нормы белка в питании животных
- •Белковые резервы организма
- •Обмен простых белков
- •Переваривание белков в желудочно-кишечном тракте моногастричных животных
- •Переваривание белков в кишечнике.
- •Особенности переваривания белков у жвачных животных
- •Дезаминирование аминокислот
- •Трансаминирование – непрямой путь дезаминирования аминокислот
- •Декарбоксилирование аминокислот
- •Окислительное расщепление аминокислот
- •Особенности обмена отдельных аминокислот
- •11. Биосинтез белка
- •Генетический код
- •Этапы синтеза белка
- •Мультиферментный механизм синтеза белка
- •12.Обмен нуклеиновых кислот Переваривание нуклеиновых кислот в желудочно-кишечном тракте
- •Промежуточный обмен нуклеиновых кислот Распад нуклеиновых кислот в тканях
- •Пиримидиновые основания
- •Биосинтез нуклеиновых кислот
- •Рекомбинантные молекулы и проблемы генной инженерии
- •Клонирование животных
- •Метод молекулярной гибридизации
- •Принцип метода
- •Способы гибридизации
- •Метод блоттинга по Саузерну
- •Полимеразная цепная реакция (пцр)
- •Необходимые приборы и реактивы
- •13. Обмен воды и солей
- •Вода, ее содержание и роль в организме
- •Потребность животного организма в минеральных веществах, их поступление и выделение
- •Микроэлементы
- •14. Биохимия крови
- •Физико-химические свойства крови
- •Буферные системы крови
- •Плазма крови и ее химический состав
- •Белки плазмы и сыворотки крови
- •Небелковые азотистые вещества крови
- •Форменные элементы крови
- •15. Биохимия мышечной ткани
- •Механизм сокращения мышцы
- •Азотистые экстрактивные вещества мышц
- •Минеральные вещества
- •Окоченение мышц
- •16. Биохимия молока и молокообразования
- •17. Биохимия почек и мочи
- •Патологические компоненты мочи
- •Особенности мочи птиц
- •18. Биохимия кожи и шерсти
- •19. Биохимия яйца
- •Биосинтез компонентов яйца
- •Предметный указатель
- •Приложения
- •Рекомендуемая литература
- •Тесты для проверки биохимических
- •Глава 8. Химия обмена углеводов
- •24. Сложноэфирные связи в молекулах триацилглицеролов подвергаются ферментативному гидролизу при участии:
- •Глава 11. Синтез белка
- •Глава 12. Обмен нуклеиновых кислот
- •Глава 13. Биохимия почек и мочи
Необходимые приборы и реактивы
• ДНК-амплификатор (термоциклер) – прибор, обеспечивающий циклическую смену температур по заданной программе (выпускаемые в настоящее время термоциклеры рассчитаны на одновременное проведение до 96 реакций);
• стандартный набор лабораторного оборудования для выделения генетического материала из исследуемых образцов, постановки электрофореза (центрифуга типа "Eppendorf), вортекс, автоматические пипетки, источник питания, электрофоретические камеры, трансиллюминатор), одноразовые наконечники и пробирки для ПЦР;
• термостабильная ДНК-полимераза, выдерживающая многократный нагрев до 96 0C; это фермент, выделяемый из бактерий, обитающих в горячих источниках (гейзерах). В настоящее время известны два штамма термофильных бактерий, из которых выделены эти ферменты (Termus aquaticus и Termus thermophilus), соответственно ферменты обозначаются Taq-полимераза и Tth-полимераза.
• Праймер – олигонуклеотид из 15-20 нуклеотидов, является затравкой для синтеза новой молекулы ДНК. Данный олигонуклеотид должен быть специфичным для исследуемого организма (возбудителя болезни). Его получают путем химического синтеза на автоматическом синтезаторе, пользуясь данными о первичной структуре (нуклеотидной последовательности) ДНК.
• дезоксинуклеозидтрифосфаты – dNTP, предшественники синтеза ДНК.
В настоящее время выпускаются специальные наборы для ПЦР, предназначенные для диагностики туберкулеза крупного рогатого скота, бруцеллеза, ящура и других инфекционных болезней животных. Обычно один набор содержит компоненты для анализа 100 образцов. На рис. 12.7 показаны результаты проведения полимеразной цепной реакции по идентификации классической чумы свиней.
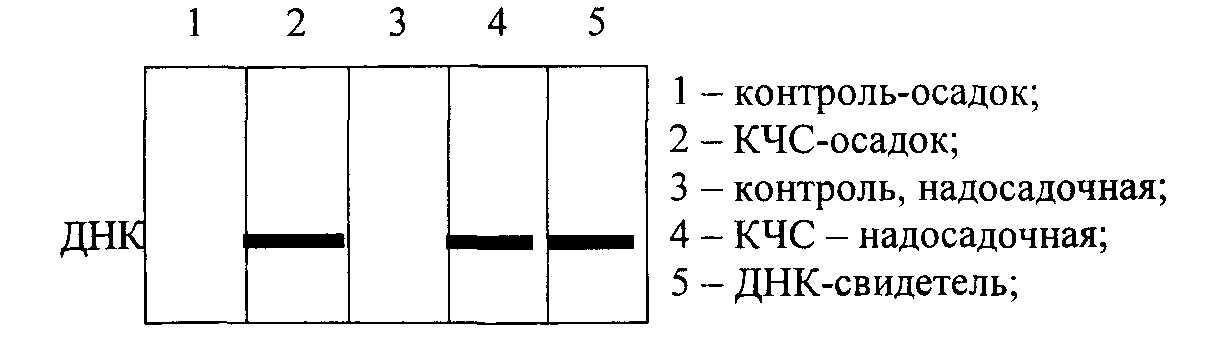
Рис. 12.7. Фотография электрофореграммы, полученной при ультрафиолетовом (УФ) освещении агарозногогеля с продуктами ПЦР. Полосы, выявляемые при УФ-освещении, – это фрагменты ДНК, амплифицированые с участием использованных в опытах праймеров. Контроль – лизат из культуры клток ПК-15, КЧС – лизат из клеток, инфицированных вирусом классической чумы свиней.
13. Обмен воды и солей
Организм животных и растений, кроме белков, углеводов и липидов, содержит обширную группу веществ неорганической природы. К ним относятся вода, анионы и катионы неорганических кислот и солей. Значительная часть солей в организме находится в растворенном состоянии. Другая часть образует прочные нерастворимые комплексы с белками, например, фосфорнокислый кальций в костной ткани, углекислый кальций в раковинах моллюсков. Некоторое количество минеральных веществ входит в состав органических веществ: железо содержится в геме гемоглобина, цитохромов, каталазы, миоглобина; магний, марганец, цинк, медь – в ряде ферментов; йод – в тироксине; кобальт – в витамине B12. Сейчас установлено, что в организме животных и растений обнаруживается до 76 различных элементов (из известных 106).
Различают макроэлементы – их содержание в тканях составляет мг% и более: Ca2+, Mg2+, Na+, K+, P5+, Сl- , S2-.
Микроэлементы – в следовых количествах (мкг%, 10-3 и менее) –Fe2+, Cu2+, Zn2+, I-, Mo2+, Co2+ и др. – однако в некоторых органах они могут содержаться в значительных количествах, например, йод в щитовидной железе.
