
- •Основы электрохимии и электрохимических технологий
- •Введение
- •Окислительно-восстановительные реакции.
- •Правила уравнивания окислительно-восстановительных реакций.
- •Порядок уравнивания окислительно-восстановительных реакций, т.Е. Приведение их в форму, обеспечивающую закон сохранения энергии (баланс массы и заряда).
- •Демонстрация переноса электронов в окислительно-восстановительных реакциях. Гальванический элемент.
- •Лекция 2. Законы Фарадея и скорость электрохимического процесса Выход по току. Применение закона Фарадея к расчету скорости обработки металлов.
- •Скорость электрохимической обработки
- •Электрохимический эквивалент сплава и практический электрохимический эквивалент.
- •Лекция 3. Равновесный потенциал электрода Электрод, ячейка. Напряжение электрода и ячейки. Равновесный потенциал. Виды равновесных потенциалов.
- •Равновесный потенциал.
- •Виды равновесных потенциалов.
- •Лекция 4. Основы теории электролитической диссоциации Равновесные явления в растворах электролитов. Теория электролитической диссоциации. Ион - дипольное и ион - ионное взаимодействие в электролитах.
- •Теория Дюбая – Гюккеля и ион - ионное взаимодействие в растворах электролитов.
- •Гидролиз солей.
- •Буферные растворы.
- •Ионные равновесия при растворении. Произведение растворимости.
- •Лекция 6 Электропроводность электролитов
- •Экспериментальное определение электропроводности.
- •Особые случаи электропроводности электролитов.
- •Электроды первого рода. Потенциал ионно-металлического электрода.
- •Электроды второго рода.
- •Хлорсеребряный электрод.
- •Окислительно – восстановительные (redox) системы.
- •Водородный электрод.
- •Хингидронный электрод.
- •Мембранный потенциал или потенциал Донана.
- •Методы изучения двойного электрического слоя.
- •Модельные представления о строении двойного электрического слоя.
- •Форма поляризационной кривой при наличии стадии массопереноса.
- •Лекция 11 Теория замедленного разряда.
- •Свойства уравнения теории замедленного разряда.
- •Лекция 12 Поляризация (перенапряжение) при образовании новой фазы. Перенапряжение при лимитирующей стадии образования двумерных и трёхмерных зародышей.
- •Перенапряжение поверхностной диффузии при электроосаждении металлов.
- •Перенапряжение образования пузырьков газа и связь размеров пузырьков с потенциалом.
- •Предельные токи при электроосаждении. Эффект м.А.Лошкарёва.
- •Электрические процессы в условиях медленной гомогенной химической реакции.
- •Критерии определения природы лимитирующейстадии.
- •Лекция 14 Примеры механизмов некоторых электрохимических реакций.
- •Примеры механизмов различных электрохимических реакций. Реакция выделения водорода (водородный электрод).
- •Кинетическая теория коррозии.
- •Коррозия при кислородной деполяризации.
- •Роль локальных элементов в возникновении коррозии и достижении её скорости.
- •Методы защиты от коррозии.
- •Пассивность металлов.
- •Электрохимическая размерная обработка металлов и сплавов
- •Основы прикладной электрохимии и электрохимических технологий Лекция 1 Основные особенности электрохимических технологий.
- •Конструктивные принципы электрохимических реакторов
- •Межэлектродный зазор
- •Токовые нагрузки
- •Сепараторы
- •Подвод и отвод компонентов реакции
- •Корректировка состава электролита
- •Масштабный фактор
- •Подбор коррозионностойких материалов
- •Экономические показатели
- •Классификация основных процессов переноса при химической и электрохимической технологии
- •Лекция 2. Распределение тока и рассеивающая способность электролитов Распределение тока. Виды распределения тока. Параметр Вагнера. Рассеивающая (локализующая) способность электролитов
- •Первичное распределение тока.
- •Вторичное распределение тока.
- •Третичное распределение тока.
- •Распределение тока при высоких плотностях тока (при наличии поверхностного тепловыделения)
- •Распределение скоростей осаждения или растворения при наличии зависимости выхода по току от плотности тока
- •Методы расчёта распределения тока.
- •Методы экспериментального определения рассеивающей (локализующей) способности электролита
- •Лекция 3. Химические источники тока (хит). Основные характеристики хит
- •Лекция 4 Первичные хит (хит первого рода, элементы)
- •Сухие марганцево-цинковые (мц) элементы
- •Первичные хит с магниевыми и литиевыми анодами
- •Первичные хит с литиевыми анодами
- •Хит с твердым электролитом
- •Лекция 5 Вторичные хит (аккумуляторы).
- •Свинцовые кислотные аккумуляторы
- •Основные неисправности свинцовых кислотных аккумуляторов.
- •Щелочные аккумуляторы
- •Лекция 6 Топливные элементы.
- •Лекция 7. Электролиз водных растворов без выделения металлов Производство водорода и кислорода
- •Производство тяжелой воды
- •Интенсификация электрохимических методов получения водорода
- •Лекция 8. Электрохимическое производство хлора, щелочи и гипохлотрта натрия
- •Теоретические основы электролиза растворов хлоридов
- •Электролиз с твердым катодом и фильтрующей диафрагмой
- •Электролиз с ртутным катодом.
- •Перспективы развития хлорной промышленности
- •Электросинтез гипохлорита натрия
- •Лекция 9 Электрохимические покрытия металлами и сплавами. Теоретические основы.
- •Два метода нанесения покрытий при электролизе
- •Назначение металлических покрытий металлами и сплавами
- •Управление свойствами и размерами покрытий
- •Использование нестационарного электролиза
- •Лекция 10 Электролитическое осаждение железа.
- •Катодный процесс при электроосаждении железа.
- •Электролиты железнения и режимы электролиза
- •Анодный процесс.
- •Лекция 11. Хромирование. Свойства и области применения хромовых покрытий
- •Некоторые особенности процесса хромирования
- •Электролиты и режимы электролиза.
- •Физико-механические свойства хромовых покрытий
- •Лекция 12. Меднение Область применения
- •Сравнительная характеристика медных электролитов.
- •Борфтористоводородные электролиты
- •Цианистые электролиты
- •Пирофосфатные электролиты
- •Лекция 13. Анодная и химическая обработка металлов Оксидирование
- •Электрохимическое и химическое полирование
- •Лекция 14. Электролиз расплавов. Общие сведения.
- •Строение расплавленных солей
- •Электропроводность расплавленных солей
- •Выход по току и удельный расход энергии при электролизе расплавов
- •Влияние физико-химических свойств электролита на процесс электролиза
- •Некоторые специфические явления при электролизе расплавов
- •Лекция 15. Производство алюминия
- •Переработка алюминиевых руд
- •Получение криолита
- •Электроды и другие материалы
- •Электролиз криолит-глиноземного расплава
- •Состав электролита
- •Конструкция и эксплуатация электролизеров
- •Рафинирование алюминия
- •Электролиз хлорида алюминия
- •Лекция 16. Гидроэлектрометаллургия
- •Лекция 17. Электролиз в металлургии благородных металлов
- •Вопросы для самопроверки, задачи и упражнения
- •Заключение Основные направления современного этапа развития электрохимии и электрохимических технологий
- •Литература
Форма поляризационной кривой при наличии стадии массопереноса.
Учитывая, что перенапряжение () есть не что иное, как:
 , (10.10)
, (10.10)
где
![]() -
равновесный потенциал, а отношение
-
равновесный потенциал, а отношение![]() к
к![]() можно
представить, исходя из:
можно
представить, исходя из:
![]() (10.11)
(10.11)
в то время как:
![]() (10.12)
(10.12)
тогда, используя уравнения (10.11) и (10.12) можно записать, что:
 , (10.13)
, (10.13)
откуда, следует, что
 (10.14)
(10.14)
Мы получили взаимосвязь между перенапряжением и плотностью диффузионного тока, т.е. форму поляризационной кривой в условиях замедленности стадии массопереноса (рис. 10.3).
Эта зависимость имеет вид:

Рис. 10.3
Поляризационная кривая при замедленности
стадии массопереноса (![]() -предельный
диффузионный ток (предельная плотность
диффузионного тока))
-предельный
диффузионный ток (предельная плотность
диффузионного тока))
Величина
![]() при достижении предельного тока
(перенапряжения) стремится к бесконечности.
Это видно из (10.14): при
при достижении предельного тока
(перенапряжения) стремится к бесконечности.
Это видно из (10.14): при![]() выражение в скобках становится равным
0, а. Согласно В.Нернсту
величина
выражение в скобках становится равным
0, а. Согласно В.Нернсту
величина![]() не
может быть рассчитана, а используется
как некая фиктивная величина. Известно
только то, что она зависит от скорости
перемешивания, уменьшаясь с увеличением
последней. Следовательно, и предельный
ток диффузии должен зависеть от скорости
перемешивания.
не
может быть рассчитана, а используется
как некая фиктивная величина. Известно
только то, что она зависит от скорости
перемешивания, уменьшаясь с увеличением
последней. Следовательно, и предельный
ток диффузии должен зависеть от скорости
перемешивания.
В настоящее время существует ряд
гидродинамических систем, для, которых
величина предельного тока (предельной
плотности тока) может быть рассчитана.
Такой системой является вращающийся
дисковый электрод, который представляет
собой торец цилиндра, помещённого в
электролит, боковая поверхность которого
покрыта изолятором. Этот электрод
вращается в жидкости с определённой
угловой скоростью
![]() (рис. 10.4).
(рис. 10.4).
Теория вращения дискового электрода была разработана В.Г. Левичем. Величина диффузионного тока по В.Г. Левичу определяется следующим уравнением:
![]() , (10.15)
, (10.15)
где
![]() - коэффициент диффузии;
- коэффициент диффузии;![]() - кинематическая вязкость раствора;
- кинематическая вязкость раствора;![]() - угловая частота вращения диска.
- угловая частота вращения диска.
Очевидно, что:
![]() (10.16)
(10.16)
Из уравнения (10.16) видно, что для вращающегося дискового электрода:
величина предельного диффузионного тока может быть рассчитана;
она пропорциональна квадратному корню из частоты вращения
 (рис. 10.5);
(рис. 10.5);она пропорциональна концентрации электрохимически активного иона;
на основании (10.16) может быть рассчитана величина Кв уравнении (10.11) и (10.12)
при известной вязкости и концентрации может быть рассчитан коэффициент диффузии;
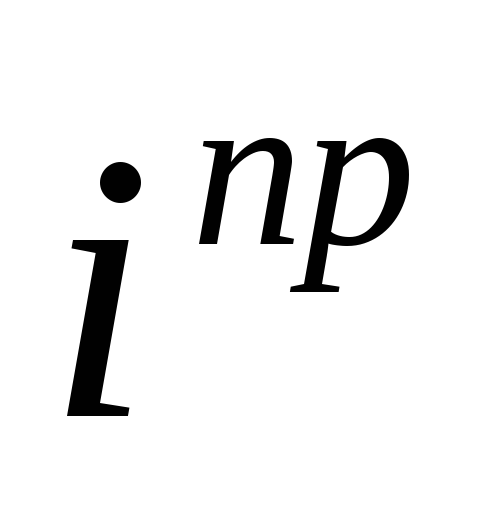 не зависит от размеров диска; такие
поверхности носят названиеравнодоступныхв диффузионном отношении поверхностей.
не зависит от размеров диска; такие
поверхности носят названиеравнодоступныхв диффузионном отношении поверхностей.
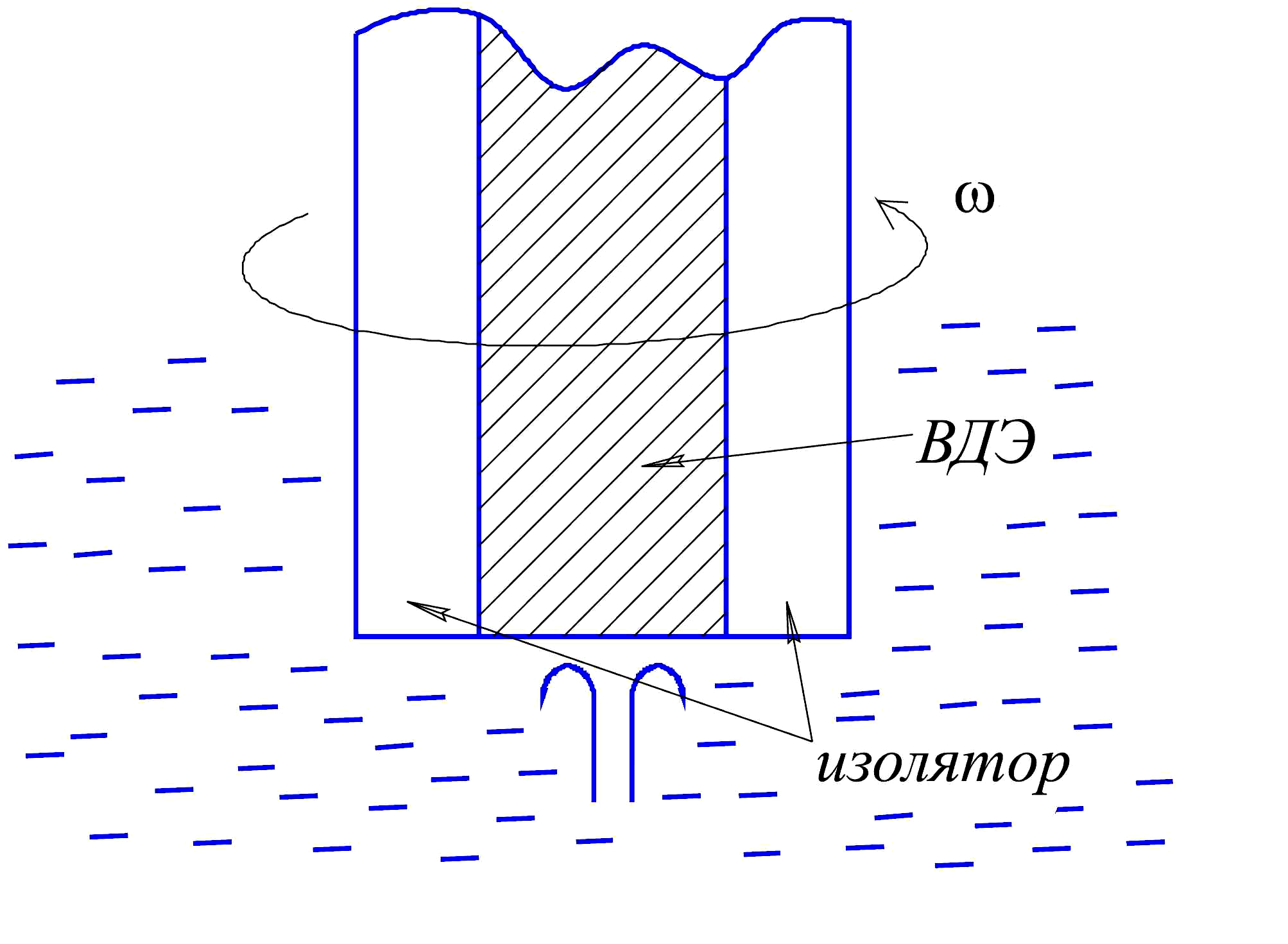
Рис. 10.4 Схема вращающегося дискового электрода
С помощью вращающегося дискового электрода можно определить составляющие тока, которые не зависят от диффузии, т.е. изучать кинетику электрохимических реакций.
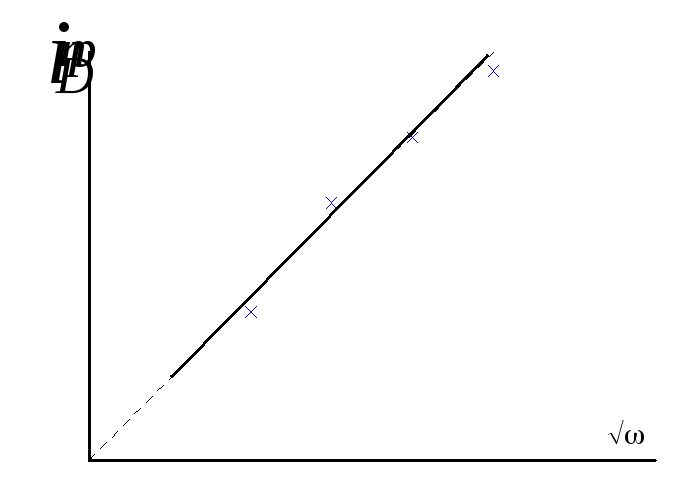
Рис. 10.5 Зависимость предельного диффузного тока от частоты вращения.
Если бы можно было достичь бесконечно большой скорости вращения, то тогда появилась бы возможность полностью ликвидировать концентрационные ограничения. Чисто математически эту проблему можно решить, построив зависимость обратных величин плотности тока от и экстраполируя ток (плотность тока) на бесконечно большую скорость вращения (см. рис. 10.6).
Учитывая, что:
![]() (10.17)
(10.17)
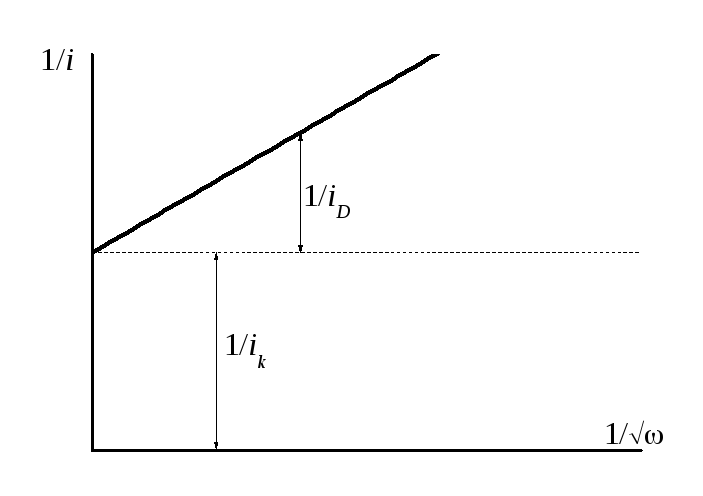
Рис. 10.6 Метод обработки экспериментальных данных, позволяющий выделить кинетический ток экстраполяцией диффузионного тока на бесконечно большую скорость вращения.
Вращающийся дисковый электрод не является единственной системой с равнодоступной поверхностью. Другими такими системами являются: электрод в ячейке с механическим перемешиванием, расположенный непосредственно под мешалкой, электрод в окрестности точки набегания, расположенный на поверхности обтекаемого шара, диска, вращающийся цилиндрический электрод и др.
В общем случае толщина диффузионного
слоя зависит от размеров электрода,
поскольку толщина диффузионного
пограничного слоя
![]() зависит
от толщины гидродинамического пограничного
слоя, который иногда называют слоем
Прандтля. Гидродинамический пограничный
слой – это такой слой, в котором происходит
изменение скорости течения жидкости
от нулевой (непосредственно на поверхности
тела) до постоянной в объёме электролита
(см. рис 10.7).
зависит
от толщины гидродинамического пограничного
слоя, который иногда называют слоем
Прандтля. Гидродинамический пограничный
слой – это такой слой, в котором происходит
изменение скорости течения жидкости
от нулевой (непосредственно на поверхности
тела) до постоянной в объёме электролита
(см. рис 10.7).

Рис. 10.7 Изменение
скорости течения жидкости по мере
приближения к твёрдому телу, где
(![]() -гидродинамический
пограничный слой,x
– расстояние от поверхности электрода)
-гидродинамический
пограничный слой,x
– расстояние от поверхности электрода)
В обычных жидкостях
![]() (10.18)
(10.18)
Уравнение (10.18) соблюдается в тех случаях,
когда безразмерный критерий (число
Шмидта) Sc=![]() ~ 103.
~ 103.
Именно такие величины Scнаблюдаются в обычных жидкостях, и в этих условиях выполняется соотношение (10.18).
Если число Шмидта ~ 1, то
![]() , (10.19)
, (10.19)
т.е. диффузионный пограничный слой численно равен гидродинамическому пограничному слою. Таким образом, в обычных жидкостях наблюдается следующая структура пограничных слоев:
гидродинамический пограничный слой;
диффузионный пограничный слой;
диффузная часть двойного слоя;
плотная часть двойного слоя.
Известно, что течение жидкости может
быть, как ламинарным, так и турбулентным.
В последнем случае в жидкости всегда
наблюдаются флуктуации скорости течения,
а, следовательно, флуктуации диффузионного
пограничного слоя
![]() .
.
Совершенно очевидно, что в таком случае
предельный ток будет колебаться вокруг
некоторого среднего значения, что
связано с колебаниями толщины
![]() .
.

Рис. 10.8 Поляризационные кривые при ламинарном (а) и турбулентном (б) течении раствора в условиях замедленности стадии массопереноса
Как видно из рис. 10.8 на предельном токе наблюдаются пульсации плотности тока, что связано с пульсацией .
Приложения основ диффузионной кинетики.
Диффузионная кинетика является основой следующих практических приложений:
определение концентрации веществ в растворе (электроаналитическая химия); поскольку предельный ток прямо пропорционален концентрации, то это используется для определения концентрации электроактивных соединений в растворе;
определение скорости течения и распределения скоростей (поскольку
 зависит от скорости течения).
зависит от скорости течения).исследование турбулентности;
хемотроника (создание датчиков, например, в сейсмологии). По колебаниям предельного тока можно судить о землетрясениях, взрывах и т.д.:
наличие предельного тока в электрохимической системе имеет огромное значение для электрохимической технологии, потому что качественные осадки в гальванотехнике могут получаться только при плотностях токов ниже предельных, а при анодном растворении в условиях предельных токов наблюдается электрополирование.
За разработку нового метода электроанализа, в основе которого лежит использование предельных диффузионных токов, Я. Гейровскому (Чехословакия) в 1959г. была присуждена Нобелевская премия.
Существует ряд других систем, для которых предельный диффузионный ток может быть рассчитан.
Вращающийся цилиндрический электрод:
![]() , (10.19)
, (10.19)
где Sh - критерий Шервуда, аRe - критерий Рейнольдса.
или:
 , (10.20)
, (10.20)
где r-радиус цилиндра,-частота вращения.
При этом
![]() ,
,![]() .
.
Уравнения (10.19) и (10.20) справедливы, когда числа Re2102…..1,5105.
Плоский электрод в свободном потоке:
![]() , (10.21)
, (10.21)
где
![]() или
или
![]() (10.22)
(10.22)
![]() т.е. при ламинарном режиме течения.
т.е. при ламинарном режиме течения.
![]() -скорость
потока вдали от электрода.
-скорость
потока вдали от электрода.
Имеются и другие системы, для которых можно рассчитывать предельные диффузионные токи: течение в плоском канале и в плоских трубах при ламинарном и турбулентном режимах течения, электроды в окрестности точки набегания. Соответствующие расчётные формулы для этих систем можно найти в справочной литературе.
Теория диффузионной кинетики (кинетика - это наука о скорости химических реакций) позволяет управлять скоростями электрохимических процессов, определяемых скоростью диффузии (конвективной диффузии) с целью уменьшения поляризации электродов и увеличения КПД электрохимических устройств.
