
- •Биохимия животных Электронный дидактический комплекс (эдк)
- •Физическая химия вода
- •Активная реакция водных растворов
- •Ионное произведение воды. Водородный показатель
- •Методы определения рН среды
- •Роль активной реакции среды в биологических процессах
- •Буферные pacтворы, состав, механизм действия
- •Буферная емкость
- •Биологическое значение буферных систем
- •Коллоидная химия
- •Классификация дисперсных систем
- •Поверхностные явления
- •Адсорбция
- •Коллоидные растворы (золи) Методы получения
- •Строение коллоидных частиц
- •Коагуляция. Седиментация. Пептизация
- •Молекулярно-кинетические свойства коллоидных растворов
- •Осмотическое давление
- •Биологическое значение явления осмоса
- •Механизмы, участвующие в сохранении изоосмии:
- •Оптические свойства коллоидных систем
- •Растворы высокомолекулярных соединений
- •Свободная и связанная вода в коллоидных pacтвopax
- •Свойства растворов вмс
- •Денатурация
- •2. Белки; биологическая роль Аминокислоты
- •Содержание белков в организме и тканях
- •Методы выделения белков
- •Методы фракционирования и очистки белков
- •Физико-химические свойства белков
- •Аминокислоты
- •Ациклические аминокислоты
- •Структура белковой молекулы
- •Классификация белков
- •Химия сложных белков
- •3. Нуклеиновые кислоты
- •Нуклеотиды и нуклеозиды
- •Структура днк
- •Рибонуклеиновые кислоты
- •4. Ферменты
- •Биосинтез и клеточная локализация ферментов
- •Химическая природа ферментов
- •Строение ферментов
- •Активный центр фермента
- •Регуляция активности ферментов
- •Механизм действия ферментов
- •Основные свойства ферментов
- •2. Зависимость активности ферментов от рН среды.
- •Факторы, определяющие активность ферментов
- •Активирование и ингибирование ферментов
- •Типы ингибирования
- •Классификация и номенклатура ферментов
- •Применение ферментов.
- •Использование иммобилизованных ферментов для производства биологических соединений
- •Иммуноферментный анализ и его использование в ветеринарии
- •5. Химия витаминов
- •Классификация и номенклатура витаминов
- •I. Жирорастворимые витамины
- •II. Витамины, растворимые в воде
- •Витамин d, антирахитический, кальциферол
- •Витамин e, антистерильный, токоферолы
- •Витамин к, антигеморрагический (филлохинон)
- •Витамин q (убихинон)
- •Водорастворимые витамины
- •Витамин b1, антиневритный, тиамин
- •Витамин b2, рибофлавин
- •Витамин b3, пантотеновая кислота
- •Витамин b5, pp, никотинамид, ниацин, антипеллагрический
- •Витамин b6, адермин, пиридоксол
- •Витамин b12, кобаламин, антианемический
- •Фолиевая кислота
- •Витамин с (аскорбиновая кислота)
- •Биотин, витамин h
- •6. Гормоны
- •Гормоны гипофиза
- •Поджелудочная железа
- •Гормоны щитовидной железы
- •Гормоны надпочечников
- •Гормоны коры надпочечников
- •Гормоны половых желез
- •Гормоны тимуса (вилочковой железы)
- •Гормоны местного действия
- •7. Обмен веществ и энергии
- •Основные этапы обмена веществ
- •Биологическое окисление
- •Окислительное фосфорилирование
- •Токсичность кислорода
- •8. Химия и обмен углеводов
- •Моносахариды
- •Производные моносахаридов.
- •Полисахариды (гликаны)
- •Гетерополисахариды (гетерогликаны)
- •Обмен углеводов
- •Катаболизм глюкозы
- •Гликогенолиз
- •Биосинтез углеводов
- •Биосинтез гликогена (гликогенез)
- •Регуляция углеводного обмена.
- •9. Химия и обмен липидов
- •Химическое строение нейтральных жиров
- •Жирные кислоты.
- •Нейтральные гликолипиды
- •Фосфолипиды (фосфатиды)
- •Сфинголипиды
- •Двойной липидный слой мембран
- •Обмен липидов
- •Переваривание липидов в желудочно-кишечном тракте
- •Промежуточный обмен липидов
- •Энергетический баланс β-окисления жирных кислот
- •Метаболизм ацетил-коэнзима а
- •Пути образования кетоновых тел
- •Биосинтез липидов
- •Метаболизм стеринов и стеридов
- •Липосомы
- •10. Обмен белков
- •Биологическая ценность белков
- •Нормы белка в питании животных
- •Белковые резервы организма
- •Обмен простых белков
- •Переваривание белков в желудочно-кишечном тракте моногастричных животных
- •Переваривание белков в кишечнике.
- •Особенности переваривания белков у жвачных животных
- •Дезаминирование аминокислот
- •Трансаминирование – непрямой путь дезаминирования аминокислот
- •Декарбоксилирование аминокислот
- •Окислительное расщепление аминокислот
- •Особенности обмена отдельных аминокислот
- •11. Биосинтез белка
- •Генетический код
- •Этапы синтеза белка
- •Мультиферментный механизм синтеза белка
- •12.Обмен нуклеиновых кислот Переваривание нуклеиновых кислот в желудочно-кишечном тракте
- •Промежуточный обмен нуклеиновых кислот Распад нуклеиновых кислот в тканях
- •Пиримидиновые основания
- •Биосинтез нуклеиновых кислот
- •Рекомбинантные молекулы и проблемы генной инженерии
- •Клонирование животных
- •Метод молекулярной гибридизации
- •Принцип метода
- •Способы гибридизации
- •Метод блоттинга по Саузерну
- •Полимеразная цепная реакция (пцр)
- •Необходимые приборы и реактивы
- •13. Обмен воды и солей
- •Вода, ее содержание и роль в организме
- •Потребность животного организма в минеральных веществах, их поступление и выделение
- •Микроэлементы
- •14. Биохимия крови
- •Физико-химические свойства крови
- •Буферные системы крови
- •Плазма крови и ее химический состав
- •Белки плазмы и сыворотки крови
- •Небелковые азотистые вещества крови
- •Форменные элементы крови
- •15. Биохимия мышечной ткани
- •Механизм сокращения мышцы
- •Азотистые экстрактивные вещества мышц
- •Минеральные вещества
- •Окоченение мышц
- •16. Биохимия молока и молокообразования
- •17. Биохимия почек и мочи
- •Патологические компоненты мочи
- •Особенности мочи птиц
- •18. Биохимия кожи и шерсти
- •19. Биохимия яйца
- •Биосинтез компонентов яйца
- •Предметный указатель
- •Приложения
- •Рекомендуемая литература
- •Тесты для проверки биохимических
- •Глава 8. Химия обмена углеводов
- •24. Сложноэфирные связи в молекулах триацилглицеролов подвергаются ферментативному гидролизу при участии:
- •Глава 11. Синтез белка
- •Глава 12. Обмен нуклеиновых кислот
- •Глава 13. Биохимия почек и мочи
Биологическое окисление
Биологическое окисление – это окислительно-восстановительные реакции, происходящие в клетках с участием ферментов, являющиеся источником энергии в организме. Химизм горения и биологического окисления, например, глюкозы происходят по общей схеме:
C6H12O6 +6O2 -> 6CO2 + 6 H2O+ 686 ккал (на 1 грамм-молекулу)
Но имеются отличия:
а) горение происходит при высокой температуре, а тканевое окисление – при 37 0C;
б) горение в воде невозможно, а тканевое окисление происходит в водной среде;
в) при горении энергия освобождается моментально в виде тепла, а при биологическом окислении энергия освобождается ступенчато, аккумулируется в молекулах АТФ.
Окисление в тканях может происходить:
а) присоединением кислорода;
б) потерей или отнятием от водорода электрона.
Под окислением понимают все химические реакции, в основе которых лежит отдача электронов и увеличение положительных валентностей. Если одно вещество окисляется, то другое – восстанавливается, т.е. присоединяет электроны.
Окислительно-восстановительные реакции – это перенос электронов, иногда и протонов.
Биологическое окисление – это совокупность окислительно-восстановительных реакций переноса электронов, происходящих в клетках.
Субстратное окисление – это отнятие электронов от промежуточных продуктов обмена углеводов, жиров и белков. Катализируется дегидрогеназами.
Тканевое дыхание – разновидность биологического окисления, при котором акцептором электрона является кислород.
Окисление в дыхательной цепи – это ферментативный перенос электронов от субстрата к кислороду по дыхательной цепи. Ферменты тканевого дыхания находятся в митохондриях, они строго упорядочены, обеспечивают передачу электронов и протонов от субстрата до кислорода, их называют метаболонами. Различают четыре группы ферментов: пиридинзависимые дегидрогеназы; флавиновые ферменты; убихинон (кофермент Q); цитохромная система.
Пиридинзависимые дегидрогеназы, к этой группе относится свыше 150 ферментов. Коферментами их являются никотинамидадениндинуклеотид (НАД+) и никотинамид-адениндинуклеотидфосфат (НАДФ+).
НАДФ+ отличается от НАД+ тем, что у второго углеродного атома рибозы атом водорода гидроксильной группы замещен остатком фосфорной кислоты.
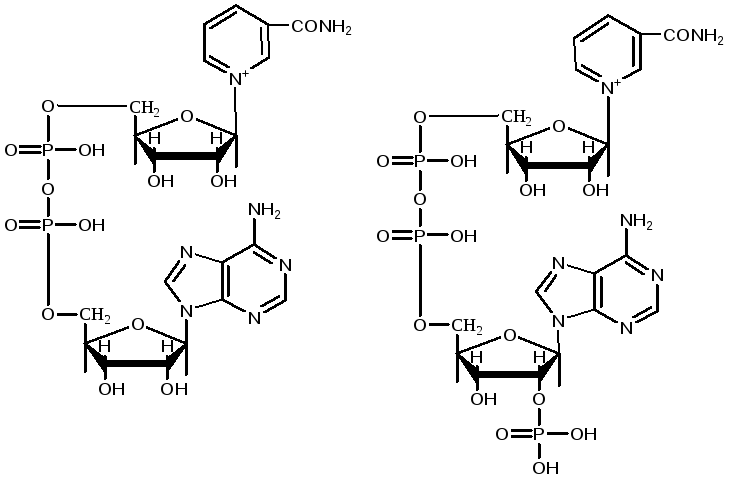
никотинамидадениндинуклеотид никотинамидадениндинуклео- (НАД+) тидфосфат (НАДФ+)
Восстановление НАД происходит путем переноса гидрид-иона (: Н-) от субстрата RH2 в положение 4 никотинамидного кольца:
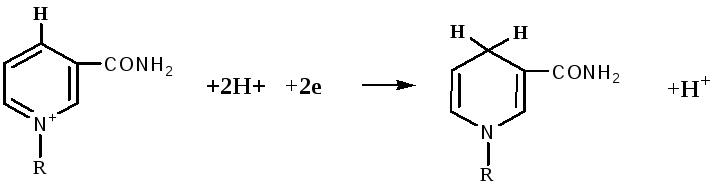
НАД+ НАДН
Флавиновые ферменты. Различают свыше 30 флавиновых ферментов. Коферментом их является флавинадениндинуклеотид (ФАД) и флавинмононуклеотид (ФМН).
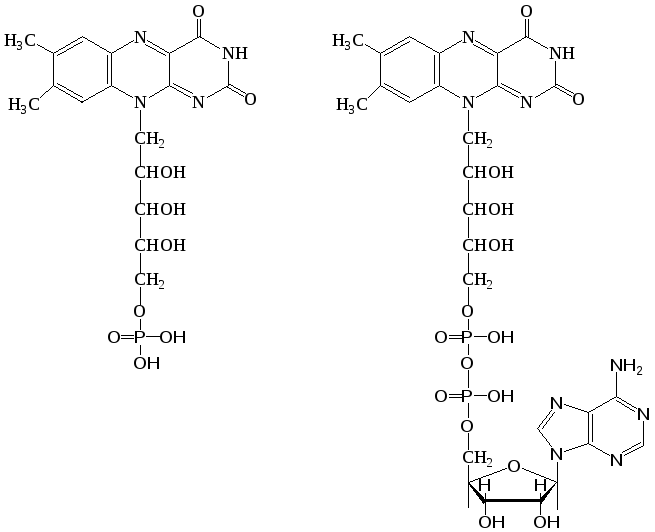
флавинмононуклеотид (ФМН) флавинадениндинук-
леотид (ФАД)
ФМН построен из молекулы витамина B2 и остатка фосфорной кислоты, а ФАД представляет собой ФМН, соединенный через фосфорную кислоту с АМФ. Восстановление ФАД (или ФМН) происходит путем переноса атомов водорода (и 2-х электронов) от субстрата RH2 в положение 1 и 10 молекулы рибофлавина:
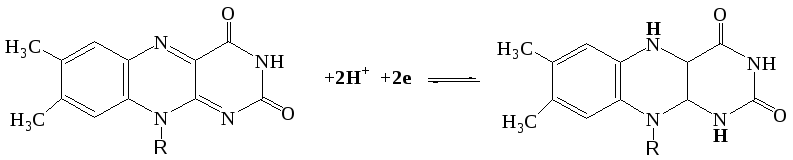
Убихинон (кофермент Q). Убихинон относится к очень широко распространенным коферментам. По химической природе представляет собой 2,3 - диметокси-5-метил-1,4-бензохинон с изопреновой цепью в 6-м положении. Число остатков изопрена в боковой цепи - 10. Восстановленная форма флавиновых ферментов (ФАДН2, ФМНН2) в цепи дыхательных катализаторов передает атомы водорода (протоны и электроны) KoQ. Как всякий хинон, KoQ может существовать как в окисленной, так и восстановленной форме (R-изопреноидная боковая цепь):
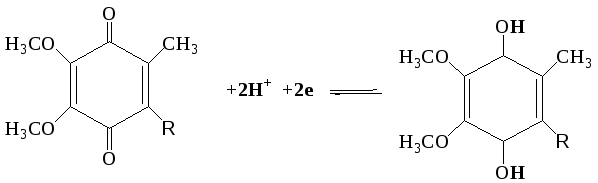
KoQ окисленный KoQ-H2 -восстановленный
Цитохромная система — цитохромоксидазы. Эти четыре группы ферментов осуществляют перенос протонов и электронов от окисляемых веществ на кислород (см. схему дыхательной цепи). Электроны, отщепленные от субстрата, передаются по дыхательной цепи до кислорода, где образуется молекула воды. В дыхательной цепи имеются механизмы, обеспечивающие синтез молекулы АТФ.
Биологическое окисление субстрата начинается с отнятия водорода - дегидрирования. Это происходит с участием НАД (или НАДФ). Дегидрогеназы, отщепив водород от окисляемого вещества, передают его флавиновым ферментам (ФАД, ФМН). Активной группой НАД является витамин В5 – амид никотиновой кислоты, принимая водород, он превращается в восстановленную форму (НАДН2). Далее происходит восстановление ФАД (ФМН), где активной группой является витамин B2. В дальнейшем атом водорода передается на убихинон, образуется восстановленная форма его KoQ.H2. Следующие ферменты дыхательной цепи – цитохромоксидазы. Эти хромопротеиды содержат железо, способное изменять свою валентность Fe2+ ↔ Fe 3+. В ходе каталитического процесса валентность железа изменяется обратимо. Различают цитохромы в, cl, с и аа3 . Последовательность передачи электронов следующая:
![]()
Цитохромы в - с1 - с являются промежуточными переносчиками, а цитохром ааЗ (цитохромоксидаза) – конечным ферментом, непосредственно взаимодействующим с кислородом. Окисленная форма Fe3+ принимает электроны от восстановленного цитохрома с, переходя в восстановленное Fe2+. Переносчиком электронов являются также белки, содержащие негеминовое железо. В этих белках несколько атомов железа связано с остатком цистеина. Указанные ферменты находятся в строгой последовательности в фиксированном состоянии на внутренней мембране митохондрий, их называют метаболонами (Рис. 7.2.).
