
- •Оглавление
- •Введение
- •Глава 1. Состав и свойства жиров
- •1.1. Химический состав жиров
- •Контрольные вопросы
- •1.2. Классификация пищевых жиров
- •Контрольные вопросы
- •1.3. Физические свойства и показатели жиров
- •Контрольные вопросы
- •1.4 Химические превращения и свойства жиров
- •Контрольные вопросы
- •1.5 Интегральные показатели качества жиров
- •Контрольные вопросы
- •1.6 Жиры и здоровое питание
- •Контрольные вопросы
- •Глава 2. Растительные масла
- •2.1. Рынок растительных масел. Изучение и прогнозирование покупательского спроса
- •Контрольные вопросы
- •2.2. Сырье и технология производства растительных масел
- •Контрольные вопросы
- •2.3. Ассортимент и товароведная характеристика жидких растительных масел
- •Отличительные потребительские свойства соевого масла – высокое содержание полиненасыщенных жирных кислот (более 60 %), соотношение -6 и -3 жирных кислот приближается к оптимальному (Табл. 13).
- •Нетрадиционные, экзотические и целебные растительные масла
- •Контрольные вопросы
- •2.4. Ассортимент и товароведная характеристика твердых растительных масел
- •Контрольные вопросы
- •Контрольные вопросы
- •2.6. Экспертиза качества и идентификация растительных масел
- •Контрольные вопросы
- •2.7. Организационно-управленческая деятельность в области товарного менеджмента пищевых жиров
- •Контрольные вопросы
- •2.8. Особенности товарного менеджмента растительных масел
- •2.8.1. Организация и управление поставкой, транспортированием и хранением растительных масел
- •2.8.2. Приемка и реализация растительных масел в торговых организациях
- •2.8.3. Управление ассортиментом и продвижением растительных масел
- •Контрольные вопросы
- •2.8.4. Оценка поставщиков
- •Глава 3. Пищевые животные топленые жиры и топленые жиры птицы
- •3.1. Состояние рынка топленых жиров и тенденции
- •Здорового образа жизни
- •3.2. Производство и ассортимент топленых жиров
- •3.2.1. Производство пищевых животных топленых жиров
- •Контрольные вопросы
- •3.3. Экспертиза качества и идентификация животных топленых жиров и топленых жиров птицы
- •3.3.1. Экспертиза животных топленых жиров
- •3.3.2. Экспертиза топленых жиров птиц
- •Контрольные вопросы
- •3.4. Особенности товарного менеджмента пищевых топленых жиров
- •Контрольные вопросы
- •Глава 4. Маргариновая продукция
- •4.1. Рынок маргариновой продукции
- •Контрольные вопросы
- •4.2. Пищевая ценность, состав и свойства маргариновой продукции, структурно-реологические основы производства
- •Контрольные вопросы
- •4.3. Ассортимент. Производство маргаринов
- •Контрольные вопросы
- •4.4 Жиры специального назначения.
- •Контрольные вопросы
- •4.5 Упаковка, маркировка, транспортирование и хранение маргариновой продукции и специальных жиров
- •Контрольные вопросы
- •4.6. Экспертиза маргариновой продукции
- •Контрольные вопросы
- •Особенности товарного менеджмента маргариновой продукции
- •Контрольные вопросы
- •Глава 5. Спреды. Топленые смеси
- •5.1 Состояние рынка спредов и топленых смесей
- •Контрольные вопросы
- •5.2 Классификация и ассортимент спредов и топленых смесей. Пищевая ценность
- •Контрольные вопросы
- •5.3 Основы технологии спредов и топленых смесей
- •5.4 Идентификация и экспертиза спредов и топленых смесей
- •Контрольные вопросы
- •Глава 6. Майонезы и майонезные соусы
- •6.1. Рынок и ассортимент майонезных продуктов
- •Контрольные вопросы
- •6.2 Пищевая ценность, классификация и ассортимент майонезной продукции
- •Контрольные вопросы
- •6.3 Производство майонезной продукции
- •Контрольные вопросы
- •Контрольные вопросы
- •6.5 Товарный менеджмент майонезной продукции
- •Контрольные вопросы:
- •Глоссарий
- •Список литературы
- •Приложение 1 Требования к допустимым уровням показателей безопасности пищевой масложировой продукции
- •Продолжение Приложения 1
- •Продолжение Приложения 1
- •Приложение 2 Требования по микробиологическим нормативам безопасности пищевой масложировой продукции
- •3 94006 Воронеж, ул. 20-летия Октября, 84
Глава 1. Состав и свойства жиров
1.1. Химический состав жиров
Натуральные жиры по происхождению делят на животные (по большей части твердые при комнатной температуре) и растительные – масла, как правило, жидкие при комнатной температуре.
С точки зрения органической химии жирами называют сложные эфиры глицерина и жирных кислот – глицериды, а точнее триглицериды (триацилглицерины), т.е. соединения глицерина с тремя молекулами жирных кислот. Ниже приведена общая формула триглицеридов, где R1, R2 и R3 – углеводородные остатки высших карбоновых кислот.
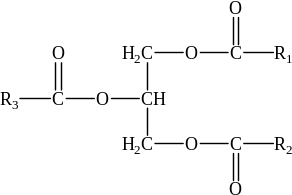
Собственно жиры (триглицериды), жироподобные вещества (липоиды) и ряд других гидрофобных веществ нежировой природы объединяют под общим названием липиды. В целом, под липидами понимают сложную смесь органических веществ, выделяемых из объектов растительного, животного и микробиологического происхождения.
Липиды (от греч. lipos – жир) – это группа веществ, различных по химическому составу и структуре, общими свойствами которых являются гидрофобность (нерастворимость в воде) и способность растворяться в малополярных органических растворителях. Наряду со сложными эфира-ми жирных кислот в число липидов часто включают стерины, жиро-растворимые витамины и другие соединения. Согласно классификации проф. Б. Н. Тютюнникова липиды делятся на простые (глицериды, церины – основа восков, церолы, углеводороды жирного ряда), сложные (фосфатиды, гликозидолипиды, липопротеиды) и циклические (стеролы и их эфиры с высокомолекулярными жирными кислотами).
Состав липидов исключительно сложен и зависит от источника получения, его состояния, методов выделения и многих других факторов. Только простых триглицеридов природного происхождения известно более 500.
В составе простых липидов отсутствует азот, фосфор и сера. К простым липидам относятся нейтральные липиды, являющиеся производными высших кислот, одно- , двух- и многоатомных спиртов (ацилглицерины, эфиры диолов, воски, алкильные липиды, плазмалогены), а также их структурные компоненты (спирты, карбоновые кислоты).
В состав сложных липидов входят фосфолипиды и сфинголипиды. Их элементный состав наряду с углеродом, водородом и кислородом включает фосфор, азот и в ряде случаев серу.
Триглицериды составляют основную массу липидов (в отдельных случаях до 95-98%). Наряду с триглицеридами встречаются диольные липиды, содержащие сложные, простые и алкенильные эфиры, структурным компонентом которых является не глицерин, а двухатомные спирты (диолы) различного строения. В значительном количестве они присут-ствуют в липидах морских организмов.
К простым липидам относят воски. Так называются входящие в состав липидов сложные эфиры высокомолекулярных одноосновных кислот и одноатомных высокомолекулярных спиртов. В состав восков входят кислоты, содержащие 24-32 атома углерода, и спирты, углеродная цепочка которых состоит из 14-30 атомов углерода.
Из растительных восков промышленное значение имеют воски, покрывающие листья пальм, воски липидов риса и подсолнечника. Из восков животного происхождения – спермацет и спермацетовое масло, шерстяной жир; насекомых – пчелиный воск.
Большая группа нейтральных липидов, в состав молекулы которых входят остатки моносахаридов, называются гликолипидами. Они выполняют функции структурных липидов – участвуют в построении мембран, формировании клейковины пшеницы, которая определяет хлебопекарное достоинство муки.
Свойства жиров зависят в основном от строения и состава жирных кислот. Всего в жирах обнаружено свыше четырехсот карбоновых кислот различного строения. Наиболее распространенные в жирах кислоты содержат от 12 до 18 атомов углерода, эти карбоновые кислоты называются жирными кислотами.
В состав пищевых жиров входят жирные кислоты с четным числом атомов углерода в углеводородной цепи от 4 до 26. Сами жирные кислоты делятся на две большие группы: насыщенные (предельные) и ненасыщенные (непредельные), содержащие двойные связи. Из насыщенных жирных кислот наиболее часто встречаются пальмитиновая (С15Н31СООН) и стеариновая (С17Н35СООН) (табл. 1).
Насыщенные жирные кислоты преобладают в жирах животного происхождения, ненасыщенные – в растительных жирах, при этом первые из перечисленных уступают вторым по биологической значимости. Насыщенные жирные кислоты используются организмом как энергетический материал. Их избыток приводит к нарушению обмена жиров и повышению уровня холестерина в крови. Среди насыщенных наибольшее значение имеет пальмитиновая кислота. Она является первичным продуктом, образующимся под действием синтетазы жирных кислот, источником для биосинтеза других насыщенных и мононенасыщенных кислот.
Таблица 1. Характеристика жирных кислот
Название кислоты |
Формула |
Молекулярная масса |
Плотность
|
|
по ИЮПАК |
Тривиальное |
|||
Бутановая Пентановая Гексановая Гептановая Октановая Нонановая Декановая Ундекановая Додекановая Тридекановая Тетрадекановая Пентадекановая Гексадекановая Гептадекановая Октадекановая Нонадекановая Эйкозановая |
Масляная Валериановая Капроновая Гептиловая Каприловая Пеларгоновая Каприновая Ундециловая Лауриновая Тридециловая Миристиновая Пентадециловая Пальмитиновая Маргариновая Стеариновая Нонадециловая Арахиновая |
C4H8O2 C5H10O2 C6H12O2 C7H14O2 C8H16O2 C9H18O2 C10H20O2 C11H22O2 C12H24O2 C13H26O2 C14H28O2 C15H30O2 C16H32O2 C17H34O2 C18H36O2 C19H38O2 C20H40O2 |
88,10 102,13 116,15 130,18 144,21 158,23 172,26 186,29 200,31 214,34 228,36 249,39 256,42 270,44 284,47 298,49 312,52 |
0,959(20) 0,942(20) 0,929(20) 0,922(20) 0,910(20) 0,907(20) 0,895(30) 0,991(25) 0,883(20) 0,846(80) 0,858(80) 0,842(80) 0,853(62) 0,853(60) 0,847(69) 0,877(24) 0,824(100) |
Свойства ненасыщенных жирных кислот зависят от степени не-насыщенности, т. е. количества двойных связей в молекуле. Моно-ненасыщенные жирные кислоты (например, олеиновая) имеют одну двойную связь, полиненасыщенные – от двух до шести двойных связей (линолевая, линоленовая, арахидоновая и др.). Ненасыщенные жирные кислоты составляют до 80-90% жидких жиров (масел) и жиров гидро-бионтов (организмов, живущих в воде). Важнейшее значение для организма человека имеют такие полиненасыщенные жирные кислоты как линолевая (2 двойные связи), линоленовая (3 двойные связи) и арахидоновая (4 двойные связи).
В природных жирах содержатся только одноосновные карбоновые кислоты. Двухосновные кислоты выделены в небольших количествах в некоторых восках и жирах, подвергшихся действию окислителей. Кислоты с разветвленной цепью углеродных атомов в жирах встречается редко. Такие кислоты входят в состав некоторых восков.
Жирные кислоты природных жиров представляют собой жидкие или твердые, но легкоплавкие вещества. Высокомолекулярные насыщенные кислоты – твердые, большинство ненасыщенных жирных кислот нормального строения – жидкие вещества, а их позиционные и геометрические изомеры – твердые. Относительная плотность жирных кислот меньше единицы (Табл. 1) и они практически нерастворимы в воде (за исключением низкомолекулярных). В органических растворителях (спирте, этиловом и петролейном эфирах, бензоле, сероуглероде и др.) они растворяются, но с увеличением молекулярной массы растворимость жирных кислот снижается.
Таким образом, жирные кислоты, входящие в состав природных жиров за редким исключением принадлежат к классу одноосновных алифатических карбоновых кислот, имеющих общую формулу RCOOH. В этой формуле R - углеводородный радикал C4-C24, который может быть насыщенным, ненасыщенным (различной степени ненасыщенности).
В природных жирах, не подвергшихся окислительным процессам, встречаются следующие основные гомологические группы жирных кис-лот:
1. Насыщенные (предельные) одноосновные кислоты.
2. Ненасыщенные (непредельные) одноосновные кислоты с одной, двумя, тремя, четырьмя и пятью двойными связями.
3. Насыщенные (предельные) гидроксикислоты.
4. Ненасыщенные (непредельные) гидроксикислоты с одной двойной связью.
5. Циклические кислоты (Табл. 2).
Таблица 2. Классификация жирных кислот
Классификация кислот |
Общая формула |
Формула и название представителя |
1 |
2 |
3 |
Насыщенные или предельные кислоты (алкановые) |
||
Кислоты прямоцепочечные (нормального строения): |
|
|
одноосноные |
Cn2H2nO2 |
CH3(CH2)14COOH пальмитиновая |
двухосновные |
Cn2H2n-2O4 |
HOOC(CH2)3COOH янтарная |
Продолжение Табл. 2
1 |
2 |
3 |
Кислоты с разветвлённой цепью (изокислоты) |
Cn2H2nO2 |
изовалерьяновая |
Ненасыщенные или непредельные кислоты |
||
Кислоты прямоцепочечные (нормального строения): |
|
|
c 1 двойной связью (алкеновые), моноеновые |
CnH2n-2O2 |
CH3(CH2)7CH=CH(CH2)7COOH олеиновая |
Полиеновые:
|
||
с двумя - диеновые |
CnH2n-4O2 |
линолевая |
с тремя - триеновые |
CnH2n-6O2 |
линоленовая |
с четырьмя - тетраеновые |
CnH2n-8O2 |
арахидоновая |
с пятью - пентаеновые |
CnH2n-10O2 |
клупанодоновая |
с шестью - гексаеновые |
CnH2n-12O2 |
докозагексаеновая |
Кислоты разветвлённые непредельные |
CnH2n-2O2 |
фриеновая (миколипеновая) |
Кислоты алициклические |
|
алепроловая |
Гидроксикислоты: |
||
Предельные моногидроксикислоты |
CnH2nO3 |
CH3CHOH-COOH молочная |
полигидроксикислоты |
|
9,10 - дигидроксистеариновая |
непредельные гидроксикислоты |
|
CH3(CH2)5CHOHCH2- -CH=CH(CH2)7COOH рицинолевая |
1. Насыщенные одноосновные жирные кислоты. В природных жирах и восках наиболее часто встречаются насыщенные одноосновные кислоты нормального строения, имеющие общую формулу СnН2nО2.
Физические свойства насыщенных жирных кислот зависят от их молекулярной массы. Так, температура кипения жирных кислот возрастает с увеличением молекулярной массы. При кипении под атмосферным давлением насыщенные жирные кислоты, начиная, с каприновой разлагаются.
При атмосферном давлении высокомолекулярные жирные кислоты перегоняются только с перегретым водяным паром, а низкомолекулярные (до каприновой включительно) перегоняются без разложения с водяным паром при температуре 100°С. По этому признаку насыщенные кислоты подразделяются на летучие и нелетучие.
Летучие жирные кислоты – это кислоты с небольшой молекулярной массой (до каприновой кислоты включительно), перегоняющиеся при атмосферном давлении без разложения.
Температура плавления жирных кислот возрастает с повышением молекулярной массы. Температура плавления бинарных смесей жирных кислот обычно бывает более низкой по сравнению с температурой плавления одного или даже обоих компонентов.
Жирные кислоты образуют эвтектические смеси, т. е. сплавы, имеющие постоянную температуру плавления, компоненты которых не могут быть разделены даже повторной кристаллизацией. Примером может служить сплав из 47,5%-ной стеариновой кислоты и 52,5%-ной пальмитиновой кислоты. Он дает эвтектическую смесь с постоянной температурой плавления 54,8°С (ниже температуры плавления каждого из составляющих компонентов).
Температура застывания насыщенных жирных кислот несколько ниже температуры их плавления вследствие переохлаждения или образования полиморфных форм.
Растворимость в воде с возрастанием молекулярной массы уменьшается, а начиная с лауриновой кислоты, все высокомолекулярные кислоты в воде практически нерастворимы.
По растворимости в воде кислоты делят на растворимые и нераст-воримые, однако такое деление весьма условно.
Насыщенные жирные кислоты растворимы почти во всех органи-ческих растворителях – диэтиловом эфире, петролейном эфире, ацетоне, хлороформе и др. В холодном спирте высокомолекулярные насыщенные кислоты растворяются плохо, но при нагревании их растворимость значительно увеличивается. Растворимость насыщенных кислот в органических растворителях падает с увеличением молекулярной массы и возрастает с повышением температуры. Плотность насыщенных жирных кислот уменьшается с увеличением молекулярной массы. У первой кислоты этого гомологического ряда с четным числом углеродных атомов – уксусной С2Н4О2 – плотность при 20°С равна 1049 кг/м3, а все последующие кислоты легче воды.
Насыщенные кислоты довольно устойчивы к действию различных реагентов – окислителей, галогенов и др.
Показатель преломления насыщенных жирных кислот возрастает с увеличением молекулярной массы.
В строении насыщенных жирных кислот имеется следующая закономерность: в подавляющем большинстве все кислоты, входящие в состав природных жиров, содержат четное число углеродных атомов.
Рассмотрим характеристики отдельных представителей насыщенных (предельных) жирных кислот.
Масляная кислота [СН3(СН2)2СООН] – бесцветная жидкость с кислым, неприятным запахом, входит в состав масла из коровьего молока (2-4%) в виде разнокислотных триглицеридов. В прогорклом масле некоторое количество ее находится в свободном состоянии.
Капроновая кислота [СН3(СН2)4СООН] – бесцветная маслянистая жидкость с резким неприятным запахом, входит в состав кокосового, коровьего, пальмового и других масел.
Каприловая кислота [СН3(СН2)6СООН] – бесцветная маслянистая жидкость с неприятным запахом, застывающая при температуре 16,5 °С, легко перегоняется с водяным паром, входит в состав кокосового, пальмового и других масел.
Каприновая кислота [СН3(СН2)8СООН] – белое кристаллическое вещество при комнатной температуре, почти нерастворима в воде, пальмовом и некоторых других маслах, а также в небольшом количестве в спермацетовом жире.
Лауриновая кислота [СН3(СН2)10СООН] – твердое кристаллическое вещество, застывающее в виде игл, с температурой плавления 44 °С. При нормальном давлении не перегоняется без разложения. В воде при температуре 20 °С практически не растворяется. Содержится в значительном количестве в кокосовом (44,0-52,0%) масле и спермацетовом жире, а также в молочных жирах.
Миристиновая кислота [СН3(СН2)12СООН] – кристаллическое вещество с температурой плавления 54,4 °С, кристаллизуется в виде тонких листочков. В воде при температуре 20 °С она почти нерастворима, малорастворима в холодных спирте и эфире, но хорошо растворяется при температуре кипения этих растворителей. Присутствует во многих животных жирах и растительных маслах. В большом количестве содержится в пальмовом, кокосовом и мускатном маслах, в молочных жирах – 8-12%, примерно столько же в спермацетовом жире, в небольших количествах – в льняном масле.
Пальмитиновая кислота [СН3(СН2)14СООН] – белое кристаллическое вещество с температурой плавления 62,9 °С, нерастворимое в воде. При нормальном давлении без пара перегоняется с разложением. Содержится почти во всех жирах, как животного, так и растительного происхождения: в пальмовом масле – 32-40%, в хлопковом – 20-24%, в соевом– 2,5-6%, в подсолнечном – 3-4%. В говяжьем сале содержится 20-30% пальмитиновой кислоты, а в кашалотовом жире – до 8%.
Стеариновая кислота [СН3(СН2)16СООН] – блестящие белые, жирные на ощупь чешуйки без запаха и вкуса, плавящиеся при 69,6 °С. Она является одной из самых распространенных в природе кислот и входит в состав почти всех жиров, особенно твердых. В говяжьем сале содержится 24-25% стеариновой кислоты, в костном жире – 19-21%, конском – до 7%, свином – 7-15%, хлопковом масле – 2%, соевом – 4,5-7,0%, подсолнечном – 2-3%.
Арахиновая кислота [СН3(СН2)18СООН] – кристаллическое вещество с температурой плавления 75,3 °С, кристаллизуется в форме небольших блестящих листочков, плохо растворяется в холодном спирте, но хорошо – в горячем. Кислота содержится в арахисовом масле (2,3-4,9%), в меньшем количестве присутствует в маслах: льняном, сурепном, какао, коровьем и др.
Бегеновая кислота [СН3(СН2)20СООН] – кристаллизуется в форме игл с температурой плавления 79,9 °С. Содержится в очень небольших количествах в арахисовом, кукурузном, рапсовом и в некоторых других жирах. Кроме того, бегеновая кислота получается при гидрогенизации ненасыщенной эруковой кислоты, выделенной из горчичного или рапсового масла.
Лигноцериновая кислота [СН3(СН2)22СООН] – кристаллизуется из горячего спирта в виде шелковистых хлопьев с температурой плавления 84,2 °С. Находится в арахисовом масле (до 5%), в буковом дегте и в небольших количествах как составная часть в некоторых липидах.
Церотиновая кислота [СН3(СН2)24СООН] – встречается в восках как в свободном состоянии, так и в виде сложных эфиров, входит в состав пчелиного воска и шерстяного жира, температура плавления 87,7 °С.
Монтановая кислота [СН3(СН2)26СООН] – содержится в восках, температура плавления 90 °С.
Мелиссиновая кислота [СН3(СН2)28СООН] – содержится в небольшом количестве в свободном состоянии в пчелином воске. Из абсолютного спирта кислота выкристаллизовывается в виде шелковистых блестящих игл или листочков. В холодном метиловом спирте и в эфире мелиссиновая кислота почти нерастворима, температура плавления 93,6°С.
2. Ненасыщенные или непредельные жирные кислоты широко распространены в природе, находятся в жирах растительного и животного происхождения. Особенно много их в жидких растительных маслах. Большинство ненасыщенных жирных кислот имеет нормальную цепь с четным числом углеродных атомов. В животных и растительных жирах содержатся главным образом кислоты с одной, двумя или тремя двойными связями. Ненасыщенные кислоты могут также различаться местом расположения двойных связей и пространственной конфигурацией (цис- и транс-изомеры), обусловливая различие в физических и химических свойствах.
Ненасыщенные жирные кислоты отличаются большой реакционной способностью. Для них характерны следующие реакции.
Присоединение галогенов. К каждой двойной связи в ненасыщенных жирных кислотах могут присоединиться два атома галогена. Насыщение двойных связей представляет собой равновесную реакцию. Скорость насыщения двойных связей кислот галогенами зависит от числа и места расположения двойных связей. Сопряженные двойные связи насыщаются галогенами труднее, чем изолированные.
Действие галогенводородов. По месту двойных связей в ненасыщенных жирных кислотах также способны присоединяться галогенводороды. Скорость реакции зависит от состава галогенводорода, состава и структуры ненасыщенной кислоты, при этом насыщение двойных связей галогенводородами происходит менее активно, чем галогенамии.
Присоединение водорода по месту двойных связей в ненасыщенных кислотах происходит в присутствии катализатора. Реакция протекает таким образом, что каждая двойная связь присоединяет одну молекулу водорода. В результате этой реакции ненасыщенные кислоты переходят в насыщенные. Процесс этот называется гидрогенизацией.
Ненасыщенные жирные кислоты ряда СnН2n-2О2 (кислоты с одной двойной связью) могут присоединять два атома водорода, превращаясь в насыщенные кислоты. Большинство кислот этого ряда имеют двойную связь между 9 и 10 углеродными атомами. У высокомолекулярных кислот, начиная с эруковой С22Н42О2, двойная связь находится не у девятого и десятого углеродных атомов, а в другом месте. Кислоты этого ряда в спирте растворяются лучше, чем насыщенные кислоты с тем же числом углеродных атомов.
Капринолеиновая кислота [С10Н18О2] имеет два изомера с положением двойных связей у 9-10 и 4-3 углеродных атомов. Входит в состав коровьего масла (около 0,2%), а также в незначительных количествах содержится в спермацетовом жире и некоторых растительные маслах.
Лауринолеиновая кислота [С12Н22О2] имеет три изомера с положением двойных связей между 9 и 10; 4 и 5 и 5 и 6 углеродными атомами. Входит в состав спермацетового жира, коровьего масла и некоторых растительных масел.
Миристолеиновая кислота [С14Н26О2] имеет пять изомеров. В небольших количествах входит в состав говяжьего и свиного жира, коровьего масла, кашалотового жира (полостного и подкожного), а также многих жиров морских животных.
Пальмитолеиновая
кислота
[С16Н30О2]
довольно широко распространена в природе
и входит в состав многих животных и
растительных жиров. Значительное
количество этой кислоты содержат жиры
рыб и морских животных. Так, в жирах
морских животных ее содержится 15-20%, а
в туловищном кашалотовом жире – до 27%.
В растительных маслах содержание
пальмитолеиновой кислоты не превышает
1%.
![]()
Олеиновая кислота [С18Н26О2] присутствует почти во всех жирах как растительного, так и животного происхождения. В чистом виде представляет собой жидкость без цвета и запаха, на воздухе и на свету со временем темнеет. При обычном давлении она перегоняется с разложением. Олеиновая кислота содержит 18 углеродных атомов в молекуле, имеет одну двойную связь, находящуюся между 9 и 10 углеродными атомами. Температура плавления 13,6-16,3°С. При насыщении водородом она переходит в стеариновую кислоту. Особенно богаты ею оливковое и миндальное масла (до 85%). Арахисовое содержит 52-63% олеиновой кислоты, льняное – 13-29%, конопляное – 6-17%. В животных жирах также содержится значительное количество олеиновой кислоты. Так, в говяжьем жире находится 43-45% этой кислоты, в костном жире – 50-59%, в конском сале – 55%, в свином жире до 51%.
Кислоты ряда СnН2n-4О2 (диеновые, кислоты с двумя двойными связями) в природных жирах представлены в основном линолевой кислотой, которая в большом количестве содержится в жидких растительных маслах. Кислоты с двумя двойными связями в небольших количествах обнаружены также в жирах наземных, морских животных и рыб.
Линолевая кислота (С18Н32О2) – светло-желтая маслянистая жидкость, нерастворимая в воде, но хорошо растворимая во многих органических растворителях. Температура плавления линолевой кислоты составляет -5°С. В натуральных жирах линолевая кислота находится в виде цис-изомера. Она имеет неразветвленную цепь углеродных атомов и две изолированные двойные связи, одна из которых расположена между 9 и 10, а вторая между 12 и 13 углеродными атомами. Линолевая кислота окисляется кислородом воздуха легче, чем олеиновая.
Содержание в растительных маслах и животных жирах (%): кокосового масла 1,5-2,6; касторового 2,0-3,0; кориандрового 7,0-7,5; горчичного 14,5-20,0; льняного 15,0-30,0; хлопкового 40,0-45,0; кукурузного 43,5-46,9; подсолнечного масла 46,0-60,0; соевого 52,0-65,0; конопляного 56,0-65,0; макового 58,0-65,0%; говяжьего жира 2,0-5,0; бараньего 3,0-4,0; свиного 3,0-8,0.
Кислоты ряда СnН2n-6О2 (триеновые – кислоты с тремя двойными связями) содержатся главным образом в жидких растительных маслах. Наличие этих кислот в маслах обусловливает их хорошую высыхаемость и образование устойчивых пленок. Важнейшими представителями этого ряда кислот, содержащихся в природных жирах, являются линоленовая и элеостеариновая.
Линоленовая кислота [С18Н30О2] – бесцветная маслянистая жидкость, на воздухе легко окисляется с полимеризацией и образованием пленок. Окисление значительно ускоряется при повышении температуры. В воде нерастворима, но хорошо растворяется в большинстве органических растворителей, температура плавления -11°С. Линоленовая кислота имеет нормальное строение и три изолированные двойные связи в цисконфигурациях.
В природных жирах линоленовая кислота является наиболее распространенной кислотой этого ряда. Встречается во многих жидких растительных маслах, особенно в высыхающих, в небольшом количестве входит в состав некоторых животных жиров. Содержание линоленовой кислоты в растительных маслах и животных жирах (%): горчичное –1-2; рапсовое – 1-2; соевое – 2-3; рыжиковое до 20; конопляное – 15-28; льняное – 41-60; говяжий жир – 0,2-0,6; свиной жир – до 0,8.
Элеостеариновая кислота (C18H30O2) имеет несколько пространственных изомеров. Один из них α-изомер с положением двойной связи у 9, 11, 13 углеродных атомов, имеющий цис-транс-транс-конфигурацию, содержится в китайском тунговом масле в количестве 66-72%. Тунговое масло относится к хорошо высыхающим маслам. Элеостеариновая кислота имеет три сопряженные двойные связи.
Кислота легко окисляется и хорошо растворяется в органических растворителях, имеет температуру плавления 48°С.
Другой пространственный изомер – β-элеостеариновая кислота, имеющая транс-транс-транс-конфигурацию. Этот изомер образуется при действии изомеризующих агентов на α-элеостеариновую кислоту. Температура плавления этого изомера 71°С.
В природных жирах кислоты ряда СnН2n-8О2 (тетраеновые кислоты с 4 двойными связями) встречаются редко, в небольших количествах. Сопряженные этиленовые связи приводят к увеличению реакционной способности жирных кислот. Такие кислоты окисляются и полимеризуются быстрее, чем соответствующие кислоты с изолированными двойными связями. Основным представителем является арахидоновая кислота.
Арахидоновая кислота (С20Н32О2) – светлая жидкость, имеет низкую температуру плавления (-49,5°С), легко окисляется кислородом воздуха. По структуре арахидоновая кислота представляет собой соединение с четырьмя изолированными двойными связями при 5, 8, 11, 14 углеродных атомах. При гидрогенизации превращается в арахиновую кислоту.
Входит в небольших количествах в состав липидов мозга, печени, крови и жира животных. В фосфатидах животного происхождения ее содержание – до 20%. В растениях арахидоновая кислота не найдена.
Представители кислот ряда СnН2n-10О2 (пентаеновые, кислоты с пятью двойными связями) находятся в жирах рыб и морских животных. Они недостаточно изучены вследствие сложности состава и трудности выделения отдельных представителей из смеси кислот в чистом виде. Наиболее распространенной кислотой этого ряда является клупанодоновая (докозапентаеновая С22Н34О2) имеет пять изолированных двойных связей, находящихся у 4, 8, 12, 15, 19 углеродных атомов в цепи. Клупанодоновая кислота – желтоватая густая жидкость с характерным неприятным запахом и температурой плавления -78°С, при гидрогенизации переходит в бегеновую кислоту.
Входит в состав почти всех жиров морских животных и рыб. Впервые была выделена из жира японских сардин, в состав которого входит в количестве до 15%.
3. Насыщенные (предельные) гидроксикислоты имеют общую формулу СnН2nО3 и входят в состав шерстяного жира и растительных восков. Одним из представителей этого ряда является гидроксистеариновая кислота С18Н36О3.
4. Ненасыщенные (непредельные) гидроксикислоты с одной двойной связью ряда (СnН2n-2О3) характеризуются присутствием в молекуле одной двойной связи и спиртовой группы -ОН. В природных жирах ненасыщенные гидроксикислоты встречаются редко и в небольших количествах.
Рицинолевая кислота (С18Н34О3) входит в состав глицеридов касторового масла в количестве 80-90%, существует в трех полиморфных модификациях с температурой плавления 5; 7,7 и 16°С. При действии оксидов азота рицинолевая кислота изомеризуется в транс-изомер – рицинэлаидиновую кислоту с температурой плавления 52 0С.
5. Двухосновные насыщенные (предельные) кислоты имеют общую формулу СnH2n(COOH)2.
Одним из представителей является японская кислота С20Н40(СООН)2, которая содержится в японском воске.
6. Циклические кислоты имеют общую формулу CnH2n-4O2. Самым известным представителем является чальмугровая кислота С18Н32О2, содержащаяся в маслах некоторых тропических растений. Температура плавления 68,5 0С.
Глицериды – сложные эфиры глицерина и жирных кислот, в общем виде обозначаются формулой
где R1, R2, R3 - радикалы жирных кислот.
В зависимости от того, какое количество гидроксильных групп глицерина будет этерифицировано, различают моно-, ди- и триглицериды. В моноглицеридах имеются одна эфирная группа и две свободные гидроксильные группы, в диглицеридах – две эфирные группы и одна свободная гидроксильная группа, в триглицеридах – три эфирные группы.
Формулы этих глицеридов:
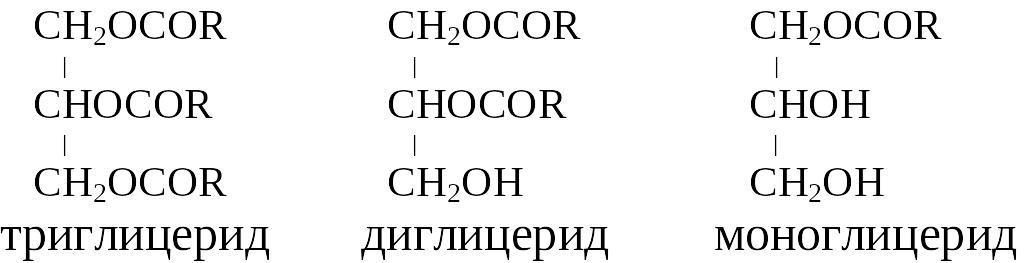
Триглицериды бывают однокислотные и разнокислотные.
В состав однокислотных триглицеридов входит одна какая-либо кислота:
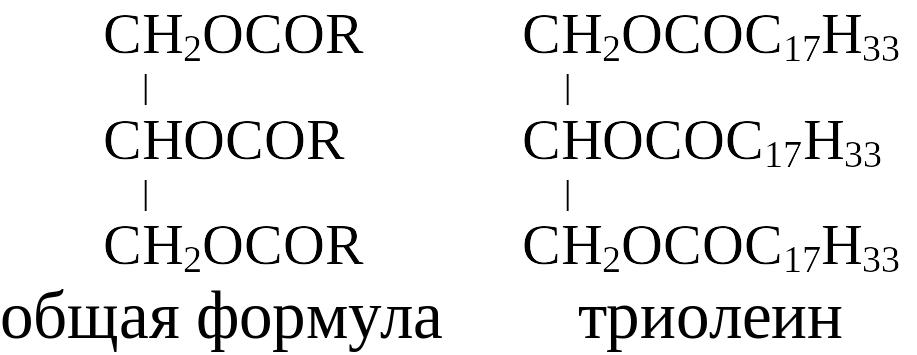
Разнокислотные триглицериды построены при участии двух или трех различных кислот. Например, двухкислотный триглицерид:
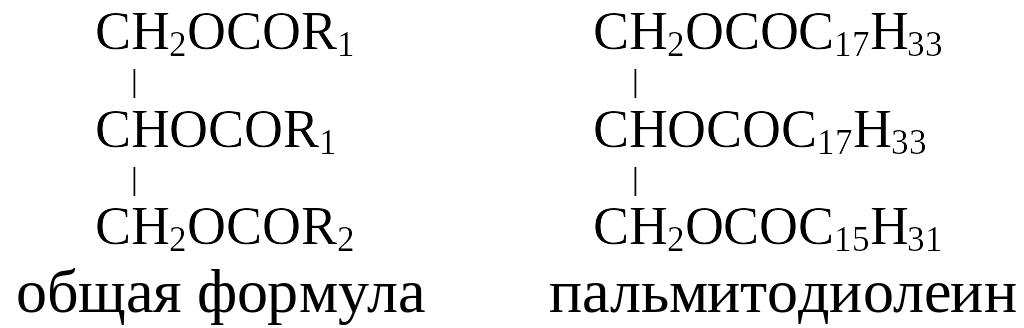
Трехкислотный триглицерид:
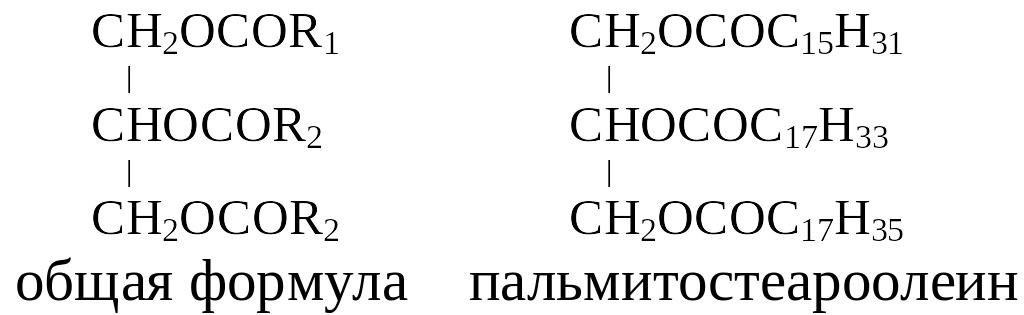
Изомерия глицеридов обусловливается различным расположением жирнокислотных остатков в молекуле, а также различием самих жирнокислотных остатков. Чтобы различить изомерные формы глицеридов, углеродные атомы глицерина обозначают либо буквами греческого алфавита, либо цифрами следующим образом:
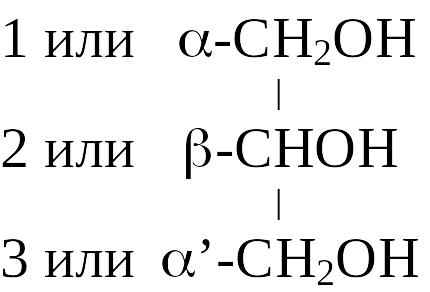
Рассмотрим возможные изомеры глицеридов.
1. Моноглицериды могут быть в виде двух изомеров:
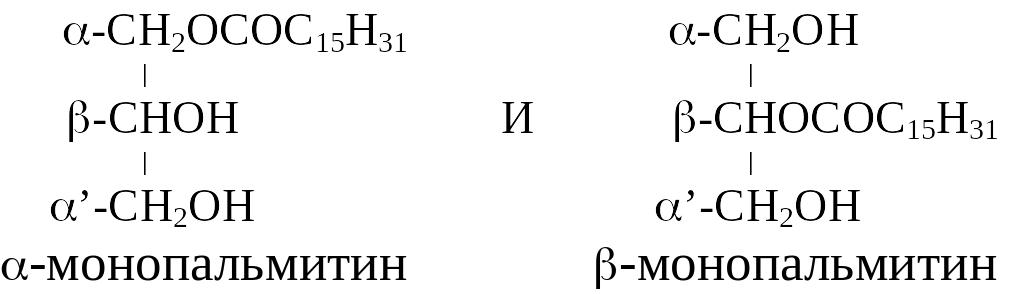
2. Диглицериды бывают однокислотные и разнокислотные, т. е. двухкислотные.
Однокислотные диглицериды могут быть в виде только двух изомеров:
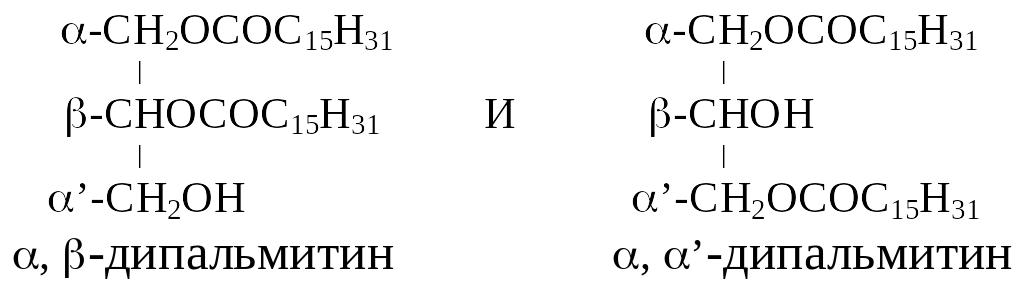
Двухкислотные диглицериды - в виде трех изомеров:

3. Триглицериды бывают однокислотные, двухкислотные и трех-кислотные.
Однокислотные триглицериды изомеров не образуют:
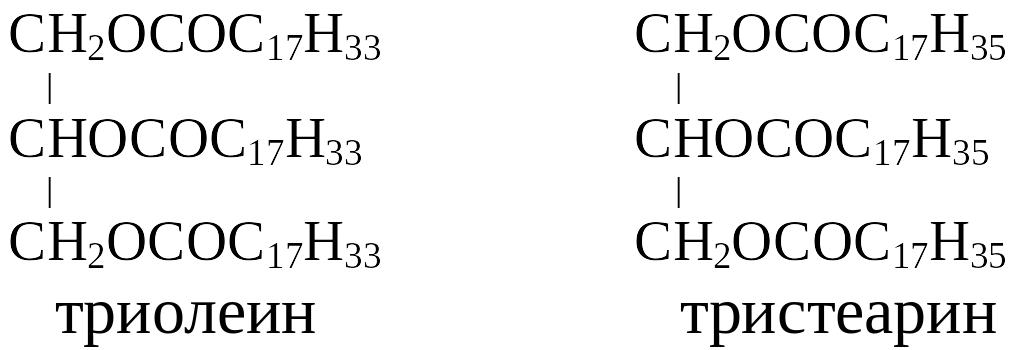
Двухкислотные триглицериды могут существовать в виде двух изомеров:

Трехкислотные триглицериды могут иметь три изомера. Для наглядности представим их формулами в общем виде:
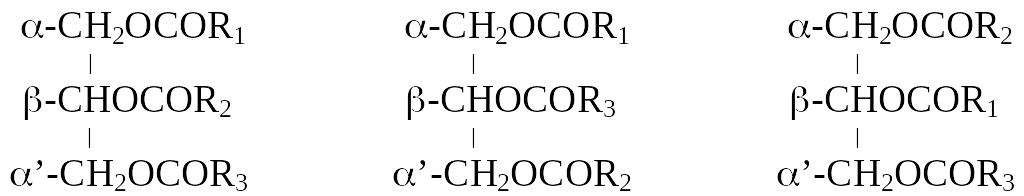
Натуральные растительные и животные жиры и масла представляют собой сложные смеси разнокислотных триглицеридов. Однокислотные триглицериды в наиболее значительном количестве встречаются в тех жирах, в которых какая-либо кислота является специфической и поэтому по содержанию намного превосходит остальные. Так, в касторовом масле содержится более 80% рицинолевой кислоты и, соответственно, в значительном количестве находятся триглицериды рицинолевой кислоты.
Все многообразие природных масел и жиров определяется различным сочетанием небольшого количества жирных кислот. В большинстве жиров содержится по 5-8 кислот, а число глицеридов во много раз больше. Так, в жирах с пятью жирными кислотами число глицеридов (с учетом позиционных изомеров) составляет 75.
Химически чистые триглицериды бесцветны, не имеют ни вкуса, ни запаха. Цветность, запах и вкусовые свойства масел и жиров обусловливаются присутствием в них веществ, сопутствующих триглицеридам, красящих веществ (пигментов), углеводородов, алифатических спиртов, фосфатидов и т.д.
Физические и химические свойства триглицеридов зависят от их химической природы (природы сложных эфиров), характера и свойств жирных кислот, входящих в состав молекулы, а также от расположения радикалов жирных кислот в молекуле триглицерида.
