
- •Тверской государственный технический университет
- •Е.А. Панкратов, н.Ю. Старовойтова
- •Химия и физика полимеров
- •Часть 1
- •Химия и физика полимеров
- •Часть I
- •Учебное пособие
- •170026, Г. Тверь, наб. А. Никитина, 22
- •Список условных сокращений
- •Введение в специальность
- •Основные понятия и определения
- •1.2. Молекулярная масса и молекулярно-массовое распределение
- •1.3. Важнейшие свойства полимерных веществ
- •1.4. Классификация полимеров
- •1.5. Номенклатура полимеров
- •Основные принципы номенклатуры регулярных линейных однотяжных органических полимеров
- •Основные принципы номенклатуры сополимеров
- •2. Синтез полимеров: поликонденсация
- •Основы теории поликонденсации
- •Характеристика процесса
- •Функциональность мономера
- •Классификация поликонденсационных процессов
- •Гомо- и гетерополиконденсация
- •Типы химических реакций, используемых при поликонденсации
- •И типы полимеров, образующихся при поликонденсации
- •Возможность образования низкомолекулярных гетероциклических соединений при поликонденсации
- •Равновесная поликонденсация
- •Особенности равновесной поликонденсации
- •Начало роста цепи
- •Процесс роста цепи
- •Остановка роста цепи
- •1. Наличие в системе выделяющегося низкомолекулярного продукта реакции и установление равновесия между прямой и обратной реакциями.
- •Механизмы реакций равновесной поликонденсации
- •Кинетика равновесной поликонденсации
- •Неравновесная поликонденсация
- •Особенности неравновесной поликонденсации
- •Кинетика неравновесной поликонденсации
- •Способы проведения поликонденсации
- •Поликонденсация в твердой фазе, расплаве, растворе
- •Поликонденсация в эмульсии
- •Межфазная поликонденсация
- •Трехмерная поликонденсация
- •Совместная поликонденсация
- •3. Синтез полимеров: полимеризация
- •3.1. Основы теории полимеризации
- •Характеристика процесса
- •Цепные и ступенчатые реакции полимеризации
- •Термодинамика полимеризации
- •Миграционная полимеризация
- •3.3. Радикальная полимеризация
- •3.3.1. Характеристика радикальных процессов
- •Мономеры
- •Инициирование
- •Рост цепи
- •Обрыв цепи
- •Кинетический анализ радикальной полимеризации Вывод общего кинетического уравнения радикальной полимеризации
- •Типичная кинетическая кривая радикальной полимеризации
- •Ингибиторы и замедлители радикальной полимеризации
- •Влияние различных факторов на скорость полимеризации и молекулярную массу полимера
- •Методы проведения полимеризации
- •Полимеризация в массе мономера
- •Полимеризация в растворителе
- •Полимеризация в суспензии
- •Эмульсионная полимеризация
- •Радикальная сополимеризация
- •Характеристика процесса
- •Уравнение состава сополимера
- •Константы сополимеризации, их физический смысл
- •Ионная полимеризация
- •Характеристика ионных процессов
- •Активные центры ионной полимеризации
- •Катионная полимеризация
- •Инициаторы катионной полимеризации
- •Реакционная способность мономеров
- •Механизм катионной полимеризации
- •Анионная полимеризация
- •Механизм действия анионных инициаторов. В зависимости от типа взаимодействий можно выделить 2 механизма инициирования анионной поликонденсации.
- •Ионно-координационная полимеризация
- •Алфиновые катализаторы
- •Катализаторы Циглера-Натта
- •Оксидные катализаторы
- •Ионная сополимеризация
- •4. Химические превращения
- •Особенности химических реакций полимеров
- •Полимераналогичные превращения
- •Реакции, приводящие к увеличению молекулярной массы
- •Реакции, приводящие к уменьшению молекулярной массы
- •Старение полимеров
- •Библиографический список
Равновесная поликонденсация
Особенности равновесной поликонденсации
Отличительные черты равновесной поликонденсации (ПК):
обратимый характер всех протекающих реакций;
деструктивные процессы, вызываемые простейшими продуктами поликонденсации;
малые значения
константы равновесия (![]() );
);
константы скорости порядка 10-7-10-3 .
Константа равновесия
![]() ,
,
где
![]() – скорость прямой реакции;
– скорость прямой реакции;
![]() –
скорость обратной реакции.
–
скорость обратной реакции.
Примеры равновесной поликонденсации: поликонденсация дикарбоновых кислот с гликолями с образованием полиэфиров (полиэтерификация); поликонденсация дикарбоновых кислот с диаминами с образованием полиамидов (полиамидирование).
Выделяют три стадии равновесной поликонденсации:
начало роста цепи макромолекулы;
процесс роста цепи макромолекулы (рост цепи);
остановка роста цепи макромолекулы (обрыв цепи).
Начало роста цепи
Взаимодействуют два реакционных центра молекул исходных мономеров:
x-R-x
+ y-R-y
![]() x-R-x●y-R'-y → x-R-z-R'-y + a
x-R-x●y-R'-y → x-R-z-R'-y + a
Реакционные центры могут быть в мономерах до начала реакции (например, получение полиэфиров взаимодействием дикарбоновых кислот с гликолями) или создаваться в процессе образования полимеров (например, получение полиэфиров взаимодействием ангидридов кислот и гликолей).
Процесс роста цепи
Взаимодействуют реакционные центры мономеров, олигомеров и полимеров:
x-[-R-z-R'-]n-y + x-[-R-z-R'-]m-y → x-[-R-z-R'-]n+m-y + a
Процесс носит вероятностный характер, что является одной из причин широкого молекулярно-массового распределения полимеров.
В течение процесса резко уменьшается количество реакционных центров, поэтому молекулярная масса получаемого полимера зависит от времени проведения процесса поликонденсации. Эта зависимость выражается уравнением Карозерса (8).
Равновесная поликонденсация обычно протекает при повышенных температурах и часто в присутствии катализаторов. В таких условиях образующиеся молекулы находятся в активном состоянии, поэтому на стадии роста постоянно протекают обратные реакции (взаимодействие растущих цепей с низкомолекулярными продуктами реакции, с исходными мономерами и монофункциональными примесями). Такие реакции называются реакциями деструкции. Наиболее распространенные реакции деструкции – гидролиз, ацидолиз, аминолиз, алкоголиз. Приведем примеры этих реакций.
Гидролиз

Ацидолиз

Аминолиз (при полиамидировании)
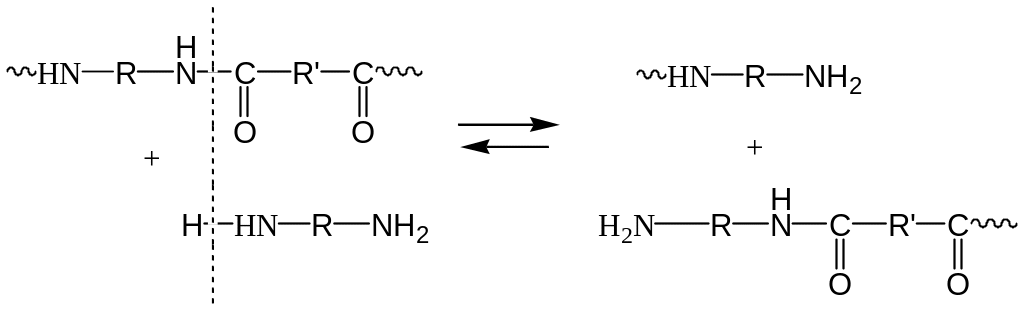
Алкоголиз (при полиэтерификации)

В результате этих реакций суммарное число амидных и эфирных группировок (z-группировок), а также свободных функциональных групп не изменяется.
В первую очередь деструкции подвергаются наиболее длинные макромолекулы. Поэтому, с одной стороны, молекулярная масса полимера всегда оказывается ниже расчетной, с другой – уменьшается разброс по молекулярным массам.
Другой особенностью стадии роста цепи является обилие обменных реакций.
Обменные реакции проходят:
за счет химически активных концевых групп полимерных цепей:
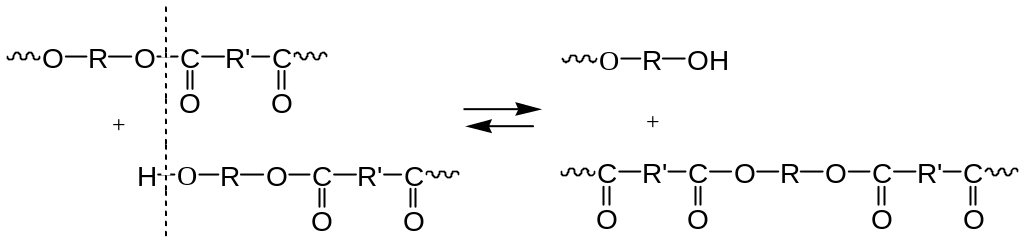
за счет взаимодействия полимерных цепей по промежуточным звеньям:
-[-HN-R-NHCO-R’-CO-]m-[-HN-R-NHCO-R’-CO-]n +
+ -[-HN-R-NHCO-R’-CO-]k-[-HN-R-NHCO-R’-CO-]l
-[-HN-R-NHCO-R’-CO-]m-[-HN-R-NHCO-R’-CO-]l +
+ -[-HN-R-NHCO-R’-CO-]k-[-HN-R-NHCO-R’-CO-]n
Доля обменных реакций повышается с ростом макромолекул. Межцепной обмен не изменяет среднюю молекулярную массу, но изменяет фракционный состав полимера.
