
- •Тверской государственный технический университет
- •Е.А. Панкратов, н.Ю. Старовойтова
- •Химия и физика полимеров
- •Часть 1
- •Химия и физика полимеров
- •Часть I
- •Учебное пособие
- •170026, Г. Тверь, наб. А. Никитина, 22
- •Список условных сокращений
- •Введение в специальность
- •Основные понятия и определения
- •1.2. Молекулярная масса и молекулярно-массовое распределение
- •1.3. Важнейшие свойства полимерных веществ
- •1.4. Классификация полимеров
- •1.5. Номенклатура полимеров
- •Основные принципы номенклатуры регулярных линейных однотяжных органических полимеров
- •Основные принципы номенклатуры сополимеров
- •2. Синтез полимеров: поликонденсация
- •Основы теории поликонденсации
- •Характеристика процесса
- •Функциональность мономера
- •Классификация поликонденсационных процессов
- •Гомо- и гетерополиконденсация
- •Типы химических реакций, используемых при поликонденсации
- •И типы полимеров, образующихся при поликонденсации
- •Возможность образования низкомолекулярных гетероциклических соединений при поликонденсации
- •Равновесная поликонденсация
- •Особенности равновесной поликонденсации
- •Начало роста цепи
- •Процесс роста цепи
- •Остановка роста цепи
- •1. Наличие в системе выделяющегося низкомолекулярного продукта реакции и установление равновесия между прямой и обратной реакциями.
- •Механизмы реакций равновесной поликонденсации
- •Кинетика равновесной поликонденсации
- •Неравновесная поликонденсация
- •Особенности неравновесной поликонденсации
- •Кинетика неравновесной поликонденсации
- •Способы проведения поликонденсации
- •Поликонденсация в твердой фазе, расплаве, растворе
- •Поликонденсация в эмульсии
- •Межфазная поликонденсация
- •Трехмерная поликонденсация
- •Совместная поликонденсация
- •3. Синтез полимеров: полимеризация
- •3.1. Основы теории полимеризации
- •Характеристика процесса
- •Цепные и ступенчатые реакции полимеризации
- •Термодинамика полимеризации
- •Миграционная полимеризация
- •3.3. Радикальная полимеризация
- •3.3.1. Характеристика радикальных процессов
- •Мономеры
- •Инициирование
- •Рост цепи
- •Обрыв цепи
- •Кинетический анализ радикальной полимеризации Вывод общего кинетического уравнения радикальной полимеризации
- •Типичная кинетическая кривая радикальной полимеризации
- •Ингибиторы и замедлители радикальной полимеризации
- •Влияние различных факторов на скорость полимеризации и молекулярную массу полимера
- •Методы проведения полимеризации
- •Полимеризация в массе мономера
- •Полимеризация в растворителе
- •Полимеризация в суспензии
- •Эмульсионная полимеризация
- •Радикальная сополимеризация
- •Характеристика процесса
- •Уравнение состава сополимера
- •Константы сополимеризации, их физический смысл
- •Ионная полимеризация
- •Характеристика ионных процессов
- •Активные центры ионной полимеризации
- •Катионная полимеризация
- •Инициаторы катионной полимеризации
- •Реакционная способность мономеров
- •Механизм катионной полимеризации
- •Анионная полимеризация
- •Механизм действия анионных инициаторов. В зависимости от типа взаимодействий можно выделить 2 механизма инициирования анионной поликонденсации.
- •Ионно-координационная полимеризация
- •Алфиновые катализаторы
- •Катализаторы Циглера-Натта
- •Оксидные катализаторы
- •Ионная сополимеризация
- •4. Химические превращения
- •Особенности химических реакций полимеров
- •Полимераналогичные превращения
- •Реакции, приводящие к увеличению молекулярной массы
- •Реакции, приводящие к уменьшению молекулярной массы
- •Старение полимеров
- •Библиографический список
Ионно-координационная полимеризация
Координационным называется процесс присоединения мономеров к активному центру, сопровождающийся образованием комплексов между активным центром и мономером.
Наиболее важный результат координации – получение полимеров, имеющих регулярную пространственную структуру, т.е. стереорегулирование. Катализаторы, вызывающие стереорегулирование в процессе присоединения мономерных звеньев, называются стереоспецифическими. Наиболее изученными являются сложные моно- и бимолекулярные комплексы металлов переменной валентности.
Стереоспецифическая полимеризация олефиновых и диолефиновых мономеров на различных катализаторах идет однотипно. Главную роль в процессе играет переходный металл, который может координировать мономер. Электроноакцепторные соединения, повышая положительный заряд на атоме переходного металла, способствуют координации мономера.
Образование активного центра осуществляется на базе связи углерод - переходный металл, которая возникает на той или иной стадии взаимодействия компонентов катализатора или уже существует в исходных продуктах. Это значит, что истинными катализаторами являются органические соединения переходных металлов либо в свободном состоянии, либо в виде комплексов или поверхностных соединений, встроенных в кристаллическую решетку твердого катализатора.
Наиболее характерными каталитическими системами стереоспецифического действия являются следующие.
Алфиновые катализаторы
Открыты Мартоном в 1947 году. Представляют собой сложный комплекс, образующийся в результате ряда последовательных реакций:
взаимодействие хлористого алкила с натрием при 10 25 С:
2 Na + R-Cl NaClR-Na
обработка образовавшегося комплекса изопропиловым спиртом:

реакция образования комплекса с участием олефина:
![]()
Предположительная структура активного центра полимеризации:

Катализатор является гетерогенным по отношению к мономеру и представляет собой комплекс, адсорбированный на NaCl.
Алфиновые катализаторы обладают высокой селективностью, т.е. действуют избирательно. Особенно активно полимеризуется бутадиен, менее активно – изопрен и стирол. Сведения о кинетике и механизме процесса отсутствуют. С открытием катализаторов Циглера-Натта потеряли свое значение, однако найденные позднее пути регулирования молекулярной массы образующегося полимера вновь возродили к ним интерес. В настоящее время алфиновые катализаторы используются для получения сополимеров бутадиена.
Катализаторы Циглера-Натта
Открыты в 1954 г. К. Циглером и затем детально исследованы Дж. Натта. Представляют собой биметаллические комплексы сложной структуры.
Наиболее характерными среди них являются продукты взаимодействия алкилов или замещенных хлоридов алюминия с галогенидами металлов переменной валентности IV-VIII групп Периодической системы.
Для большинства компонентов при образовании каталитических систем наблюдается реакция, в результате которой изменяется валентное состояние атома металла, что и приводит к образованию высокоактивного стереоспецифического катализатора. Этот процесс зависит как от строения металла, так и от природы лиганда, а также от среды, температуры и является достаточно сложным.
Пример
Рассмотрим катализатор состава ТiCl4 – Al(C2H5)3. При смешении компонентов в зависимости от температуры происходит несколько реакций:

Образовавшийся биметаллический комплекс (IV), содержащий восстановленный атом Ti, является основой формирования активного центра. Предполагаются следующие этапы координационно-ионной полимеризации: образование комплекса мономера с катализатором и внедрение мономера. При этом мономер выступает в роли донора -электронов, а переходный металл катализатора является акцептором. За счет координации с донором образуется -комплекс, возникновение которого приводит к ослаблению связи Ti----CH2 в катализаторе. Внедрение мономера по этой связи облегчается:
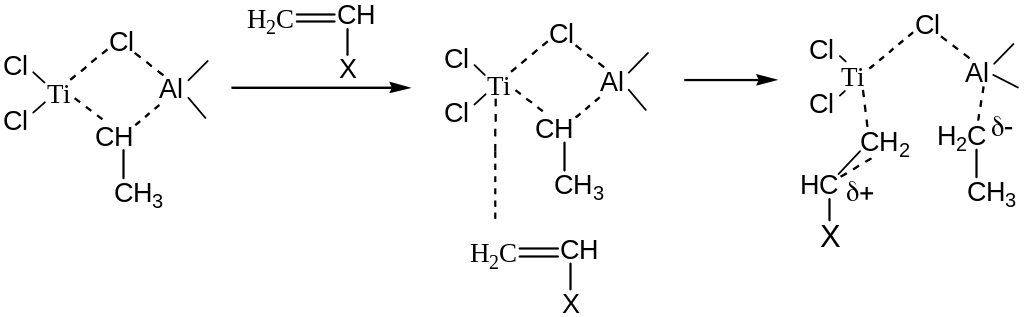 После
разделения зарядов в структуру
каталитического комплекса входит
молекула мономера с образованием нового
шестичленного цикла в комплексе
катализатора с последующей перестройкой
снова в четырехчленный цикл:
После
разделения зарядов в структуру
каталитического комплекса входит
молекула мономера с образованием нового
шестичленного цикла в комплексе
катализатора с последующей перестройкой
снова в четырехчленный цикл:

Этот механизм согласуется с экспериментальными данными, из которых следует, что наиболее склонны к полимеризации мономеры с повышенной электронной плотностью на двойной связи. Если оценивать распределение зарядов, то растущая цепь несет частичный отрицательный заряд. Скорость внедрения существенно зависит от стерического фактора, это объясняет различия активности разных мономеров. Таким образом, в координационной полимеризации следует учитывать два фактора, от которых зависит активность мономера:
электронная плотность на двойной связи, определяющая скорость координации;
стерическая структура мономера, обеспечивающая наименьшую трудность внедрения мономера по связи металл – углерод.
Ограничение роста цепи осуществляется двумя способами:
перенос гидрид-иона с конца растущей цепи на противоион (переходный комплекс каталитического комплекса);
передача цепи на металлалкил (реакция обмена).
Передача цепи на мономер имеет меньшее значение. Кроме алкила металла в обрыве цепи могут принимать участие примеси, находящиеся в реакционной среде.
-аллильные комплексы переходых металлов
Катализаторы Циглера-Натта характеризуются крайне нестабильной -связью «переходный металл – углерод» (Ti-C). В качестве катализаторов ионной полимеризации можно использовать и -комплексы, в которых -связь металл – углерод является непрочной – -аллильные комплексы Ni, Co, Cr (в том числе, в комбинации с галогенидами металлов – AlCl3, TiCl4, VCl3). Общую формулу строения -аллильных комплексов можно представить в виде

Здесь X – галоген, Me – металл.
Такие комплексы получили наибольшее распространение для полимеризации диенов – они моделируют структуру активного центра растущей цепи. При этом можно получить две пространственные конфигурации (в зависимости от положения метильной группы относительно плоскости четырехчленного кольца комплекса):

Соответственно структура звеньев в полимере будет строго определенной: из син-конфигурации – транс-звено, из анти-конфигурации – цис-звено.
Инициирование происходит при взаимодействии стабильного -аллильного комплекса с мономером, при этом -связь катализатора превращается в -связь, а бутадиен координируется у атома металла. Далее под действием координированной молекулы связь металл – углерод ослабевает, и происходит внедрение молекулы с восстановлением четырехзвенного -аллильного комплекса. Схема инициирования:

Рост цепи происходит аналогично схеме полимеризации на катализаторах Циглера-Натта. Механизм полимеризации под действием -аллильных комплексов представляет собой последовательность актов координации мономера на комплексе, образования -связи и вхождения мономера в цепь с регенерацией -аллильного комплекса.
Схема роста цепи:

Если координация диена с атомом металла происходит по обеим двойным связям, то формируется цис-конфигурация цепи, если по одной, то преимущественно реализуется термодинамически более выгодная трансформа. Существенное влияние на строение цепи полидиена оказывает и природа лиганда Х в комплексе. Если лиганды представляют собой кислотные группы, т.е. сильно электроотрицательны, то металл в комплексе имеет большой положительный заряд. Это способствует образованию антиформы -комплекса и, соответственно, цис-1,4-структуры полидиена. Если лиганды – галогены, то их электроотрицательность меньше и, следовательно, меньше значение положительного заряда на атоме металла. С понижением электроотрицательности галогена (от хлора к иоду) растет доля транс-1,4-формы в полидиене (табл. 16).
Таблица 16. Содержание цис- и транс-звеньев в полибутадиене,
синтезированном на -аллилникельгалогенидах в бензольном
растворе [1]
Форма |
Содержание звеньев, % (в зависимости от природы галогена) |
||
Cl |
Br |
I |
|
1,4-цис |
89 |
46 |
0 |
1,4-транс |
7 |
53 |
97 |
1,2-звенья |
4 |
1 |
3 |
Ограничение роста цепи может происходить по механизму «живых» цепей. Также возможна передача цепи на мономер с регенерацией активного центра:

