
- •Тверской государственный технический университет
- •Е.А. Панкратов, н.Ю. Старовойтова
- •Химия и физика полимеров
- •Часть 1
- •Химия и физика полимеров
- •Часть I
- •Учебное пособие
- •170026, Г. Тверь, наб. А. Никитина, 22
- •Список условных сокращений
- •Введение в специальность
- •Основные понятия и определения
- •1.2. Молекулярная масса и молекулярно-массовое распределение
- •1.3. Важнейшие свойства полимерных веществ
- •1.4. Классификация полимеров
- •1.5. Номенклатура полимеров
- •Основные принципы номенклатуры регулярных линейных однотяжных органических полимеров
- •Основные принципы номенклатуры сополимеров
- •2. Синтез полимеров: поликонденсация
- •Основы теории поликонденсации
- •Характеристика процесса
- •Функциональность мономера
- •Классификация поликонденсационных процессов
- •Гомо- и гетерополиконденсация
- •Типы химических реакций, используемых при поликонденсации
- •И типы полимеров, образующихся при поликонденсации
- •Возможность образования низкомолекулярных гетероциклических соединений при поликонденсации
- •Равновесная поликонденсация
- •Особенности равновесной поликонденсации
- •Начало роста цепи
- •Процесс роста цепи
- •Остановка роста цепи
- •1. Наличие в системе выделяющегося низкомолекулярного продукта реакции и установление равновесия между прямой и обратной реакциями.
- •Механизмы реакций равновесной поликонденсации
- •Кинетика равновесной поликонденсации
- •Неравновесная поликонденсация
- •Особенности неравновесной поликонденсации
- •Кинетика неравновесной поликонденсации
- •Способы проведения поликонденсации
- •Поликонденсация в твердой фазе, расплаве, растворе
- •Поликонденсация в эмульсии
- •Межфазная поликонденсация
- •Трехмерная поликонденсация
- •Совместная поликонденсация
- •3. Синтез полимеров: полимеризация
- •3.1. Основы теории полимеризации
- •Характеристика процесса
- •Цепные и ступенчатые реакции полимеризации
- •Термодинамика полимеризации
- •Миграционная полимеризация
- •3.3. Радикальная полимеризация
- •3.3.1. Характеристика радикальных процессов
- •Мономеры
- •Инициирование
- •Рост цепи
- •Обрыв цепи
- •Кинетический анализ радикальной полимеризации Вывод общего кинетического уравнения радикальной полимеризации
- •Типичная кинетическая кривая радикальной полимеризации
- •Ингибиторы и замедлители радикальной полимеризации
- •Влияние различных факторов на скорость полимеризации и молекулярную массу полимера
- •Методы проведения полимеризации
- •Полимеризация в массе мономера
- •Полимеризация в растворителе
- •Полимеризация в суспензии
- •Эмульсионная полимеризация
- •Радикальная сополимеризация
- •Характеристика процесса
- •Уравнение состава сополимера
- •Константы сополимеризации, их физический смысл
- •Ионная полимеризация
- •Характеристика ионных процессов
- •Активные центры ионной полимеризации
- •Катионная полимеризация
- •Инициаторы катионной полимеризации
- •Реакционная способность мономеров
- •Механизм катионной полимеризации
- •Анионная полимеризация
- •Механизм действия анионных инициаторов. В зависимости от типа взаимодействий можно выделить 2 механизма инициирования анионной поликонденсации.
- •Ионно-координационная полимеризация
- •Алфиновые катализаторы
- •Катализаторы Циглера-Натта
- •Оксидные катализаторы
- •Ионная сополимеризация
- •4. Химические превращения
- •Особенности химических реакций полимеров
- •Полимераналогичные превращения
- •Реакции, приводящие к увеличению молекулярной массы
- •Реакции, приводящие к уменьшению молекулярной массы
- •Старение полимеров
- •Библиографический список
Рост цепи
Рост цепи – основная стадия радикальной полимеризации, ответственная за образование макромолекулы. Она заключается в последовательном присоединении молекул мономера к активному центру, причем строение центра как свободнорадикальной частицы сохраняется.
В общем виде реакция роста цепи может быть представлена следующим образом:
![]()
![]()
…………………………….
![]()
Если принять допущение, что реакционная способность растущего радикала не зависит от его длины, то скорость роста цепи подчиняется выражению
![]() ,
,
где
![]() – константа скорости реакции роста
цепи;
– константа скорости реакции роста
цепи;
![]() – концентрация растущих радикалов;
– концентрация растущих радикалов;
![]() – концентрация мономера.
– концентрация мономера.
Рост цепи – быстрая реакция, ~ 104 л/мольс. Энергия активации низкая, 20-35 кДж/моль (это в несколько раз ниже энергии активации инициирования пероксидными инициаторами).
Для винильных мономеров возможны два способа присоединения радикала к двойной связи: к замещенному и к незамещенному атому углерода. В результате образуются полимеры, звенья в которых соединяются по типу «голова к хвосту» или «голова к голове» («хвост к хвосту»):
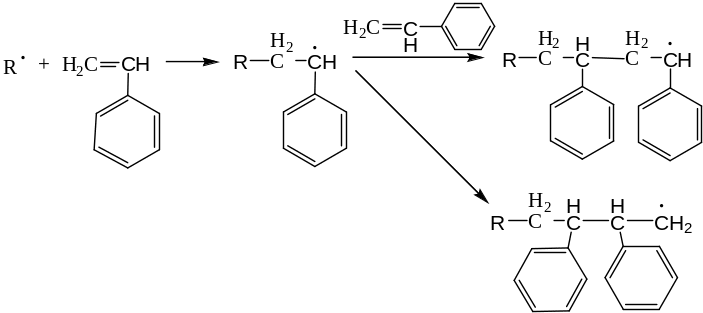 Расчеты
теплот реакции показывают, что
преимущественно происходит присоединение
по типу «голова к хвосту».
Расчеты
теплот реакции показывают, что
преимущественно происходит присоединение
по типу «голова к хвосту».
Обрыв цепи
Обрыв цепи – это реакция гибели активных центров. Истинный обрыв цепи приводит к обрыву материальной и кинетической цепи. Эта реакция может произойти на любой стадии полимеризации, что приводит к получению макромолекул различной длины.
Различают 2 способа обрыва цепи.
Рекомбинация – соединение растущих макрорадикалов друг с другом с образованием валентной связи. Реакция описывается схемой
![]() ,
,
где
![]() – константа скорости реакции обрыва
рекомбинацией.
– константа скорости реакции обрыва
рекомбинацией.
Скорость реакции обрыва рекомбинацией описывается уравнением
![]() ,
,
где
![]() – концентрация растущих макрорадикалов.
– концентрация растущих макрорадикалов.
Диспропорционирование – межмолекулярная перегруппировка посредством передачи атома водорода от одного макрорадикала к другому. В результате реакции образуются две макромолекулы, одна из которых имеет на конце двойную связь:
![]() ,
,
где
![]() – константа скорости реакции обрыва
диспропорционированием.
– константа скорости реакции обрыва
диспропорционированием.
Скорость реакции обрыва диспропорционированием описывается уравнением
![]() ,
,
где – концентрация растущих макрорадикалов.
При полимеризации большинства мономеров возможен обрыв по обоим механизмам, причем чем выше реакционная способность растущего радикала, тем больше доля реакции обрыва диспропорционированием.
В общем случае
![]() ,
,
тогда
![]() .
.
Уравнение характеризует скорость реакции обрыва цепи вследствие бимолекулярного обрыва.
Обрыв цепи протекает со скоростью, на несколько порядков более высокой, чем скорость роста цепи. Энергия активации обрыва цепи близка нулю.
Обрыв цепи часто сопровождается обрывом только материальной цепи при сохранении кинетической, т.е. с сохранением свободнорадикального центра. Такие реакции называются реакциями передачи цепи.
Передача кинетической цепи – бимолекулярная реакция, в которой участвуют макрорадикал и какой-либо из компонентов реакционной смеси. Ее можно отнести к реакциям замещения. Наиболее активны в передаче цепи вещества, содержащие подвижные атомы водорода или галогена. Обычно реакция передачи цепи сопровождается образованием неактивной («мертвой») макромолекулы и новой частицы, содержащей неспаренный электрон:
![]()
![]() .
.
В зависимости от
реакционной способности образующегося
радикала
![]() скорость
реакции может увеличиваться, уменьшаться
или оставаться постоянной. В случае
образования стабильных радикалов
полимеризация может прекратиться
совсем, в этом случае происходит
ингибирование.
скорость
реакции может увеличиваться, уменьшаться
или оставаться постоянной. В случае
образования стабильных радикалов
полимеризация может прекратиться
совсем, в этом случае происходит
ингибирование.
Различают следующие типы реакций передачи цепи:
Не приводящие к ингибированию – реакции передачи цепи на мономер, инициатор, полимер, растворитель.
Сопровождающиеся ингибированием – реакции, идущие в присутствии ингибиторов и замедлителей.
Все реакции передачи цепи, за исключением передачи цепи на полимер, приводят к уменьшению молекулярной массы полимера.
Реакции передачи цепи используются для получения теломеров и для получения полимеров с заданной молекулярной массой.
Передача цепи
на мономер
– это взаимодействие макрорадикала
![]() с мономером M,
приводящее к образованию макромолекулы
с мономером M,
приводящее к образованию макромолекулы
![]() и новой свободнорадикальной частицы
из молекулы мономера
.
и новой свободнорадикальной частицы
из молекулы мономера
.
Передача цепи
на инициатор
– это взаимодействие макрорадикала
![]() с инициатором
с инициатором
![]() ,
в результате которого образуется
макромолекула
и новая свободнорадиальная частица из
молекулы инициатора
,
в результате которого образуется
макромолекула
и новая свободнорадиальная частица из
молекулы инициатора
![]() .
В такой реакции могут принимать участие
инициаторы, содержащие подвижный атом
водорода, например гидропероксиды.
.
В такой реакции могут принимать участие
инициаторы, содержащие подвижный атом
водорода, например гидропероксиды.
Передача цепи
на растворитель
– это взаимодействие макрорадикала
с растворителем
![]() ,
при котором происходит образование
полимера
и новой свободнорадикальной частицы
из молекулы растворителя
,
при котором происходит образование
полимера
и новой свободнорадикальной частицы
из молекулы растворителя
![]() .
.
Передача цепи
на полимер
– процесс взаимодействия макрорадикалов
с полимером
![]() ,
который приводит к образованию
свободнорадикальных центров на
полимерных молекулах
,
который приводит к образованию
свободнорадикальных центров на
полимерных молекулах
![]() .
.
Отношение константы скорости реакции передачи цепи к константе скорости реакции роста цепи называется константой передачи цепи.
Схемы реакций,
уравнения скорости передачи цепи и
констант передачи цепи даны в
табл. 10.
Здесь
![]() ,
,
![]() ,
,
![]() ,
,
![]() ,
,
![]() – концентрации макрорадикала, мономера,
инициатора, растворителя и полимера
соответственно;
– концентрации макрорадикала, мономера,
инициатора, растворителя и полимера
соответственно;
![]() ,
,
![]() ,
,
![]() ,
,
![]() – константы скорости реакций передачи
цепи на мономер, инициатор, растворитель
и полимер соответственно;
– константы скорости реакций передачи
цепи на мономер, инициатор, растворитель
и полимер соответственно;
![]() ,
,
![]() ,
,
![]() ,
,
![]() – скорости реакций передачи цепи на
мономер, инициатор, растворитель и
полимер соответственно;
– скорости реакций передачи цепи на
мономер, инициатор, растворитель и
полимер соответственно;
![]() ,
,
![]() ,
,
![]() – константы передачи цепи на мономер,
инициатор, растворитель соответственно.
– константы передачи цепи на мономер,
инициатор, растворитель соответственно.
Очевидно, что
реакция передачи цепи на мономер
конкурирует с реакцией роста цепи.
Образование полимера возможно в случае,
когда
![]() .
.
Таблица 10. Количественные характеристики различных способов
передачи цепи
Способ передачи цепи
|
Схема реакции
|
Уравнение скорости передачи цепи |
Константа передачи цепи |
На мономер |
|
|
|
На инициатор |
|
|
|
На растворитель |
|
|
|
На полимер |
|
|
------ |
Растворитель
легко вступает в реакции передачи цепи,
если его молекула содержит подвижные
атомы или группы атомов (как правило,
атомы водорода или галогена). К таким
растворителям относятся хлор- и
бромзамещенные углеводороды и
алкилзамещенные ароматические
соединения, в которых подвижен атом
водорода в алкильном радикале.
Растворители с высокими значениями
![]() называются регуляторами
цепи, они
являются активными переносчиками и
значительно снижают молекулярную массу
полимера. Наиболее высокие значения
наблюдаются
для СCl4,
СBr4
и меркаптанов. В табл. 11 приведены
константы передачи цепи на растворитель
для некоторых широко используемых
растворителей.
называются регуляторами
цепи, они
являются активными переносчиками и
значительно снижают молекулярную массу
полимера. Наиболее высокие значения
наблюдаются
для СCl4,
СBr4
и меркаптанов. В табл. 11 приведены
константы передачи цепи на растворитель
для некоторых широко используемых
растворителей.
Подбирая растворители и условия процесса, можно настолько повысить скорость реакции передачи цепи, что в результате получаются низкомолекулярные полимеры, концевые звенья которых содержат продукты распада молекул растворителя. Такой процесс называется теломеризацией, сами полимеры – теломерами, а агенты передачи цепи – телогентами.
Эти реакции используются в промышленности, т.к. позволяют получать соединения с активными функциональными концевыми группами.
Пример
nCH2=CH2![]() Cl-[-CH2-CH2-]n-CCl3 ,
n=215
Cl-[-CH2-CH2-]n-CCl3 ,
n=215
Передача цепи на полимер приводит к получению разветвления и используется для получения привитых сополимеров. Роль этой реакции повышается с увеличением конверсии мономера в полимер (т.е. в конце процесса) и с повышением температуры. Предельный случай передачи цепи на полимер – образование сшитых полимеров.
Количественное
определение константы передачи цепи
на полимер очень сложно. Флори предложил
уравнение, связывающее плотность
ветвления ρ
(число ветвлений на одну молекулу
мономера, вступившего в полимеризацию)
с константой передачи цепи на полимер
![]() и степенью завершенности реакции p
и степенью завершенности реакции p
![]() .
.
Таблица 11. Значения константы передачи цепи для некоторых растворителей
Растворитель |
Химическая формула |
104 при 60С, мономер - стирол |
Бензол |
С6Н6 |
0,023 |
Толуол |
С6Н6-СН3 |
0,125 |
Этилбензол |
С6Н6-С2Н5 |
0,67 |
Четыреххлористый углерод |
СCl4 |
90 |
Четырехбромистый углерод |
СBr4 |
22000 |
н-бутилмеркаптан |
С4Н9-S-H |
210000 |
