
- •Тверской государственный технический университет
- •Е.А. Панкратов, н.Ю. Старовойтова
- •Химия и физика полимеров
- •Часть 1
- •Химия и физика полимеров
- •Часть I
- •Учебное пособие
- •170026, Г. Тверь, наб. А. Никитина, 22
- •Список условных сокращений
- •Введение в специальность
- •Основные понятия и определения
- •1.2. Молекулярная масса и молекулярно-массовое распределение
- •1.3. Важнейшие свойства полимерных веществ
- •1.4. Классификация полимеров
- •1.5. Номенклатура полимеров
- •Основные принципы номенклатуры регулярных линейных однотяжных органических полимеров
- •Основные принципы номенклатуры сополимеров
- •2. Синтез полимеров: поликонденсация
- •Основы теории поликонденсации
- •Характеристика процесса
- •Функциональность мономера
- •Классификация поликонденсационных процессов
- •Гомо- и гетерополиконденсация
- •Типы химических реакций, используемых при поликонденсации
- •И типы полимеров, образующихся при поликонденсации
- •Возможность образования низкомолекулярных гетероциклических соединений при поликонденсации
- •Равновесная поликонденсация
- •Особенности равновесной поликонденсации
- •Начало роста цепи
- •Процесс роста цепи
- •Остановка роста цепи
- •1. Наличие в системе выделяющегося низкомолекулярного продукта реакции и установление равновесия между прямой и обратной реакциями.
- •Механизмы реакций равновесной поликонденсации
- •Кинетика равновесной поликонденсации
- •Неравновесная поликонденсация
- •Особенности неравновесной поликонденсации
- •Кинетика неравновесной поликонденсации
- •Способы проведения поликонденсации
- •Поликонденсация в твердой фазе, расплаве, растворе
- •Поликонденсация в эмульсии
- •Межфазная поликонденсация
- •Трехмерная поликонденсация
- •Совместная поликонденсация
- •3. Синтез полимеров: полимеризация
- •3.1. Основы теории полимеризации
- •Характеристика процесса
- •Цепные и ступенчатые реакции полимеризации
- •Термодинамика полимеризации
- •Миграционная полимеризация
- •3.3. Радикальная полимеризация
- •3.3.1. Характеристика радикальных процессов
- •Мономеры
- •Инициирование
- •Рост цепи
- •Обрыв цепи
- •Кинетический анализ радикальной полимеризации Вывод общего кинетического уравнения радикальной полимеризации
- •Типичная кинетическая кривая радикальной полимеризации
- •Ингибиторы и замедлители радикальной полимеризации
- •Влияние различных факторов на скорость полимеризации и молекулярную массу полимера
- •Методы проведения полимеризации
- •Полимеризация в массе мономера
- •Полимеризация в растворителе
- •Полимеризация в суспензии
- •Эмульсионная полимеризация
- •Радикальная сополимеризация
- •Характеристика процесса
- •Уравнение состава сополимера
- •Константы сополимеризации, их физический смысл
- •Ионная полимеризация
- •Характеристика ионных процессов
- •Активные центры ионной полимеризации
- •Катионная полимеризация
- •Инициаторы катионной полимеризации
- •Реакционная способность мономеров
- •Механизм катионной полимеризации
- •Анионная полимеризация
- •Механизм действия анионных инициаторов. В зависимости от типа взаимодействий можно выделить 2 механизма инициирования анионной поликонденсации.
- •Ионно-координационная полимеризация
- •Алфиновые катализаторы
- •Катализаторы Циглера-Натта
- •Оксидные катализаторы
- •Ионная сополимеризация
- •4. Химические превращения
- •Особенности химических реакций полимеров
- •Полимераналогичные превращения
- •Реакции, приводящие к увеличению молекулярной массы
- •Реакции, приводящие к уменьшению молекулярной массы
- •Старение полимеров
- •Библиографический список
Анионная полимеризация
Анионная полимеризация – процесс полимеризации, в котором растущая цепь представляет собой отрицательно заряженную частицу (анион).
Характеристики растущей цепи:
природа концевого атома (зависит только от природы мономера);
удаленность концевого атома от противоиона (зависит от природы противоиона, свойств реакционной среды и температуры).
Концевыми атомами могут быть:
углерод (полимеризация за счет раскрытия связи С=С);
кислород (полимеризация кислородсодержащих гетероциклов или мономеров по связи С=О);
сера (полимеризация серосодержащих гетероциклов или мономеров по связи С=S);
азот (некоторые азотсодержащие мономеры) и другие.
Мономеры для анионной полимеризации:
ненасыщенные соединения винильного и диенового рядов;
карбонилсодержащие мономеры;
гетероциклические соединения.
Наиболее активны в анионной полимеризации непредельные мономеры, двойная связь которых обеднена электронной плотностью, т.е. имеющие электроноакцепторные заместители. Поэтому этилен с трудом, а другие олефины совсем не полимеризуются по анионному механизму. Способность гетероциклов к анионной или катионной полимеризации зависит от числа атомов в цикле (см. табл. 14).
Инициирование
Инициаторы анионной полимеризации: производные щелочных и щелочноземельных металлов – алкилы, алкоксиды, арилы, амиды, цианиды (табл. 15).
Механизм действия анионных инициаторов. В зависимости от типа взаимодействий можно выделить 2 механизма инициирования анионной поликонденсации.
1. Непосредственное присоединение инициирующего агента к мономеру:
![]()
2. Перенос электрона на мономер с образованием анионной частицы без присоединения инициатора или его фрагмента к мономеру:

Примеры
Взаимодействие 1,3-бутадиена с натрием:
CH2=CH-CH=CH2 + Na •CH2=CH-CH=CH2‾ Na+
Инициирование непредельного мономера системой натрий + нафталин:

CH2-CHХ‾ Na+ + CH2=CHХ •CH2CHХCH2CHХ‾ Na+
Х - электроноакцепторный заместитель.
Продукт реакции можно рассматривать как бифункциональный реагент, способный инициировать полимеризацию по радикальному и по ионному механизмам. Однако обычно радикальные центры быстро исчезают вследствие рекомбинации, приводящей к образованию дианионных центров, способных расти с обоих концов:
![]()
Таблица 15. Примеры взаимодействия различных инициаторов
с мономерами
Инициатор |
Уравнение в общем виде |
Пример реакции |
Алкил металла, RMe |
М + RMe R-M-Me |
Мономер – стирол; инициатор – н-бутиллитий СН2=СН(С6Н6) + С4Н9Li С4Н9-СН2-СН(С6Н6)‾ Li+ |
Амид металла, R2NMe |
М + R2NMe R2N -M-Me |
Мономер – стирол; инициатор – амид калия СН2=СН(С6Н6) + NН2К NН2-СН2-СН(С6Н6)‾ К + |
Рост цепи
На каждой стадии присоединения молекулы мономера образуется металлоорганическое соединение, содержащее поляризованную связь металл – углерод.
В случае неполярной среды процесс роста цепи безобрывен, т.к. промежуточные металлоорганические соединения относительно устойчивы в углеводородной среде. Это приводит к значительному возрастанию степени полимеризации в ходе процесса.
В процессе роста также происходит регулирование структуры цепи. Так, в присутствии свободных анионов мономер присоединяется со стороны углеродного атома с наименьшей электронной плотностью:
 Здесь
Здесь
![]() .
.
Установлено, что в присутствии некоторых металлоорганических соединений проявляется специфичность, обеспечивающая строго определенное пространственное присоединение мономера. Особенно характерен этот эффект для литийорганических соединений.
Ограничение роста цепи
В анионной полимеризации реакции кинетического обрыва цепи часто отсутствуют. При этом процесс продолжается вплоть до полного исчерпания мономера. Достаточно устойчивые растущие полимерные анионы называют «живущими» полимерами. При добавлении к такому полимеру новой порции мономера полимеризация возобновляется. Такое свойство позволяет получать блоксополимеры добавлением мономеров, способных полимеризоваться на «живых» концах.
Для дезактивации «живущих» цепей добавляется протонодонорное вещество, способное взаимодействовать с активным концевым карбанионом. Например, «живые» макромолекулы полистирола можно дезактивировать добавлением воды:
~CH2-C![]() H(С6Н5)
+ Н2О
~CH2-CH2
(С6Н5)
+ НО
H(С6Н5)
+ Н2О
~CH2-CH2
(С6Н5)
+ НО
Условия существования «живых» полимерных цепей:
неполярная среда;
отсутствие в реакционной массе протонодонорных реагентов (спиртов, аминов и др.);
относительно низкие температуры;
инертная атмосфера.
В зависимости от типа мономера и полярности среды различают несколько разновидностей анионной полимеризации, отличающихся механизмом и кинетикой процесса. Их классификация показана на рис. 9.

Рис. 9. Разновидности анионной полимеризации
Кинетика анионной полимеризации зависит также от типа инициатора.
Пример
Анионная полимеризация ненасыщенных неполярных мономеров в полярной среде. Полимеризация стирола, инициированная амидом калия в среде кипящего жидкого аммиака (-33С).
1. Инициирование состоит из диссоциации амида калия
KNH2
![]() K+
+ NH2
K+
+ NH2
и собственно инициирования:

Скорость инициирования
![]() . (57)
. (57)
2. Рост цепи
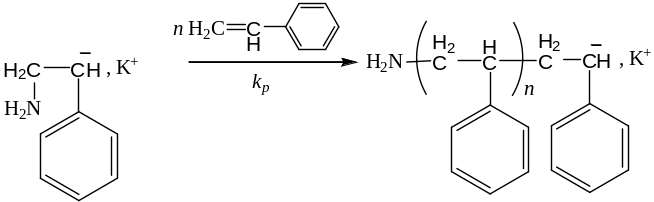
Обозначив
концентрацию растущих активных центров
![]() ,
получим для скорости роста выражение
,
получим для скорости роста выражение
![]() . (58)
. (58)
Обрыв цепи в основном протекает в результате передачи цепи на растворитель или примеси:

Скорость обрыва можно представить уравнением
![]() , (59)
, (59)
где
![]() – константа скорости обрыва передачей
цепи на растворитель.
– константа скорости обрыва передачей
цепи на растворитель.
При условии
стационарного состояния (п.3.3.6)
концентрация активных центров
![]() постоянна,
,
тогда можно записать:
постоянна,
,
тогда можно записать:
![]() . (60)
. (60)
Подставив выражение (60) в уравнение для скорости роста, получим
![]() . (61)
. (61)
Средняя степень полимеризации в этой системе
 (62)
(62)
где
![]() – константа передачи цепи на аммиак.
– константа передачи цепи на аммиак.
Значения констант скорости роста в анионной полимеризации и в радикальном процессе близки. Однако концентрации растущих анионов в анионной полимеризации значительно выше, поэтому скорость ее в 104-107 раз выше, чем скорость радикальной полимеризации. На скорость обрыва значительное влияние оказывает растворитель.
