
- •Содержание
- •Часть 1. Предмет патологии. Учение о болезни (Куликов в.П., Доронина н.Л.)... 8
- •Часть 2. Механизмы развития болезней (Куликов в.П., Доронина н.Л.) 15
- •Часть 3* Патология органов и систем (Куликов в.П., Доронина н.Л.) 157
- •Часть 4. Ситуационные задачи (Куликов в.П., Костюченко л.А., Доронина н.Л,
- •Часть 5. Тестовые задания (Куликов в.П., Костюченко л.А., Воронцов в.В.,
- •Часть 6. Задания для подготовки к занятиям. Вопросы к экзамену (Куликов в.П.,
- •Часть 1. Предмет патологии. Учение о болезни.
- •I. Предмет патологии.
- •IIII Понятие болезни. Патологические реакции, процессы, состояния. Симптом и синдром. Классификация, стадии развития и исходы болезней.
- •IV. Умирание. Терминальные состояния.
- •VI. Патогенез заболеваний. Саногенез.
- •VII. Лечение заболеваний
- •Часть 2. Общая патология. 2.1 .Повреждение клетки.
- •IV. Общий адаптационный синдром. Схема развития симпато-адреналовой и гипоталамо-гипоФизарно-адреналовой реакций при стрессе. Стресс-реализующие и стресс-лимитирующие системы.
- •Стадии стресса или общего адаптационного синдрома:
- •V. Дистресс Болезни адаптации. Ятоогенные осложнения вследствие использования аналогов стресс-реализующих гормонов.
- •IV. Механизм Формирования патологии у плода при алкоголизме беременной женщины.
- •V. Методы изучения наследственных болезней.
- •2.4. Нарушение регионального кровообращения. Тромбозы и эмболии.
- •7. Характер движения крови по сосудам:
- •IV. Виды региональных нарушений кровообращения и их механизмы. Сладж-Феномен.
- •V. Методы оценки сосудистой гемодинамики.
- •2.5. Патология гемостаза.
- •V. Гипокоагуляиии. Связанные с дефицитом плазменных прокоагулянтов
- •2.6. Гипоксия.
- •I. Понятие гипоксии.
- •V. Адаптивные реакции организма: срочные и долговременные (дыхательные, гемодинамические, гемические, тканевые). Срочная адаптация к гипоксии (или 1-ая стадия долговременной адаптации)*
- •2.7. Патофизиология боли.
- •II. По характеру:
- •III. Понятия обморока и коллапса. Отличия от шока.
- •IV. Кома. Этиология и патогенез отдельных видов ком (печеночная, уремическая, диабетическая).
- •2.9. Воспаление.
- •III. Стадии опухолевого роста.
- •IV. Свойства опухолевого роста.
- •V. Опухолевые маркеры. Механизмы изменения иммунного надзора при
- •2.13. Патология углеводного обмена. Сахарные диабеты.
- •IV. Нарушение платочного метаболизма липидов. Жировая инфильтрация органов.
- •V Этиология и патогенез атеросклероза. Стадии развития атеросклероза и осложнения.
- •2.15. Патология белкового обмена.
- •IV. Вторичные нарушения обмена аминокислот. Патология конечных этапов белкового обмена, роль печени и почек е метаболизме аммиака. Нарушение обмена пуриновых и пиримидиноеых оснований.
- •Часть 3. Патология органов и систем. 3.1. Патология красной крови.
- •IV. Этиология и патогенез гемолитических анемий.
- •2. Липидзависимые мембранопатии:
- •3. Ферментопатии:
- •4. Гемоглобинопатии:
- •V. Этиология и патогенез дизэритропоэтических анемий.
- •VI. Компенсаторные реакции организма при анемиях.
- •3.2. Лейкоцитозы и лейкопении. Лейкозы.
- •I. Лейкоцитозы.
- •IV. Лейкемоидные реакции. Виды. Причины возникновения.
- •V. Лейкозы. Общая характеристика,
- •I. По виду клетки-«родоначальницы» лейкоза:
- •VI. Лабораторная характеристика лейкозов. Отличия лейкозов от лейке-моидных реакций.
- •VII. Общие изменения е организме при лейкозах.
- •3.3. Сердечная недостаточность.
- •2. Гипертрофия левого предсердия
- •1. Гипертрофия правого желудочка
- •2. Гипертрофия левого желудочка
- •1, Нервная регуляция.
- •1А} Норма
- •IV, Диагностика аритмий.
- •3.7. Патология артериального давления и сосудистого тонуса.
- •Резервный
- •VI. Компенсаторные процессы при недостаточности внешнего дыхания.
- •IV. Расстройства функции тонкого и толстого кишечника: секреции, переваривания, всасывания и моторики.
- •1. Усиление перистальтики кишечника.
- •2. Ослабление перистальтики кишечника.
- •V. Нарушение барьерной функции кишечника. Дисбактеоиоз.
- •I Повышение проницаемости мембранПовреждение мембран клеток с их частичной или полной деструкцией
- •Часть 4. Ситуационные задачи.
- •Часть 5. Тестовые задания.
- •Часть 6. План практических занятий. Вопросы к экзамену. 6.1. План практических занятий по патофизиологии.
3.7. Патология артериального давления и сосудистого тонуса.
/. Артериальное давление: происхождение и виды.
Артериальное давление — интегративное отражение состояния центральной гемодинамики.
Величина АД определяется 4-мя компонентами:
Сердечная компонента - создает градиент давления, сообщая крови необходимую кинетическую энергию; показатели работы сердца (параметры сердечного выброса) рассмотрены в теме «Сердечная недостаточность» (УО, МОК, СИ).
Компонента ОЦК - объем крови в сосудистом русле; снижается при повышении проницаемости сосудов, снижении онкотического давления плазмы; регулируется РААС.
Сосудистая компонента - определяется сосудистым тонусом; существенно изменять свой диаметр способны только резистивные сосуды; интегральными показателями сосудистого тонуса являются общее периферическое сопротивление (ОПСС) и удельное периферическое сопротивление (УПСС).
Компонента вязкости крови, которая в обычных условиях не подвержена значительным колебаниям.
Регуляций АД и сосудистого тонуса: А. Местные (периферические) механизмы:
Местные механизмы саморегуляции сосудистого тонуса обеспечивают адекватный кровоток в органах в зависимости от уровня метаболизма в них. /. Миогенная регуляция (эффект Бейлиса).
Резкое повышение АД сопровождается сокращением гладкой мускулатуры арте-риол жизненно важных органов, в результате объемная скорость кровотока в этих органах не изменяется или возрастает незначительно, а при падении АД гладкие мышцы сосудов расслабляются, что позволяет поддерживать должную объемную скорость регионального кровотока.
П. ЭНДОТЕЛИАЛЬНЫЕ ФАКТОРЫ.
Сосудистый эндотелий является местом образования целого ряда соединений, участвующих в регуляции сосудистого тонуса, функции тромбоцитов и свертывания крови.
В настоящее время выделяют несколько вазодилатирующих и вазоконстрикторных субстанций.
Вазодилатирующие факторы: 1. Эндотелиальный расслабляющий фактор (оксид азота, N0), обеспечивает выраженную релаксацию гладких мышц артерий, артериол и вен, а также препятствует адгезии и агрегации тромбоцитов.
2 Простациклин также относится к числу важнейших вазодилататоров, препятствующих вазоконстрикторному эффекту тромбоксана Аг и агрегации тромбоцитов.
208
3. Эндотелиальный гиперполяризующий фактор (ЭГПФ), также вырабатываемый эндоте-лиальными клетками, вызывает гиперполяризацию мембран гладкомышечных клеток и снижает их чувствительность к разнообразным констрикторным влияниям. В азоконстрикторные факторы:
Эндотелин-1 (ЕТг) является наиболее мощным из всех известных вазоконстрикторов.
Тромбоксан А2 и простагландин РОН2 относятся к числу активных эндотелиальных вазоконстрикторов, обладающих также свойством активировать агрегацию тромбоцитов и тромбообразование.
Тканевой ангиотензин II (АЛ) относится к числу мощных вазоконстрикторов, образующихся в эндотелии различных сосудистых областей.
В физиологических условиях существует оптимальное соотношение выработки эндотелиальных вазодилатирующих и вазоконстрикторных субстанций, которое полностью соответствует метаболическим потребностям органа и основным параметрам центральной гемодинамики.
При действии на сосудистый эндотелий различных повреждающих факторов (гипоксии, чрезмерной концентрации катехоламинов, ангиотензина II, серотонина, высокого уровня АД, ускорения кровотока и др.) начинают преобладать вазоконстрикторные механизмы регуляции сосудистого тонуса, и развивается так называемая дисфункция эндотелия. Она характеризуется повышением тонуса сосудистой стенки, ускорением агрегации тромбоцитов, процессов пристеночного тромбообразования и т.п. III Продукты метаболизма.
В интенсивно работающем органе под действием продуктов метаболизма (ионов Н+, аденозина, АТФ, АДФ, АМФ, СО2, молочной кислоты и др.) и БАВ (брадикинина, гис-тамина и др.) также происходит снижение тонуса артериол, прекапиллярных сфинктеров и увеличивается число функционирующих капилляров. При снижении метаболизма эти эффекты уменьшаются, происходит адекватное ограничение органного кровотока.
Б. Центральные механизмы регуляции
1. Афферентное звено представлено многочисленными баро- и хеморецепторами, расположенными в нескольких рефлексогенных зонах сосудистой системы (аорта, сино-каротидная зона, сосуды легких и др.) (рис. З.7.1.).
Барорецепторы реагируют на степень и скорость растяжения стенки сосудов (или полостей сердца). При повышении АД или наполнения камер сердца барорецепторы отвечают усилением афферентной импульсации, при снижении АД - ее уменьшением.
Хеморецепторы дуги аорты, синокаротидной зоны и других рефлексогенных зон (сердце, почки, органы пищеварения) аналогично реагируют на изменение в крови концентрации 02, ССЬ, ионов Н+.
Чувствительные волокна от баро- и хеморецепторов дуги аорты и каротидного синуса проходят в составе синокаротидного нерва, ветвей языкоглоточного нерва и депрес-сорного нерва.
2. Центральное звено.
Центральное звено регуляции сосудистого тонуса - вазомоторный (сосудо-двигательный) центр - представлено различными функционально связанными между собой нервными структурами, расположенными в продолговатом, спинном мозге, гипоталамусе, коре больших полушарий.
Известна так называемая игиемическая реакция ЦНС. При значительном снижении системного АД (около 40 мм рт.ст.) возникает ишемия сосудо-двигательного центра и активация симпатической нервной системы. Медиатором последней является норадреналин, вьвывающий тахикардию (р1 -рецепторы) и увеличение тонуса сосудов (ос* и осг-, рецецторь!).
209
Синсжаротидмый
нерй
Коротцдиый
синус
Лелый
сеа«*гчный депрессорный иера
Обшся
сонма» ертерня
Уздоьотый
гонглий
Коротмдиый
синус Проаы*
сердечный депресеориый
Правый
блуждавшим м#рв Проеоя
щщкнюцнчшш артерия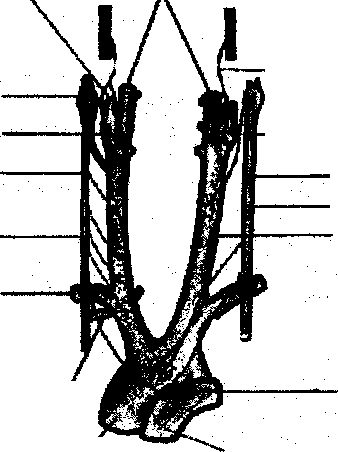
Возаротиькй
шртаниьгй
дере
:Щтрт
Аортальные тельце
Яегочиой ортерй«8
Рис. 3.7.1. Баро- и хеморецепторы аорты и каротидного синуса.
3. Эфферентное звено.
Включает нервные и гуморальные механизмы регуляции сосудистого тонуса. В зависимости от скорости развития циркуляторных эффектов различают: 1) механизмы быстрого кратковременного действия; 2) механизмы промежуточного действия; 3) механизмы длительного действия.
К механизмам быстрого кратковременного действия относятся нервные рефлекторные реакции, возникающие при раздражении баро- и хеморецепторов описанных рефлексогенных зон, а также при ишемии ЦНС. Эти реакции развиваются в течение нескольких секунд и реализуются через рефлекторные изменения активности симпатической и парасимпатической нервных систем, а также через изменение концентрации гуморальных веществ - адреналина и норадреналина. Раздражение барорецепторов аорты и каротидного синуса (например, при повышении АД или механическом воздействии на эти зоны) закономерно приводит к снижению симпатических (вазоконстрикторных) и усилению парасимпатических (депрессорных) влияний. В результате снижается сосудистый тонус, а также частота и сила сокращения сердца, что способствует нормализации АД. Наоборот, при падении АД (например, при кровопотере) импульсация с барорецепторов уменьшается, и начинают преобладать симпатические влияния - увеличение ЧСС, сердечного выброса и сосудистого тонуса.
Аналогичным образом возникает ответ на раздражение рецепторов растяжения предсердий и рецепторов растяжения желудочков, например, при быстром увеличений их наполнения. В результате снижения тонуса симпатических и повышения активности парасимпатических нервов развивается брадикардия и вазодилатация.
Возбуждение хеморецепторов дуги аорты и каротидного синуса при снижении напряжения Ог, повышении напряжения СО2 или увеличении концентрации ионов Н+ в крови приводит к сужению резистивных сосудов и подъему АД. К такому же эффекту приводит рефлекторная реакция на ишемию ЦНС, например, при недостаточном кровоснабжении головного мозга, гипоксемии или резком падении АД. Повышение концентрации Н+ и СОг сопровождается раздражением хеморецепторов ствола мозга и значительным подъемом АД.
Симпатической нервной системе принадлежит ведущая роль в регуляции тонуса периферических сосудов. Влияние адреналина и норадреналина на тонус различных сосудистых областей зависит от концентрации этих веществ в крови и от соотношения
210
в разных сосудах а- и р-адренорецепторов. Как известно, возбуждение а-рецепторов сопровождается сокращением гладких мышц, а возбуждение р-рецеиторов - их расслаблением.
Главным регуляторным механизмом промежуточного действия является почечная ренин-ангиотензиновая система. Ее активация, наступающая при снижении кровоснабжения почек любого генеза. Выделением ренина, который способствует превращению ан-гиотензиногена в ангиотензин I. Последаий под действием АПФ превращается в ангиотензин II, обладающий мощным вазоконстрикторным действием. Кроме того, ан-гиотензин II возбуждает центральные и периферические симпатические структуры. Все это приводит к росту периферического сопротивления и повышению (нормализации) АД. Следует помнить, что существует альтернативный путь трансформации АГв АН, без участия АПФ.
К регуляторным механизмам длительного действия относят системы контроля за объемом жидкости (гормональные системы альдостерона, вазопрессина, тироксина, глю-кокортикоидов).
Компенсаторные механизмы при изменении АД:
Бароцептивный рефлекс: повышение АД в дуге аорты и каротидном синусе -> активация блуждающего нерва -> снижение ЧСС.
Рефлекс Берцольда-Яриша: повышение АД -» раздражение рецепторов эндокарда ~» через активацию блуждающего нерва -> снижение ЧСС.
Возбуждение тормозных а2-адренорецепторов на пресинаптической мембране ои-адренергических синапсов сосудов -» пресинаптическое торможение.
При повышении АД за счет увеличения фильтрационного давления повышается диурез.
Адреналин ослабляет канальцевую реабсорбцию Ыа+, вследствие чего повышается диурез.
Повышение тонуса сосудов -> ишемия почек -> выделение почечных простагландинов (медуллин) -» расширение сосудов.
Выделение в предсердиях НУГ -> повышение клубочковой фильтрации.
Повышение тонуса сосудов -> ишемия почек —> выделение ренина в ЮГА -» активация РААС -^сужение сосудов + альдостерон -» увеличение осмолярности плазмы -> выброс вазопрессина -» еще больший подъем АД.
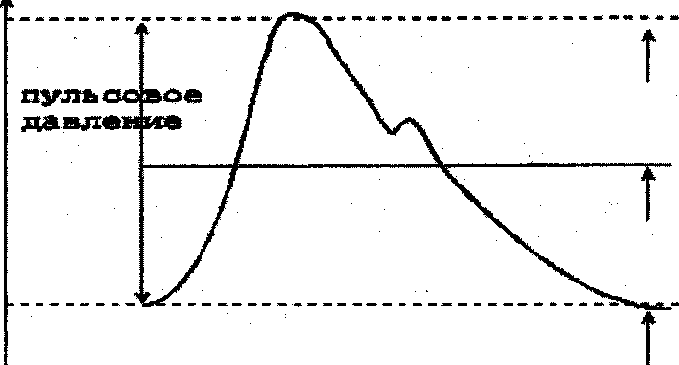
В клинической практике наиболее часто используются следующие виды АД крови: минимальное (диастолическое), пульсовое, среднее гемодинамическое и максимальное (систолическое) давление (рис.3.7'.2.).
- Диастоличеекое давление представляет собой величину минимального давления крови, достигаемую к концу диастолического периода сердечного цикла. Минимальное давление зависит от степени проходимости или величины оттока крови через систему прекапиляров, упруго-вязких свойств артериальных сосудов.
* Систолическое давление равно максимальному давлению, достигаемому в момент, соответствующий выбросу крови из сердца в аорту. Максимальное давление характеризует запас энергии, которым обладает движущаяся масса крови на данном участке сосуда.
Среднее гемодинамическое давление определяется интегрированием (усреднением) текущего значения АД за время сердечного цикла.
Ориентировочно величину среднего давления можно определить по формулам:
ВецлераиБогера:Рт = 0,42Рз + 0,58Р(1,
Хикема: Рт = Р<1 + (Рз - Рд) / 3,
где Рз - систолическое (максимальное) давление, .Р<1 - диастоличеекое (минимальное) давление.
211
Х20
80
Р,мм рт.са?
СЖСФОЯ*
аду **Н- ^ВЬ. ТТ 4бЬ ЧввЯПЛ*'!'4Й&.
ВД |мМб1 до!Я1 щАДО
диастол*
Рис. 3.7.2. Давление крови в аорте [ЬИ:р://еНтап.ги/риЫ/АМСМ/2.Ь1;т1].
1
//. Классификация нарушений артериального давления. Теории развития гипертонической болезни. Патогенез гипертонической болезни. Классификация нарушений АД:
, Преходящие:
гипертензивные реакции,
гипотензивные реакции.
2. Острые:
гипертонический криз,
гипотонии.
3. Стойкие:
А) Артериальные гипертонии
а) Первичная (эссенциальная) артериальная гипертония.
Ъ) Вторичные (симптоматические) артериальные гипертонии,
почечные (ренопривная и вазоренальная или реноваскулярная),
эндокринные (надпочечниковые: минералокортикоидные, глюкокорти-коидные, катехоламиновые, гипертиреоидные),
нейрогенные,
■ гемодинамические.В) Артериальные гипотонии
а) Физиологическая артериальная гипотония.
■ конституциональная,
■ адаптивная (тренированность, высокогорье).Ъ) Нейроциркуляторная (первичная) гипотония.
с) Симптоматические (вторичные) гипотонии (при язвенной болезни желудка и двенадцатиперстной кишки, гепатите, пневмонии и туберкулезе, интоксикации, ревматоидном артрите, остеохондрозе шейного отдела позвоночника).
Артериальная гипертония (гипертензия) - стойкое повышение АД.
Артериальная гипотония (гипотензия) - стойкое понижение АД.
Термины «гипер-» и «гипотония» применяются для обозначения в большей степени сосудистого тонуса, а термины «гипер-» и «гипотензия» - для обозначения артериального давления.
Гипертоническая болезнь (эссенциальная гипертония, первичная артериальная гипертензия) - заболевание, характеризующееся стойким (первичным) повышением АД
212
("неизвестной природы") при отсутствии патологических изменений какого-либо органа, устранение которых может привести к его нормализации.
В 1962 г. в рекомендациях экспертов ВОЗ впервые было предложено выделять три стадии артериальной гипертензии в зависимости от наличия и тяжести поражения органов-мишеней (табл. 3.7.1.)* Долгие годы считалось, что у больных с поражением органов-мишеней антигипертензивная терапия должна быть более интенсивной, чем у больных без поражения таких органов.
Таблица 3,7.1. Классификация АД [по ВОЗ, 1962].
|
Характеристика |
АД> мм.рт.ст. |
Типовые клинические проявления |
|
1 Нижняя граница нормы |
100/60 |
- |
|
Верхняя граница нормы |
139/89 |
- |
|
Артериальная гипертония |
|
|
|
Пограничная |
140-159/90-94 |
Функциональные, |
|
I стадия (легкая) |
160-179/95404 | |
|
II стадия (среднетяжелая) |
180-200/105-114 |
Гипертрофия левого желудочка, ангиоре-тинопатия, нарушения мозгового кровообращения. |
|
III стадия (тяжелая) |
> 200/115 и > |
Склеротические изменения. |
|
Артериальная гипотония |
< 100/60 |
Нарушения мозгового кровообращения, обморок, коллапс, шок. |
Согласно рекомендациям ВОЗ и Международного общества по гипертензии (МОГ) 1999 г. под артериальной гипертензией понимается уровень систолического АД 140 мм рт.ст. и более, и/или уровень диастолического АД 90 мм рт.ст. и более, у людей, которые не получают антигипертензивных препаратов.
В таблице 3.7.2. показана современная классификация артериального давления.
Таблица 3.7.2. Классификация артериального давления [по ВОЗ-МОГ, 1999].
|
Класс АД* |
АД, ммрт. ст. |
|
|
Систолическое |
диастолическое | |
|
Оптимальное АД |
< 120 |
<80 |
|
Нормальное АД |
< 130 |
<85 |
|
Повышенное нормальное АД |
130-139 |
85-89 |
|
Артериальная гипертензия |
|
|
|
1-я степень ("мягкая") |
140-159 |
90-99 |
|
Подгруппа: пограничная |
140-149 |
90-94 |
|
2-я степень ("умеренная") |
160-179 |
100-109 |
|
3-я степень ("тяжелая") |
> 180 |
>110 |
|
Изолированная систолическая гипертензия |
>140 |
<90 |
|
Подгруппа: пограничная |
140-149 |
<90 | |
* Если показатели систолического и диастолического АД находятся в разных классах, уровень АД у данного больного относят к более высокому классу.
Теории развития гипертонической болезни (эссенциальной гипертензии).
1. Гипотеза Э. Гелльгорна и соавт.
Инициальным патогенетическим фактором является стойкая повышенная возбудимость и реактивность (гиперергия) высших симпатических нервных центров (в частности, расположенных в заднем отделе гипоталамуса). Факторами, вызывающими стойкую гипе-рергию этих центров, является длительное, повторное возбуждение эмоциональных центров, тесно связанных с симпатическими ядрами гипоталамуса.
Повышение тонуса прессорных (симпатических) центров ведет к спазму сосудов, увеличению сердечного выброса и повышению АД, обусловливает гиперпродукцию гуморальных факторов с прессорным действием адреналина, норадреналина, вазопрессина,
213
АКТГ,
кортикостероидов, а также гиперсекрецию
ренина в юкстагломерулярном аппарате
(ЮГА)
почек.
2, Гипотеза Е. Муирад, А. Гайтона и соавт.
Инициальным фактором развития гипертензии является генетически обусловленный пониженный уровень ЫаС1- и водовыделительной функции почек, что ведет к накоплению избытка натрия и воды в организме, включая ткань сосудистых стенок, в том числе их гладкие мыпщы. В связи с этим развивается гиперволемия, повышаются тонус сосудов и чувствительность их стенок к прессорным гормонам и другим биологически активным факторам.
3, Гипотеза нарушения функций мембранных ионных насосов проф. Ю.В. Постнова.
Инициальным фактором в патогенезе артериальной гипертензии является генерализованный наследственный дефект мембранных ионных насосов клеток, включая глад» комышечные клетки стенок артериол. Дефект этот заключается в снижении активности кальциевого насоса, локализующегося в мембранах эндоплазматической сети, и натриевого насоса, локализующегося в плазмолемме. В результате уменьшается «откачивание» Са+2 из цитоплазмы в эндоплазматическую сесть и Иа+ из цитоплазмы в межклеточное пространство. Избыток Са+2 и Ыа+ в цитоплазме гладкомышечных клеток сосудов вызывает их спазм, а также повышение чувствительности к прессорным факторам.
4, Гипотеза проф. Г Ф. Лонга и проф. А.Л. Мясникова.
Инициальным патогенетическим фактором развития ГБ является растормажива-ние центров ССС (снижение тормозного влияния коры головного мозга на подкорковые вегетативные нервные центры, прежде всего пресеорные).
Этиологическими факторами являются стрессоры. Первичное звено патогенеза -возбуждение симпатических центров -> включение еимпатоадреналовой реакции, подключение ЮГА почек -» альдостерон -» накопление Иа"1" -» увеличение ОЦК + набухание сосудистой стенки .*-» повышение ее реактивности. Длительный спазм гладких мышц сосудов -> накопление Са+2 в цитоплазме мышечных волокон -» активация РНК-полимеразы -> гипертрофия гладкомышечных элементов сосудистой стенки.
Клинико-потегенетинеские формы эссенциальной гипертонии [по Кушаковско-му].
Гиперадренерическая (Ланг, Мясников).
Гипергидратационная.
Ангиотензин-зависимая.
Кальций-зависимая (Постнов, Орлов).
Цереброишемичеекая.
В табл. 3.7.3. и 3.7.4. представлены прогностические факторы артериальной гипертензии (стратификация факторов риска).
Стратификация риска ГБ позволяет врачу составить более объективное (хотя и упрощенное) представление о долговременном прогнозе заболевания у каждого конкретного больного с целью выбора оптимальной тактики индивидуального лечения.
214


Таблица
3.7.3. Прогностические факторы артериальной
гипертензии [по ВОЗ-МОГ, 1999]
В. Поражение органов-мишеней
С. Сопутствующие клинические состояния
I. Используемые для оценки риска
Уровни систолического и диастоличе-ского АД (артериальная гипертензия 1-3 степени)
Мужчины старше 55 лет
Женщины старше 65 лет
Курение
Уровень сыворотки общего холестерина более 6,5 ммоль/л (250 мг/дл)
Сахарный диабет
Указания на преждевременное развитие сердечно-сосудистого заболевания в семейном анамнезе
И. Другие факторы, оказывающие неблагоприятное влияние на прогноз
Пониженные уровни холестерина ЛПВП
Повышенные уровни холестерина ЛПНП
Микроальбуминурия (30-300 мг/сут) при сахарном диабете
Нарушенная толерантность к глюкозе
Ожирение
Сидячий образ жизни
Повышенные уровни фибриногена
Социально-экономическая группа с высоким риском
Этническая группа с высоким риском
Географический регион с высоким риском
Гипертрофия левого желудочка (по данным электрокардиографии, эхокардио-графии или рентгенографии органов грудной клетки)
Протеинурия (>300 мг/сут) и/или небольшое повышение концентрации креати-нина в плазме (1,2-2,0 мг/дл)
Ультразвуковые или рентге-ноангиографнческие признаки атеросклеротического поражения сонных, подвздошных и бедренных артерий, аорты
Генерализованное или фокальное еужение артерий сетчатки
Сосудистое заболевание головного мозга
Ишемический инсульт
Геморрагический инсульт
Преходящее нарушение мозгового кровообращения
Заболевание сердца
Инфаркт миокарда
Стенокардия
Реваскуляризация коронарных артерий
Застойная сердечная недостаточность
Заболевание почек
Диабетическая нефропатия
Почечная недостаточность (содержание креатинина в плазме крови выше 2,0 мг/дл)
Сосудистое заболевание
Расслаивающая аневризма
Поражение артерий с клиническими проявлениями
Выраженная гипертоническая ретинопатия
Кровоизлияния или экссудаты
Отек соска зрительного нерва
Примечание. Поражения органов-мишеней (ПОМ) соответствуют II стадии гипертонической болезни по классификации экспертов ВОЗ 1996 г., а сопутствующие клинические состояния - III стадии заболевания.
215
|
Таблица 3.7.4. Уровень риска сердечно-сосудистых осложнений у больных с артериальной гипертензией разной степени с целью определения прогноза* [по ВОЗ-МОГ, 1999]. | |||
|
Факторы риска (кроме артериальной гипертензии) и анамнез болезни |
Уровень риска при артериальной гипертензии | ||
|
1-я степень («мягкая») |
2-я степень ("умеренная") |
3-я степень ("тяжелая") | |
|
: Нет других факторов риска |
Низкий |
Средний |
Высокий |
|
1-2 других фактора риска |
Средний |
Средний |
Очень высокий |
|
3 и более других факторов риска, ПОМ или сахарный диабет |
Высокий |
Высокий |
Очень высокий |
|
Сопутствующее заболевание* * |
Очень высокий |
Очень высокий |
Очень высокий |
* Типичные примеры риска развития мозгового инсульта или инфаркта за 10 лет: низкий риск - менее 15%; средний риск - примерно 15-20%; высокий риск - примерно 20-30%; очень высокий риск - 30% или выше. ** См. табл. 3.7.3. ПОМ - поражение органов-мишеней (см. табл. 3/7.3Л.
Порочные круги при гипертонической болезни:
Рениновый: повышение АД ~» артериальный спазм -> ишемия почек -* выброс ренина из ЮГА -> активация РААС -> повышение АД.
Сердечный: гиперволемия ~» закон Анрепа (сила сердечных сокращений пропорциональна давлению (сопротивлению), против которого она работает) г-» рост УО ~» повышение АД.
Атеросклероз вызывает поражение депрессорных зон.
Сосудистый: спазм гладких мышц сосудов -» накопление Са+2 в цитоплазме мышечных волокон -> активация РНК-полимеразы -» гипертрофия и гиперплазия гладкомы-шечных элементов сосудистой стенки.-» повышение периферического сосудистого сопротивления.
///. Симптоматические гипертензии.
Симптоматические (вторичные) артериальные гипертонии (гипертензии) -
стойкое повышение АД, являющееся проявлением (симптомом) какого-либо заболевания.
1. Почечные артериальные гипертензии:
Вжоренолъная: атеросклероз почечной артерии, фибромускулярная дисплазия, аор-тоартериит, васкулиты, эндартериит, тромбоз, эмболия, аневризмы почечной артерии, атрезия и гипоплазия почечных артерий, артериовенозные фистулы, стенозы и тромбозы вен, гематомы, травмы сосудов почек; неоплазмы, сдавливающие почечные артерии -> ишемия почек -» выброс ренина из ЮГА -» активация РААС -> повышение АД.
Реноприеная: поражение (гломерулонефрит, хронический пиелонефрит, диабетический гломерулосклероз, амилоидоз, гидронефроз) или удаление паренхимы почек -> дефицит почечных простагландинов А и Е -> повышение АД.
2. Эндокринные артериальные гипертензии:
■ Минералокортикоидные (первичный альдостеронизм или синдром Конна): гиперплазия или опухоль клубочковой зоны коры надпочечников -> повышение продукции альдостерона -» усиление реабсорбции Ка+ и воды -» увеличение концентрации Ка+ в плазме -» гиперосмия плазмы -» стимуляция секреции вазопрессина ->рост ОЦК -> повышение АД.
Увеличение концентрации Ка* в плазме -» повышение транспорта ионов Иа* через мембраны клеток -» накопление избытка Ка+ в клетках -» набухание клеток, в том
216
числе и стенок сосудов -» сужение их просвета + увеличение чувствительности к катехоламинам, вазопресеину, АГИ-» повьппение АД.
Глюкокортикоидные: гиперплазия или гормонально-активные опухоли пучковой зоны коры надпочечников (синдром Иценко-Кушинга) и базофильных клеток передней доли гипофиза (болезнь Иценко-Кушинга) .-> пермиссивное действие глю-кокортикоидов на эффект адреналина + слабая минералокортикоидная активность глюкокортикоидов -» повьппение АД.
Катехоламиновые: феохромоцитома (опухоль мозгового вещества надпочечников) -» гиперпродукция адреналина и норадреналина -> повышение АД.
Гипертиреоидные: тиреотоксикоз -» гиперпродукция тироксина и трийодтиронина -» увеличение силы и частоты сердечных сокращений (прямое кардиостимули-рующее действие гормонов + увеличение чувствительности сердца к катехолами-нам)^ увеличение УО -> повышение АД.
Вазопрессиновые: повышение секреции гипоталамусом вазопрессина (вазопресси-нома) -» сужение сосудов + задержка воды с увеличением ОЦК -» повышение АД.
Нейрогенные артериальные гипертензии формируются при органических поражениях нервных структур (сосудистые, воспалительные заболевания, опухоли ЦНС, травмы мозга), регулирующих системную гемодинамику (нервы, продолговатый, спинной мозг, гипоталамус, кора больших полушарий) -» преобладание прессорных влияний над депрес-сорными.
Гемодинамические артериальные гипертензии возникают при поражении сердца и крупных сосудов:
Атеросклероз аорты -> поражение делрессорных зон аорты -> повьппение АД.
Коарктация аорты -> по закону Анрепа (сила сердечных сокращений пропорциональна давлению (сопротивлению), против которого она работает) -> рост УО -» повышение АД.
Недостаточность аортальных клапанов -> рост УО по закону Франка-Старлинга (чем больше наполняется сердце во время диастолы, тем сильнее оно сокращается в систолу) -» повьппение АД.
Полная атриовентрикулярная блокада.
Реологическая гипертензия: увеличение вязкости крови (болезнь Вакеза, полици-темия, эритроцитозы, гиперпротеинэмия) -> повышение АД.
Васкулиты (аорто-артериит или болезнь Такаясу) -> уменьшение диаметра сосудов -> повышение АД.
5. Особые формы вторичных артериальных гипертензии
Солевая и пищевая гипертензия. Причинами данной формы артериальной гипертензии являются: чрезмерное употребление соли; веществ, богатых тирамином (некоторые сорта сыра и марки красного вина).
Медикаментозные гипертензии могут сформироваться на фоне приема глюкокортикоидов; минералокортикоидов; контрацептивных препаратов, содержащих прогестерон и эстроген; симпатических аминов; индометацина и др.
IV. Осложнения артериальных гипертензии.
Гипертонический криз - одно из наиболее частых и тяжелых осложнений гипертонической болезни и симптоматических артериальных гипертензии, характеризующееся острым повышением артериального давления до индивидуально высоких цифр и резким обострением симптоматики заболевания с преимущественным преобладанием церебральных и сердечно сосудистых расстройств;
Вторичная (некардиогенная) сердечная недостаточность; гипертрофия миокарда, инфаркт миокарда.
217
Инсульт (ишемический и геморрагический). *

Первично-сморщенная почка (артериологиалиноз и артериолоеклероз почечных сосудов -» нарушение почечной гемодинамики -» структурные изменения в нефронах и интеретициальнойткани -^ постепенно нарастающая гибель почечных нефронов, со-провождающаясй уменьшением массы действующих нефронов), клиническим проявлением которой является хроническая почечная недостаточность (никтурия, поли-урия, понижение относительной плотности мочи, азотемия).
Ангиоретинопатия.
V. Типы нарушения гемодинамики при артериальной гипертензии.
Для оценки патогенетических механизмов артериальной гипертензии важное значение имеет измерение параметров центральной гемодинамики. Основным методом для этого служит эхокардиография (Эхо-КГ). Важнейший параметр центральной гемодинамики - У О - ударный объем сердца. УО в покое равен в среднем 60-75 мл. Производным от У О является МОК - минутный объем кровотока (или сердечный выброс -СВ по терминологии используемой в ЭхоКГ). В норме равен в среднем 4-6 л/мин. Вычисляется как У О х ЧСС (частота сердечных сокращений). Для каждого человека существует должный минутный объем кровотока (ДМОК), который можно расчитать зная массу тела, рост и пол. На практике чаще пользуются не ДМОК, а СИ - сердечным индексом, который можно легко рассчитать по формуле:
МОКСИ = —-
, где МОК- минутный объем кровотока, 8- площадь поверхности тела которая определяется по формуле ДЮ-Буа или с помощью номограммы ДЮ-Буа. Сердечный индекс в условиях основного обмена у здорового человека в среднем равен 2,5-4,2 л/(мин хм2).
Еще один важнейший параметр, необходимый для оценки патофизиологических механизмов нарушения АД, - периферическое сосудистое сопротивление. ОПСС - общее периферическое сосудистое сопротивление (дин хсх см"5) характеризует суммарное сосудистое сопротивление, создаваемое резистивными сосудами, в основном артериолами, и поэтому служит для изучения артериального тонуса, его изменений при различных патологических и физиологических состояниях. В норме ОПСС составляет от 900 до 2500 дин х с х см"5. ОПСС расчитывается по формуле:
ОПСС-(Рш х 79,92)/МОК
, где 79,92- фазегор перевода миллиметров ртутного столба в дины на см2, Рт - среднее АД, которое расчитывается по формуле Хикема (см. выше)
Более правильно, с точки зрения сопоставимости результатов измерения у людей различных росто-вееовых параметров, является использование показателя УПСС - удельное периферическое сопротивление сосудов. В норме УПСС колеблется в пределах 35-45 у. е. Рассчитывается по формуле: УПСС = Рт/СИ где Рт- среднее артериальное давление в мм.рт.ст., СИ- сердечный индекс в л/(мин * м2).
В зависимости от значения СИ и ПСС различают типовые нарушения гемодинамики при ГБ.
Типы нарушения гемодинамики при артериальной гипертензии.
Фактически типы нарушений гемодинамики при артериальной гипертензии позволяют врачу сориентироваться во вкладе сердечной компоненты (УОэ МОК, СИ) и сосуди-
218
стой компоненты (ОПСС, УПСС) в механизмы повышения артериального давления. С этой целью используют и количественные значения изменения СИ
Гиперкинетический тип - характерно увеличение сердечного выброса (СИ более 4,2) при нормальном или сниженном ОПСС. Преимущественно повышается систолическое АД.
Гипокинетический тип - характерно снижение сердечного выброса (СИ менее 2,5) при повышении ОПСС. Характеризуется преимущественным повышением диастолическо-го АД.
Эукинетический тип - характеризуется увеличением АД на фоне нормального значения СИ (2,5-4,2).
На ранних стадиях развития ГБ и с целью выявления дизрегуляции сердечнососудистой системы может быть использована оценка реакции АД на физическую нагрузку.
Выделяют три типа реакций АД на физическую нагрузку:
Нормокинетический тип - повышение АД адекватно физической нагрузке, ОПСС - снижается, пульсовое АД увеличивается. АД повышается за счет систолического, в то время как диастолическое АД снижается. Повышение систолического АД всегда пропорционально данному виду физической нагрузки и имеет свои пределы (не выше 160 мм.рт.ст при нагрузке из расчета Шт на кг массы тела).
Гиперкинетический тип - неадекватное повышение АД при физической нагрузке при нормальном или сниженном ОПСС, пульсовое АД растет. АД растет за счет систолического, которое всегда увеличивается непропорционально данной физичекой нагрузке и его границы выше нормы. Диастолическое АД может не изменяться или повышается незначительно.
Гипокинетический тип - повышение АД неадекватно физической нагрузке. При этом УО снижен, ОПСС повышенно, пульсовое АД уменьшено. Повышение АД происходит за счет выраженного роста диастолического АД.
VI. Понятие артериальной гипотонии.
Артериальная гипотония характеризуется снижением артериального давления ниже 100/60 мм рт.ст. (для лиц в возрасте до 25 лет) и ниже 105/65 мм рт.ст. (для лиц старше 25 лет).
Гипотензия артериальная ортостатическая - снижение систолического артериального давления в ортостатическом положении на 20 мм рт.ст. и более.
/. Физиологическая артериальная гипотония - гипотония, обусловленная в основном конституциональными и наследственными факторами, встречается у совершенно здоровых людей, выполняющих обычную физическую работу, не сопровождается какими-либо жалобами и патологическими изменениями в организме. Известна физиологическая гипотония проходящего характера у спортсменов. П. Патологические артериальные гипотонии:
1. Гипотоническая болезнь (первичная артериальная гипотония, нейроциркуляторная дистония по гипотоническому типу, нейроциркуляторная гипотония) - заболевание, характеризующееся стойким снижением АД.
В основе первичной артериальной гипотонии лежит повышение тонуса парасимпатического отдела вегетативной нервной системы, нарушение функции высших вегетативных центров вазомоторной регуляции, ведущее к стойкому уменьшению общего периферического сопротивления току крови. Компенсаторное увеличение сердечного выброса в этих случаях оказывается недостаточным для нормализации артериального давления. Скорость кровотока при первичной хронической артериальной гипотонии обычно не
219
изменена. Объём циркулирующей крови находится в пределах нормы или несколько снижен, иногда имеется склонность к нормоволемической полицитемии.
Указанные сдвиги, возможно, обусловлены уменьшением глюкокортикоидной активности коры надпочечников при неизменной минералкортикоидной активности.
Основное значение в возникновении гипотонической болезни, по-видимому, принадлежит длительному психо-эмоциональному напряжению, в отдельных случаях - психической травме. По современным представлениям, первичная гипотония является особой формой невроза высших сосудодвигательных центров с нарушением регуляции сосудистого тонуса.
2. Вторичные (симптоматические) артериальные гипотонии:
По течению вторичные артериальные гипотонии могут быть классифицированы на острые и хронические формы.
Острые вторичные артериальные гипотензии рассмотрены в разделе «Экстремальные состояния» (шок, коллапс, синкопе).
Этиология хронических вторичных артериальных гипотензии:
Варикозное расширение вен нижних конечностей.
Беременность поздних сроков.
Полиурия.
Хроническая надпочечниковая недостаточность.
Длительный постельный режим.
Синдром гипербрадикинизма (отсутствуют киназы, расщепляющие брадикинин), наследственно обусловленный и приобретенный (при демпинг-синдроме). Ортоста-тическая гипотензия при гипербрадикинизме возникает после еды, способствующей освобождению кининов из стенки кишечника и поджелудочной железы, и сопровождается ярким покраснением лица вследствие действия кининов на сосуды кожи.
Нарушение дуги барорефлекса на различных уровнях (при сухотке спинного мозга, В^-дефицитной анемии, хроническом алкоголизме, сахарном диабете, сирингомие-лии, миелите, порфирии, полинейропатии Гийена-Барре).
Прием ганглиоблокаторов, изобарина, лабеталола, прозозина, нитратов.
3.8. Дыхательная недостаточность.
Внешнее (легочное) дыхание - совокупность процессов, совершающихся в легких и обеспечивающих нормальный газовый состав артериальной крови. Внешнее дыхание обеспечивается сочетанием трех процессов:
Легочная вентиляция - газообмен между атмосферой и альвеолярным пространством.
Диффузия газов в легких через альвеолярно-капиллярную мембрану - газообмен между кровью и альвеолярным пространством.
■Легочная перфузия - кровоток по малому кругу кровообращения.
Регуляция дыхания.
Основной мышцей, генерирующей отрицательное внутригрудное давление, является диафрагма. Диафрагма имеет фиксированную к ребрам и поясничным позвонкам мышечную часть и сухожильный центр, иннервируется диафрагмальными нервами (Сз-з). При сокращении она опускается вниз и оттесняет содержимое брюшной полости. Усиление вдоха осуществляется наруэюными меэюреберными мышцами, иннервация которых осуществляется межреберными нервами Т;.^, и вспомогательной мускулатурой (кива-тельная и лестничная мышцы), последняя наиболее значима при дыхательных нарушениях, выполнении физической нагрузки.
При спокойном дыхании выдох - пассивный процесс, основанный на эластическом восстановлении исходного состояния легких и стенки грудной клетки. При усиленной
220
вентиляции, например, при физической нагрузке, выдох становится активным за счет сокращения мышц брюшной стенки и внутренних межреберных мышц. Эти же группы мышц участвуют в феномене Вальсальвы.
В основе механизма регуляции дыхания лежит деятельность дыхательного центра головного мозга (ДЦ), которые формируют автоматическую дыхательную активность.
ДЦ - это группа нейронов (6 типов), расположенных в стволе мозга (продолговатый мозг и варолиев мост), обеспечивающих ритмическое чередование фаз дыхания. Пусковая регуляция их активности в основном принадлежит хеморецепторам. Этот уровень регуляции может быть подавлен волевым влиянием коры головного мозга. Примерами такого влияния могут быть управление дыханием, вздохи и подвздохи.
Основная часть дыхательного центра располагается на дне 4-го желудочка и состоит из двух групп нейронов: вдоха (дорсальная) и выдоха (вентральная). Нейроны вдоха включаются автоматически, нейроны выдоха - только при форсированном выдохе. Переключение дыхательных фаз обеспечивает рефлекс Геринга-Брейера - при растяжении легочной паренхимы возбуждаются рецепторы растяжения в трахее, бронхах и бронхиолах; афферентные волокна идут в составе блуждающего нерва в дыхательный центр. При растяжении мышечных веретен срабатывает рефлекс с межреберных мышц.
Еще два наиболее важных центра: апнойный - стимулирует вдох, и центр пневмоторакса - ограничивает вдох путем торможения активности группы нейронов дорсальной части.
Хеморецепторьц регулирующие процесс дыхания, располагаются как периферически, так и центрально (пневмотаксический центр).
В норме регуляция осуществляется центральными рецепторами продолговатого мозга, чувствительными к изменению концентрации ионов водорода и РаССЬ в ликворе. Этот рефлекторный акт очень чувствителен к малому повышению РаСОг и реализуется очень быстро.
Наружная
сонная артерия
X
Внутренняя
сонная
артерия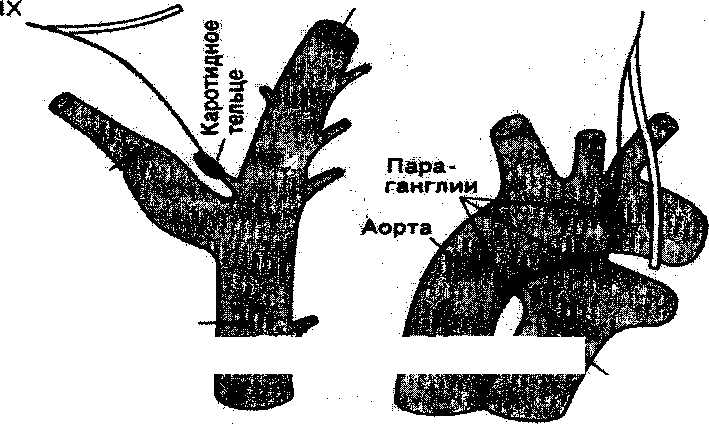
Об1ЩЯ
сонная
артерия __. _ _ _
Легочная артерия
Рис. 3.8.1. Каротидные (А) и аортальные (Б) тельца и отходящие от них афферентные волокна [по Шмидту Р. И Тевсу Г., 1996].
Существуют также и периферические хеморецепторьц которые располагаются в каротидном и аортальном синусах (рис. З.8.1.). Они чувствительны к повышению парциального напряжения в артериальной крови СО2 и снижению-О?. Афферентация от них идет по языкоглоточному нерву (IX пара черепных нервов от каротидных телец) и блуждающему нерву (X пара черепных нервов от аортальных телец).
221
Выраженность гипоксии, при которой С^-рецепторы значительно активируются, выходит далеко за рамки физиологических значений (снижении РаСЬ < 8 кРа или 60 мм
рт.ст.).
Барорецепторы в сосудах (дуга аорты и каротидный синус) возбуждаются при повышении АД. Происходит уменьшение глубины и частоты дыхания. Снижение АД сопровождается торможением задержки дыхания на вдохе, дыхание становится глубже.
В регуляции дыхания принимают участие гормоны. Адреналин и прогестерон увеличивают вентиляцию.
(. Классификация основных нарушений дыхания.
В клинической практике основные дыхательные нарушения описываются следующими терминами:
Эупное - нормальная вентиляция легких в покое.
Гипервентиляция ■- увеличение частоты (ЧД) и глубины дыхания при снижении РаСОг менее 40 мм рт.ст.
Гипоеентиляция - уменьшение частоты и глубины дыхания при увеличении РаСОг более 40 мм рт.ст.
Гиперпнбе - увеличение глубины дыхания независимо от изменений частоты дыхания.
Тохипное - увеличение частоты дыхания.
Апное -остановка дыхания.
Диспное - одышка, тягостное субъективное ощущение нехватки воздуха, отражающее восприятие повышенной работы дыхательной мускулатуры.
Ортопное - одышка в горизонтальном положении, требующая перехода в вертикальное положение.
Асфиксия - удушье.
■ Полипное - частое поверхностное дыхание.Патологические типы дыхания.

Схематическое изображение основных патологических типов дыхания представлено на рисунке 3.8.2.
Чейн^От:ок.са.
Громка
Виота
Куссмауля
А пней зис
Рис, 3.8.2. Патологические типы дыхания.
1. Периодические типы дыхания
■ Дыхание Чейна-Стокеа - паузы чередуются с дыхательными движениями, которые сначала нарастают по глубине, затем убывают.
222
Дыхание Грокка - поверхностное дыхание чередуется с дыхательными движениями, которые сначала нарастают по глубине, затем убывают.
Дыхание Биота (дыхание кластерного типа) - паузы чередуются с дыхательными движениями нормальной частоты и глубины,
В основе патогенеза периодического дыхания лежит понижение возбудимости ДЦЬ что может возникать при органических поражениях головного мозга - травмах, инсультах, опухолях, воспалительных процессах, диабетическом и уремическом ацидозе и др.
Предполагают, что на фоне пониженной возбудимости дыхательный центр не реагирует на нормальную концентрацию СОг и Н^-ионов в крови. Для возбуждения дыхательного центра требуются большие их концентрации. Время накопления этих раздражителей до пороговой дозы определяет длительность паузы. Дыхательные движения создают вентиляцию легких, СО2 вымывается из крови, дыхательные движения вновь прекращаются, либо их амплитуда снижается и т.д.
2. Терминальные типы дыхания
Дыхание Куссмауля - шумное глубокое дыхание; характерно для пациентов с нарушением сознания при диабетической, уремической комах. Дыхание Куссмауля возникает в результате нарушения возбудимости дыхательного центра на фоне гипоксии мозга, ацидоза, токсических явлений.
Апнейстическое дыхание характеризуется продолжительным судорожным усиленным вдохом, изредка прерывающимся выдохом. Такой вид дыхательных движений возникает в эксперименте после перерезки у животного обоих блуждающих нервов и ствола на границе между верхней и средней третью моста.
Гаспинг-дыхание (от англ. «§азр» - ловить воздух, задыхаться) возникает в самой терминальной фазе асфиксии: единичные глубокие, редкие, убывающие по силе «вздохи», длительная задержка дыхания на выдохе с редкими короткими вдохами. Источником импульсов при данном виде дыхательных движений являются клетки каудальной части продолговатого мозга при прекращении функции вышележащих отделов мозга вследствие недоношенности или повреждений мозга.
3. ТИПЫ ДИССОЦИИРОВАННОГО ДЫХАНИЯ • ^У^^ )А м, №) о—^1 <
■ Парадоксальные движения диафрагмы.
ш Асимметрии движения левой и правой половины грудной клетки.
■ «Атаксическое» уродливое дыхание Грокко-Фругони характеризуется диссоциациейдыхательных движений диафрагмы и межреберных мышц, наблюдается при нарушениях мозгового кровообращения, опухолях мозга и других тяжелых расстройствах нервной регуляции дыхания.
Дыхательная недостаточность (ДН) - патологическое состояние, развивающееся вследствие нарушения внешнего дыхания, при котором не обеспечивается поддержание адекватного условиям газового состава артериальной крови.
ДН по течению может быть классифицирована на острую и хроническую формы. А)Остра1яДН:
Умеренная (РаОг > 70 мм рт.ст.). ^
Средняя (Ра02 = 50-70 мм рт.ст.). ОнРог У/1ъ,е Сегч Ь*е//&
Тяжелая(Ра02< 50ммрт.ст.). л^. * с^ о>а^^ Б) Хроническая ДН: <^ ч. *^~
Компенсированная (НЬОаИ » 95%).
Субкомпенсированная (НЬ02 < 93%).
Декомпенсированная (НЬОг < 75%).
223
Патофизиологическая классификация нарушений внешнего дыхания.
1. Нарушения альвеолярной вентиляции:а) альвеолярная гиповентжяция
■ нарушение биомеханики дыхания (по обструктивному или рестриктивномутипу),
■ нарушение регуляции дыхания,Ъ) альвеолярная гипервентиляция
■ активная,■■ пассивная.
2. Нарушения перфузии легких:а) легочная гипертензия,
Ь) легочная гипотензия.
Нарушение вентиляционно-перфузионных отношений.
Нарушение диффузионной способности легких.
Смешанные нарушения.
Асфиксия (в переводе с греч..— «без пульса») - состояние гипоксии, сочетающееся с повьппением напряжения углекислого газа в крови и тканях, сопровождается тяжелыми расстройствами нервной, дыхательной, сердечно-сосудистой систем.
Механическая асфиксия возникает при наличии препятствия на пути поступления воздуха в дыхательные пути: воспалительные процессы (отек гортани, дифтерия), обтури-рующие и компрессирующие дыхательные пути опухоли, бронхоспазм, западение языка, аспирация инородных тел, воды, рвотных масс, пищи, крови и т.п. Стадии острой механической асфиксии:
Усиленная деятельность дыхательного центра (инспираторная одышка): возбуждение симпатической нервной системы (зрачки расширены, увеличение АД, ЧСС) демо-нохронизация на ЭЭГ.
Экспираторная одышка: АД увеличено, преобладание эффектов парасимпатической нервной системы (ЧСС снижается, регистрируются медленные высокоамплитудные сокращения - «вагус-пульс»; зрачки сужены), угнетение биотоков мозга.
Тормозной процесс: претерминальная остановка дыхания, АД начинает падать, угасают рефлексы, исчезают биотоки мозга.
Терминальное дыхание (гаспинг-дыхание): судороги, непроизвольное мочеиспускание и дефекация, понижение артериального и венозного давления, смерть от паралича дыхания, сердцебиение продолжается еще 5-8 мин.
//. Этиология и патогенез обструктивных и рестриктивных типов нарушения вентиляции легких. Легочное сердце.
Для осуществления эффективной легочной вентиляции необходимо два условия:
■ беспрепятственное прохождение воздуха по бронхиальному дереву до респираторного отдела легких;
■ наличие достаточного количества альвеол, способных к газообмену*Соответственно этим положениям выделяют два типа нарушения вентиляции легких.
Обструктивный тип связан с нарушением прохождения воздуха по бронхиальному дереву.
Причины бронхообструщии:
спазм гладкой мускулатуры бронхов,
воспалительная инфильтрация и отек слизистой бронхов,
гиперсекреция слизи,
врожденная и приобретенная деформация бронхов (бронхоэктатическая болезнь),
обтурация бронхов (кровь, экссудат, опухоли, инородные тела),
224
■ экспираторным коллапсом мелких бронхов (компрессия мелких бронхов на выдохепри затрудненном выдохе) при бронхитах, бронхиальной астме, эмфиземе легких.Рестриктивный тип связан либо с уменьшением суммарной площади альвеоляр-
но-капиллярного газообмена, либо со снижением способности легочной ткани к растяжению и расправлению при дыхании (чаще всего эти две причины взаимосвязаны).
Причины рестриктивных нарушений альвеолярной вентиляции; 1. Собственно заболевания органов дыхания:
* инфильтративные изменения легочной ткани,
пневмосклероз,
эмфизема легких (деструкция межальвеолярных перегородок, переполнение легких воздухом, сдавление бронхов на выдохе),
уменьшение объема функционирующей паренхимы легкого (резекция легкого, ателектаз, врожденная гипоплазия легкого, заболевания плевры, ограничивающие экскурсию легкого).
2 Внелегочные нарушения:
деформация грудной клетки и позвоночника,
нарушения деятельности дыхательной мускулатуры,
венозная гиперемия легких при левожелудочковой недостаточности, я увеличение объема брюшной полости,
болевой синдром, приводящий к ограничению подвижности диафрагмы.
При заболеваниях органов дыхания имеется, как правило, сочетание обструктивных и рестриктивных нарушений - комбинированная вентиляционная недостаточность с преобладанием одной из форм. Выделение этих форм помогает понять ведущий механизм вентиляционной недостаточности и назначить патогенетически обоснованное лечение. Легочное сердце - гипертрофия правого желудочка при заболеваниях легких. Синдром легочного сердца развивается при ухудшении аэрации альвеол —> срабатывает рефлекс Эйлера (при нарушении вентиляции альвеол развивается спазм легочных артериол) ~> перегрузка ПЖ давлением -> гипертрофия ПЖ.
///. Расстройства альеволярной вентиляции, обусловлвнныв нарушениями регуляции дыхания. Альвеолярная гипервентиляция. А) Нарушения акта вдоха.
Причины нарушения акта вдоха:
1. Дефицит возбуждающей афферентации.
Синдром асфиксии новорожденных - незрелость хеморецепторов у недоношенных детей. Для дополнительной стимуляции дыхательного центра используют похлопывание по ягодицам, обрызгивание холодной водой.
Синдром Пиквика - сонливость с гицовентиляцией и апное вследствие снижения тонуса ретикулярной формации и повышения порога возбудимости центральных хеморецепторов.
2. Избыток тормозной афферентации.
Остановка дыхания на вдохе при раздражении слизистой верхних дыхательных путей, например, при остром респираторном заболевании, действии химических и механических агентов (срабатывает тормозной тригемино-вагусный рефлекс Кречме-ра\
Сильные болевые ощущения, сопровождающие акт дыхания (травма грудной клетки, плеврит, воспаление дыхательных мышц).
3. Избыток возбуждающей афферентации.
а) «Перевозбуждение» ДЦ может характеризоваться развитием альвеолярной гипо-вентиляция при тахипноэ, что является следствием увеличения функционального мертвого пространства (стрессорные воздействия; некоторые поражения структур
225
среднего
мозга воспалительного, травматического,
опухолевого генеза; нарушения мозгового
кровообращения и др.) Ь)
Избыток
афферентации рефлекторного происхождения
иногда
возникает при раздражении
брюшины, термических или болевых
воздействиях на кожные покровы.
4. Хаотическая
афферентация.
Поступление к ДЦ и мотонейронам дыхательных мышц различных афферентных влияний, имеющих неупорядоченный характер по критерию обеспечения газбоб-менной функции легких, что возможно во время пения, игры на духовых инструментах, у стеклодувов и т.д.
Формирование мощных потоков афферентной импульсации различной модальности (болевой, психогенной, хеморецепторной, барорецепторной и др.) и нарушающие дыхательного ритмогенеза (обширные травмы, ожоги, острый период ИМ и
ДР-)-Б) Патология дыхательного центра*
Причины повреждения ДЦ: энцефалиты, нарушения мозгового кровообращения,
опухоли, травмы, токсические воздействия на головной мозг.
Патология ДЦ проявляется патологическими типами дыхания (см. выше).
В) Патология эфферентных путей. _
Причины формирования дефектов в эфферентных путях:
Травмы шейного отдела спинного мозга - сохраняется естественное диафрагмальное дыхание, но нарушается иннервация дыхательных межреберных мышц.
Повреждение диафрагмальных мотонейронов (при сирингомиелии, рассеянном склерозе, полиомиелите) - сохраняется только произвольное дыхание. Формируется синдром "проклятия Ондины'* - отсутствие непроизвольного дыхания, остановка дыхания при засыпании. Синдром идиопатической гиповентиляции (синдром Ондины) проявляется сонливостью, головными болями, ночным апное, одышкой при физической нагрузке, правожелудочковой СН, болеют преимущественно молодые мужчины.
Повреждение в области Ы-холинорецепторов: ятрогенное - при передозировке миоре-лаксантов; при миастении - слабость дыхательных мышц из-за врожденного или аутоиммунного повреждения И-холинорецепторов.
Г) Миогенные расстройства.
Причины повреждения дыхательной мускулатуры:
Мышечные дистрофии (дистрофия Дюшена).
Миозиты.
Альвеолярная гипервентиляция
2. Пассивная гипервентиляция обусловлена неправильным подбором режима искусственной вентиляции.
2. Активная гипервентиляция обусловлена избытком афферентации:
психогенная (истерия),
церебральная (опухоли и т.д.),
рефлексогенная (травмы).
226
IV.
Нарушения
перфузии легких, вентиляционно-перфузионных
отношений, диффузионной способности
легких. Нарушение
перфузии легких.
1. Легочная гипертензия:
а) Прекапиллярная форма
Тромбоэмболия легочной артерии (ТЭЛА),
Рефлекс Эйлера (снижение рОг в альвеолах ведет к гипоксической вазоконст-рикции)
Ь) Посткапиллярная форма (застой крови) при левожелудочковой недостаточности
(митральный стеноз, кардиосклероз, ГБ,ИМ). с) Смешанная форма
Рефлекс Китаева при сердечной недостаточности (повышение давления в ЛП -» спазм легочных артериол).
ДМЖП и ДМПП со сбросом крови слева направо.
2. Легочная гипотензия (коллапс, шок, пороки Фалло) (см. темы «Экстремальные состояния», «Сердечная недостаточность).
Нарушение вентиляционно-перфузионных отношений.
Соотношение между вентиляцией и кровотоком принято характеризовать с помощью так называемого показателя вентиляционно-перфузионных отношений (Уд/От)? который в норме равен 0,8-4 А что отражает адекватность минутного объема альвеолярной вентиляции минутному объему кровотока в легких.
Снижение показателя вентиляционно-перфузионных отношений наблюдается при локальной альвеолярной гиповентиляции: расстройства обструктивного типа, нарушения эластичности легочной ткани, локальное неравномерное действие сил вдоха и выдоха, парадоксальное или маятникообразное дыхание при одностороннем параличе диафрагмальной мышцы, легочно-плевральных сращения, деформация грудной клетки.
Увеличение показателя вентиляционно-перфузионных отношений наблюдается при локальной закупорке, стенозе (облитерации) или спазме сосудов системы легочной артерии.
Нарушение диффузионной способности легких,
В таблице 3.8.1. представлены показатели, характеризующие нормальное содержание кислорода и углекислого газа в воздухе и крови.
Диффузия газов в легких осуществляется в соответствие с законом Фика.
Закон диффузии Фика: диффузионный поток прямо пропорционален градиенту концентрации веществ.
Коэффициент диффузии для СО2 в 23 раза больше, чем для Ог':
Диффузионная способность легких (В), в норме равна 30 мл/мин.мм рт.ст.
У02
Б-
АР02
Уо2 - количество поглощенного кислорода,
А Ро2 - средний градиент парциального давления 02 между альвеолярным пространством и кровью легочных капилляров.
Эффективность газообмена в альвеолах ВАЗ, где <3 - показатель легочной перегрузки.
227
Таблица 3.8.1. Нормальное содержание кислорода и углекислого газа в воздухе и крови
|
|
02, мм рт.ст |
С02, мм рт.ст |
|
Атмосферный воздух |
150 |
0,2 1 |
|
1 Альвеолярный воздух |
100 |
40 |
|
Выдыхаемый воздух |
114 |
29 |
|
Артериальная кровь |
100 |
40 |
|
Венозная кровь |
40 |
46 |
Причины нарушения диффузии:
Диффузный фибрдзирующий алъвеблит (болезнь Хаммана-Рича).
Недостаток сурфактанта (синдром гиалиновых мембран у новорожденных).
Пневмокониоз (силикоз, асбестоз, бериллиоз) - фиброз легких в результате длительного вдыхания пыли.
Воспалительные и токсические поражения.
V. Оценка нарушений внешнего дыхания. Основные методы оценки внешнего дыхания
Статические легочные объемы за исключением ОЕЛ могут быть измерены методом спирографии или спироанализа (пневмотахографии). Часть динамических легочных объемов (МОД, ФЖЕЛ, МВД) можно получить при помощи спирографии. Однако наиболее информативные показатели объемной скорости дыхания (ПОС, МОС25-75 и др.) получают методом спироанализа. Пиковую объемную скорость выдоха можно измерить так же при помощи пикфлуометра - портативного прибора для самоконтроля больных с обструктив-ными заболеваниями легких.
Спироанализ в настоящее время является основным, высокоинформативным рутинным методом исследования внешнего дыхания и практически вытеснил традиционную спирографию. Спироанализаторы являются приборами открытого типа (вдох осуществляется из атмосферы), что позволяет использовать их для проведения функциональных ингаляционных проб. Еще одним преимуществом спироанализаторов является автоматическая коррекция дыхательных объемов в зависимости от температуры окружающей среды и атмосферного давления в системе ВТР8 (Воду ТетрегаШге Ргеззиге 8а1ига1ед - температура 37° С, атмосферное давление и полное насыщение водяными парами), что позволяет стандартизовать результаты измерений, выполненных в различных условиях. Спироанализаторы, как правило, компьютеризированы и осуществляют автоматическое измерение необходимых параметров, а так же их сопоставление с должными величинами.
Бронхиальное сопротивление может быть измерено при помощи спироанализатора оснащенного специальным устройством или методом бодиплетизмографии. Последний требует дорогостоящего оборудования и используется только специализированными крупными клиниками и отделениями. Бодиплетизмография позволяет так же измерить общую емкость легких и остаточный объем.
Для оценки диффузионной способности легких необходим газоанализатор гелия и СО. Эта методика используется только в специализированных клиниках.
Основные показатели функции внешнего дыхания.
1. Статические объемы:
Жизненная емкость легких (у&а! сараску, ЖЕЛ, УС) - это разница легочного объема при состоянии полного выдоха и полного вдоха. Она включает в себя дыхательный объем (ДО, ТУ, VI), резервный объем вдоха (РОвд., 1КУ) и резервный объем выдоха (Ровыд.,ЕКУ).
Резервный объем выдоха (РОвыд., ЕКУ) - это максимальный объем, который может выдохнуть обследуемый, начиная с уровня функциональной остаточной емкости легких (ФОБ, РКС). Как самостоятельный показатель используется редко.
228
Резервный объем вдоха (РОвд., 1КУ) - это объем, который способен вдохнуть исследуемый после среднего спокойного вдоха.
Емкость вдоха (1С) - это максимальный объем, который может вдохнуть исследуемый от уровня ФОБ; равняется сумме дыхательного объема и резервного объема вдоха. Дыхательный объем (ДО, V*, ТУ) - это объем газа, который вдыхается и выдыхается во время дыхательного цикла при спокойном дыхании. ДО должен рассчитываться как средняя величина после регистрации по меньшей мере шести дыхательных циклов. Функциональная остаточная емкость (ФОБ, РКС) - это объем газа в легких и дыхательных путях после спокойного выдоха; сумма резервного объема выдоха и остаточного объема.
Остаточный объем (ОО, КУ) - это объем газа, который остается в легких по окончании полного выдоха.
Общая емкость легких (ОЕЛ, ТЬС) - это объем газа в легких по окончании полного вдоха.
Внутригрудной объем (ВГО,ТОУ) - это объем газа в грудной клетке. Обычно ВГО определяется бодиплетизмографическим методом. Основные статические объемы представлены на рисунке 3.8.3.
!
Емкость
вдоха
Функциональная
1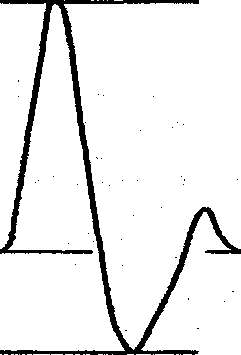
38 о
т
Резервный объем вдоха
/Дых, объем/ \ 1 \
