
- •Содержание
- •Часть 1. Предмет патологии. Учение о болезни (Куликов в.П., Доронина н.Л.)... 8
- •Часть 2. Механизмы развития болезней (Куликов в.П., Доронина н.Л.) 15
- •Часть 3* Патология органов и систем (Куликов в.П., Доронина н.Л.) 157
- •Часть 4. Ситуационные задачи (Куликов в.П., Костюченко л.А., Доронина н.Л,
- •Часть 5. Тестовые задания (Куликов в.П., Костюченко л.А., Воронцов в.В.,
- •Часть 6. Задания для подготовки к занятиям. Вопросы к экзамену (Куликов в.П.,
- •Часть 1. Предмет патологии. Учение о болезни.
- •I. Предмет патологии.
- •IIII Понятие болезни. Патологические реакции, процессы, состояния. Симптом и синдром. Классификация, стадии развития и исходы болезней.
- •IV. Умирание. Терминальные состояния.
- •VI. Патогенез заболеваний. Саногенез.
- •VII. Лечение заболеваний
- •Часть 2. Общая патология. 2.1 .Повреждение клетки.
- •IV. Общий адаптационный синдром. Схема развития симпато-адреналовой и гипоталамо-гипоФизарно-адреналовой реакций при стрессе. Стресс-реализующие и стресс-лимитирующие системы.
- •Стадии стресса или общего адаптационного синдрома:
- •V. Дистресс Болезни адаптации. Ятоогенные осложнения вследствие использования аналогов стресс-реализующих гормонов.
- •IV. Механизм Формирования патологии у плода при алкоголизме беременной женщины.
- •V. Методы изучения наследственных болезней.
- •2.4. Нарушение регионального кровообращения. Тромбозы и эмболии.
- •7. Характер движения крови по сосудам:
- •IV. Виды региональных нарушений кровообращения и их механизмы. Сладж-Феномен.
- •V. Методы оценки сосудистой гемодинамики.
- •2.5. Патология гемостаза.
- •V. Гипокоагуляиии. Связанные с дефицитом плазменных прокоагулянтов
- •2.6. Гипоксия.
- •I. Понятие гипоксии.
- •V. Адаптивные реакции организма: срочные и долговременные (дыхательные, гемодинамические, гемические, тканевые). Срочная адаптация к гипоксии (или 1-ая стадия долговременной адаптации)*
- •2.7. Патофизиология боли.
- •II. По характеру:
- •III. Понятия обморока и коллапса. Отличия от шока.
- •IV. Кома. Этиология и патогенез отдельных видов ком (печеночная, уремическая, диабетическая).
- •2.9. Воспаление.
- •III. Стадии опухолевого роста.
- •IV. Свойства опухолевого роста.
- •V. Опухолевые маркеры. Механизмы изменения иммунного надзора при
- •2.13. Патология углеводного обмена. Сахарные диабеты.
- •IV. Нарушение платочного метаболизма липидов. Жировая инфильтрация органов.
- •V Этиология и патогенез атеросклероза. Стадии развития атеросклероза и осложнения.
- •2.15. Патология белкового обмена.
- •IV. Вторичные нарушения обмена аминокислот. Патология конечных этапов белкового обмена, роль печени и почек е метаболизме аммиака. Нарушение обмена пуриновых и пиримидиноеых оснований.
- •Часть 3. Патология органов и систем. 3.1. Патология красной крови.
- •IV. Этиология и патогенез гемолитических анемий.
- •2. Липидзависимые мембранопатии:
- •3. Ферментопатии:
- •4. Гемоглобинопатии:
- •V. Этиология и патогенез дизэритропоэтических анемий.
- •VI. Компенсаторные реакции организма при анемиях.
- •3.2. Лейкоцитозы и лейкопении. Лейкозы.
- •I. Лейкоцитозы.
- •IV. Лейкемоидные реакции. Виды. Причины возникновения.
- •V. Лейкозы. Общая характеристика,
- •I. По виду клетки-«родоначальницы» лейкоза:
- •VI. Лабораторная характеристика лейкозов. Отличия лейкозов от лейке-моидных реакций.
- •VII. Общие изменения е организме при лейкозах.
- •3.3. Сердечная недостаточность.
- •2. Гипертрофия левого предсердия
- •1. Гипертрофия правого желудочка
- •2. Гипертрофия левого желудочка
- •1, Нервная регуляция.
- •1А} Норма
- •IV, Диагностика аритмий.
- •3.7. Патология артериального давления и сосудистого тонуса.
- •Резервный
- •VI. Компенсаторные процессы при недостаточности внешнего дыхания.
- •IV. Расстройства функции тонкого и толстого кишечника: секреции, переваривания, всасывания и моторики.
- •1. Усиление перистальтики кишечника.
- •2. Ослабление перистальтики кишечника.
- •V. Нарушение барьерной функции кишечника. Дисбактеоиоз.
- •I Повышение проницаемости мембранПовреждение мембран клеток с их частичной или полной деструкцией
- •Часть 4. Ситуационные задачи.
- •Часть 5. Тестовые задания.
- •Часть 6. План практических занятий. Вопросы к экзамену. 6.1. План практических занятий по патофизиологии.
IV. Вторичные нарушения обмена аминокислот. Патология конечных этапов белкового обмена, роль печени и почек е метаболизме аммиака. Нарушение обмена пуриновых и пиримидиноеых оснований.
Нарушение переаминирования.
Недостаточность в организме витамина В6 (фосфорилированная форма витамина Вб - фосфопиродоксаль - является активной группой трансаминаз - специфических ферментов переаминирования между амино- и кетокислотами). Беременность, голодание, заболевания печени, длительный прием сульфаниламидов оказывают тормозящий эффект на синтез витамина В6 и могут послужить основой нарушения обмена аминокислот.
Патологическое усиление реакции переаминирования возможно в условиях повреждения печени и инсулиновой недостаточности, когда значительно увеличивается содержание свободных аминокислот.
Нарушение синтеза трансаминаз (при белковом голодании).
Нарушение гормональной регуляции активности трансаминаз (глюкокортикоиды и тиреоидные гормоны стимулируют трансаминирование).
При некрозах отдельных органов (миокард, легкие, поджелудочной железы, печень) наблюдается выход трансаминаз в кровь, что имеет диагностическое значение. Нарушение дезаминирования
Ослабление может возникнуть вследствие нарушения окислительных процессов в тканях (гипоксия, гиповитаминозы С, В6 (пиродоксин), В2 (рибофлавин), РР (никотиновая кислота)).
Понижение активности аминооксидаз вследствие ослабления их синтеза (диффузное поражение печени, белковая недостаточность).
■ Понижение активности аминооксидаз вследствие относительной недостаточностиих активности (увеличение содержания в крови свободных аминокислот).Следствием нарушения окислительного дезаминирования аминокислот будет ослабление мочевинообразования, увеличение концентрации аминокислот (гипераминоаци-демия) и увеличение выведения их с мочой (аминоацидурия).
Гипераминоаиидемия - повышение концентрации аминокислот в крови.
Аминоаиидурия - повышение содержания аминокислот в моче.
Патология конечных этапов белкового обмена.
Азотистые продукты конечных этапов белкового обмена: мочевина, аммиак, мочевая кислота, креатинин, индикан.
Состав остаточного азота (норма 20-30 мг%): на 50% состоит из азота мочевины, ОКОЛО 25% его приходится на долю аминокислот, остальная часть приходится на различные азотистые продукты.
Немочевинную часть называют резидуалъным азотом.
Гиперазотемия - увеличение остаточного азота в крови.
Печеночная или продукционая азотемия связана с недостаточным образованием в печени мочевины. В этих случаях увеличивается количество резидуального азота.
Почечная или ретенционная азотемия обусловлена нарушением выделительной функции почек. Увеличивается содержание остаточного азота за счет азота моче-вины.
Механизмы цитопатогенного действия аммиака и пути его обезвреживания.
Катаболизм аминокислот в тканях происходит постоянно со скоростью ~ 100 г/сут. При этом в результате дезаминирования аминокислот освобождается большое количество аммиака. Значительно меньшее его количества образуется при дезаминировании биоген-
137
ных аминов и нуклеотидов. Механизм токсического действия аммиака на организм в целом связан со снижением скорости реакций в цикле трикарбоновых кислот (следствие -дефицит макроэргов), угнетением обмена аминокислот (реакции трансаминирования) и синтеза из них нейромедиаторов.
Аммиак в крови при рН=7,4 существует почти целиком в виде NН4+. Повышение в крови концентрации аммиака вызывает алкалоз, увеличивает сродство гемоглобина к кислороду, что потенцирует гипоэргическое состояние. Высокие концентрации аммиака стимулируют синтез глутамина из глутамата в нервной ткани, накопление которого в клетках нейроглии приводит к повышению осмотического давления и может спровоцировать отек мозга. Снижение концентрации глутамата нарушает обмен аминокислот и нейромедиаторов, в частности гамма-аминомасляной кислоты, в результате чего нарушается проведение нервного импульса, возникают судороги. Ион NH4+ практически не поникает через цитоплазматические и митохондриальные мембраны. Избыток иона аммония способен нарушить трансмембранный перенос Nа+ и К+, в результате конкуренции за ионные каналы, что влияет на возбудимость тканей.
Пути обезвреживания аммиака.
Восстановительное аминировние происходит в малом объеме и не имеет существенного значения в механизмах детоксикации.
Образование амидов аспарагиновой и глутаминовой кислот (аспарагина и глутамина) осуществляется в основном в нервной ткани.
Образование солей аммония происходит в почечной ткани: доставляемые с кровью амиды аспарагиновой и глутаминовой кислот гидролизуются под действием глутами-назы и аспарагиназы, образуя аспартат и глутамат с высвобождением аммиака, который нейтрализуется путем образования солей аммония, в частности хлорида аммония, удаляемых с мочой.
Основной путь - синтез мочевины, осуществляемый в печени в орнитиновом цикле. Нарушение обмена пуриновых и пиримидиновых оснований.
Конечным продуктом пуринового обмена является мочевая кислота. Гиперурике-мия - избыточное содержание мочевой кислоты в плазме крови.
Типичное заболевание, связанное с гиперурикемией, - подагра. Заболевание сопровождается кристаллизацией мочевой кислоты в мезенхимальных тканях и синоваиль-ной жидкости.
Гиперурикемия возникает в результате избыточного образования или снижения экскреции мочевой кислоты, либо сочетания этих двух процессов.
Первичная гиперурикемия развивается вследствие врожденных дефектов метаболизма (недостаточности гипоксантинфосфорибозилтрансферазы или повышенной активности 5-фосфорибозил-1-пирофосфат-синтетазы), снижения содержания в крови уратсвя-зывающего белка.
Вторичная гиперурикемия обусловлена увеличением скорости биосинтеза пуринов (гликогеноз I типа, миело- и лимфопролиферативные нарушения, некоторые гемоглобинопатии, пернициозная анемия, инфекционный мононуклеоз, некоторые карциномы), либо уменьшения экскреции мочевой кислоты вследствие повреждения почек, лечения диуретиками и др.
Непосредственным токсическим действием на клетки мочевая кислота не обладает. Все проблемы от повышения ее плазменной концентрации возникают вследствие нарушения растворимости в водных средах организма. Степень растворимости в воде прямо пропорциональна степени ионизации молекулы. Попадая в кислую среду (соединительная ткань богата кислыми продуктами - глюкуроновая, хондроитинсерная кислоты; моча при снижении величины рН), мочевая кислота выпадает в осадок, вызывая появление симптоматики полиартрита и мочекаменной болезни.
Нарушение приримидинового обмена проявляется в виде оротатацидурии (повышенное выделение с мочой оротовой кислоты), причиной которой является дефицит
138
дегидрогеназы, катализирующей две последние стадии синтеза уридинтрифосфата. Недостаток уридинтрифосфата приводит к отставанию в физическом и умственном развитии.
V. Нарушения белкового состава плазмы крови.
Сведения о суммарном количестве белков плазмы (общий белок крови) получают обычно рефрактометрическим и фотометрическим биуретовыми методами. Плазма крови человека в норме содержит более 100 видов белков. Нормальная концентрация общего белка в плазме крови - 65-85 г/л. Фракционный анализ белков крови проводят при помощи электрофореза. Важнейшие белковые фракции плазмы:
Преальбумины - выполняют преимущественно транспортную функцию (перенос тироксина, витамина А). Нормальные величины - ОД 8 - 0,37 г/л.
Альбумиы - связывают и транспортируют воду, магний, кальций, билирубин, жирные кислоты, многие лекарственные вещества (антибиотики, барбитураты, сердечные гликозиды и др.). Известно более 20 генетических вариантов альбумина, что никак не связано со склонностью к заболеваниям, но может проявляться расслоением альбуминовой фракции при электрофорезе на две, или более полосы (бисальбуминемия). Наследственное отсутствие альбумина (анальбуминемия) может проявляться склонностью к отекам. Нормальное содержание альбумина в плазме крови - 37 - 55 г/л.
-a1 глобулины. Основные белки этой фракции - a1 антитрипсин, гликопротеиды, липопротеиды, серомукоид.
a1-антитрипсин - глобулин, на долю которого приходится около 80% антипроте-азной активности крови. Это основной ингибитор трипсина, химотрипсина, плазмина, калликреина, ренина. Важнейший клинически значимый эффект a1- антитрипсина - подавление активности лейкоцитарной эластазы. a1- антитрипсин - белок острой фазы, его выработка увеличивается при реакциях, запускаемых через фактор ФНО, ИЛ1 ИЛ6. Нормальные величины -1,4 - 3,2 г/л.
- a2 - глобулины. Основные представители этой фракции - a2- макроглобулин,гаптоглобин, церулоплазмин.
а2-макроглобулин - гликопротеид, ингибитор протеаз. Включается в инактивацию протеаз после истощения других ингибиторов, обладающих более высоким сродством к соответствующим ферментам, сх2-макроглобулин инактивирует плазменный каллик-реин и компоненты системы комплемента. Синтез данного белка происходит в основном в печени. При гипоальбуминемйи компенсаторно повышается синтез a2-макроглобулина в печени, что приводит к увеличению a2-фракции на электрофореграмме. Нормальные величины - 1,5 - 2,4 г/л.
Гаптоглобин. Его значение может заключаться в связывании свободного гемоглобина в сыворотке при ДВС - синдроме и предохранении организма от потери железа. Нормальные величины - 0,5 - 3,5 г/л.
Церулоплазмин - медьсодержащий a2-гликопротеид. Церулоплазмин окисляет Ре до Fе3+, что обеспечивает транспорт железа трансферрином; активирует окисление аскорбиновой кислоты, катехоламинов, серотонина и сульфгидрильных соединений, ликвидирует супероксидрадикалы кислорода, предотвращая окисление полиеновых кислот. Нормальные величины - 0,25 - 0,45 г/л.
-b-глобулины. Основные представители - трансферрин и гемопексин. Трансферрин - гликопротеид, основной переносчик железа к клеткам. Измерение
трансферрина в плазме используется для дифференциальной диагностики анемий и для мониторинга их лечения. В норме железом насыщается 1/3 имеющегося в крови трансферрина. При более высоком насыщении трансферрина железо связывается и с другими протеинами сыворотки. Нормальные величины - 2 - 4 г/л.
139
Гемопексин связывает гем, порфирин и гемсодержащие хромопротеиды (гемоглобин, миоглобин, каталазу), доставляя их в печень. Распад комплексов гемопексина происходит в печени, где железо может быть повторно использовано. Нормальные величины -0,6-1,2 г/л.
- у-глобулины - иммуноглобулины сыворотки крови. Различаются 5 основных классов иммуноглобулинов (А, М, О, Е, О). Внутри класса возможны различия, обусловленные структурой цепей. Парапротеины - это иммуноглобулины с измененной структурой, или их фрагменты. Парапротеины часто не способны адекватно выполнять функцию антител.
Гипопротеинемия - снижение концентрации общего белка в крови. Причины; голодание, нарушение всасывание белков, заболевания печени, кровопотеря и др.
Следует различать абсолютную гипопротеинемию (например, при увеличенном выделении белка почками, нарушении протеосинтеза при циррозе печени и др.). Относительная гипопротеинемия возможна в результате избыточного введения кровозаме-нителей, при значительном уменьшении выделения мочи (олигоурия, анурия).
Гиперпротеинемия - повышение концентрации общего белка в крови. Основные причины повышения общего белка в крови - уменьшение обьема плазмы при дегидратации и повышение синтеза отдельных белков. В связи с этим различают абсолютную ги-перпротеинемию (например, при повышении синтеза и, следовательно, концентрации иммуноглобулинов), и относительную (например, при дегидратации).
Парапротеинемия - появление в крови нехарактерных (патологических) белков. Парапротеины принадлежат к фракции гамма-глобулинов. Например, при миеломной болезни наблюдается неконтролируемый синтез легких цепей гамма-глобулинов. При это^ развивается гиперпротеинемия, которая превышает порог реабсорбции белка в почечных канальцах, вследствие небольшого молекулярного веса, легкие цепи появляются в моче (белок Бенс-Джонса). На электрофореграмме белков плазмы, а также мочи это характеризуется появлением нетипичной белковой фракции, обозначаемой как М-протеины.
Диспротеинемия - нарушение нормального соотношения белковых фракций крови. Снижение альбуминов наблюдается при кахексиях, нефротическом синдроме, инфекционном воспалении, циррозе печени. Увеличение алъфа-2-глобулиновой фракции наблюдается при острых инфекциях, некрозах, остром ревматизме, злокачественных новообразованиях. Бета-глобулиновая фракция возрастает при подпеченочной желтухе, гепатитах, нефротическом синдроме. Гамма-глобулины увеличиваются при хроническом воспалении, хронических полиартритах, циррозе печени, миеломной болезни. Снижение этой фракции отмечается при наследственной патологии (болезнь Брутона).
Диспротеинемии возникают чаще всего при нарушении функции печени, почек, воспалительных заболеваниях и злокачественных новообразованиях. При остром воспалении отмечается увеличение в плазме крови альфа-2-глобулиновой фракции и несколько позже гамма-глобулинов. Для хронического воспаления характерно увеличение гамма-глобулинов, которое может сочетаться с незначительным увеличением альфа-глобулинов и снижением альбуминов. В период обострения воспаления наблюдается значительный прирост альфа-2-глобулйнов, например, при ревматизме. Острый гепатит характеризуется незначительным уменьшением альбуминов и увеличением в крови бета- и гамма-глобулинов. При хроническом гепатите и циррозе печени наблюдается значительное снижение концентрации альбуминов, сочетающееся с увеличением гамма-глобулинов. При злокачественных опухолях внепеченочной локализации количество альбуминов снижается на фоне увеличения альфа-2-глобулиновой фракции, а затем бета и гамма-глобулинов.
140
2.16. Патология водно-солевого обмена и кислотно-основного равновесия.
А) Патология водно-солевого обмена.
Водно-электролитный обмен - это совокупность процессов поступления, всасывания, распределения и выделения из организма воды и электролитов. Он обеспечивает постоянство ионного состава, кислотно-основного равновесия и объема жидкостей внутренней среды организма. Ведущую роль в нем играет вода.
Функции воды:
внутренняя среда организма;
структурная;
всасывание и транспорт веществ;
участие в биохимических реакциях;
конечный продукт обмена;
выделение при участии почек конечных продуктов обмена. Распределение воды:
1. Внеклеточное пространство - 27%:
а) экстравазалъная жидкость - 19-21%, (жидкость соединительной ткани - 4-
5%, костной - 4-5%, интерстициальная -10-12%); Ь) интравазальная жидкость - 5-7%, (жидкость кровеносных сосудов - 4-5%,
лимфатических сосудов -1-2%)
Трансцеллюлярная жидкость - 1-2% (плевральная, брюшной полости, суставов, лик-вор, секреты желез).
Внутриклеточное пространство -71 -72%.
В среднем вода составляет 45-65% от массы тела, но содержание ее в организме варьирует в зависимости от органов и тканей. Мозг - 70-84%, почки - 82%, сердце и легкие - 79%, мышцы - 76%, кожа - 72%, печень - 70%, костная ткань - 10%.
Вода, которая поступает алиментарным (с пищей) путем называется экзогенной, а образовавшаяся в качестве продукта биохимических превращений - эндогенной.
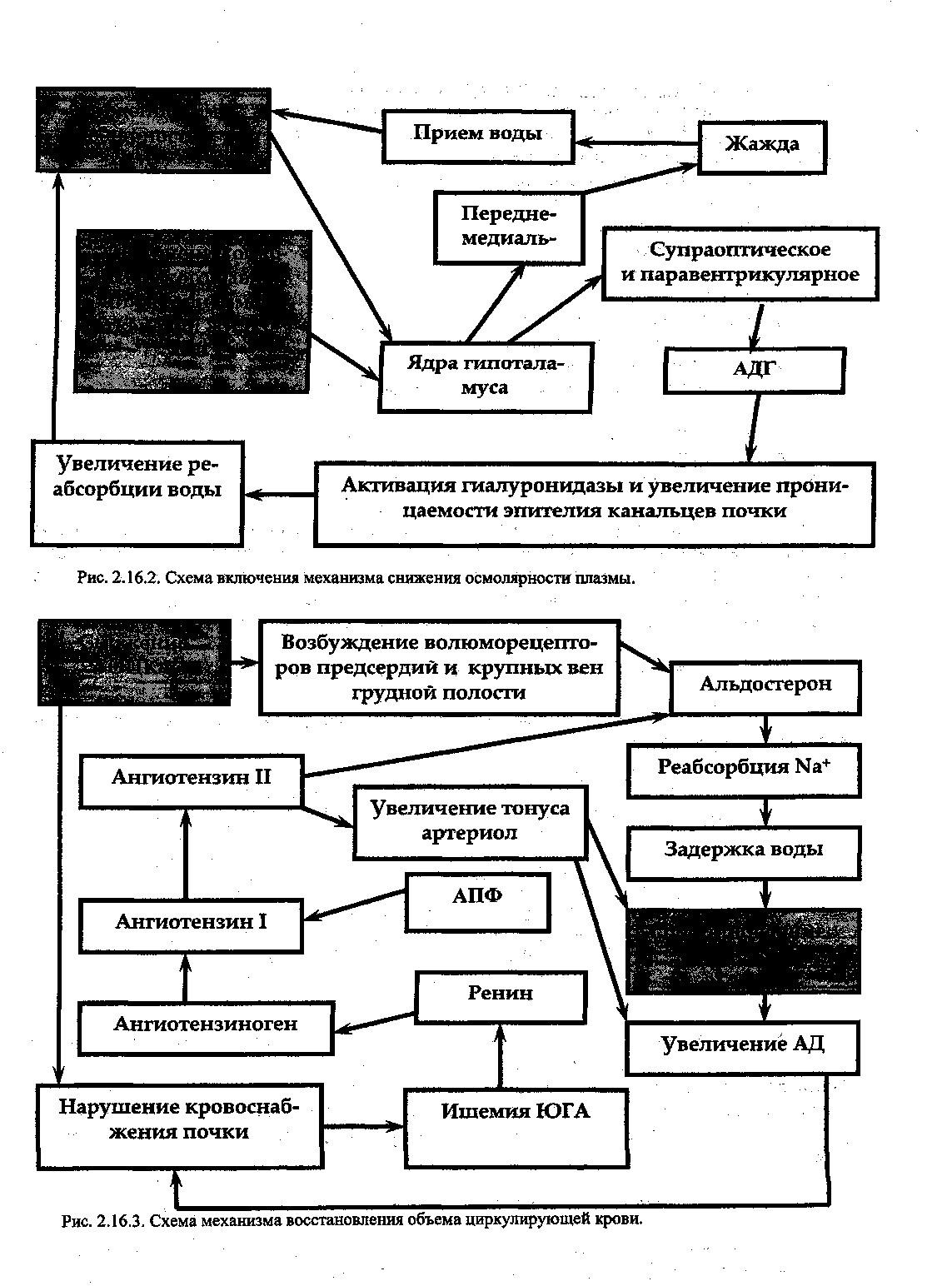
Содержание воды регулируется чувством жажды, которое появляется вследствие гиповолемии и увеличения осмолярности биосред (рис. 17.2., 17.3.).
Обычно суточная потребность человека в жидкости не превышает 2,5 л. Этот объем складывается из воды, входящей в состав пищи (около 2,5 л) и оксидационной воды, образующейся при окислении главным образом жиров (0,3-0,4 л.).
Минимальная потребность организма ъ воде складывается из 400-500 мл - потери с потом, 400-500 мл - испарение из легких, 500 мл - выведение осмотических веществ. Всего - 1500 мл, меньше - обезвоживание.
Потеря 10% воды - опасна, 20% - несовместима с жизнью. Без воды можно прожить 7-10 дней. Это зависит от характера питания - белковая пища требует дополнительное поступление воды, так как образуется большое количество метаболитов (мочевина и др.), для выведения которых необходима жидкость.
Гормональная регуляция водно-электролитногого обмена. Антидиуретический гормон (АДГ, вазопрессин).
Осморецепторы гипоталамуса реагируют на увеличение осмолярности внеклеточной жидкости и увеличивают синтез АДГ в гипоталамусе, который поступает в нейроги-пофиз, а затем в кровь. АДГ активирует гаалуронидазу,-> увеличение проницаемости эпителия почечных канальцев -> увеличение реабсорбции воды и снижение осмолярности плазмы. Гипокалиемия и гиперкальциемия снижает чувствительность рецепторов к вазопрес-сину и вызывает полиурию. Снижение секреции АДГ вызывают тиреоидные гормоны. При гипофункции щитовидной железы секреция вазопрессина усиливается, что ведет к задержке воды и отекам.
141
Альдостерон - минералокортикоид, выделяется корой надпочечников. Основным регулятором его секреции является ренин-ангиотензин-альдоетероновая система (РААС). При снижении давления крови в клубочках или ишемии юкстагломерулярного аппарата (ЮГА) снижается растяжимость клеток ЮГА и происходит выброс ренина. Ренин действует на ангиотензиноген, превращая его в ангиотензин I. Под действием ангитен-зин-конвертазы (ангиотещин-превращающего фермента, АПФ) ангиотензин I превращается в ангиотензин II, а тот стимулирует секрецию альдостерона. Возможно прямое действие на секрецию альдостерона через стимуляцию волюморецепторов при снижении объема циркулирующей крови (ОЦК). Альдостерон увеличивает реабсорбцию натрия в дистальных почечных канальцах в
обмен на калий, что ведет к увеличению реабсорбции воды. Альдостерон, кроме того,
стимулирует всасывание натрия в кишечнике.
Подобным действием обладают стероидные гормоны (глюкокортикоиды в больших
дозах, женские и мужские половые гормоны).
Натрийуретическим свойством обладают простагпандины, медуллин.
Натрийуретический гормон (НУГ, натрийуретический фактор предсердия, предсерд-ный натрийуретический пептид) выделяется клетками предсердий, усиливает фильтрационную способность клубочков, вызывая дилатацию приносящих почечных арте-риол и констрикцию выносящих почечных артериол; обеспечивает увеличение фильтрации воды и выводит натрий и воду из организма. НУГ уменьшает синтез ренина, альдостерона и АДГ, вызывает прямую вазодилатацию.
Паратгормон вьфабатывается в паращитовидных железах, усиливает резорбцию кальция из кости и увеличивает его концентрацию в крови, накапливает фосфор в костях, снижая его концентрацию в крови. Активация рецепторов глюкокортикоидов на остеокластах увеличивает чувствительность этих клеток к действию паратгормона.
Тиреокалъциотонин (нальцитонин) вырабатывается в щитовидной железе, тормозит остеокласты и снижает концентрацию кальция в крови, увеличивая концентрацию фосфора.
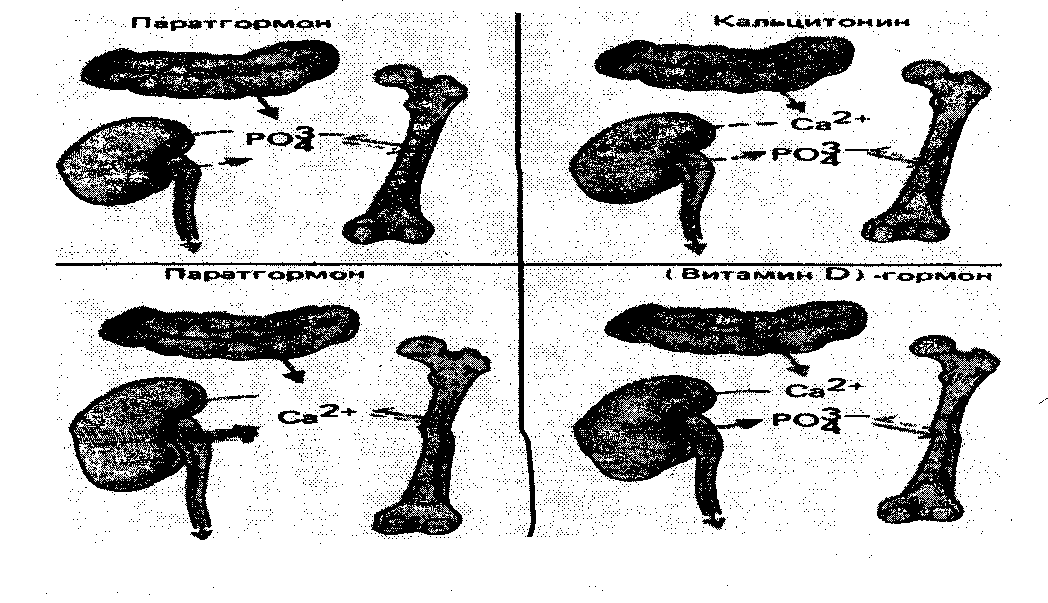
На рисунках схематически представлены механизмы действия гормонов, регулирующих обмен кальция и фосфата - 2.16.1.; снижения осмолярности плазмы крови -2.16.2.; восстановления ОЦК — 2.16.3.
142

143
/. Виды, этиология и патогенез дисгидрий.
Классификация дисгидрий в зависимости от изменения объема воды:
1. Гипергидратация (положительный водный баланс) - недостаточное поступление либо избыточное выделение жидкости.
2. Гипогидратация (отрицательный водный баланс) - избыточное поступление либо недостаточное выделение жидкости.
Каждая из форм подразделяется на:
Экстрацеллюлярную;
Интрацеллюлярную;
Тотальную;
■ Комбинированную (в одном секторе - гипергидратация, в другом - гипогидратация, например, при употреблении алкоголя развивается внутриклеточная гипогидратация и внеклеточная - гипергидратация). В зависимости от осмотической концентрации гипер- и гипогидратации подразделяют на:
изоосмолярную;
гипоосмолярную; ■ гиперосмолярную,
Осмолярность раствора определяется по количеству частиц растворенных в одном кг растворителя (воды) (мОсм/кг воды). Прямое измерение осмолярности осуществляется криоскопическим методом - по разнице температур замерзания дистиллированной воды и исследуемого раствора. На практике чаще используется расчетный метод.
Расчетная осмолярность плазмы крови определяется по формуле:
Ро8m=2*Nа+глюкоза+мочевина (норма 285-310 мОсм/кг воды)
В таблице 2.16.1. представлены нормативы концентрации основных, растворенных в сыворотке крови веществ.
Таблица 2.16.1. Концентрация растворенных веществ в сыворотке крови.
|
Вещество |
Концентрация в плазме |
|
Na+ - натрий |
135- 150ммоль/л |
|
К+ - калий |
3,5 - 5,5 ммоль/л |
|
СГ~хлор |
95-105 ммоль/л |
|
НСОз" - гидрокарбонат |
24 - 32 ммоль/л |
|
Са+2 - кальций |
2,12-2,60 ммоль/л |
|
Р04-3 - окись фосфора |
3,5-4,5 ммоль/л |
|
NH4 - аммоний |
10,6 - 28,2 мкмоль/л |
|
Глюкоза |
3,57 - 6,05 ммоль/л |
|
Мочевина |
3-7 ммоль/л |
Количественная оценка ОЦК проводится с помощью метода разведения красителя, полностью растворяющегося в плазме крови (синего Эванса), введенного в вену руки. После разбавления красителя в большом круге кровообращения, через 10-15 минут, забирают кровь из вены другой руки для определения установившейся концентрации разведенного вещества. Концентрацию краски в крови определяют колориметрическим методом.
ОЦК - количество краски (мг) : средняя концентрация краски (мг/л)
Качественная характеристика ОЦК основана на анамнезе, жалобах пациента, осмотре, измерении АД и пульса. При дегидратации отмечается сухость в подмышечных и паховых областях (косвенно говорит о потере около 1500 мл воды), сухость и исчерче-
144
ность языка, снижение тургора тканей и кожи, снижение тонуса глазных яблок, повышение ЧСС и снижение АД. Напротив, при гипергидратации организма выявляются отеки, влажные хрипы в легких, напряжение глазных яблок.
При дисгидриях происходит изменения показателя гематокрита - соотношение объема форменных элементов крови к объему плазмы. Как правило, при снижении ОЦК отмечается его увеличение, а при гипергидратации - снижение.
При гипергидратации отмечается снижение общего белка плазмы, в случае дегидратации - его увеличение. Креатинин и мочевина плазмы крови в случае их повышения позволяют выявить почечную недостаточность.
Кроме того, для диагностики дисгидрий важным показателем является количество выделенной мочи за определенное время (суточный диурез, норма 1-2 л/сут.). В экстренных состояниях определяют почасовой диурез, (норма 50-60 мл в час).
1) ГИПОГИДРАТАЦИЯ:
а) Изоосмолярная возникает при острой кровопотере, плазмопотерях при обширныхожогах (теряется изотоническая жидкость).
б) Гиперосмолярная развивается в результате потери воды с небольшой потерейэлектролитов, превышающей ее поступление и эндогенное образование, что возможно при чрезмерном потоотделении, гипервентиляции, поносе, полиурии.
в) Гипоосмолярная развивается в тех случаях, когда организм теряет много жидкости, содержащей электролиты, а возмещение потери происходит меньшим объемомводы без введения соли {повторная рвота, понос, чрезмерное потоотделение, поли-урия (несахарный и сахарный диабет, патология почек)).
Из гипоосмотического внеклеточного пространства часть жидкости устремляется в клетки, что приводит к развитию внутриклеточного отека. Чувство жажды при этом отсутствует. 2) ГИПЕРГИДРАТАЦИЯ:
а) Изосмолярная возникает при вливании больших количеств физиологического(рингеровского) раствора в эксперименте или больным в послеоперационном периоде.
Изоосмолярная гипергидратация не вызывает перераспределения жидкости между внутри- и внеклеточными фазами, осмотические свойства которых не изменены.
б) Гипоосмолярная (водное отравление) возникает при избыточном накоплении водыбез соответствующей задержки электролитов.
при повышенной продукции АДГ (синдром Пархона, разбавленной гипонат-рийемии) или олигоанурии (при острой почечной недостаточности).
в результате внутривенного вливания больших количеств изотонического раствора глюкозы, которая быстро потребляется клетками.
При водном отравлении вначале падает осмотическая концентрация внеклеточной жидкости благодаря ее разведению избытком воды. Осмотический градиент между "интерстицием" и клетками обуславливает передвижение части межклеточной воды в клетки и их набухание. Объем клеточной воды может повышаться на 15%.
в) Гиперосмолярная возникает при введении гипертонических растворов в объемах,превышающих возможность достаточно быстрого выделения их почками (при вынужденном питье морской воды). При этом происходит передвижение воды из клеток вовнеклеточное пространство, ощущаемое как тяжелое чувство жажды.
В таблице 2.16.2. представлены основные дифференциально-диагностические критерии различных вариантов дисгидрий.
145
|
Таблица 2.16.2. Дифференциальная диагностика типов дисгидрий |
| |||
|
Тип дисгидрий |
оцк |
Осмотическое давление плазмы |
Содержание №Г в плазме | |
|
\ Дегидратация гипотоническая |
1 |
ь |
1 | |
|
Дегидратация изотоническая |
1 |
N |
N | |
|
Дегидрадация гипертоническая |
1 |
I |
Т | |
|
Гипергидратация гипотоническая |
Т |
1 |
1 1 | |
|
Гипергидратация изотоническая |
Т |
N |
N | |
|
_ Гипергидратация гипертоническая |
Т |
Т |
т 1 | |
Примечание. |- повышено; |- снижено; N - в норме
//- Патогенез отеков и водянок.
Отек - типовой патологический процесс, характеризующийся избыточным накоплением жидкости в межклеточном пространстве, в результате нарушения обмена между плазмой крови и периваскулярной жидкостью.
Анасарка - отек подкожной клетчатки.
Водянка - скопление внеклеточной жидкости в серозных полостях (асцит - водянка брюшной полости, гидроторакс - водянка плевральной полости, водянка яичка - скопление жидкости между оболочками яичка).
Транссудат - отечная жидкость невоспалительного характера.
Экссудат - отечная жидкость воспалительного характера.
Общие механизмы развития отеков:
Повышение гидростатического давления в венозном отделе капилляра.
Понижение коллоидно-осмотического давления плазмы крови, прежде всего развитие гипопротеинемии.
Снижение механического противодавления ткани процессу фильтрации, наступающее при ее разрыхлении.
Повышение онкотического и осмотического давления интерстициальной жидкости, а также усиление способности белков к связыванию воды (набуханию).
Повышение проницаемости гемато-паренхиматозного барьера.
Нарушение оттока лимфы.
Нарушение нейро-эндокринной регуляции функции почек, и, прежде всего нарушение регуляции экскреции натрия почками.
Патогенетическая классификация отеков.
Гемодинамический отек возникает вследствие повышения давления крови в венозном отделе капилляров, что уменьшает величину реабсорбции жидкости при продолжающейся ее фильтрации (сердечная недостаточность, недостаточность клапанов вен, венозный тромбоз).
Онкотический отек развивается вследствие понижения онкотического давления крови, либо повышения его в межклеточной жидкости. Гипоонкия крови чаще всего бывает обусловлена снижением уровня белка и главным образом альбуминов. Гипо-протеинемия может возникнуть в результате недостаточного поступления белка в организму нарушения синтеза альбуминов при заболеваниях печени, чрезмерной потери белков плазмы крови с мочой при некоторых заболеваниях почек. Гиперонкия тканей может возникнуть в результате альтерации, нарушения проницаемости клеточных мембран.
Мембраногенный отек формируется вследствие значительного возрастания проницаемости сосудистой стенки при воспалении, действии токсинов, аллергических реакциях.
Осмотический отек может возникать и вследствие понижения осмотического давления крови или повышения его в межклеточной жидкости. Принципиально гипоос-
146
мия крови может возникать, но быстро формирующиеся при этом тяжелые расстройства гомеостаза "не оставляют" времени для развития его выраженной формы. Гиперосмия тканей, как и их гиперонкия, чаще носит ограниченный характер. Она может возникать вследствие нарушения вымывания электролитов и метаболитов из тканей при нарушении микроциркуляции, снижения активного транспорта ионов через клеточные мемраны при тканевой гипоксии, массивной "утечки" ионов из клеток при их альтерации, увеличения степени диссоциации солей при ацидозе.
5. Лимфогенный отек формируется при повышении давления в лимфатических сосудов и возрастании проницаемости их стенки. Длительно существующий лимфогенный отек сопровождается разрастанием соединительной ткани и развитием слоновости. Этиологическая классификация отеков.
(в скобках указан патогенетический механизм отека)
Сердечный (центральный гемодинамический, застойный).
Венозный (периферический гемодинамический).
Почечный (нефритический, нефротический).
Эндокринный (при альдостеронизме).
Голодный (онкотический).
Кахектический (онкотический).
Печеночный (онкотический).
Воспалительный (мембраногенный).
Аллергический (мембраногенный).
10. Токсический (мембраногенный).
11 ♦ Лимфатический (с развитием слоновости). 12. Нейрогенный (питьевой).
Почечные отеки.
Нефритический отек формируется вследствие преимущественного поражения почечных клубочков. Основную роль при поражении клубочкового аппарата почки играет активация РААС, следствием которой является задержка натрия и воды. Кроме того, формированию отека способствует повышение проницаемости клубочков из-за их иммуноком-плексного повреждения (при гломерулонефрите, системной красной волчанке).
Нефротический отек возникает вследствие поражения преимущественно турбулярно-го аппарата нефронов.
Поражение канальцевого аппарата почки сопровождается гиперпротеинурией, а ее следствием является гипоонкия плазмы. Снижение онкотического давления крови неизбежно приводит к потере ее жидкой части, развивается гиповолемия -> раздражение осмо-и волюморецепторов гипоталамуса. Возбуждение осморецепторов - стимул для выброса АДГ, волюморецепторов - альдостерона. Оба гормона способствую задержке воды. Сердечные отеки. Схематически патогенез сердечного отека представлен на рисунке 2.16.4.
147
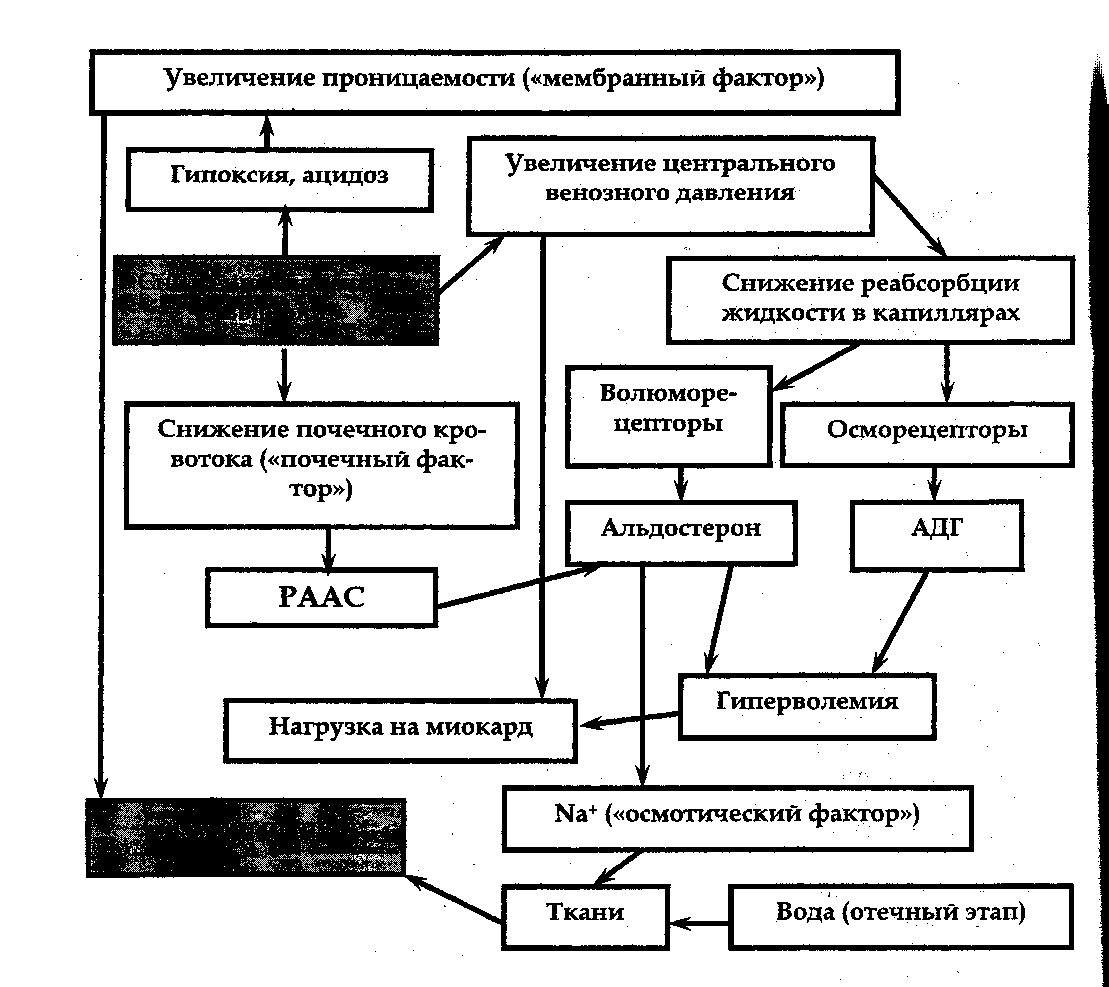
Рис. 2 Л 6.4. Схема патогенеза сердечных отеков.
///. Этиология и патогенез электролитных нарушений в организме.
Минеральный обмен - совокупность процессов всасывания, распределения, усвоения и вьщеления минеральных веществ, находящихся в организма преимущественно в виде неорганических соединений.
Всего в организме обнаруживается свыше 70 элементов таблицы Д.И. Менделеева.
По количественному содержанию в организме они делятся на макроэлементы (составляют 0,01 % и более от массы тела - К, Са, Мg, Nа, Р, Сl) и микроэлементы (составляют менее 0,01 % от массы тела - Мп, 2п, Сг, Си, Ре, Со, А1, 8е).
Основную часть минеральных веществ организма составляют хлористые, фосфорнокислые и углекислые соли натрия, кальция, калия, магния. Соли в жидкостях организма находятся в частично или полностью диссоциированном виде, поэтому минеральные вещества присутствуют в форме ионов (катионов и анионов). Функции минеральных веществ:
пластическая (кальций, фосфор, магний);
поддержание осмотического давления (калий, натрий, хлор);
148
поддержание буферности биологических жидкостей (фосфор, калий, натрий);
поддержание коллоидных свойств тканей (все элементы);
детоксикационная (железо в составе цитохрома Р-450, сера в составе глутатиона);
проведение нервного импульса (натрий, калий);
участие в ферментативном катализе в качестве кофактора или ингибитора;
участие в гормональной регуляции (йод, цинк и кобальт входят в состав гормонов). Промежуточный и конечный обмен минеральных веществ.
Поступают минеральные вещества в организм в свободном или связанном виде. Основная часть минералов всасывается в кишечнике путем активного транспорта при участии белков-переносчиков. Из желудочно-кишечного тракта они поступают в кровь и лимфу, где связываются со специфическими транспортными белками, выводятся из организма в виде солей с мочой, калом, потом.
Характеристика отдельных элементов.
Натрий - основной ("большой") катион внеклеточной жидкости. Составляет 0,08 % от массы тела, 135-150 мМ/л плазмы. Участвует в возникновении и поддержании электрохимического потенциала на плазматических мембранах клеток; регулирует состояние водно-солевого обмена, активность ферментов. При отсутствии или ограничении 3* поступлении натрия в организм его выделение с мочой почти полностью прекращается. Всасывается в верхнем отделе тонкого кишечника при участии белков-переносчиков с затратой АТФ. Суточная потребность варьирует в зависимости от водно-солевого обеспечения организма. Депонируется в коже и мышцах. Кишечная потеря натрия происходитпри диареях.
Калий - составляет 0,25% от массы тела. Во внеклеточном пространстве содержится только 2% от общего количества (в плазме 3,5-5,5 мМ/л), остальное *. в клетках (150 мМ/л), где связан с углеводными соединениями. Всасывается на протяжении всего желудочно-кишечного тракта. Частично калий депонируется в печени и коже, оставшийся поступает в общий кровоток. Калиевый обмен очень быстро протекает в мышцах, кишечнике, почках и печени. Катион играет ведущую роль в возникновении и проведении нервного импульса, необходим для синтеза белков (на 1 г белка - 20 мг ионов калия), АТФ, гликогена, принимает участие в формировании потенциала покоя. Выделяется в основном с мочой и меньше с калом.
Кальций - внеклеточный катион, составляет 1,9 % от массы тела, концентрация в плазме крови в норме составляет 2,1-2,65 мМ/л. Содержание повышается в период роста или беременности. Функционирует как составная часть опорных тканей или мембран, участвует в проведении нервного импульса и инициации мышечного сокращения, поддержании осмотического равновесия, является одним из факторов гемокоагуляции, обеспечивает целостность мембран (способствует плотной упаковке мембранных белков) ограничено участвует, вместе с инсулином активирует проникновение глюкозы в клетки. Всасывается в верхнем отделе кишечника. Степень его усвоения зависит от рН среды (соли кальция в кислой среде нерастворимы). Жиры и фосфаты препятствуют всасыванию кальция. Для полного усвоения из кишечника необходимо наличие активной формы витамина D3.
Витамин D3 увеличивает синтез кальций-связывающего белка в энтероцитах, увеличивает содержание в энтероцитах кишки фосфолипидов, что повышает ее проницаемость для кальция, стимулирует рост и дифференцировку энтероцитов, что увеличивает всасывание, как кальция, так и фосфора.
Синтез витамина D3 происходит в коже под действием ультрафиолетового излучения. Сначала образуется провитамин Бз, под действием тепла в коже происходит его изомеризация в витамин Бз, поступает в печень, там происходит его гидроксилирование, затем поступает в почки, где происходит еще одно гидроксилирование и образуется активная форма. В почках этот процесс регулирует паратгормон, женские и мужские половые гормоны, СТГ - стимуляторы образования витамина D3.
149
Неорганический фосфор содержится преимущественно в костной ткани, составляет 1% от массы тела. В плазме крови при физиологических рН фосфор на 80 % представлен двухвалентным и на 20 % одновалентным анионом фосфорной кислоты. Фосфор входит в состав коферментов, нуклеиновых кислот, фосфопротеинов, фосфолипидов. Вместе с кальцием фосфор образует апатиты - основу костной ткани.
Магний составляет 0,05% от массы тела. В клетках его содержится в 10 раз больше, чем во внеклеточной жидкости. Многого магния в мышечной костной, нервной ткани, печеночной паренхиме. Образует комплексы с АТФ, цитратом, рядом белков; входит в состав почти 300 ферментов. Комплексы магния с фосфолипидами снижают текучесть клеточных мембран. Магний участвует в поддержании нормальной температуры тела, работе нервно-мышечного аппарата.
Хлор - важнейший анион внеклеточного пространства, составляет 0,06% от массы тела, большая часть его содержится в желудочном соке. Хлор участвует в поддержании осмотического равновесия, активирует амилазу и пептидазы. Всасывается в верхних отделах кишечника, выделяется в основном с мочой. Концентрация хлора и натрия обычно изменяются параллельно.
Медь входит в состав многих ферментов и биологически активных металлопро-теинов, участвует в синтезе коллагена и эластина, является компонентом цитохрома с электронтранспортной цепи.
Сера составляет 0,08% от массы тела, поступает в организм в связанном виде в составе аминокислот и сульфат-ионов, является компонентом эндогенных желчных кислот и гормонов, в составе глутатиона участвует в биотрансформации ядов.
Железо входит в состав железосодержащих белков и гема гемоглобина, цитохро-мов, пероксидаз.
В таблице 2.16.3. представлены основные причины и клинические проявления нарушений минерального обмена.
Изменение нервно-мышечной возбудимости при нарушении минерального обмена определяется формулой, в числителе которой - сумма ионов Na+, К+, бикарбоната и фосфата, а в знаменателе - Са++, Мg++ и Н+. Рост числителя и уменьшение знаменателя повышает нервно-мышечную возбудимость.
150
|
Таблица 2.16.3. Нарушения минерального обмена |
| ||
|
1 Тип |
1 Основные причины |
Проявления | |
|
Гипернатрийемия (более 150 мМ/л) |
■ солевая перегрузка, ■ нееахарный диабет, ■ поражения почек,: ■ обезвоживание. |
Увеличение нервно-мышечной ; возбудимости, судороги, ги-пертензия, отеки. | |
|
Гипонатрийемия |
■ гипоальдестеронизм, ■ диуретики-блокаторы карбоан-гидразы, ■ сульфаниламиды, ■ разведение крови, ■ ранняя хроническая инфекция, ■ сердечная недостаточность IIIстепени, ■ цирроз печени, ■ травмы, ■ кишечная непроходимость. |
Снижение нервно-мышечной возбудимости, миастения, тахикардия, гипотония. | |
|
Гиперкалийемия (более 5,5-8 мМ/л) |
■ КВг, КС1 (р-ры, содержащие калий, вводят только капельно!), ■ почечная недостаточность, ■ выход калия из поврежденныхклеток (травма, ожог, операция), ■ гистамин, ■ ацетилхолин, ■ метаболический ацидоз и шок, ■ струйное переливание крови(вследствие концентрационногоградиента из эритроцитов вкровь), ■ дегидратация, ■ адреналовая недостаточность. |
Мышечные параличи, брадикар-дия, аритмия, ацидоз, остановка сердца в фазу диастолы. | |
|
Гипокалийемия (менее 3,5-6 мМ/л) | |
■ глюкокортикоиды, ■ диуретики и салуретики, ■ диарея, ■ гиперальдостеронизм, ■ стресс, ■ алкалоз или ацидоз с нарушениемфункции почек, ■ синдром и болезнь Иценко-Кушинга. |
Снижение нервно-мышечной возбудимости (из-за гиперполяризации), миастения, атония кишечника, аритмии (нарушения процессов реполяризации), снижение -секреции соляной кислоты, алкалоз. | |
|
Гиперкалыдийемия, гипофос-фатемия |
■ гиперпродукция паратгормона, ■ гипервитаминоз Б, ■ гипотиреоз. |
Жажда, полиурия, диспепсия, 1 гипотония мышц, гиперрефлексия, гипертензия, остеопороз. | |
|
Гипокальцийемия и гипер-фосфатемия |
■ дефицит паратгормона, ■ гиповитаминоз В, ■ поражения почечных клубочков. | |
Повышение нервно-мышечной 1 возбудимости, тетанические судороги, гипокоагуляция, гипо-тензия, рахит, катаракта. | |
|
Гипермагнийемия |
■ уремия, ■ диабетический ацидоз. |
Угнетение ЦНС, нарушение ды-1 хания, брадикардия, гипотония. | |
|
Гипомагнийемия |
■ ахолия, ■ панкреатиты, алкоголизм, ■ диарея. |
Повышение нервно-мышечной!возбудимости, гиперрефлексия,тремор, тетания, тахикардия,гипертония. 1 | |
Б) Патология кислотно-основного равновесия.
Кислотно-основное состояние (КОС),-. соотношение между активными массами водорода и гидроксильных ионов.
151
Для нормального течения физиологических процессов, в частности ферментативных и обменных реакций, необходима строго постоянная реакция крови и тканей.
Для оценки характера нарушений кислотно-основного состояния (КОС) принято оценивать концентрацию Н+ в артериальной крови.
РН - отрицательный логарифм концентрации протонов водорода.
рН артериальной крови человека (при 37°С) колеблется в пределах от 7,37 до 7,43, составляя в среднем 7,40. Увеличение рН крови более 7,45 свидетельствует о защелачива-ниц (алкалемии, алкалозе), уменьшение рН менее 7,35 -о закислении (ацидемгш, ацидозе).
Характерная для крови человека слабощелочная реакция поддерживается в очень узких пределах, несмотря на постоянно изменяющееся поступление в кровь кислых продуктов метаболизма. Такое постоянство чрезвычайно важно для правильного протекания обменных процессов в клетках, так как деятельность всех ферментов, участвующих в метаболизме, зависит от рН. При патологических сдвигах рН крови активность разных ферментов изменяется в разной степени, и в результате точное взаимодействие между реакциями обмена может нарушиться. Так, например сдвиг рН крови на 0,1 вызывает выраженное нарушения функции дыхательной, сердечно-сосудистой и других систем организма; снижение рН на 0,3 может привести к развитию ацидотической комы, а сдвиг на 0,4 и более зачастую несовместим с жизнью.
В регуляции кислотно-щелочного равновесия участвуют несколько механизмов: буферные системы, газообмен в легких, секреторная функция желудочно-кишечного тракта выделительная функция почек.
Буфер - это слабая кислота или основание, которые противостоят изменению рН при добавлении сильной кислоты или основания.
1. Бикарбонатный буфер - отношение угольной кислоты к ее кислой соли (бикарбонату). В норме то отношение составляет 1:20. На долю бикарбонатного буфера приходится 7-9% от общей буферной емкости крови.

Н2С03 1
[НЗ-К --
ИаНСОз 20
отношение однозамещенного фосфата натрия к двузаме-
МаН2Р04 {слабая кислота)
[Н] = К- —
ЫагНРСМ {щелочь)
3. Белковый буфер. Буферные свойства белков обусловлены способностью аминокислот к ионизации.
НРг [Н]-К — ИаРг
К буферным белкам относятся, в частности, белки плазмы крови - альбумин, содержащийся в эритроцитах гемоглобин. На долю последнего приходится большая часть буферной емкости белковой буферной системы крови, до 75% всей буферной емкости крови.
НЬ02[Н]=К—
ньн
152
Физиологические системы регуляции КОС.
Легкие - это первая линия защиты в поддержании кислотно-основного гомеостаза, поскольку они обеспечивают механизм почти немедленной регуляции выделения кислоты. В то же время любые нарушения дыхания, сопровождающиеся увеличением или уменьшением минутной альвеолярной вентиляции, могут стать причиной развития нарушений КОС.
Вдыхаемый воздух содержит очень низкую концентрацию СО2. Почти вся углекислота крови является продуктом клеточного метаболизма. По мере образования в процессе клеточного метаболизма СО2 легко диффундирует в капилляры и транспортируется к легким в трех основных формах: растворенный СО2; анион бикарбоната; карбаминовое соединение.
СО2 очень хорошо растворяется в плазме. Около 5 % общей двуокиси углерода в артериальной крови находится в форме растворенного газа, а 90 % - в форме бикарбоната. Последний является продуктом реакции СО2 с водой с образованием Н2СО3 и ее диссоциацией на водород и ион бикарбоната:
карбоангидразаС02 + Н20 <г > Н2С03 < > Н+ + НСОз".
Реакция между СОг и Н2О протекает медленно в плазме и очень быстро в эритроцитах, где присутствует внутриклеточный фермент карбоангидраза. Она облегчает реакцию между СО2 и Н2О с образованием Н2СО3.
По мере накопления НСОз" внутри эритроцита анион диффундирует через клеточную мембрану в плазму. Мембрана эритроцита плохо проницаема для Н+, как и вообще для катионов, поэтому ионы водорода остаются внутри клетки. Электрическая нейтральность клетки в процессе диффузии НСОз" в плазму обеспечивается потоком ионов хлора из плазмы в эритроцит.
Часть Н+, остающихся в эритроцитах, соединяется с гемоглобином. В периферических тканях, где концентрация СО2 высока и значительное количество Н+ накапливается эритроцитами, связывание Н+ облегчается деоксигенацией гемоглобина. Восстановленный гемоглобин лучше связывается с Н+, чем оксигенированный. Таким образом, деоксигена-ция артериальной крови в периферических тканях способствует связыванию Н+ посредством образования восстановленного гемоглобина. Это увеличение связывания СО2 с гемоглобином известно как эффект Холдейна.
Третьей формой транспорта СО2 являются карбаминовые соединения, образованные в реакции СО2 с концевыми аминогруппами белков крови. Основным белком крови, связывающим СО2 является гемоглобин. Этот процесс описывается реакцией:
Нb-NH2 + С02 <-» Нb-NH х СООН <-> Нb-NHСОО" + Н+.
Реакция СО2 с аминогруппами протекает быстро. Как и в случае более легкого связывания СО2 с восстановленным гемоглобином, образование карбаминовых соединений легче протекает с деоксигенированной формой гемоглобина. Карбаминовые соединения составляют около 5 % общего количества СО2, транспортируемого артериальной кровью.
Регуляция выделения СО2 достигается изменением скорости объема легочной вентиляции. Повышение вентиляции приводит к снижению артериального рС02 и наоборот. Афферентные сигналы, изменяющие альвеолярную вентиляцию, связаны с хеморецепто-рами, которые регулируют функции дыхательного центра.-Эти рецепторы находятся в продолговатом мозге, аортальном и каротидном тельцах и реагируют на изменения рС02 и концентрации Н+.
153
При увеличении кислотности крови, повышение содержания ионов Н+ приводит к возрастанию легочной вентиляции. Н+ связываются с ЫаНСОз с образованием Н2СОз. Н2СО3 разлагается на СО2 и Н2О. При этом молекулы С02 выводятся в большом количестве и рН возвращается к нормальному уровню.
При увеличении содержания оснований наступает гиповентиляция, в результате напряжение С02 и концентрация ионов Н+ возрастают, сдвиг реакции крови в щелочную сторону частично или полностью компенсируется.
Почки - их функция состоит в удалении нелетучих кислот. Почки должны удалять в сутки 40-60 ммоль ионов Н+, накапливающихся за счет образования нелетучих кислот.
Их выделение происходит в проксимальных канальцах и собирательных трубках почек, где секретируются Н+, а в качестве буферных систем участвуют фосфаты, сульфаты (т.е. титруемые кислоты) и аммиак. Однако до того как может произойти экскреция всех кислот, почки должны реабсорбировать НСОз", профильтровавшийся клубочками.
Способность канальцев почек к реабсорбции НСОз" высока. Самым важным местом реабсорбции НСОз" являются проксимальные канальцы, где посредством специального механизма происходит всасывание 90 % бикарбоната.
При защелачивании Н+ задерживается в клетках почечных канальцев, а НСО"з не реабсорбируясь выделяется.
Основная часть Н* в моче должна быть выведена в форме солей (фосфаты, соли аммония и др.).
В клетках почечных канальцев процесс образования аммиака (NНз) происходит также за счет дезаминирования аминокислот (глутаминовой).
Аммиак поступает в канальцевую мочу, где, соединяясь с Н+, образует ионы аммония (NH4), последние, присоединяя ионы СГ, образуют хлорид аммония и выводятся с мочой. Nа+, освобожденный от СГ в моче, всасывается в клетки почечных канальцев, соединяется с освобожденными от Н+ ионами НСО"з и реабсорбируется в виде бикарбоната Nа.
Желудочно-кишечный тракт. Клетки слизистой оболочки желудка секретируют НС1 в очень высокой концентрации. При этом из крови ионы хлора поступают в полость желудка в соединении с Н+, образующимися в эпителии желудка при участии угольной ангидразы. Взамен хлоридов в плазму транспортируется бикарбонат. Существенного за-щелачивания крови при этом не происходит, поскольку ионы хлора желудочного сока достаточно быстро вновь всасываются в кровь в кишечнике. Железы слизистой оболочки кишечника секретируют щелочной сок, богатый бикарбонатами. При этом плазма пополняется Н+ в составе НС1. Кратковременный сдвиг реакции сразу же уравновешивается обратным всасыванием бикарбоната в кишечнике.
Печень участвует в поддержании кислотно-основного равновесия за счет удаления в основном кислых продуктов. В печени осуществляется синтез мочевины из шлаков, в частности таких, как аммиак и хлорид аммония. Мочевина выводится почками. При острой и хронической почечной недостаточности синтез мочевины усиливается.
В настоящее время для анализа кислотно-основного равновесия наиболее часто используется метод Аструпа. Метод основан на определении трех значений рН у пациента: 1 - истинное значение рН крови; 2 и 3 - рН крови этого же больного, помешенной в искусственно создаваемую среду с соответственно 3% и 8% концентрациями СО2 (28 мм. рт. ст. и 58 мм. рт. ст.) при полном насыщении гемоглобина кислородом и температуре 37°С.
Линия зависимости («буферная линия») по этому методу строится на криволинейной номограмме Сиггард-Андерсена (рис. 2.16.5.). Показатели номограммы представлены в таблице 2.16.4.
154
|
Таблица 2.16.4. Показатели номограммы Сиггаард-Андерсена |
|
| |
|
Символическое изображение показателя |
Основная характеристика |
Пределы нормальных показателей |
Средняя величина |
|
рН |
Величина активной реакции раствора |
7,35—7,45 |
7,4 |
|
Рсо2 |
Парциальное давление углекислого газа над жидкостью. При нормальном содержании С02 в артериальной крови Рсо2 = 40 мм рт. ст. Смещение величины Рсо2 вправо (свыше 40 мм рт. ст.) говорит о накоплении ее избытка в крови (дыхательный ацидоз); смещение влево (ниже 40 мм рт. ст.) — о недостаточном количестве С02 в крови (дыхательный алкалоз) |
4,66-5,99 кПа (35-45 мм рт. ст.) |
5,32 кПа (40 мм рт. ст.) |
|
АВ . |
Истинный бикарбонат крови — содержание НС03~~ в истинной (т.е. взятой у конкретного больного в данных обстоятельствах) крови |
19-25 ммоль/л |
23 ммоль/л |
|
| 8В |
Стандартный бикарбонат — тот же бикарбонат НС03~~ взятой у больного крови, но приведенной к стандартным условиям (т.е. искусственно помещенной в среду, в которой Рсо2=40 мм рт. ст., содержание окисленного гемоглобина НЬО2=100%, температура 37°С) |
20-27 " |
24 " |
|
ВВ |
Сумма оснований всех буферных систем крови (т.е. щелочных компонентов бикарбонатной, фосфатной, белковой и гемоглоби-новой системы) |
40-60 " |
50 " |
|
ВЕ |
Избыток (или дефицит) оснований. Изменения содержания буферных оснований крови по сравнению с нормальными для данного больного NBB. NВВ - та же сумма всех основных компонентов буферных систем взятой у больного крови, но искусственноприведенной к стандартным условиям (рН 7,38, Рсо2 = 40 мм рт.ст., температура 37°С). Зависимость выражается формулой:ВЕ-ВВ-NВВ. Другими словами, ВЕ показывает, какое количествомиллимолей NаНСОз следует добавить (или условно удалить),чтобы рН стало 7,38 (при 37°С). Положительное значение ВЕ указывает на избыток оснований (или на дефицит кислот), а отрицательное — на дефицит оснований (или избыток кислот) |
±2,3 |
0 |
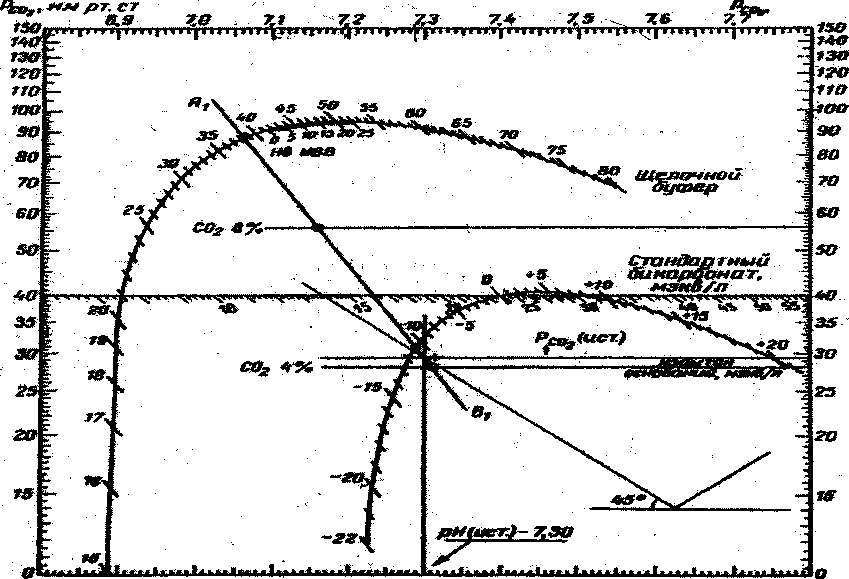
мм /гп &т
Рис. 2Л6.5. Номограмма Зигарда-Андерсена для определения кислотно-щелочного состояния
[по Бунятяну А.А., 1982].
155
/. Этиология и патогенез нарушений кислотно-основного состояния. Компенсаторные механизмы. Ацидоз- это такое нарушение КОС, при котором в крови появляется относительный или абсолютный избыток кислот или недостаток оснований.
Алкалоз - это такое нарушение КОС, при котором имеется избыток оснований или недостаток кислот.
Классификация нарушений кислотно-основного равновесия. I. Ацидоз:
Газовый (дыхательный.).
Негазовый.
метаболический
выделительный
экзогенный
комбинированный (например, кетоацидоз + лактоацидоз; метаболический + выделительный и др.).
3. Смешанный (например, газовый + негазовый при асфиксии)П. Алкалоз;
Газовый (дыхательный).
Негазовый.
выделительный
экзогенный
По степени компенсации все ацидозы и алкалозы подразделяются на I. Компенсированные - это состояния, при которых в уравнении рН изменяются абсолютные количества угольной кислоты и натрия гидрокарбоната, но соотношение их остается 1:20. При этом рН существенно не изменяется, что служит показателем компенсации. И. Декомпенсированные, когда изменяется не только общее количество угольной кислоты и натрия гидрокарбоната, но и их соотношение, о чем свидетельствует сдвиг рН крови за пределы нормы. Ацидоз: I. Газовый
* снижение выведения СО2 при нарушениях внешнего дыхания (массивные пневмонии, ателектазы легких, бронхиальная астма, обструктивная форма эмфиземы легких, нарушения дыхания у ослабленных больных в раннем послеоперационном периоде, при синдроме трахео- бронхиальной непроходимости и т.д.).
■ высокая концентрация СО2 в окружающей среде.
При нарушении вентиляции легких основная компенсация дыхательного ацидоза осуществляется почками путем усиленного выведения Н4" и повышения реабсорбции ионов НСОз" (в виде бикарбоната натрия). Такая компенсаторная реакция является целесообразной лишь до определенного момента. К выраженному респираторному ацидозу присоединяется второй патологический процесс - метаболический алкалоз.
П. Негазовый
кетоз (кетоацидоз) - сахарный диабет, голодание, нарушения функции печени, лихорадка, гипоксия и др.
лактатацидоз - тканевая гипоксия, нарушение функций печени, инфекции
обширные воспалительные процессы, ожоги, травмы
задержка кислот при почечной недостаточности (диффузный нефрит, уремия)
потеря щелочей - почечный канальцевый ацидоз, гипоксия, интоксикация сульфани-ламидами/диарея, гиперсаливация
длительное употребление кислой пищи, прием кислот внутрь
156
Характерной компенсаторной реакцией при метаболическом ацидозе является дыхательный алкалоз.
Основные клинические проявления ацидоза: одышка, тахикардия, гипертония, гиперсекреция бронхиальных желез, рвота, диарея, с последующим угнетением сердечной деятельности, формированием аритмии, гипотонии.
Алкалоз: I» Газовый - усиленное выведение СО2 при гипервентиляции (неврозы, высотная болезнь,
ныряльщики, во время длительной операции или у реанимируемого больного).
При гипервентиляции развивается вазоконстрикция церебральных сосудов.
Компенсация дыхательного алкалоза осуществляется почками: задерживаются ионы Н* и выделяется НСОз", увеличивается количество органических кислот, в основном молочной кислоты. Таким образом, все компенсаторные реакции являются целесообразными лишь относительно, так как приводят к возникновению метаболического ацидоза.
II. Негазовый.
■ потеря кислот — многократно повторяющаяся рвота, кишечная непроходимость, токсикоз беременных, гиперсекреция желудочного сока; 11 длительный прием щелочной пищи, стероидных препаратов, введение нитрата №, альдостеронизм с гипокалийемией (приводит к избыточному выведению ионов Н* почками и перемещению Н+ в клеточный сектор).
Компенсация метаболического алкалоза осуществляется за счет появления дыхательного ацидоза, но такая компенсация приводит к раздраженшо дыхательного центра и гипервентиляции.
Основные клинические проявления алкалоза: ослабление дыхательной функции легких, повышение нервно-мышечной возбудимости, тетания, тахикардия, гипотония, зало-ры.
