
- •C.М. Дрюцкая
- •Введение
- •Тема 1. Введение. Классы и номенклатура неорганических соединений. Основные законы и понятия химии. Закон эквивалентов.
- •1.1. Теоретические сведения
- •Химические свойства оксидов
- •Получение кислот
- •Химические свойства кислот
- •Получение оснований
- •Химические свойства оснований
- •Получение солей
- •Химические свойства средних солей
- •Числовые приставки
- •Систематические и тривиальные названия некоторых веществ
- •Систематические и международные названия некоторых сложных веществ
- •Названия наиболее распространенных кислот и их анионов
- •1.2. Контрольные вопросы и задания
- •1.3. Примеры решения задач
- •1.4. Индивидуальные задания
- •Варианты контрольного задания
- •Варианты контрольного задания
- •1.5. Тестовые задания
- •Тема 2. Способы выражения концентрации (состава) раствора.
- •2.1. Теоретические сведения
- •2.2. Контрольные вопросы и задания
- •2.3. Примеры решения задач
- •2.4. Индивидуальные задания
- •Варианты контрольного задания
- •2.5. Тестовые задания
- •Тема 3. Химическая термодинамика.
- •3.1. Теоретические сведения
- •3.2. Контрольные вопросы и задания
- •3.3. Примеры решения задач
- •Стандартные термодинамические функции
- •3.4. Индивидуальные задания
- •Варианты контрольного задания
- •Варианты контрольного задания
- •3.5. Тестовые задания
- •Тема 4. Химическая кинетика. Термодинамика химического равновесия
- •4.1.Теоретические сведения
- •4.2. Контрольные вопросы и задания
- •4.3. Примеры решения задач
- •4.4. Индивидуальные задания
- •Варианты контрольного задания
- •4.5. Тестовые задания
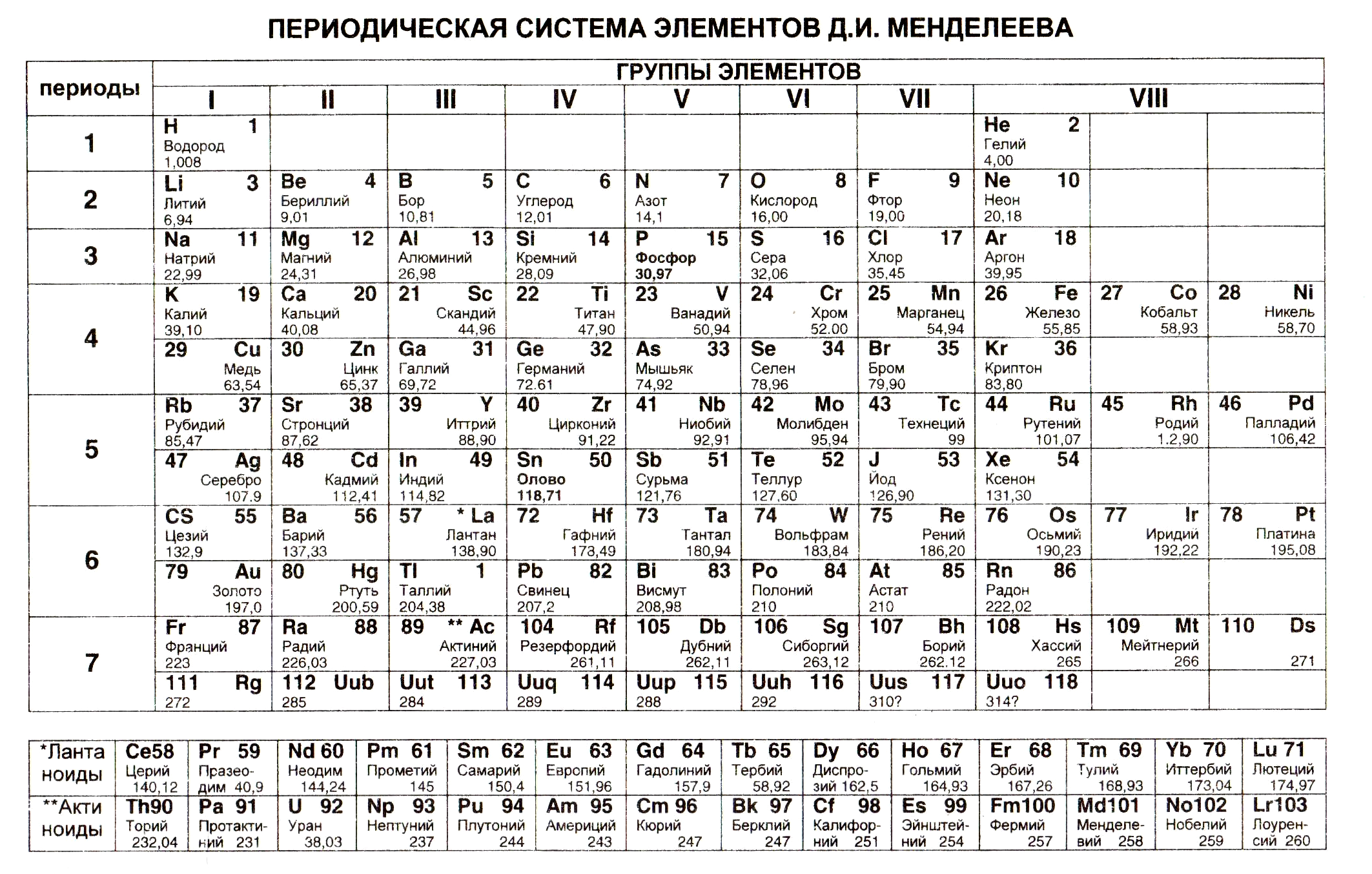
- •Тема 5. Строение атома. Периодический закон и периодическая система элементов д.И. Менделеева. Химическая связь и строение соединений. Межмолекулярные взаимодействия.
- •5.1. Теоретические сведения
- •Основные характеристики протона, нейтрона и электрона
- •Корпускулярно-волновые свойства частиц
- •Число подуровней на энергетических уровнях
- •Число орбиталей на энергетических подуровнях
- •Последовательность заполнение атомных орбиталей
- •Электронные формулы элементов
- •Потенциалы (энергии) ионизации i1, эВ
- •Потенциалы (энергии) ионизации i1, эВ элементов V группы
- •Значение энергии (Eср) сродства к электрону для некоторых атомов.
- •Относительная электроотрицательность элементов
- •Свойства веществ в разных агрегатных состояниях
- •Сравнительная характеристика аморфных и кристаллических веществ
- •Свойства кристаллических решеток
- •5.2. Контрольные вопросы и задания
- •5.3. Примеры решения задач
- •План характеристики элемента по положению в Периодической системе д.И. Менделеева
- •5.4. Индивидуальные задания
- •Варианты контрольного задания
- •Исходные данные
- •5.5. Тестовые задания
- •Тема 6. Реакции с переносом электронов. Окислительно-восстановительные равновесия и процессы
- •6.1. Теоретические сведения
- •Характеристика элементов и их соединений в овр
- •Типы овр
- •Составление уравнений окислительно-восстановительных реакций
- •Участие ионов в различных средах
- •Стандартные электродные потенциалы металлов
- •6.2. Контрольные вопросы и задания
- •6.3. Примеры решения задач
- •6.4. Индивидуальные задания
- •Варианты контрольного задания
- •Исходные данные
- •6.5. Тестовые задания
- •Тема 7. Лигандообменные равновесия и процессы. Комплексные соединения
- •Координационные числа ионов - комплексообразователей
- •Основные комплексообразователи в кс
- •Среднее поле
- •Слабое поле
- •Геометрическая структура кс и тип гибридизации
- •Видимый спектр длин волн (нм) и окраска кс при их поглощении
- •Варианты контрольного задания
- •Тема 8. Осмотические свойства растворов. Протолитические равновесия и процессы. Электролитическая ионизация. Степень и константа ионизации
- •Теория электролитической ионизации (диссоциации).
- •Варианты контрольного задания
- •Тема 9. Гетерогенные равновесия и процессы. Произведение растворимости, условия образования и растворения осадков
- •Условия смещения гетерогенного равновесия:
- •Варианты контрольного задания
- •Тема 10. Ионное произведение воды. РН. Гидролиз солей
- •Изменение окраски некоторых индикаторов
- •Примеры буферных растворов.
- •Уравнения Гендерсона – Гассельбаха
- •Варианты контрольного задания
- •Объем учебной дисциплины «Общая и неорганическая химия» и виды учебной работы для студентов очного отделения фармацевтического факультета
- •Календарный план лабораторных занятий по общей и неорганической химии для студентов дневного отделения фармацевтического факультета
- •I семестр (продолжительность - 5 часов)
- •Календарный план лекций по общей и неорганической химии для студентов дневного отделения фармацевтического факультета
- •I семестр (продолжительность - 2 часа)
- •Название важнейших кислот и солей.
- •Значения некоторых фундаментальных физческих постоянных
- •Термодинамические свойства веществ.
- •Стандартные электродные потенциалы (е0) некоторых систем
- •Константы устойчивости комплексных ионов
- •Константы нестойкости некоторых комплексных ионов
- •Константы ионизации кислот и оснований (Ки)
- •Коэффициенты активности (f) ионов при ионных силах раствора
- •Растворимость кислот, оснований и солей в воде
- •Константы растворимости
- •Ответы тестовых заданий
- •Оглавление
Значения некоторых фундаментальных физческих постоянных
|
Постоянная |
Обозначение |
Численное значение |
|
Скорость света в вакууме Постоянная Планка Элементарный электрический заряд Постоянная Авогадро Постоянная Фарадея Газовая постоянная (универсальная) Абсолютный нуль температуры Нормальная атмосфера Стандартный молярный объем Атомная единица массы Масса покоя электрона Масса покоя протона |
с h e NA F R
t р Vm а.е.м. |
2,9979246·108 м/с 6,62618·10-34 Дж·с 1,602189·10-19 Кл 6,022045·1023 моль-1 9,64846·104 Кл/моль 8,3144 Дж/(моль·К)
- 273,150 С 101325 Па 22,41383·10-3 м3/моль 1,660565586·10-27 кг 1,10953447·10-31 кг 1,672648586·10-27 кг |
ПРИЛОЖЕНИЕ 3
Термодинамические свойства веществ.
|
Вещество |
ΔН0298, кДж/моль |
ΔS0298, Дж/(моль·К) |
ΔG0298, кДж/моль |
|
Ag(т) |
0 |
42,7 |
0 |
|
AgCl(т) |
- 125,5 |
96,1 |
- 109,7 |
|
Ag2O(т) |
- 32,2 |
121,7 |
- 10,8 |
|
Al(т) |
0 |
28,33 |
0 |
|
Al2O3(т) |
- 1675,69 |
50,92 |
- 1582,27 |
|
Al(OH)3(т) |
- 1276,1 |
83,8 |
- 1157,0 |
|
AlН(г) |
248,95 |
187,75 |
193,0 |
|
Ва(г) |
0 |
64,9 |
0 |
|
ВаО(т) |
- 553,6 |
70,3 |
- 528,0 |
|
Ва(ОН)2(т) |
- 946,1 |
103,8 |
- 886,2 |
|
BaSO4(т) |
- 1465,0 |
132,2 |
- 1458,8 |
|
ВаСО3(т) |
- 1211,0 |
112,1 |
- 1244,41 |
|
BaSiO3(т) |
- 1590,1 |
109,6 |
- 1525,9 |
|
Br2(г) |
0 |
245,3 |
0 |
|
Br2(ж) |
0 |
152,3 |
0 |
|
С(алмаз) |
0 |
2,4 |
0 |
|
C(графит) |
0 |
5,7 |
0 |
|
CCl4(ж) |
- 135,4 |
214,4 |
- 64,6 |
|
CH4(г) |
- 74,9 |
186,2 |
- 50,8 |
|
C2H2(г) |
226,8 |
200,8 |
209,2 |
|
C2H4(г) |
52,3 |
219,4 |
68,1 |
|
C2H6(г) |
- 89,7 |
229,5 |
- 32,9 |
|
C6H6(ж) |
82,9 |
269,2 |
129,7 |
|
C2H5OH(ж) |
- 277,6 |
160,7 |
- 174,8 |
|
СН3ОН(ж) |
-201,2 |
126,8 |
- |
|
C2H5OH(г) |
-235,3 |
- |
- |
|
C6H12O6(т) |
- 1273,0 |
- |
- 919,5 |
|
CO(г) |
- 110,5 |
197,5 |
- 137,1 |
|
CO2(г) |
- 393,5 |
213,7 |
- 394,4 |
|
CS(г) |
70,8 |
151,1 |
64,5 |
|
Ca(т) |
0 |
41,63 |
0 |
|
СаС2(т) |
- 62,7 |
70,22 |
- 67,72 |
|
Са(НСО3)2(ж) |
- 1925,22 |
129,91 |
- 1725,82 |
|
CaCO3(т) |
- 1207,0 |
88,7 |
- 1127,7 |
|
CaF2(т) |
- 1214,6 |
68,9 |
- 1161,9 |
|
Ca3N2(т) |
- 431,8 |
105 |
- 368,6 |
|
CaO(т) |
- 635,5 |
39,7 |
- 604,2 |
|
Ca(OH)2(т) |
- 986,6 |
76,1 |
- 896,8 |
|
CaSO4(т) |
- 1422,33 |
108,26 |
- 1310,51 |
|
CaSO4 · 0,5 H2O(т) |
- 1431,32 |
106,59 |
- 1319,04 |
|
CaSO4 · 2 H2O(т) |
- 1760,62 |
183,92 |
- 1563,74 |
|
CaSiO3(т) |
- 1585,55 |
81,93 |
- 1609,92 |
|
Ca3(PO4)2(т) |
- 4122,31 |
240,77 |
- 3886,15 |
|
Ga(т) |
0 |
41,1 |
0 |
|
Ga2О(г) |
- 95,25 |
284,44 |
- 180,02 |
|
GaО(г) |
146,8 |
213,71 |
82,51 |
|
Ga2О3(т) |
- 1091,0 |
84,94 |
- 1116,31 |
|
GaН(г) |
214,3 |
199,67 |
154,8 |
|
GaF2(г) |
- 534,45 |
279,39 |
- 617,71 |
|
GaF3(т) |
- 1175,0 |
96,0 |
- 941,4 |
|
GaCl2(г) |
- 241,24 |
300,91 |
- 330,91 |
|
GaCl3(т) |
- 524,7 |
133,4 |
- 492,8 |
|
Cl2(г) |
0 |
222,9 |
0 |
|
Cl2O(г) |
76,6 |
266,2 |
94,2 |
|
ClO2(г) |
105,0 |
257,0 |
122,3 |
|
Cl2O7(ж) |
251,0 |
- |
- |
|
Cr2O3(т) |
- 1440,6 |
81,2 |
- 1050,0 |
|
Cr(OH)3(т) |
- 987,4 |
80,5 |
- 900,9 |
|
Cu(т) |
0 |
33,3 |
0 |
|
CuO(т) |
- 162,0 |
42,6 |
- 129,9 |
|
Cu(OH)2(т) |
- 444,0 |
70,2 |
- 359,8 |
|
(CH3)2CO(г) |
- 216,19 |
294,65 |
- 151,73 |
|
Fe(т) |
0 |
27,15 |
0 |
|
FeO(т) |
- 264,8 |
60,8 |
- 244,3 |
|
Fe2O3(т) |
- 822,2 |
87,4 |
- 740,3 |
|
Fe3O4(т) |
- 1117,1 |
146,2 |
- 1014,2 |
|
FeCl3(т) |
- 401,8 |
119,4 |
- 302,0 |
|
Fe(OH)3(т) |
- 841,0 |
96,6 |
- 6946 |
|
FeS(т) |
-100,5 |
60,3 |
-100,8 |
|
FeSO4(т) |
-929,5 |
121,0 |
-825,5 |
|
F2(г) |
0 |
202,9 |
0 |
|
H2(г) |
0 |
130,52 |
0 |
|
HBr(г) |
- 36,3 |
198,6 |
- 53,3 |
|
HCN(г) |
135,0 |
113,1 |
125,5 |
|
HCl(г) |
- 91,8 |
186,8 |
- 94,79 |
|
HCl(ж) |
-166,9 |
56,5 |
-131,2 |
|
HF(г) |
- 270,7 |
178,7 |
- 272,8 |
|
HJ(г) |
26,6 |
206,5 |
1,8 |
|
HN3(ж) |
294,0 |
328,0 |
238,8 |
|
H2O(г) |
- 241,8 |
188,7 |
- 228,6 |
|
H2O(ж) |
- 285,8 |
70,1 |
- 237,3 |
|
H2S(г) |
- 21,0 |
205,7 |
- 33,8 |
|
H2SO4(ж) |
- 813,99 |
156,90 |
- 690,14 |
|
HNO3(ж) |
-174,3 |
155,7 |
-80,9 |
|
Hg(CNO)2(т) |
- 118,33 |
177,11 |
- 27,75 |
|
Hg(ж) |
0 |
76,1 |
0 |
|
J2(т) |
0 |
116,7 |
0 |
|
J2(г) |
0 |
260,6 |
0 |
|
JH(г) |
214,7 |
207,55 |
152,85 |
|
K(т) |
0 |
64,3 |
0 |
|
KCl(т) |
- 435,9 |
82,6 |
- 408,0 |
|
KClO3(т) |
- 391,2 |
143,0 |
- 289,9 |
|
К2О(т) |
-363,2 |
94,1 |
-323,1 |
|
KNO3(т) |
-493,2 |
132,9 |
-393,1 |
|
KOH(т) |
- 424,7 |
59,4 |
- 380,2 |
|
Li(т) |
0 |
28,0 |
0 |
|
Mg(т) |
0 |
32,5 |
0 |
|
MgCl2(т) |
- 641,1 |
89,9 |
- 591,6 |
|
Mg3N2(т) |
- 461,1 |
87,9 |
- 400,9 |
|
MgO(т) |
- 601,8 |
26,9 |
- 569,6 |
|
Mg(OH)2(т) |
- 924,66 |
63,18 |
- 833,75 |
|
MgSO4(т) |
- 1287,42 |
91,55 |
- 1173,25 |
|
MgCO3(т) |
-1113,0 |
65,7 |
-1029,3 |
|
N2(г) |
0 |
191,5 |
0 |
|
NH3(г) |
- 46,2 |
192,6 |
- 16,7 |
|
NH4NO2(т) |
- 256 |
- |
- |
|
NH4Br(т) |
- 270,1 |
112,8 |
- 174,7 |
|
NH4Cl(т) |
-314,4 |
95,9 |
-204,3 |
|
NH4NO3(т) |
- 365,4 |
151 |
- 183,8 |
|
N2O(г) |
82,0 |
219,9 |
104,1 |
|
NO(г) |
90,3 |
210,6 |
86,6 |
|
N2O3(г) |
83,3 |
307,0 |
140,5 |
|
NO2(г) |
33,5 |
240,2 |
51,5 |
|
N2O4(г) |
9,6 |
303,8 |
98,4 |
|
NH4Cl(т) |
- 315,39 |
94,5 |
- 204,0 |
|
N2O5(т) |
- 42,7 |
178 |
114,1 |
|
Na(т) |
0 |
51,4 |
0 |
|
NaOH(т) |
- 426,3 |
64,2 |
- 380,7 |
|
NaOH(ж) |
-470,0 |
48,1 |
-419,2 |
|
Na2SiO3(т) |
-1525,4 |
113,8 |
-1427,7 |
|
NaCl(т) |
-411,4 |
72,1 |
-384,0 |
|
Ni(т) |
0 |
29,8 |
0 |
|
NiO(т) |
- 239,7 |
38,0 |
- 211,6 |
|
O2(г) |
0 |
205,0 |
0 |
|
O3(г) |
0 |
238,8 |
0 |
|
OF2(г) |
25,1 |
247,0 |
42,5 |
|
Р(белый) |
0 |
44,3 |
0 |
|
Р(красный) |
0 |
22,8 |
0 |
|
РН3(г) |
5,44 |
210,1 |
13,39 |
|
P2O3(т) |
- 820 |
173,5 |
- |
|
P2O5(т) |
- 1492 |
114,5 |
- 1348,8 |
|
Pb(т) |
0 |
64,9 |
0 |
|
PbO(т) |
- 219,3 |
66,1 |
- 189,1 |
|
PbO2(т) |
- 276,6 |
74,9 |
- 218,3 |
|
PCl3(г) |
- 287,02 |
311,71 |
- 267,98 |
|
PCl5(г) |
- 374,89 |
364,47 |
- 305,10 |
|
S(ромб.) |
0 |
31,8 |
0 |
|
SO2(г) |
- 296,9 |
248,1 |
- 300,2 |
|
SO3(г) |
- 395,8 |
256,7 |
- 371,2 |
|
SO3(ж) |
-439,2 |
95,5 |
-362,0 |
|
Si(т) |
0 |
18,7 |
0 |
|
SiCl4(ж) |
- 687,8 |
239,7 |
- |
|
SiH4(г) |
34,7 |
204,6 |
57,2 |
|
SiO2(т) |
- 910,9 |
41,8 |
- 856,7 |
|
Sn(т) |
0 |
51,6 |
0 |
|
SnO(т) |
- 286,0 |
56,5 |
- 256,9 |
|
SnO2(т) |
- 580,8 |
52,3 |
- 519,3 |
|
SrCO3(т) |
- 1227,0 |
97,2 |
- 1255,97 |
|
Ti(т) |
0 |
30,6 |
0 |
|
TiCl4(ж) |
- 804,2 |
252,4 |
- 737,4 |
|
TiO2(т) |
- 943,9 |
50,3 |
- 888,6 |
|
TlH(г) |
204,62 |
215,1 |
140,52 |
|
WO3(т) |
- 842,7 |
75,9 |
- 763,9 |
|
Zn(т) |
0 |
41,6 |
0 |
|
ZnO(т) |
- 350,6 |
43,6 |
- 320,7 |
ПРИЛОЖЕНИЕ 4
ПРИЛОЖЕНИЕ 5
