
- •Оглавление
- •Введение (как пользоваться учебно-методическим пособием)
- •Занятие № 1 классификация, номенклатура и структурная изомерия органических соединений. Электронное строение атомов элементов-органогенов
- •Блок информации
- •Классификация соединений по строению углеродного скелета
- •Важнейшие классы органических соединений
- •Построение названия органического соединения
- •Пример названия по заместительной номенклатуре iupac
- •Характеристические (функциональные) группы, их обозначение по номенклатуре iupac и соответствующие им классы органических соединений
- •Названия важнейших углеводородных радикалов
- •Валентное состояние и строение атома углерода в алифатических углеводородах
- •Правила техники безопасности при работе в химической лаборатории
- •Занятие № 2 химическая связь в органических молекулах. Классификация химических реакций. Реакционная способность алканов. Алкенов и алкадиенов
- •План изучения темы
- •Бромирование непредельных соединений
- •Окисление алкенов в мягких условиях (реакция Вагнера)
- •Блок информации
- •Типы химических связей атомов в молекулах органических соединений
- •Характеристика ковалентных связей
- •Свойства насыщенных углеводородов (алканов)
- •Свойства ненасыщенных углеводородов ряда этилена (алкенов)
- •Блок информации для выполнения самостоятельной работы
- •Конформации молекул алифатических углеводородов
- •Вопросы для тестового контроля
- •Занятие № 3 взаимное влияние атомов в молекулах органических соединений. Реакционная способность ароматических углеводородов
- •Влияние заместителей на последующее электрофильное замещение в ароматическом ядре
- •Вопросы для тестового контроля
- •Занятие № 4 химические свойства галогеналканов, спиртов и фенолов
- •План изучения темы
- •Получение этилхлорида из этилового спирта
- •Дегидратация этилового спирта
- •Свойства фенолов
- •Указания по выполнению самостоятельной работы № 2
- •Указания по выполнению самостоятельной работы № 3
- •Вопросы для тестового контроля
- •Заполните схему!
- •15. Возрастание кислотных свойств соединений:
- •Реакции окисления спиртов
- •31. Заполните схему!
- •Заполните схему!
- •Занятие № 5 кислотно-основные свойства органических соединений. Реакционная способность аминов
- •Получение этиленгликолята меди (II)
- •Образование фенолята натрия и разложение его кислотой
- •Сравнение основности алифатических и ароматических аминов
- •Блок информации
- •Значения pKa некоторых кислот Бренстеда
- •Кислотность различных классов соединений
- •Свойства первичных алифатических аминов
- •Вопросы для тестового контроля
- •3. Метиламин
- •Занятие № 6 реакционная способность оксосоединений
- •План изучения темы
- •Диспропорционирование формальдегида в водных растворах
- •Отношение ацетальдегида и ацетона к окислению щелочными растворами оксидов тяжёлых металлов
- •Открытие ацетона переводом его в йодоформ
- •Блок информации
- •Свойства альдегидов
- •Вопросы для тестового контроля
- •Занятие № 7 химические свойства карбоновых кислот и их функциональных производных
- •План работы на предстоящем занятии
- •Открытие щавелевой кислоты
- •Получение этилацетата
- •Блок информации
- •Свойства насыщенных монокарбоновых кислот
- •Кислотные свойства карбоновых кислот
- •Производные угольной кислоты
- •Указания по выполнению самостоятельной работы № 4
- •Вопросы для тестового контроля
- •Занятие № 8 итоговое занятие по теме «гомофункциональные производные углеводородов»
- •Занятие № 9 гетерофункциональные алифатические соединения - метаболиты и биорегуляторы
- •Доказательство наличия двух карбоксильных групп в винной кислоте
- •Доказательство наличия гидроксильных групп в винной кислоте
- •Блок информации
- •Классификация кислород- и азотсодержащих гетерофункциональных соединений
- •Свойства α-гидроксикислот
- •Специфические свойства α-, β-, γ-гидроксикислот
- •Свойства α-аминокислот
- •Специфические свойства α-, β-, γ-аминокислот
- •Вопросы для тестового контроля
- •Занятие № 10 гетерофункциональные соединения бензольного ряда. Биологически активные производные пятичленных гетероциклических соединений
- •Свойства пятичленных гетероциклов с одним гетероатомом (π-избыточных систем)
- •Свойства пятичленных гетероциклов с двумя гетероатомами
- •Электронное строение молекулы пиррола
- •Типы атомов азота в гетероциклах
- •Указания по выполнению самостоятельной работы № 6
- •Указания по выполнению самостоятельной работы № 7
- •В опросы для тестового контроля
- •Занятие № 11 Биологически важные производные шестичленных гетероциклов. Производные пурина
- •Растворимость мочевой кислоты и её натриевой соли в воде
- •Открытие мочевой кислоты (мурексидная проба)
- •Блок информации
- •Свойства шестичленных гетероциклов (π-недостаточных систем)
- •Электронное строение молекулы пиридина
- •Задания для тестового контроля
- •Занятие № 12 итоговое занятие по теме «метаболиты и родоначальники важнейших групп лекарственных препаратов»
- •Занятие № 13 углеводы. Моносахариды
- •Доказательство наличия гидроксильных групп в глюкозе
- •Восстановление гидроксида меди (II) глюкозой в щелочной среде (проба Троммера)
- •Восстановление аммиачного раствора оксида серебра глюкозой (реакция Толленса, реакция «серебряного зеркала»)
- •Химические свойства глюкозы (продолжение)
- •Химические свойства глюкозы (продолжение)
- •Вопросы для тестового контроля
- •Занятие № 14 углеводы. Дисахариды и полисахариды
- •Сравнение свойств лактозы и сахарозы
- •Качественная реакция на крахмал
- •Блок информации
- •Классификация полисахаридов
- •Указания по выполнению самостоятельной работы № 8
- •Задания для тестового контроля
- •Занятие № 15
- •Реакция на присутствие серусодержащих α-аминокислот
- •Блок информации
- •Классификация аминокислот белков
- •Основные виды взаимодействий, фиксирующих вторичную и третичную структуру пептидов и белков
- •Указания по выполнению самостоятельной работы № 9
- •Вопросы для тестового контроля
- •Занятие № 16 нуклеиновые кислоты. Омыляемые липиды
- •Щелочной гидролиз (омыление) жира
- •Занятие № 17 итоговое занятие по теме «углеводы, аминокислоты, пептиды, белки, нуклеиновые кислоты, омыляемые липиды»
- •Занятие № 18 стероиды. Алкалоиды. Зачёт по практическим навыкам
- •План изучения материала
- •Общие реакции на алкалоиды
- •Блок информации
- •Родоначальные структуры стероидов
- •Классификация алкалоидов
- •Перечень практических навыков, выносимых на зачётное занятие
- •Примерные экзаменационные вопросы по биоорганической химии
- •Литература Основная
- •Дополнительная
- •305041, Г. Курск, ул. К. Маркса, 3.
- •305041, Г. Курск, ул. К. Маркса, 3.
Реакция на присутствие серусодержащих α-аминокислот
В пробирку поместите 10 капель раствора яичного белка и вдвое больший объём 10% раствора гидроксида натрия. Содержимое пробирки прокипятите в течение 1 мин. К полученному щелочному раствору добавьте 5 капель 10% раствора ацетата свинца и вновь прокипятите. Что при этом наблюдается?
Напишите схему проведенных реакций на примере цистеина. Какие ещё α-аминокислоты белков можно открыть с помощью данной реакции?
Блок информации
Граф 28
Классификация аминокислот белков
ГЛИЦИН (Гли)
АЛАНИН (Ала)
ВАЛИН* (Вал)
ЛЕЙЦИН*(Лей)
ИЗОЛЕЙЦИН*(Иле)
ФЕНИЛАЛАНИН*(Фен)
ТРИПТОФАН*(Три)
ПРОЛИН (Про)
ГИДРОКСИЛСОДЕРЖАЩИЕ
СЕРИН (Сер)
ТРЕОНИН*(Тре)
ТИРОЗИН (Тир)
СЕРУСОДЕРЖАЩИЕ
ЦИСТЕИН (Цис)
ЦИСТИН (Цис-Цис)
МЕТИОНИН*(Мет)






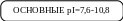
АСПАРАГИНОВАЯ
КИСЛОТА (Асп)
ГЛУТАМИНОВАЯ
КИСЛОТА (Глу)
ЛИЗИН*(Лиз)
АРГИНИН (Арг)
ГИСТИДИН (Гис)
pI – изоэлектрическая точка * - незаменимые аминокислоты
Таблица 18
Основные виды взаимодействий, фиксирующих вторичную и третичную структуру пептидов и белков
Ковалентные |
Нековалентные |
|
Дисульфидные связи |
Ионные связи |
Водородные связи |
Между простран-ственно сближенными цистеиновыми остатками |
Образуются
за счет притяжения между разноименно
заря-женными группами
|
внутрицепочечные |
Стабилизируют третичную структуру |
Стабилизируют вторичную и третичную структуру |
|
Указания по выполнению самостоятельной работы № 9
Раздел для самостоятельного изучения: Установление первичной структуры пептидов. Определение аминокислотной последовательности.
Актуальность изучаемого раздела: Полиамидные цепи полипептидов построены единообразно. Специфичность пептидов и белков определяется не только аминокислотным составом, но и аминокислотной последовательностью.
План изучения
Сущность метода деградации пептидов по Эдману (фенилизотиоцианатный метод).
Идентификация полученных ФТГ-производных.
Понятие о методе Сенгера (динитрофенилирование).
Вопросы для самоконтроля
1. Напишите схему реакции фенилизотиоцианата с глутаминовой кислотой.
2. Напишите строение ФТГ-производных, образующихся при расщеплении по Эдману трипептида Цис-Асп-Вал.
3. Напишите формулу трипептида и назовите его, если при его деградации по Эдману получены ФТГ-производные в последовательности:
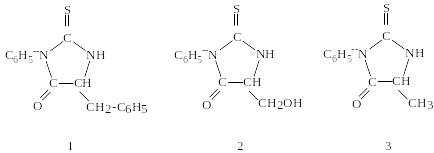
Форма контроля. Проверка упражнений, тестовый контроль на занятии.
Приложение
Вопросы для тестового контроля
УКАЖИТЕ СООТВЕТСТВИЯ!
1.
гетероциклическая аминокислота а) фенилаланин г) валин
алифатическая аминокислота б) тирозин д) аланин
в) триптофан
2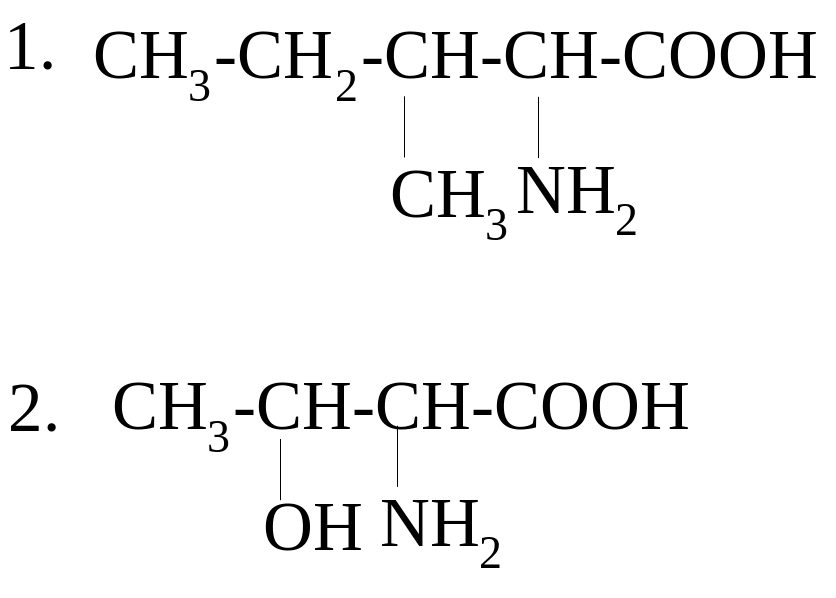 .
.
а) валин
б) лейцин
в) изолейцин
г) серин
д) треонин
3.
триптофан а) алифатическая аминокислота
глютаминовая кислота б) ароматическая аминокислота
фенилаланин в) гетероциклическая аминокислота
4.
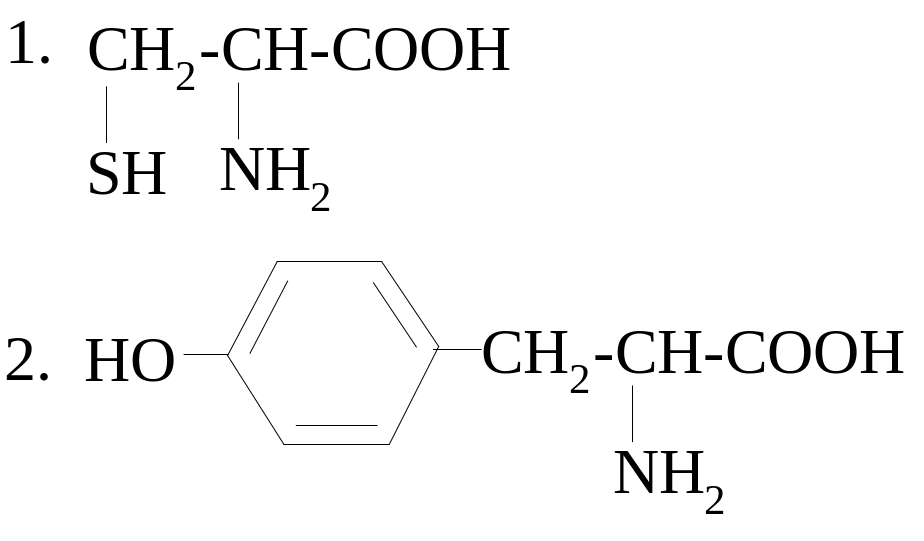 а)
тирозин
а)
тирозин
б) триптофан
в) серин
г) цистеин
д) цистин
5.
нейтральные аминокислоты а) валин г) глутаминовая кислота
кислые аминокислоты б) аланин д) лизин
в) аспарагиновая кислота
6.
аспарагиновая кислота а) алифатическая аминокислота
гистидин б) ароматическая аминокислота
фенилаланин в) гетероциклическая аминокислота
7.
серин а) кислая аминокислота
лизин б) основная аминокислота
в) нейтральная аминокислота
8.
триптофан а) алифатическая аминокислота
тирозин б) ароматическая аминокислота
серин в) гетероциклическая аминокислота
9.
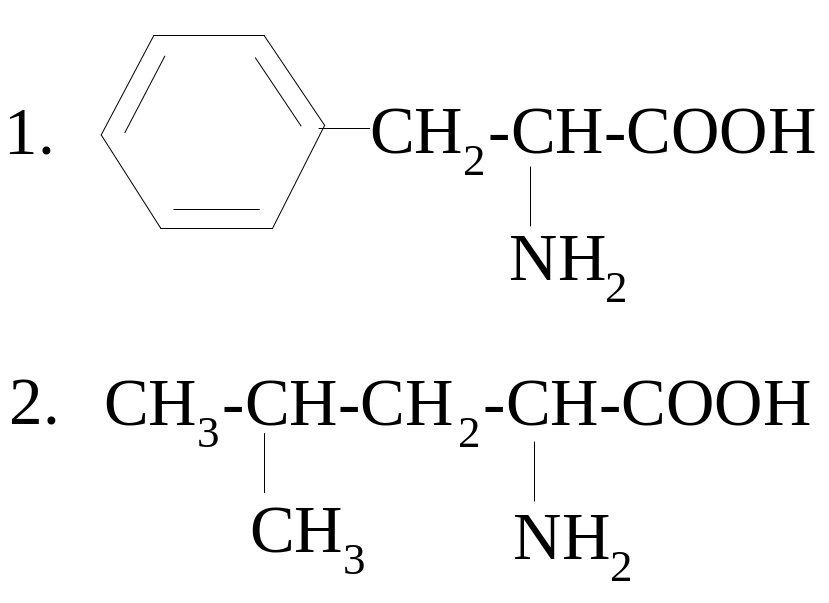
а) фенилаланин
б) тирозин
в) триптофан
г) валин
д) лейцин
е) изолейцин
10.
аргинин а) кислая аминокислота
цистин б) основная аминокислота
в) нейтральная аминокислота
УКАЖИТЕ ПРАВИЛЬНЫЙ ОТВЕТ (ОТВЕТЫ)!
11.
ГИДРОКСИЛСОДЕРЖАЩИЕ АМИНОКИСЛОТЫ:
аргинин 3. серин 5. треонин
метионин 4. цистеин
12.
СЕРУСОДЕРЖАЩИЕ АМИНОКИСЛОТЫ:
метионин 3. серин 5. треонин
аргинин 4. цистеин
13. ПРОЕКЦИОННАЯ ФОРМУЛА L-АЛАНИНА:
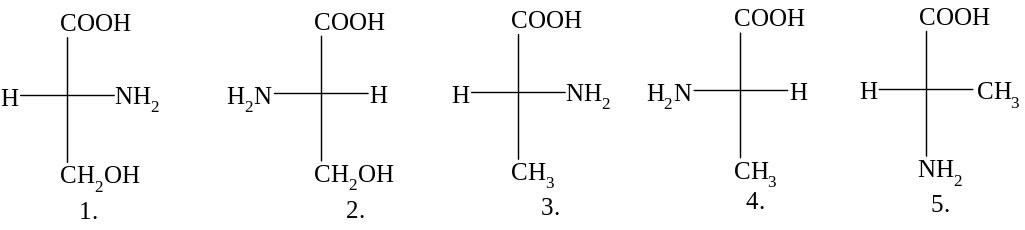
14. ПРОЕКЦИОННАЯ ФОРМУЛА ЭНАНТИОМЕРА D-ВАЛИНА:

15. ПРОЕКЦИОННАЯ ФОРМУЛА L-СЕРИНА:
16.
ПРОЕКЦИОННАЯ ФОРМУЛА ЭНАНТИОМЕРА L-ВАЛИНА:
17.
ИЗОЭЛЕКТРИЧЕСКАЯ ТОЧКА ЛИЗИНА НАХОДИТСЯ:
в нейтральной области pH
в кислой области pH
в щелочной области pH
18.
ИЗОЭЛЕКТРИЧЕСКАЯ ТОЧКА ИЗОЛЕЙЦИНА НАХОДИТСЯ:
в нейтральной области pH
в кислой области pH
в щелочной области pH
19.
В СИЛЬНОКИСЛОЙ СРЕДЕ ВАЛИН СУЩЕСТВУЕТ В ВИДЕ:
1. биполярного иона 2. катиона 3. аниона
20.
П![]() РИ
pH=3 ГЛИЦИН СУЩЕСТВУЕТ В
ВИДЕ:
РИ
pH=3 ГЛИЦИН СУЩЕСТВУЕТ В
ВИДЕ:
21.
ИЗОЭЛЕКТРИЧЕСКАЯ ТОЧКА АСПАРАГИНОВОЙ КИСЛОТЫ НАХОДИТСЯ:
в нейтральной области pH
в кислой области pH
в щелочной области pH
22.
В СИЛЬНОКИСЛОЙ СРЕДЕ АЛАНИН СУЩЕСТВУЕТ В ВИДЕ:
1. биполярного иона 2. катиона 3. аниона
23. ПРИ pH=12 ГЛИЦИН СУЩЕСТВУЕТ В ВИДЕ:
24. ВПИШИТЕ НЕДОСТАЮЩЕЕ СЛОВО (БУКВУ)!
МОЛЕКУЛЫ ПЕПТИДОВ ПОСТРОЕНЫ ИЗ ОСТАТКОВ ______-СТЕРЕОИЗОМЕРОВ α-АМИНОКИСЛОТ.
УКАЖИТЕ СООТВЕТСТВИЯ!
2 5.
5.
2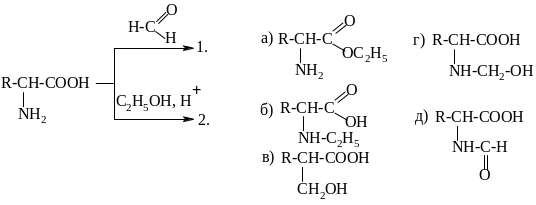 6.
6.
27.
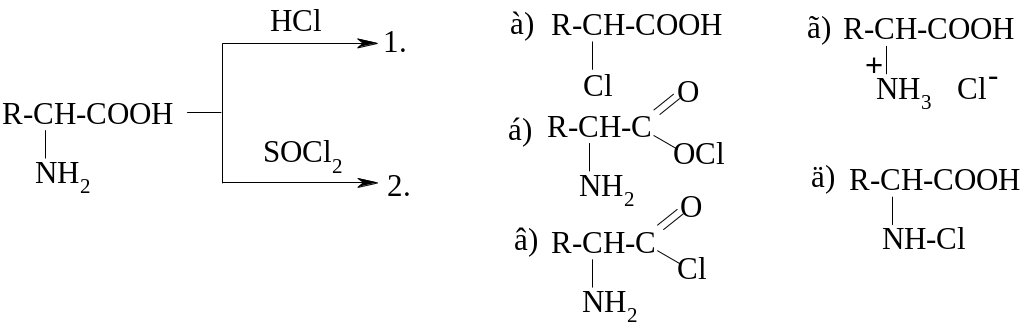
28.
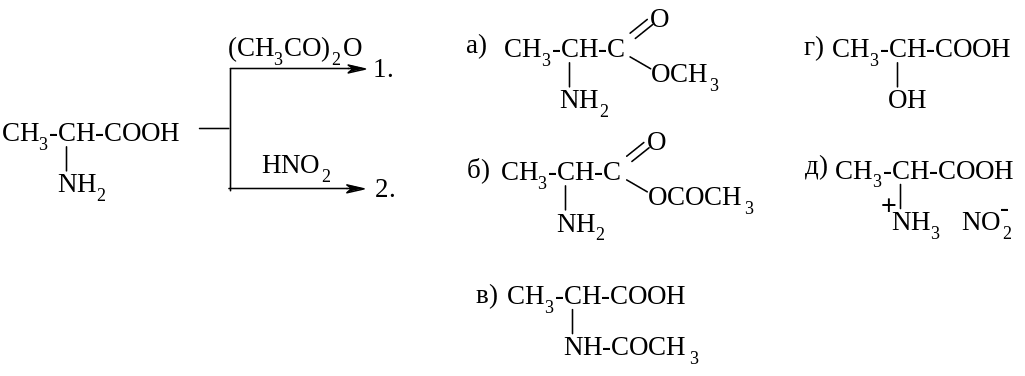
УКАЖИТЕ ПРАВИЛЬНЫЙ ОТВЕТ (ОТВЕТЫ)!
29.
КАЧЕСТВЕННОЙ РЕАКЦИЕЙ НА АРОМАТИЧЕСКИЕ АМИНОКИСЛОТЫ ЯВЛЯЕТСЯ РЕАКЦИЯ С:
(CH3CO)2Pb 4. конц. HNO3
конц. H2SO4 5. разбавленной HNO3
(CH3COO)2Pb 6. HNO2
30.
ФЕНИЛАЛАНИН И ТИРОЗИН МОЖНО РАЗЛИЧИТЬ ПО РЕАКЦИИ С:
конц. HNO3 3. FeCl3 5. HCl
конц. H2SO4 4. HNO2
31.
ПРИ ДЕКАРБОКСИЛИРОВАНИИ ГИСТИДИНА in vitro ОБРАЗУЕТСЯ :
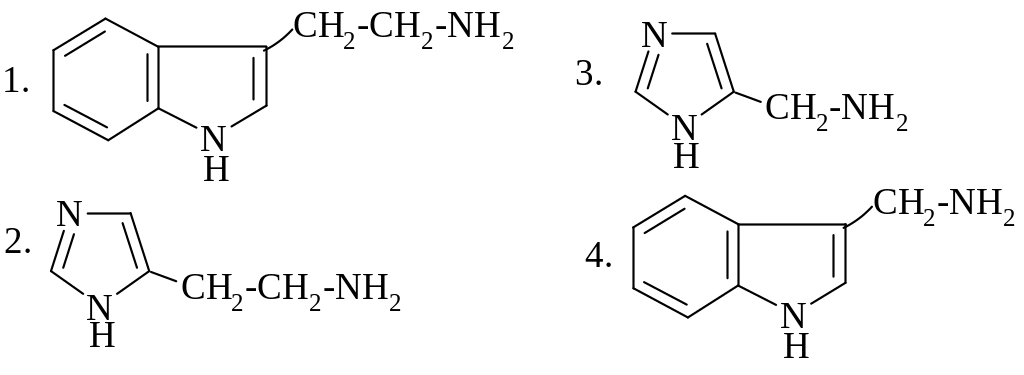
32.
ПРИ ДЕЗАМИНИРОВАНИИ ВАЛИНА in vitro ОБРАЗУЮТСЯ:
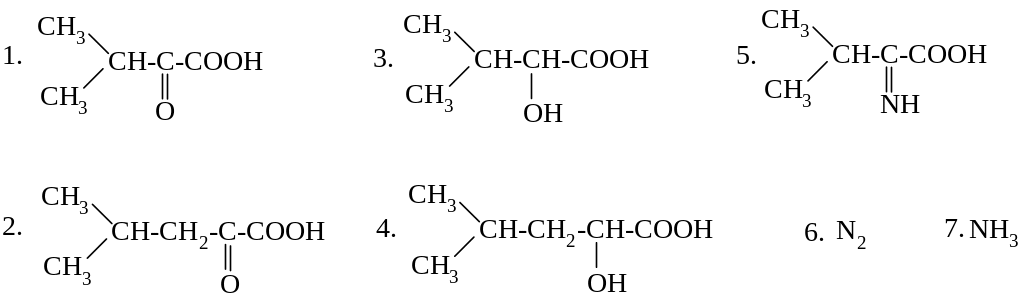
33.
КАЧЕСТВЕННОЙ РЕАКЦИЕЙ НА СЕРУСОДЕРЖАЩИЕ АМИНОКИСЛОТЫ ЯВЛЯЕТСЯ РЕАКЦИЯ С:
(CH3CO)2Pb 4. конц. HNO3
конц. H2SO4 5. разбавленной HNO3
(CH3COO)2Pb 6. HNO2
34.
ПРИ ДЕКАРБОКСИЛИРОВАНИИ ТРИПТОФАНА in vitro ОБРАЗУЕТСЯ:
35.
ФОРМУЛА ПРОДУКТА ДЕКАРБОКСИЛИРОВАНИЯ ГИСТИДИНА in vivo:
36.
ПРИ ОКИСЛИТЕЛЬНОМ ДЕЗАМИНИРОВАНИИ АЛАНИНА in vivo ОБРАЗУЕТСЯ:
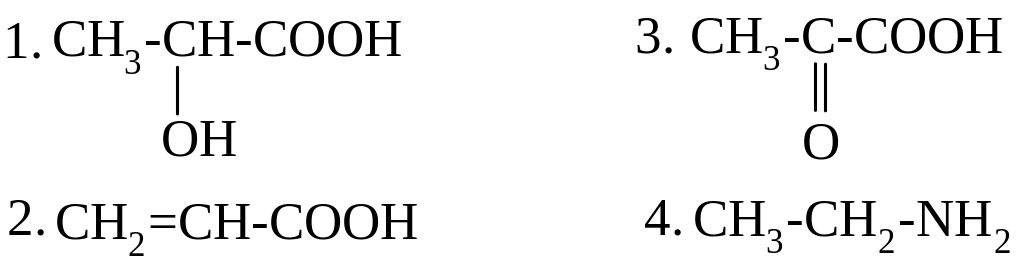
37.
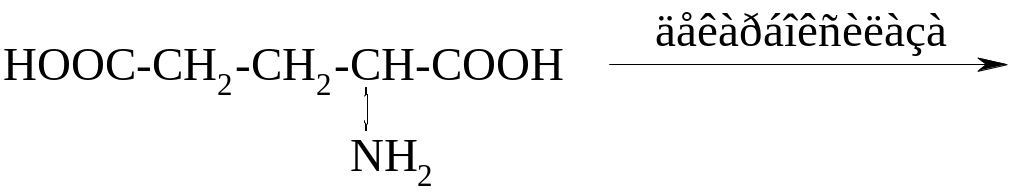
В РЕЗУЛЬТАТЕ РЕАКЦИИ ОБРАЗУЕТСЯ
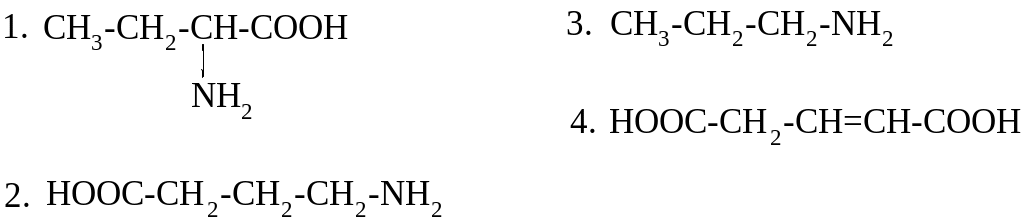
38.
ПРИ ОКИСЛИТЕЛЬНОМ ДЕЗАМИНИРОВАНИИ АСПАРАГИНОВОЙ КИСЛОТЫ in vivo ОБРАЗУЕТСЯ:

3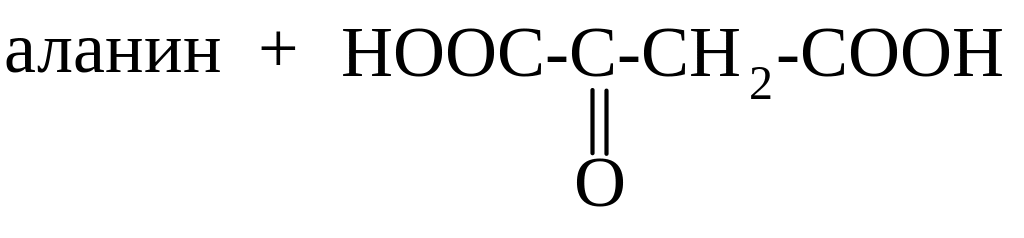 9.
9.
В РЕЗУЛЬТАТЕ ПЕРЕАМИНИРОВАНИЯ
ОБРАЗУЮТСЯ:

40.
Д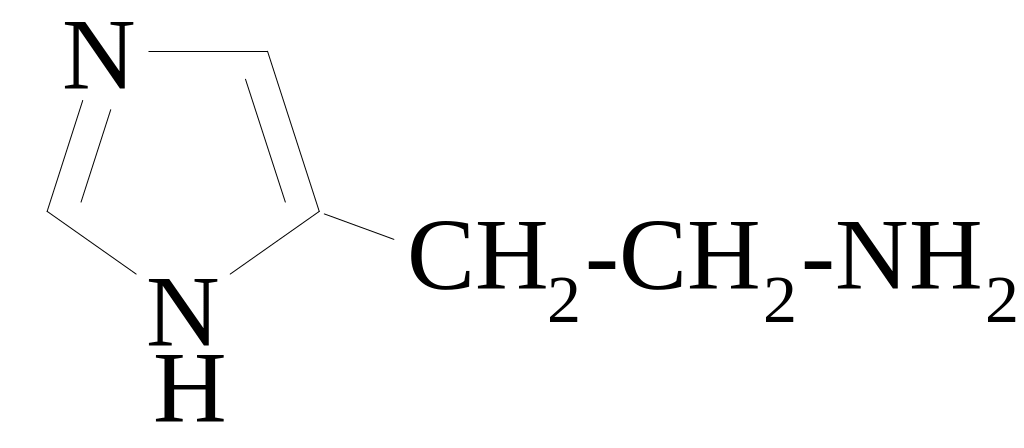 АННОЕ
СОЕДИНЕНИЕ ЯВЛЯЕТСЯ ПРОДУКТОМ:
АННОЕ
СОЕДИНЕНИЕ ЯВЛЯЕТСЯ ПРОДУКТОМ:
декарбоксилирования триптофана
декарбоксилирования гистидина
неокислительного дезаминирования гистидина
4. дезаминирования триптофана in vitro
ВПИШИТЕ НЕДОСТАЮЩЕЕ СЛОВО (СЛОВА)!
4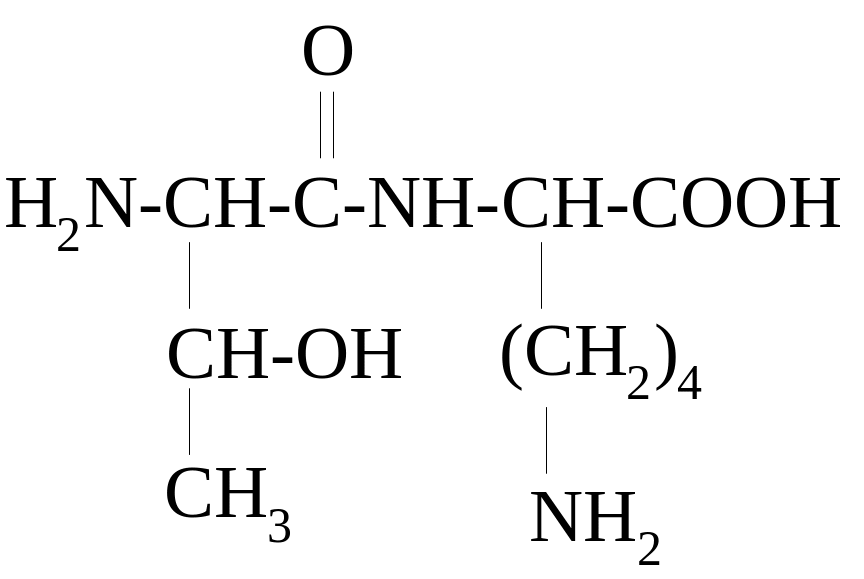 1.
1.
НАЗВАНИЕ ДИПЕПТИДА
______________________________________.
4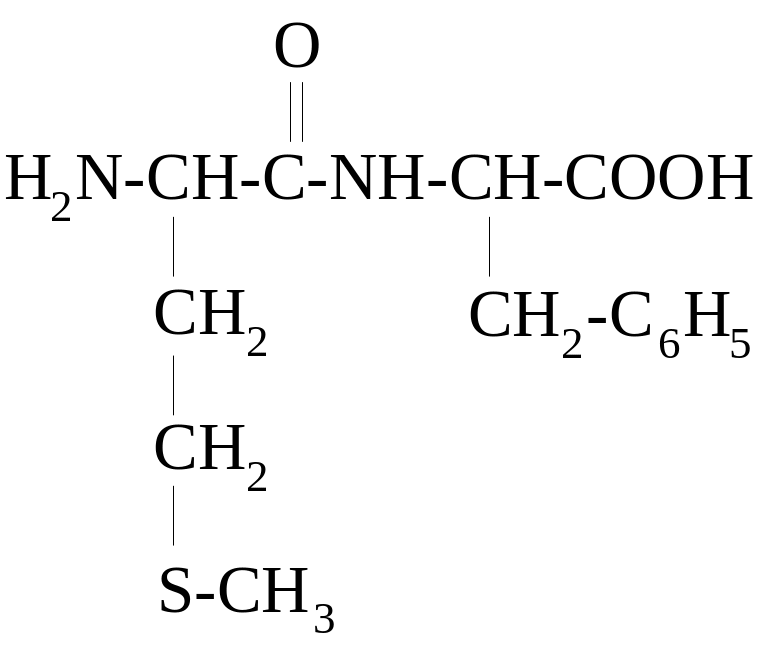 2.
2.
НАЗВАНИЕ ДИПЕПТИДА
______________________________________.

43.
НАЗВАНИЕ ДИПЕПТИДА
______________________________________.
4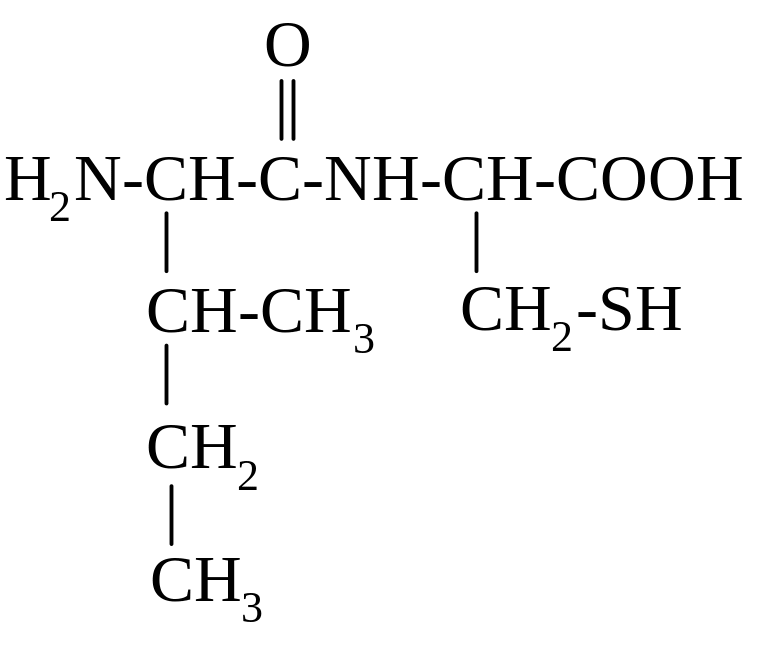 4.
4.
НАЗВАНИЕ ДИПЕПТИДА
______________________________________.
45.
РЕАКЦИЯ С КОНЦЕНТРИРОВАННОЙ АЗОТНОЙ КИСЛОТОЙ ЯВЛЯЕТСЯ КАЧЕСТВЕННОЙ НА _________________ АМИНОКИСЛОТЫ. ОНА НАЗЫВАЕТСЯ ______________________________ РЕАКЦИЕЙ.
46.
ПРИ НАГРЕВАНИИ ФЕНИЛАЛАНИНА С КОНЦЕНТРИРОВАННОЙ АЗОТНОЙ КИСЛОТОЙ ПОЯВЛЯЕТСЯ ___________________ ОКРАШИВАНИЕ, КОТОРОЕ В ЩЕЛОЧНОЙ СРЕДЕ ИЗМЕНЯЕТСЯ НА _____________________.
УКАЖИТЕ ПРАВИЛЬНЫЙ ОТВЕТ (ОТВЕТЫ)!
47.
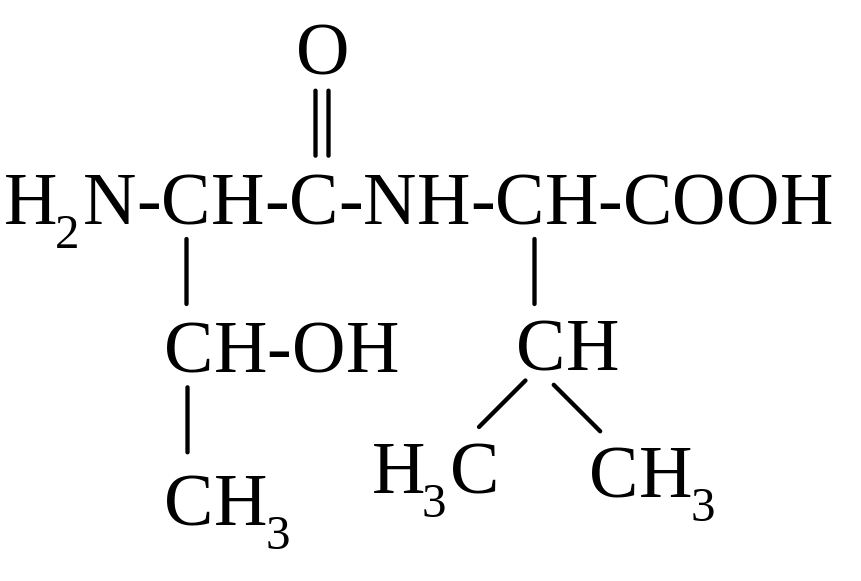
НАЗВАНИЕ ДИПЕПТИДА:
серилвалин
валилсерин
треонилсерин
серинвалин
треонинсерин
6. треонилвалин
4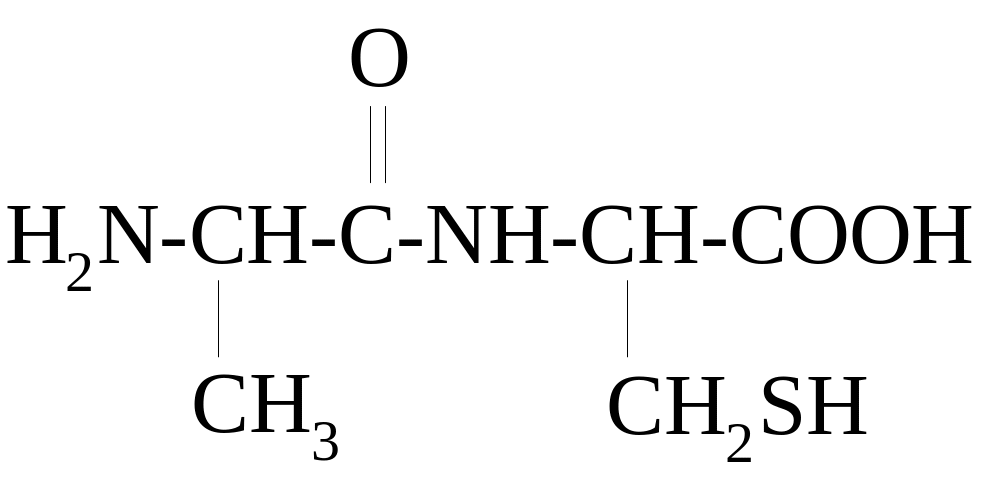 8.
8.
НАЗВАНИЕ ДИПЕПТИДА:
серилцистеин
серилметионин
аланинцистеин
аланилцистеин
цистеилсерин
цистеинсерин
49.
П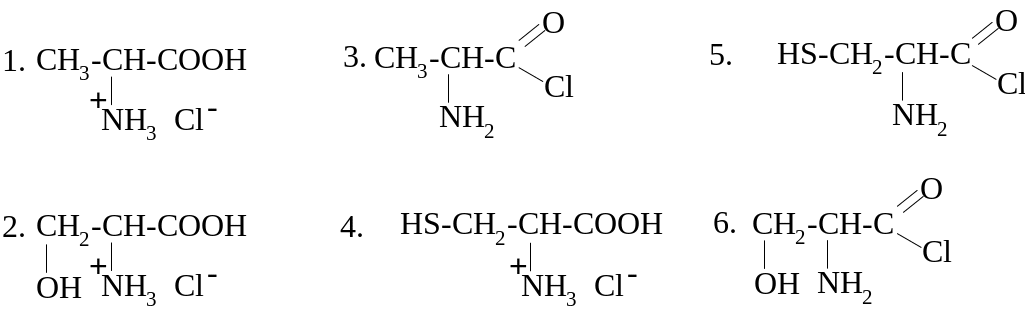 РИ
КИСЛОТНОМ (В ПРИСУТСТВИИ HCl)
ГИДРОЛИЗЕ АЛА-ЦИС
ОБРАЗУЮТСЯ:
РИ
КИСЛОТНОМ (В ПРИСУТСТВИИ HCl)
ГИДРОЛИЗЕ АЛА-ЦИС
ОБРАЗУЮТСЯ:
50.
ПРИ ЩЕЛОЧНОМ ГИДРОЛИЗЕ (NaOH) ДИПЕПТИДА ГЛИ-АЛА ОБРАЗУЮТСЯ:

51.
ПРИ ФЕРМЕНТАТИВНОМ ГИДРОЛИЗЕ ВАЛ-ТРЕ ОБРАЗУЮТСЯ:

52.
П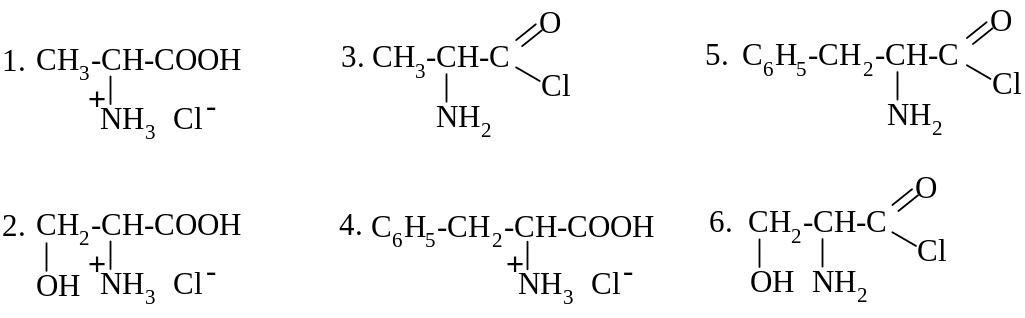 РИ
КИСЛОТНОМ (В ПРИСУТСТВИИ HCl)
ГИДРОЛИЗЕ АЛА-ФЕН
ОБРАЗУЮТСЯ:
РИ
КИСЛОТНОМ (В ПРИСУТСТВИИ HCl)
ГИДРОЛИЗЕ АЛА-ФЕН
ОБРАЗУЮТСЯ:
53.
П РИ КИСЛОТНОМ (В ПРИСУТСТВИИ HCl) ГИДРОЛИЗЕ АЛА-ЦИС ОБРАЗУЮТСЯ:
54.
Д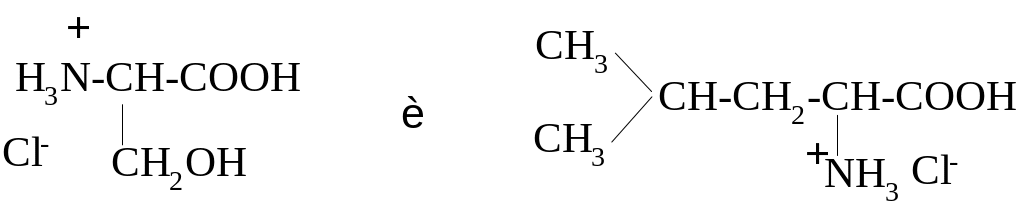 АННЫЕ
СОЕДИНЕНИЯ МОГУТ БЫТЬ ПРОДУКТАМИ:
АННЫЕ
СОЕДИНЕНИЯ МОГУТ БЫТЬ ПРОДУКТАМИ:
кислотного гидролиза Тре-Вал
ферментативного гидролиза Вал-Тре
кислотного гидролиза Сер-Лей
кислотного гидролиза Сер-Иле
кислотного гидролиза Лей-Сер
55.
ЭЛЕКТРОННОЕ И ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПЕПТИДНОЙ СВЯЗИ
ВЫРАЖЕНО ФОРМУЛОЙ:
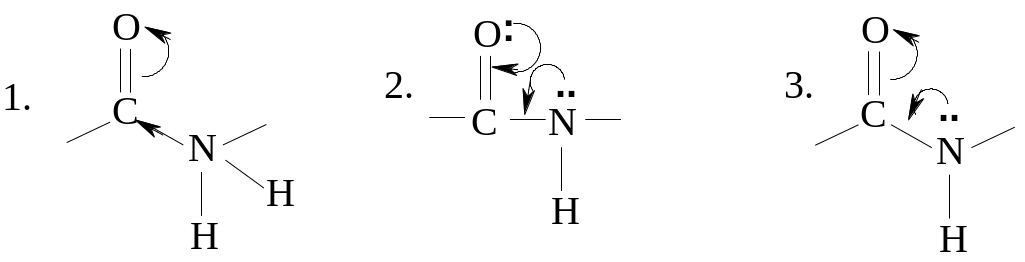
56.
РЕАГЕНТАМИ ДЛЯ БИУРЕТОВОЙ РЕАКЦИИ ЯВЛЯЮТСЯ:
1. конц. HNO3
2. CuSO4 + NaOH
3. (CH3COO)2Pb
4. CuSO4 + HCl
5. (CH3CO)2O
57.
РЕАКЦИЯ БЕЛКОВ С ГИДРОКСИДОМ МЕДИ (II) ЯВЛЯЕТСЯ КАЧЕСТВЕННОЙ.
на серусодержащие аминокислоты белков
на ароматические аминокислоты белков
на пептидные связи
на многоатомные спирты
58. ВПИШИТЕ НЕДОСТАЮЩИЕ СЛОВА (БУКВЫ, ЦИФРЫ)!
ПЕПТИДНАЯ СВЯЗЬ ПРЕДСТАВЛЯЕТ СОБОЙ ____ , _____-СОПРЯЖЁННУЮ СИСТЕМУ, В КОТОРОЙ ДЕЛОКАЛИЗОВАНО ___________ ЭЛЕКТРОНА.

