
- •Оглавление
- •Введение (как пользоваться учебно-методическим пособием)
- •Занятие № 1 классификация, номенклатура и структурная изомерия органических соединений. Электронное строение атомов элементов-органогенов
- •Блок информации
- •Классификация соединений по строению углеродного скелета
- •Важнейшие классы органических соединений
- •Построение названия органического соединения
- •Пример названия по заместительной номенклатуре iupac
- •Характеристические (функциональные) группы, их обозначение по номенклатуре iupac и соответствующие им классы органических соединений
- •Названия важнейших углеводородных радикалов
- •Валентное состояние и строение атома углерода в алифатических углеводородах
- •Правила техники безопасности при работе в химической лаборатории
- •Занятие № 2 химическая связь в органических молекулах. Классификация химических реакций. Реакционная способность алканов. Алкенов и алкадиенов
- •План изучения темы
- •Бромирование непредельных соединений
- •Окисление алкенов в мягких условиях (реакция Вагнера)
- •Блок информации
- •Типы химических связей атомов в молекулах органических соединений
- •Характеристика ковалентных связей
- •Свойства насыщенных углеводородов (алканов)
- •Свойства ненасыщенных углеводородов ряда этилена (алкенов)
- •Блок информации для выполнения самостоятельной работы
- •Конформации молекул алифатических углеводородов
- •Вопросы для тестового контроля
- •Занятие № 3 взаимное влияние атомов в молекулах органических соединений. Реакционная способность ароматических углеводородов
- •Влияние заместителей на последующее электрофильное замещение в ароматическом ядре
- •Вопросы для тестового контроля
- •Занятие № 4 химические свойства галогеналканов, спиртов и фенолов
- •План изучения темы
- •Получение этилхлорида из этилового спирта
- •Дегидратация этилового спирта
- •Свойства фенолов
- •Указания по выполнению самостоятельной работы № 2
- •Указания по выполнению самостоятельной работы № 3
- •Вопросы для тестового контроля
- •Заполните схему!
- •15. Возрастание кислотных свойств соединений:
- •Реакции окисления спиртов
- •31. Заполните схему!
- •Заполните схему!
- •Занятие № 5 кислотно-основные свойства органических соединений. Реакционная способность аминов
- •Получение этиленгликолята меди (II)
- •Образование фенолята натрия и разложение его кислотой
- •Сравнение основности алифатических и ароматических аминов
- •Блок информации
- •Значения pKa некоторых кислот Бренстеда
- •Кислотность различных классов соединений
- •Свойства первичных алифатических аминов
- •Вопросы для тестового контроля
- •3. Метиламин
- •Занятие № 6 реакционная способность оксосоединений
- •План изучения темы
- •Диспропорционирование формальдегида в водных растворах
- •Отношение ацетальдегида и ацетона к окислению щелочными растворами оксидов тяжёлых металлов
- •Открытие ацетона переводом его в йодоформ
- •Блок информации
- •Свойства альдегидов
- •Вопросы для тестового контроля
- •Занятие № 7 химические свойства карбоновых кислот и их функциональных производных
- •План работы на предстоящем занятии
- •Открытие щавелевой кислоты
- •Получение этилацетата
- •Блок информации
- •Свойства насыщенных монокарбоновых кислот
- •Кислотные свойства карбоновых кислот
- •Производные угольной кислоты
- •Указания по выполнению самостоятельной работы № 4
- •Вопросы для тестового контроля
- •Занятие № 8 итоговое занятие по теме «гомофункциональные производные углеводородов»
- •Занятие № 9 гетерофункциональные алифатические соединения - метаболиты и биорегуляторы
- •Доказательство наличия двух карбоксильных групп в винной кислоте
- •Доказательство наличия гидроксильных групп в винной кислоте
- •Блок информации
- •Классификация кислород- и азотсодержащих гетерофункциональных соединений
- •Свойства α-гидроксикислот
- •Специфические свойства α-, β-, γ-гидроксикислот
- •Свойства α-аминокислот
- •Специфические свойства α-, β-, γ-аминокислот
- •Вопросы для тестового контроля
- •Занятие № 10 гетерофункциональные соединения бензольного ряда. Биологически активные производные пятичленных гетероциклических соединений
- •Свойства пятичленных гетероциклов с одним гетероатомом (π-избыточных систем)
- •Свойства пятичленных гетероциклов с двумя гетероатомами
- •Электронное строение молекулы пиррола
- •Типы атомов азота в гетероциклах
- •Указания по выполнению самостоятельной работы № 6
- •Указания по выполнению самостоятельной работы № 7
- •В опросы для тестового контроля
- •Занятие № 11 Биологически важные производные шестичленных гетероциклов. Производные пурина
- •Растворимость мочевой кислоты и её натриевой соли в воде
- •Открытие мочевой кислоты (мурексидная проба)
- •Блок информации
- •Свойства шестичленных гетероциклов (π-недостаточных систем)
- •Электронное строение молекулы пиридина
- •Задания для тестового контроля
- •Занятие № 12 итоговое занятие по теме «метаболиты и родоначальники важнейших групп лекарственных препаратов»
- •Занятие № 13 углеводы. Моносахариды
- •Доказательство наличия гидроксильных групп в глюкозе
- •Восстановление гидроксида меди (II) глюкозой в щелочной среде (проба Троммера)
- •Восстановление аммиачного раствора оксида серебра глюкозой (реакция Толленса, реакция «серебряного зеркала»)
- •Химические свойства глюкозы (продолжение)
- •Химические свойства глюкозы (продолжение)
- •Вопросы для тестового контроля
- •Занятие № 14 углеводы. Дисахариды и полисахариды
- •Сравнение свойств лактозы и сахарозы
- •Качественная реакция на крахмал
- •Блок информации
- •Классификация полисахаридов
- •Указания по выполнению самостоятельной работы № 8
- •Задания для тестового контроля
- •Занятие № 15
- •Реакция на присутствие серусодержащих α-аминокислот
- •Блок информации
- •Классификация аминокислот белков
- •Основные виды взаимодействий, фиксирующих вторичную и третичную структуру пептидов и белков
- •Указания по выполнению самостоятельной работы № 9
- •Вопросы для тестового контроля
- •Занятие № 16 нуклеиновые кислоты. Омыляемые липиды
- •Щелочной гидролиз (омыление) жира
- •Занятие № 17 итоговое занятие по теме «углеводы, аминокислоты, пептиды, белки, нуклеиновые кислоты, омыляемые липиды»
- •Занятие № 18 стероиды. Алкалоиды. Зачёт по практическим навыкам
- •План изучения материала
- •Общие реакции на алкалоиды
- •Блок информации
- •Родоначальные структуры стероидов
- •Классификация алкалоидов
- •Перечень практических навыков, выносимых на зачётное занятие
- •Примерные экзаменационные вопросы по биоорганической химии
- •Литература Основная
- •Дополнительная
- •305041, Г. Курск, ул. К. Маркса, 3.
- •305041, Г. Курск, ул. К. Маркса, 3.
Вопросы для тестового контроля
УКАЖИТЕ СООТВЕТСТВИЕ!
1.
![]() атом
тип гибридизации
атом
тип гибридизации
а) sp3
б) sp2
в) sp
2.
атом тип гибридизации
![]()
а) sp3
б) sp2
в) sp
3.
атом тип гибридизации
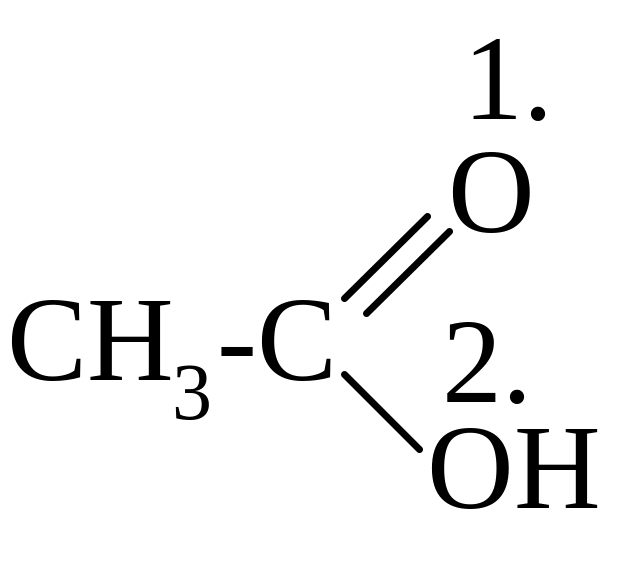
а) sp3
б) sp2
в) sp
4.
атом тип гибридизации
![]()
а) sp3
б) sp2
в) sp
5.
атом валентный угол
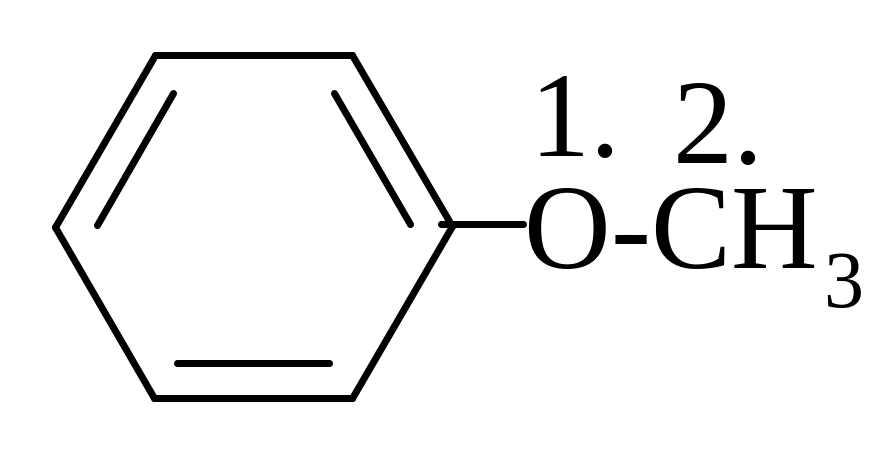 а)
109о28’
а)
109о28’
б) 120о
в) 180о
6.
атом валентный угол
а) 109о28’
б) 120о
в) 180о
7.
тип гибридизации валентный угол
атома углерода
1. sp3 а) 120о г) 109о28’
2. sp2 б) 180о д) 360о
3. sp в) 90о
8.
атом валентный угол
![]()
а) 109о28’
б) 120о
в) 180о
УКАЖИТЕ ПРАВИЛЬНЫЙ ОТВЕТ!
9.
ЭЛЕКТРОННАЯ КОНФИГУРАЦИЯ АТОМА АЗОТА В МОЛЕКУЛЕ
АНИЛИНА (АМИНОБЕНЗОЛА):

10.
ЭЛЕКТРОННАЯ КОНФИГУРАЦИЯ АТОМА УГЛЕРОДА
В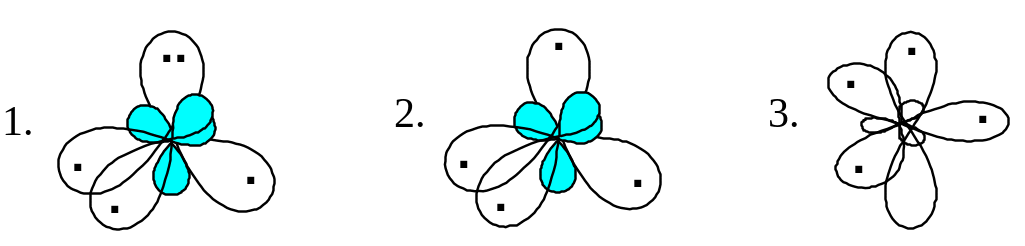 МОЛЕКУЛЕ ЭТЕНА:
МОЛЕКУЛЕ ЭТЕНА:
11.
ЭЛЕКТРОННАЯ КОНФИГУРАЦИЯ АТОМА АЗОТА В МОЛЕКУЛЕ
МЕТИЛАМИНА (CH3-NH2 ):

12.
ЭЛЕКТРОННАЯ КОНФИГУРАЦИЯ АТОМА УГЛЕРОДА В МОЛЕКУЛЕ
ПРОПАНА:

ВПИШИТЕ НЕДОСТАЮЩИЕ СЛОВА!
13.
σ
 -СВЯЗЬ
ОБРАЗУЕТСЯ В РЕЗУЛЬТАТЕ
ПЕРЕКРЫВАНИЯ АТОМНЫХ
ОРБИТАЛЕЙ, А π-СВЯЗЬ – ЗА СЧЁТ
ПЕРЕКРЫВАНИЯ АТОМНЫХ
ОРБИТАЛЕЙ.
-СВЯЗЬ
ОБРАЗУЕТСЯ В РЕЗУЛЬТАТЕ
ПЕРЕКРЫВАНИЯ АТОМНЫХ
ОРБИТАЛЕЙ, А π-СВЯЗЬ – ЗА СЧЁТ
ПЕРЕКРЫВАНИЯ АТОМНЫХ
ОРБИТАЛЕЙ.
14.
В МОЛЕКУЛЕ ЭТЕНА ЗА СЧЁТ ОСЕВОГО ПЕРЕКРЫВАНИЯ _______________________-ГИБРИДИЗОВАННЫХ ОРБИТАЛЕЙ ОБРАЗУЕТСЯ С-С σ-СВЯЗЬ, А ЗА СЧЁТ БОКОВОГО ПЕРЕКРЫВАНИЯ ________________ ОРБИТАЛЕЙ С-С π-СВЯЗЬ.
УКАЖИТЕ СООТВЕТСТВИЯ!
15
связь длина связи
C-C а) 0,120 нм
C=C б) 0,134 нм
 в)
0,154 нм
в)
0,154 нм
16.
связь тип и длина связи
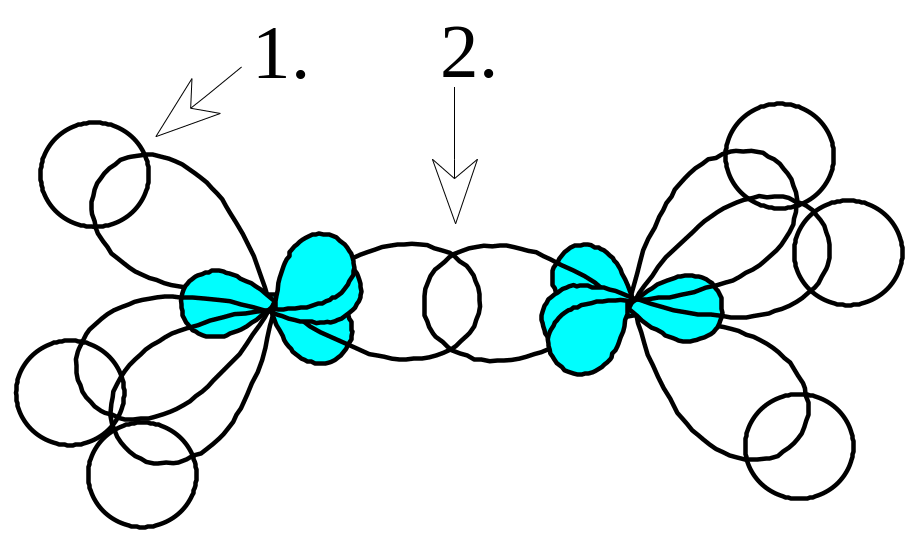 а)
σ-связь
а)
σ-связь
б) π-связь
в) 0,154 нм
г) 0,110 нм
17.
![]() длина
связи связь
длина
связи связь
0,154 нм а)
0,134 нм б) C=C
0,120 нм в) С-С
г) С-Н
18.
связь энергия связи
C-C а) 814 кДж/моль
C=C б) 620 кДж/моль
![]() в)
348 кДж/моль
в)
348 кДж/моль
УКАЖИТЕ ПРАВИЛЬНЫЙ ОТВЕТ!
19.
ЭНЕРГИЯ СВЯЗИ – ЭТО ЭНЕРГИЯ:
1. необходимая для образования связи
2. выделяющаяся при образовании связи
3. выделяющаяся при сгорании 1 моль органического соединения
ЗАПОЛНИТЕ СХЕМУ!
(вставьте в квадраты номера нужных ответов)
20.
ПОРЯДОК УВЕЛИЧЕНИЯ ЭНЕРГИИ СВЯЗИ:


 1
[ ] 2 [ ] 3 [ ] 1.
C-H
1
[ ] 2 [ ] 3 [ ] 1.
C-H
2. C-C
3. Cl-Cl
21.
ПОРЯДОК УВЕЛИЧЕНИЯ ЭНЕРГИИ СВЯЗИ:
1 [ ] 2 [ ] 3 [ ] 1. Н-Н
2. C-С
3. Br-Br
22.
ПОРЯДОК УВЕЛИЧЕНИЯ ПОЛЯРНОСТИ СВЯЗИ:
1 [ ] 2 [ ] 3 [ ] 1. C-H
2. C-N
3. C-Cl
23.
ПОРЯДОК УВЕЛИЧЕНИЯ ПОЛЯРНОСТИ СВЯЗИ:
1 [ ] 2 [ ] 3 [ ] 1. C-I
2. C-Br
3. C-Cl
24.
ПОРЯДОК УВЕЛИЧЕНИЯ ПОЛЯРНОСТИ СВЯЗИ:
1 [ ] 2 [ ] 3 [ ] 1. C-Cl
2. C-H
3. C-I
25.
ПОРЯДОК УВЕЛИЧЕНИЯ ПОЛЯРНОСТИ СВЯЗИ:
1 [ ] 2 [ ] 3 [ ] 1. O-H
2. C-H
3. N-H
26.
ПОРЯДОК УВЕЛИЧЕНИЯ ПОЛЯРИЗУЕМОСТИ СВЯЗИ:
1 [ ] 2 [ ] 3 [ ] 1. C-C
2. C-H
3. C-Br
27.
ПОРЯДОК УВЕЛИЧЕНИЯ ПОЛЯРИЗУЕМОСТИ СВЯЗИ:
1 [ ] 2 [ ] 3 [ ] 1. C-O
2. C-H
3. C-Br
28.
ПОРЯДОК УВЕЛИЧЕНИЯ ПОЛЯРИЗУЕМОСТИ СВЯЗИ:
1 [ ] 2 [ ] 3 [ ] 1. C-H
2. C-Cl
3. C-Br
29.
ПОРЯДОК УВЕЛИЧЕНИЯ ПОЛЯРИЗУЕМОСТИ СВЯЗИ:
1 [ ] 2 [ ] 3 [ ] 1. С-С σ
2. C-С π
3. С-H
УКАЖИТЕ СООТВЕТСТВИЯ!
30
 тип связи
тип связи
а) ковалентная неполярная
б) ковалентная полярная
в) ионная
г) водородная
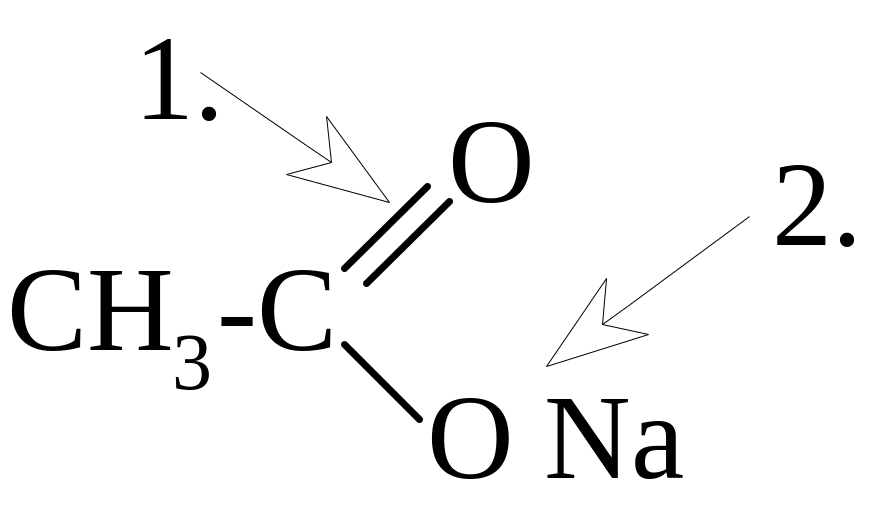
31. тип связи
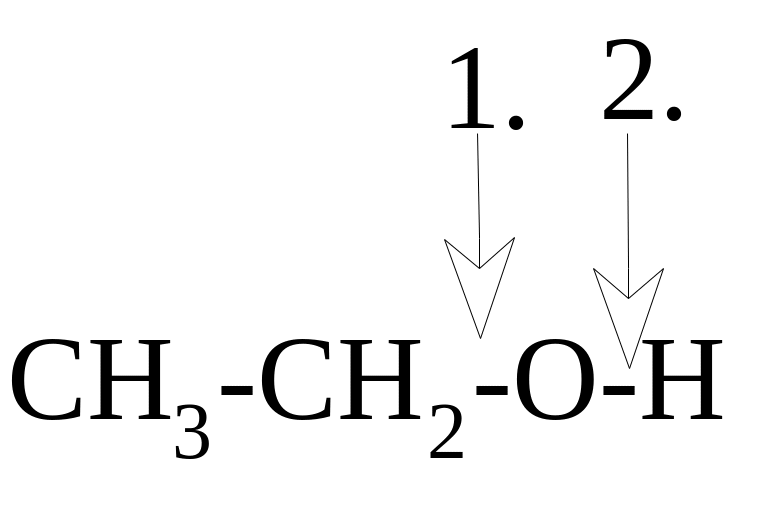 а) ковалентная
неполярная
а) ковалентная
неполярная
б) ковалентная полярная
в) ионная
г) водородная
32.
ВПИШИТЕ НЕДОСТАЮЩЕЕ СЛОВО!
π -СВЯЗЬ ПОЛЯРИЗУЕТСЯ ЧЕМ σ-СВЯЗЬ.
УКАЖИТЕ ПРАВИЛЬНЫЙ ОТВЕТ!
33.
 CH3-Cl
+ NaOH CH3-OH
+ NaCl ЭТО РЕАКЦИЯ:
CH3-Cl
+ NaOH CH3-OH
+ NaCl ЭТО РЕАКЦИЯ:
1. замещения 3. присоединения
2. отщепления 4. окисления
34.
c. H2SO4
 CH3-CH2-OH
CH2=CH2
+ H2O
ЭТО РЕАКЦИЯ:
CH3-CH2-OH
CH2=CH2
+ H2O
ЭТО РЕАКЦИЯ:
1. замещения 3. присоединения
2. отщепления 4. окисления
35.
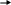 CH2=CH2
+ HCl CH3-CH2-Cl
ЭТО РЕАКЦИЯ
CH2=CH2
+ HCl CH3-CH2-Cl
ЭТО РЕАКЦИЯ
1. замещения 3. присоединения
2. отщепления 4. окисления
3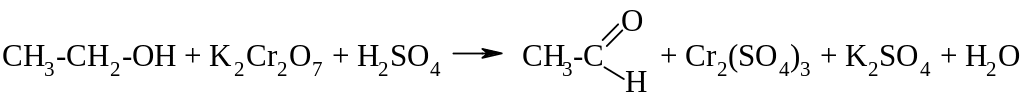 6.
6.
ЭТО РЕАКЦИЯ
1. замещения 3. присоединения
2. отщепления 4. окисления
37.
ТИП РАЗРЫВА СВЯЗИ C-Cl: 1. гомолитический
2. гетеролитический
УКАЖИТЕ СООТВЕТСТВИЯ!
38.
тип разрыва связи примеры связей
гомолитический a) C-C в) C-Cl д) Cl-Cl
гетеролитический б) C-H г) C-O
39.
тип разрыва связи примеры связей
радикальный a) H-H в) C-H д) Br-Br
ионный б) C-Br г) C-O
40.
связь тип разрыва
Cl-Cl а) гомолитический
C-Br б) гетеролитический
O-H
41.
тип реагента примеры
электрофил a) Cl - г) NH3
нуклеофил б) Br. д) NO2+
в) HO -
УКАЖИТЕ ПРАВИЛЬНЫЕ ОТВЕТЫ!
42.
ФАКТОРЫ, СПОСОБСТВУЮЩИЕ ГЕТЕРОЛИТИЧЕСКОМУ ТИПУ РАЗРЫВА СВЯЗИ:
неполярность связи 4. полярный растворитель
высокая полярность связи 5. неполярный растворитель
УФ-облучение 6. кислотный или основный катализ
43.
ФАКТОРЫ, СПОСОБСТВУЮЩИЕ ГОМОЛИТИЧЕСКОМУ ТИПУ РАЗРЫВА СВЯЗИ:
УФ-облучение 3. высокая полярность связи 5. неполярный
нагревание 4. полярный растворитель растворитель
44.
ЭЛЕКТРОФИЛАМИ ЯВЛЯЮТСЯ:
1. OH- 3. Br - 5. H+
2. Cl+ 4. SO3
45.
НУКЛЕОФИЛАМИ ЯВЛЯЮТСЯ: 1. NH3 3. OH -
2. Cl+ 4. H+
46.
УКАЖИТЕ СООТВЕТСТВИЯ!
реагент тип реагента
1. NH3 а) электрофил
2. OH- б) нуклеофил
3. H+ в) радикал
47.
УКАЖИТЕ ПРАВИЛЬНЫЙ ОТВЕТ!
СВОБОДНЫЙ РАДИКАЛ – ЭТО:
частица, имеющая положительный заряд
нейтральная частица с неспаренным электроном
нейтральная частица с неподелённой электронной парой
частица, имеющая отрицательный заряд
48.
ВПИШИТЕ НЕДОСТАЮЩЕЕ СЛОВО!
НАЗВАНИЕ СОЕДИНЕНИЯ ПО НОМЕНКЛАТУРЕ IUPAC - __________________

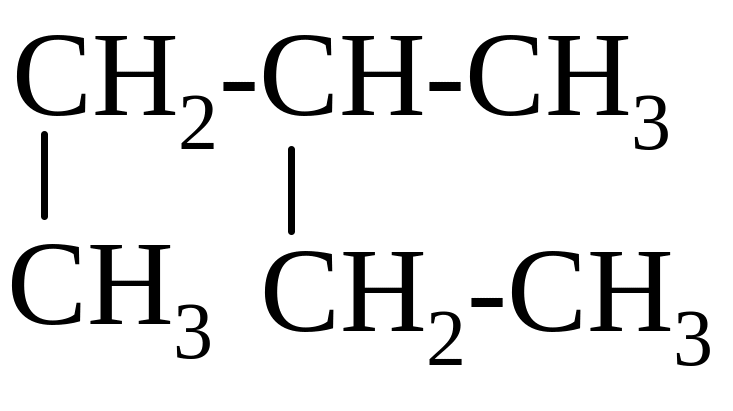
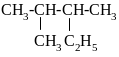 а)
б)
в)
а)
б)
в)

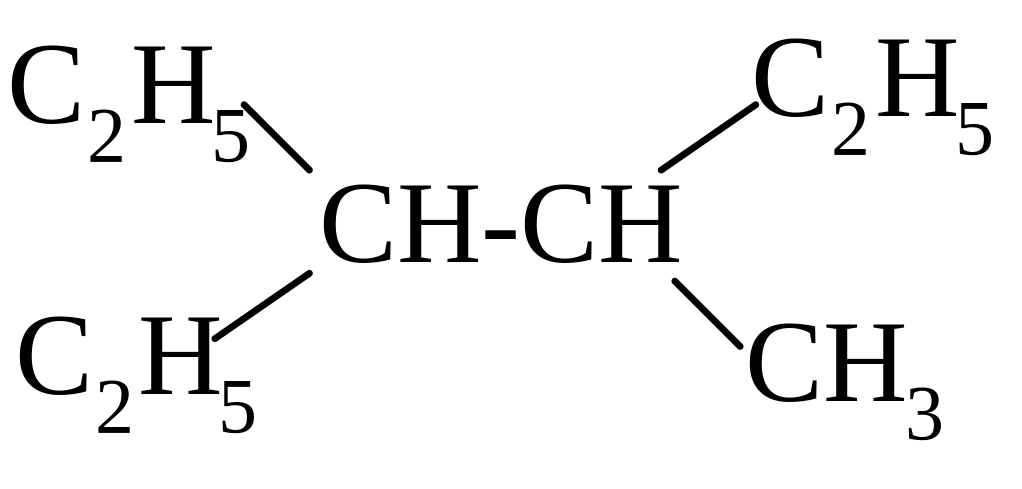
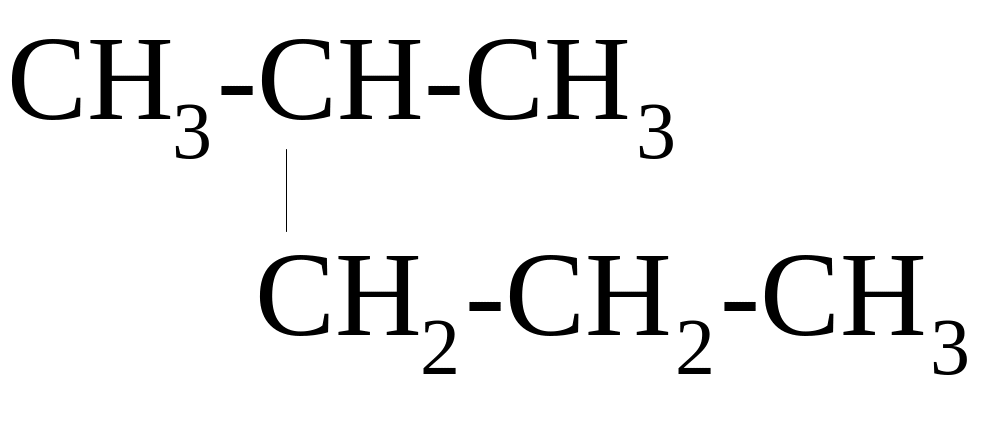 г)
д)
е)
г)
д)
е)

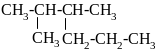 ж)
з)
ж)
з)
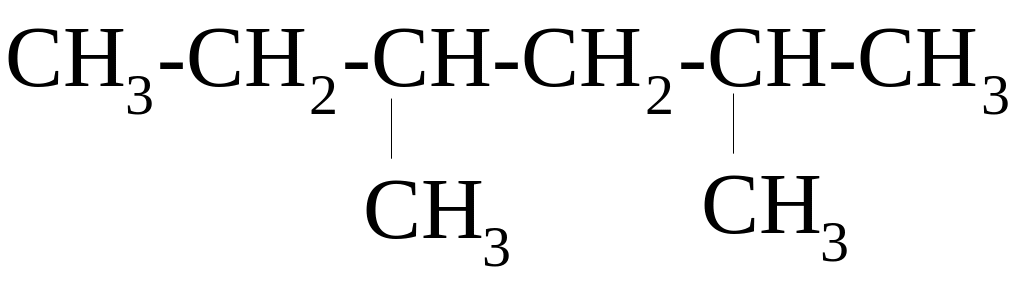
и)
УКАЖИТЕ СООТВЕТСТВИЯ!
49.
СВЯЗИ В МОЛЕКУЛЕ ЭТАНА
связь её тип
C-C a) σ-связь в) полярная
C-H б) π-связь г) неполярная
50.
НАЗВАНИЯ РАДИКАЛОВ
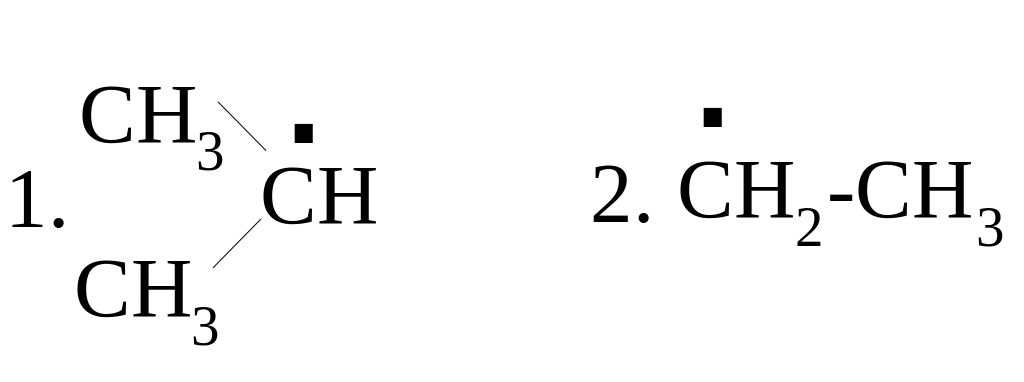 строение
название
строение
название
а) этен в) метил д) изопропил
б) этил г) пропил е) 2-этил
51.
радикал его тип
1. CH3-CH2. a) первичный в) третичный
2. . CH2-CH2-CH2-CH3 б) вторичный г) четвертичный
52.
алкан радикал, могущий образоваться при разрыве C-H связи
этан a) этин в) пропил д) изопропил
пропан б) этил г) изоэтил
53.
радикал
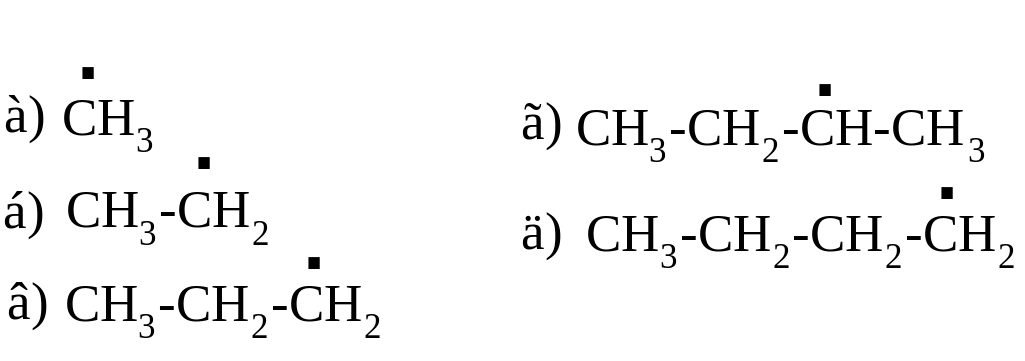 его строение
его строение
этил
бутил
УКАЖИТЕ ПРАВИЛЬНЫЙ ОТВЕТ!
54.
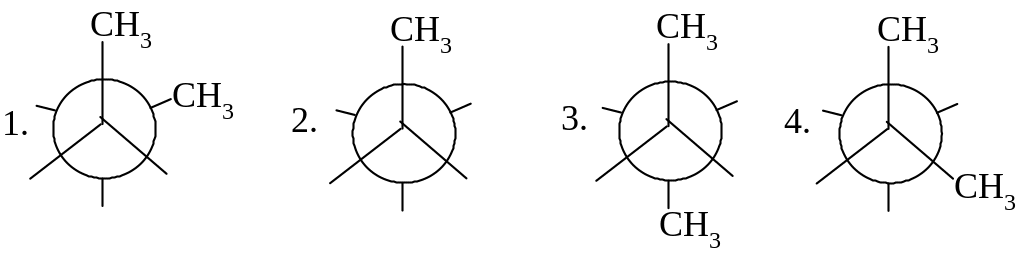
ФОРМУЛА НЬЮМЕНА СКОШЕННОЙ КОНФОРМАЦИИ ПЕНТАНА (C2-C3):

55.
ФОРМУЛА НЬЮМЕНА ЗАТОРМОЖЕННОЙ КОНФОРМАЦИИ БУТАНА (C2-C3):
56.
РЕАКЦИЯ ХЛОРИРОВАНИЯ ПРОПАНА ПРОТЕКАЕТ ПО МЕХАНИЗМУ:
1. радикального присоединения 3. электрофильного присоединения
2. радикального замещения 4. окисления
57.
РЕАКЦИИ, ХАРАКТЕРНЫЕ ДЛЯ АЛКАНОВ:
1. SE 2. SN 3. SR 4. AE
58.
УФ-ОБЛУЧЕНИЕ В РЕАКЦИИ БРОМИРОВАНИЯ ЭТАНА НЕОБХОДИМО ДЛЯ:
разрыва С-С-связи 3. получения радикалов брома
разрыва C-H-связей 4. образования связи C-Br
59.
УКАЖИТЕ СООТВЕТСТВИЯ!
РЕАКЦИЯ БРОМИРОВАНИЯ МЕТАНА
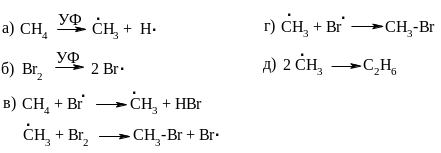 стадия
реакции
стадия
реакции
инициирование
рост цепи
обрыв цепи
ЗАПОЛНИТЕ СХЕМУ!
(вставьте в квадраты номера нужных ответов)
60.
ПОСЛЕДОВАТЕЛЬНОСТЬ СТАДИЙ В РЕАКЦИЯХ РАДИКАЛЬНОГО ЗАМЕЩЕНИЯ:
1 [ ] 2 [ ] 3 [ ] 1. стадия роста цепи
2. стадия инициирования
3. стадия роста радикалов
4. стадия обрыва цепи
61.
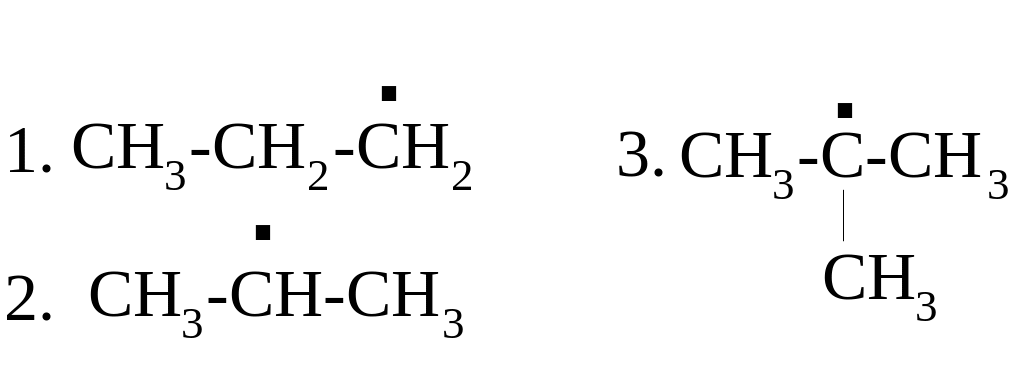 ПОРЯДОК
УВЕЛИЧЕНИЯ СТАБИЛЬНОСТИ РАДИКАЛОВ:
ПОРЯДОК
УВЕЛИЧЕНИЯ СТАБИЛЬНОСТИ РАДИКАЛОВ:
1 [ ] 2 [ ] 3 [ ]
62.
ПОРЯДОК УВЕЛИЧЕНИЯ СТАБИЛЬНОСТИ РАДИКАЛОВ:

1 [ ] 2 [ ] 3 [ ]
УКАЖИТЕ ПРАВИЛЬНЫЙ ОТВЕТ!
63.
ОСНОВНЫМ ПРОДУКТОМ НИТРОВАНИЯ БУТАНА ЯВЛЯЕТСЯ:
1. 1-нитробутан 2. 2-нитробутан 3. 3-нитробутан 4. 4-нитробутан
64.
ОСНОВНОЙ ПРОДУКТ РЕАКЦИИ ХЛОРИРОВАНИЯ БУТАНА:
1. 1-хлорбутан 2. 2-хлорбутан 3. 1,2-дихлорбутан
65.
ОСНОВНЫМ ПРОДУКТОМ ХЛОРИРОВАНИЯ ПРОПАНА ЯВЛЯЕТСЯ:
1-хлорпропан 3. 3-хлорпропан
2-хлорпропан
66.
ОСНОВНЫМ ПРОДУКТОМ РЕАКЦИИ ХЛОРИРОВАНИЯ 2-МЕТИЛБУТАНА ЯВЛЯЕТСЯ:
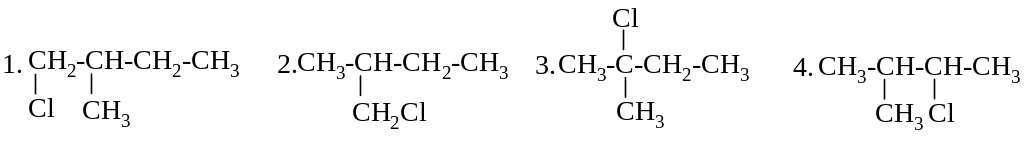
67.
ВПИШИТЕ НЕДОСТАЮЩЕЕ СЛОВО!
НАЗВАНИЕ СОЕДИНЕНИЯ ПО IUPAC - ________________________
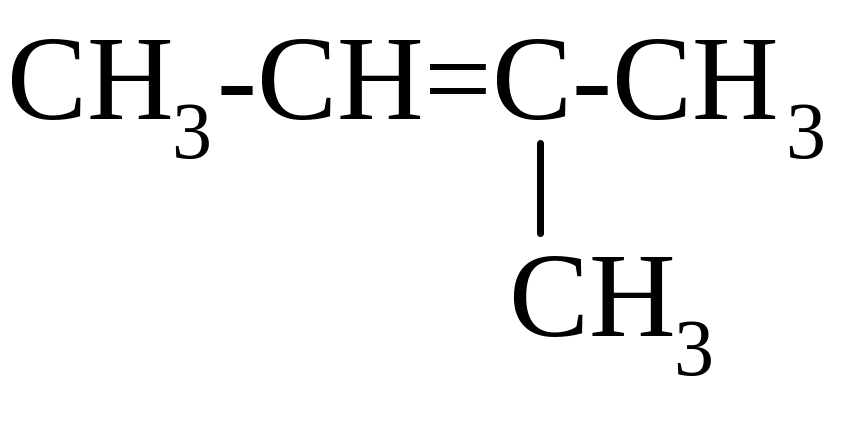
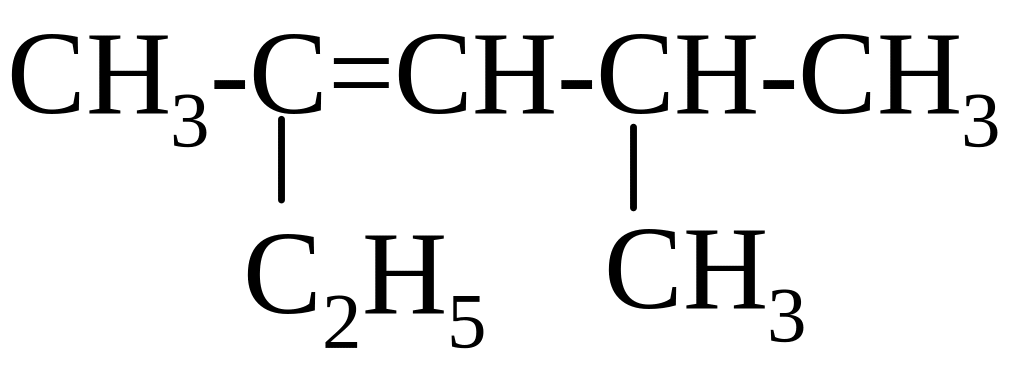
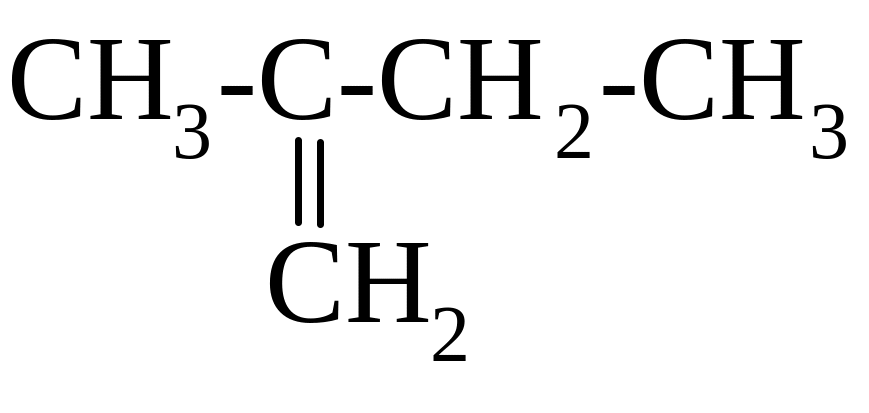 а)
б)
в)
а)
б)
в)
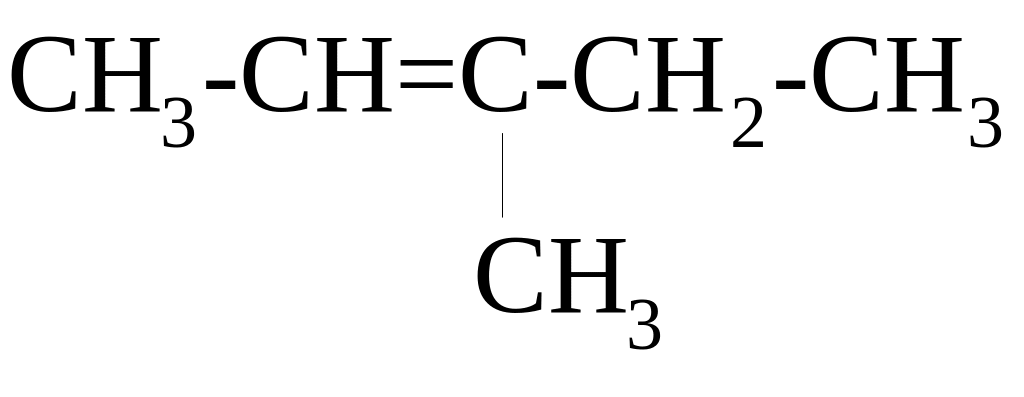
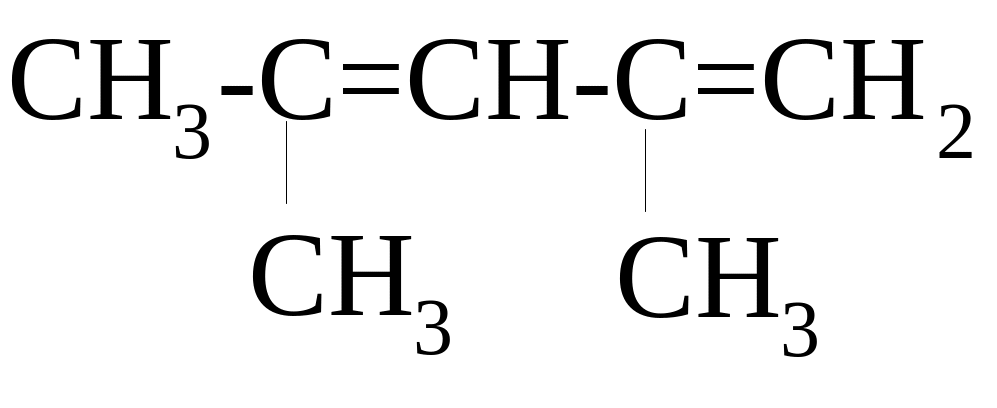
г) д)
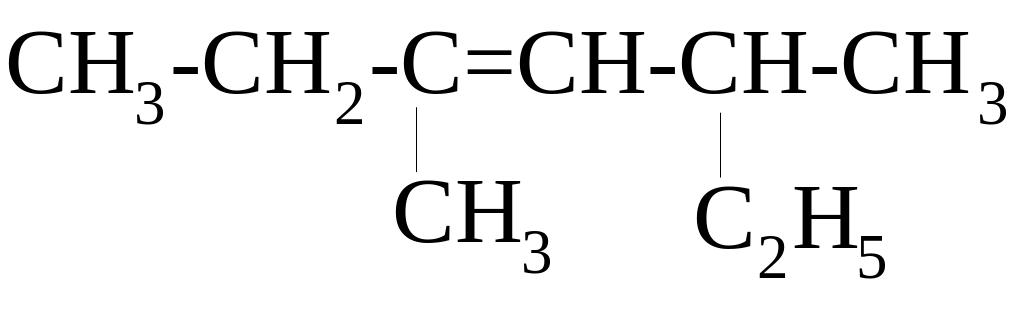
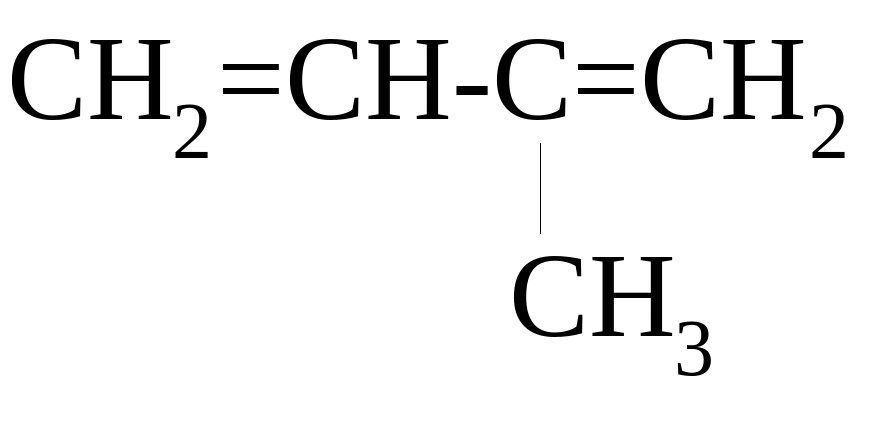 д)
е)
д)
е)
68.
ВПИШИТЕ НЕДОСТАЮЩИЕ СЛОВА!
В МОЛЕКУЛЕ ЭТЕНА С-С σ-СВЯЗЬ ОБРАЗОВАНА ЗА СЧЁТ ___________________
ПЕРЕКРЫВАНИЯ _____________-ГИБРИДИЗОВАННЫХ АТОМНЫХ ОРБИТАЛЕЙ
АТОМОВ УГЛЕРОДА.
УКАЖИТЕ ПРАВИЛЬНЫЙ ОТВЕТ (ОТВЕТЫ)!
69.
ЦИС, ТРАНС-ИЗОМЕРИЯ ХАРАКТЕРНА ДЛЯ:
пентена-1 3. бутена-1 5. бутена-2
пентена-2 4. пропена
70.
ЦИС, ТРАНС-ИЗОМЕРИЯ ХАРАКТЕРНА ДЛЯ:
1. пентена-1 2. бутена-2 3. 2,3-диметил-бутена-2 4. пропена
7 1.
1.
НАЗВАНИЕ ДАННОГО СОЕДИНЕНИЯ -
цис-бутен-2 4. транс-бутен-1
цис-бутен-1 5. цис-1,2-диметилэтен
транс-бутен-2 6. транс-1,2-диметилэтен
72.
C-C π-СВЯЗЬ В ПРОПЕНЕ ОБРАЗОВАНА ЗА СЧЁТ:
1. осевого перекрывания sp2-гибридных орбиталей
2. осевого перекрывания sp3-гибридных орбиталей
3. бокового перекрывания sp2-гибридных орбиталей
4. бокового перекрывания негибридных орбиталей
5. бокового перекрывания sp3-гибридных орбиталей
73.
В МОЛЕКУЛЕ ЭТЕНА С-С σ-СВЯЗЬ ОБРАЗОВАНА ЗА СЧЁТ:
1. осевого перекрывания sp2-гибридных орбиталей
2. осевого перекрывания sp3-гибридных орбиталей
3. бокового перекрывания sp2-гибридных орбиталей
4. бокового перекрывания негибридных орбиталей
5. бокового перекрывания sp3-гибридных орбиталей
ВПИШИТЕ НЕДОСТАЮЩЕЕ СЛОВО!
74.
ЭНЕРГИЯ С-С σ-СВЯЗИ _________________ , ЧЕМ ЭНЕРГИЯ С-С π-СВЯЗИ.
75.
C-C π-СВЯЗЬ В ПРОПЕНЕ ОБРАЗОВАНА ЗА СЧЁТ ____________________ ПЕРЕКРЫВАНИЯ ______________________ ОРБИТАЛЕЙ.
УКАЖИТЕ ПРАВИЛЬНЫЕ ОТВЕТЫ!
76.
РЕАКЦИИ, ХАРАКТЕРНЫЕ ДЛЯ АЛКЕНОВ:
электрофильное присоединение 3. окисление
нуклеофильное присоединение 4. нуклеофильное замещение
77.
РЕАКЦИИ, ХАРАКТЕРНЫЕ ДЛЯ ЭТЕНА:
1. окисление 2. AE 3. AN 4. SR
УКАЖИТЕ СООТВЕТСТВИЯ!
78.
название реакции реагент, условия
реакция гидратации a) H2, Ni г) HCl
реакция гидрирования б) H2O, H+ д) H2O, OH-
реакция гидрохлорирования в) Cl2, H2O
79.
РЕАКЦИИ ЭТЕНА
H2O,H+
 1
a) алкан
1
a) алкан
б) галогеналкан
HCl в) этанол
 CH2=CH2
2 г) диол (гликоль)
CH2=CH2
2 г) диол (гликоль)
H2,Ni,p,to
3
УКАЖИТЕ ПРАВИЛЬНЫЙ ОТВЕТ!
80.
ЭЛЕКТРОННОЕ ОБЛАКО π-СВЯЗИ В АЛКЕНАХ ЯВЛЯЕТСЯ МЕСТОМ ДЛЯ АТАКИ:
электрофила 2. нуклеофила 3. аниона
81.
ЛИМИТИРУЮЩЕЙ СТАДИЕЙ РЕАКЦИИ АЕ ЯВЛЯЕТСЯ:
1. образование π-комплекса 3. образование карбокатиона
2. превращение карбокатиона в конечный 4. образование свободного радикала
продукт
УКАЖИТЕ СООТВЕТСТВИЯ МЕЖДУ НОМЕРОМ В СХЕМЕ И ФОРМУЛОЙ!
82.
HCl Cl -

 CH2=CH2
1 2 3
CH2=CH2
1 2 3
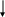 a)
CH3-CH2+ в)
CH3-CH2-Cl д)
CH2=CH2
a)
CH3-CH2+ в)
CH3-CH2-Cl д)
CH2=CH2
б) CH2=CH2 г) +CH3-CH2 Cl+
H+
83.
МЕХАНИЗМ РЕАКЦИИ ГИДРОХЛОРИРОВАНИЯ ПРОПЕНА:
HCl Cl -
 CH3-CH=CH2
1 2 3
CH3-CH=CH2
1 2 3
-Cl -
a) CH3-CH2-CH2+ в) CH2=CH-CH3 г) CH3-CH2-CH2-Cl
+
б) CH3-CH-CH3 H+ д) CH3-CH-CH3
|
Cl
84.
МЕХАНИЗМ РЕАКЦИИ ГИДРОБРОМИРОВАНИЯ БУТЕНА-1:
HBr Br -
Бутен-1 1 2 3
- Br -
+
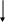 a) CH2=CH-CH2-CH3
в) CH2-CH2-CH2-CH3
д) CH3-CH-CH2-CH3
a) CH2=CH-CH2-CH3
в) CH2-CH2-CH2-CH3
д) CH3-CH-CH2-CH3
|
H+ Br
+ г) Br- CH2-CH2-CH2-CH3
б) CH3-CH-CH2-CH3
85.
МЕХАНИЗМ РЕАКЦИИ ГИДРАТАЦИИ ЭТЕНА:

86.
ВПИШИТЕ НЕДОСТАЮЩИЕ СЛОВА!
ПРАВИЛО МАРКОВНИКОВА: ПРИ ПРИСОЕДИНЕНИИ РЕАГЕНТОВ ТИПА Н+Х-
К НЕСИММЕТРИЧНЫМ АЛКЕНАМ __________________ ВОДОРОДА ПРИСОЕДИНЯЕТСЯ К ________________________ ГИДРОГЕНИЗИРОВАННОМУ АТОМУ УГЛЕРОДА ПРИ ДВОЙНОЙ СВЯЗИ.
ЗАПОЛНИТЕ СХЕМУ!
(вставьте в квадраты номера нужных ответов)
87.
П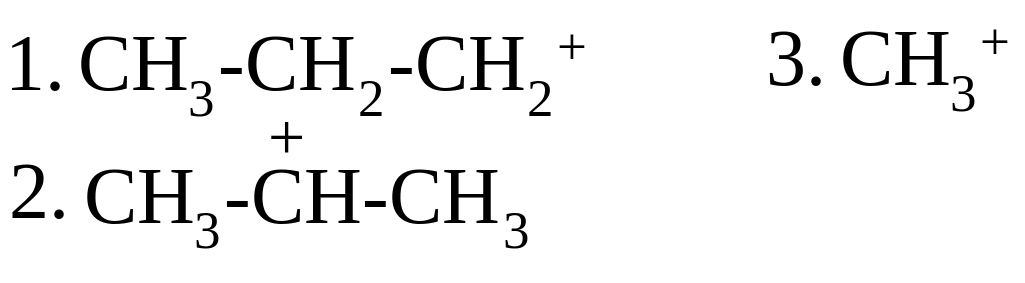 ОРЯДОК
УВЕЛИЧЕНИЯ СТАБИЛЬНОСТИ КАРБОКАТИОНОВ:
ОРЯДОК
УВЕЛИЧЕНИЯ СТАБИЛЬНОСТИ КАРБОКАТИОНОВ:
1 [ ] 2 [ ] 3 [ ]
88.
ПОРЯДОК УВЕЛИЧЕНИЯ СТАБИЛЬНОСТИ КАРБОКАТИОНОВ:
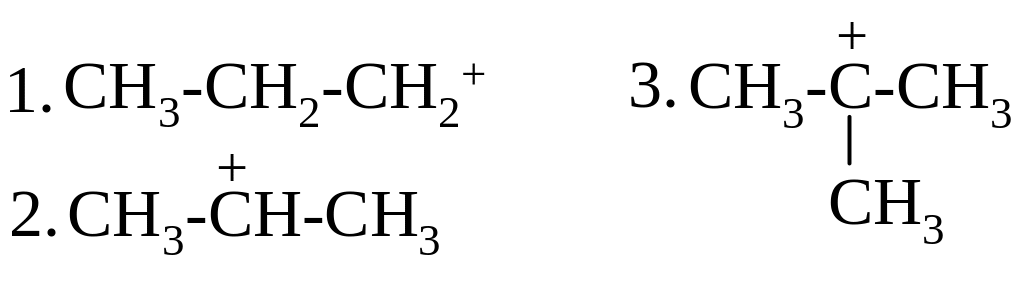
1 [ ] 2 [ ] 3 [ ]
УКАЖИТЕ ПРАВИЛЬНЫЙ ОТВЕТ!
89.
КАТАЛИЗАТОРОМ В РЕАКЦИЯХ ГИДРАТАЦИИ АЛКЕНОВ ЯВЛЯЕТСЯ:
1. H2SO4 2. HCl 3. NaOH 4. Ni
90.
ОСНОВНОЙ ПРОДУКТ РЕАКЦИИ ГИДРАТАЦИИ ПРОПЕНА:
CH3-CH2-CH3 3. CH3-CH-CH3 4. CH3-CH-CH2
CH3-CH2-CH2-OH | | |
OH OH OH
91.
ПРИ ВЗАИМОДЕЙСТВИИ БУТЕНА-1 С БРОМНОЙ ВОДОЙ ОБРАЗУЕТСЯ:
1,2-дибромбутен 3. 1-бромбутен-1 5. 1-бромбутан
1,2-дибромбутан 4. 2-бромбутен-1
УКАЖИТЕ СООТВЕТСТВИЯ!
9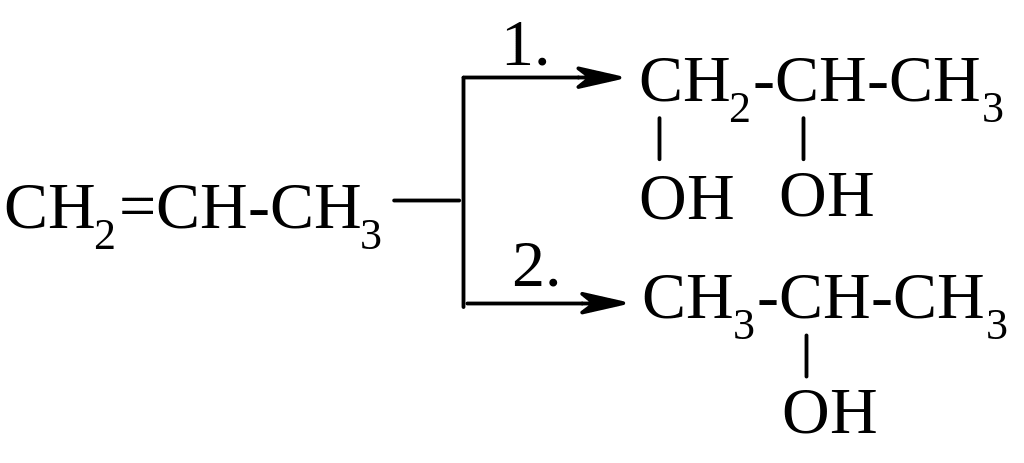 2.
2.
а) KOH
б) KMnO4, H2O, 20oC
в) H2O, H+
г) H2O, OH-
д) KMnO4, 100oC
93.
КАЧЕСТВЕННЫЕ РЕАКЦИИ АЛКЕНОВ:
реакция наблюдаемый эффект
с бромной водой а) обесцвечивание раствора
с KMnO4 (20оС) б) образование бурого осадка
в) появление характерного запаха
г) образование малинового осадка
94.
формула тип диена
1. CH2=C=CH2 a) изолированный
2. CH3-CH=CH-CH=CH2
3. CH3-CH=CH-CH2-CH=CH2 б) кумулированный
в) сопряжённый
УКАЖИТЕ ПРАВИЛЬНЫЕ ОТВЕТЫ!
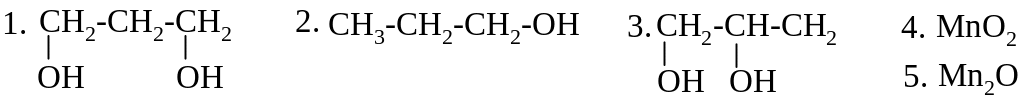
9![]() 5.
5.
ПРОДУКТАМИ РЕАКЦИИ ЯВЛЯЮТСЯ:
96.
КАЧЕСТВЕННЫМИ РЕАКЦИЯМИ АЛКЕНОВ ЯВЛЯЮТСЯ РЕАКЦИИ С:
HBr 3. KMnO4 при комнатной температуре
бромной водой 4. H2 (в присутствии Ni)
5. Cl2
97.
ПРОДУКТАМИ РЕАКЦИИ ГИДРИРОВАНИЯ БУТАДИЕНА-1,3 (1 МОЛЬ РЕАГЕНТА) МОГУТ БЫТЬ:
1. CH3-CH2-CH=CH2
2. CH3-CH=CH-CH3
3. CH3-CH2-CH2-CH3
98.
СТРУКТУРНЫМИ ИЗОМЕРАМИ БУТАДИЕНА-1,.3 ЯВЛЯЮТСЯ:
бутадиен-1,2 4. бутин-1
циклобутан 5. бутин-2
метилциклопропан
