- •Оглавление
- •Введение (как пользоваться учебно-методическим пособием)
- •Занятие № 1 классификация, номенклатура и структурная изомерия органических соединений. Электронное строение атомов элементов-органогенов
- •Блок информации
- •Классификация соединений по строению углеродного скелета
- •Важнейшие классы органических соединений
- •Построение названия органического соединения
- •Пример названия по заместительной номенклатуре iupac
- •Характеристические (функциональные) группы, их обозначение по номенклатуре iupac и соответствующие им классы органических соединений
- •Названия важнейших углеводородных радикалов
- •Валентное состояние и строение атома углерода в алифатических углеводородах
- •Правила техники безопасности при работе в химической лаборатории
- •Занятие № 2 химическая связь в органических молекулах. Классификация химических реакций. Реакционная способность алканов. Алкенов и алкадиенов
- •План изучения темы
- •Бромирование непредельных соединений
- •Окисление алкенов в мягких условиях (реакция Вагнера)
- •Блок информации
- •Типы химических связей атомов в молекулах органических соединений
- •Характеристика ковалентных связей
- •Свойства насыщенных углеводородов (алканов)
- •Свойства ненасыщенных углеводородов ряда этилена (алкенов)
- •Блок информации для выполнения самостоятельной работы
- •Конформации молекул алифатических углеводородов
- •Вопросы для тестового контроля
- •Занятие № 3 взаимное влияние атомов в молекулах органических соединений. Реакционная способность ароматических углеводородов
- •Влияние заместителей на последующее электрофильное замещение в ароматическом ядре
- •Вопросы для тестового контроля
- •Занятие № 4 химические свойства галогеналканов, спиртов и фенолов
- •План изучения темы
- •Получение этилхлорида из этилового спирта
- •Дегидратация этилового спирта
- •Свойства фенолов
- •Указания по выполнению самостоятельной работы № 2
- •Указания по выполнению самостоятельной работы № 3
- •Вопросы для тестового контроля
- •Заполните схему!
- •15. Возрастание кислотных свойств соединений:
- •Реакции окисления спиртов
- •31. Заполните схему!
- •Заполните схему!
- •Занятие № 5 кислотно-основные свойства органических соединений. Реакционная способность аминов
- •Получение этиленгликолята меди (II)
- •Образование фенолята натрия и разложение его кислотой
- •Сравнение основности алифатических и ароматических аминов
- •Блок информации
- •Значения pKa некоторых кислот Бренстеда
- •Кислотность различных классов соединений
- •Свойства первичных алифатических аминов
- •Вопросы для тестового контроля
- •3. Метиламин
- •Занятие № 6 реакционная способность оксосоединений
- •План изучения темы
- •Диспропорционирование формальдегида в водных растворах
- •Отношение ацетальдегида и ацетона к окислению щелочными растворами оксидов тяжёлых металлов
- •Открытие ацетона переводом его в йодоформ
- •Блок информации
- •Свойства альдегидов
- •Вопросы для тестового контроля
- •Занятие № 7 химические свойства карбоновых кислот и их функциональных производных
- •План работы на предстоящем занятии
- •Открытие щавелевой кислоты
- •Получение этилацетата
- •Блок информации
- •Свойства насыщенных монокарбоновых кислот
- •Кислотные свойства карбоновых кислот
- •Производные угольной кислоты
- •Указания по выполнению самостоятельной работы № 4
- •Вопросы для тестового контроля
- •Занятие № 8 итоговое занятие по теме «гомофункциональные производные углеводородов»
- •Занятие № 9 гетерофункциональные алифатические соединения - метаболиты и биорегуляторы
- •Доказательство наличия двух карбоксильных групп в винной кислоте
- •Доказательство наличия гидроксильных групп в винной кислоте
- •Блок информации
- •Классификация кислород- и азотсодержащих гетерофункциональных соединений
- •Свойства α-гидроксикислот
- •Специфические свойства α-, β-, γ-гидроксикислот
- •Свойства α-аминокислот
- •Специфические свойства α-, β-, γ-аминокислот
- •Вопросы для тестового контроля
- •Занятие № 10 гетерофункциональные соединения бензольного ряда. Биологически активные производные пятичленных гетероциклических соединений
- •Свойства пятичленных гетероциклов с одним гетероатомом (π-избыточных систем)
- •Свойства пятичленных гетероциклов с двумя гетероатомами
- •Электронное строение молекулы пиррола
- •Типы атомов азота в гетероциклах
- •Указания по выполнению самостоятельной работы № 6
- •Указания по выполнению самостоятельной работы № 7
- •В опросы для тестового контроля
- •Занятие № 11 Биологически важные производные шестичленных гетероциклов. Производные пурина
- •Растворимость мочевой кислоты и её натриевой соли в воде
- •Открытие мочевой кислоты (мурексидная проба)
- •Блок информации
- •Свойства шестичленных гетероциклов (π-недостаточных систем)
- •Электронное строение молекулы пиридина
- •Задания для тестового контроля
- •Занятие № 12 итоговое занятие по теме «метаболиты и родоначальники важнейших групп лекарственных препаратов»
- •Занятие № 13 углеводы. Моносахариды
- •Доказательство наличия гидроксильных групп в глюкозе
- •Восстановление гидроксида меди (II) глюкозой в щелочной среде (проба Троммера)
- •Восстановление аммиачного раствора оксида серебра глюкозой (реакция Толленса, реакция «серебряного зеркала»)
- •Химические свойства глюкозы (продолжение)
- •Химические свойства глюкозы (продолжение)
- •Вопросы для тестового контроля
- •Занятие № 14 углеводы. Дисахариды и полисахариды
- •Сравнение свойств лактозы и сахарозы
- •Качественная реакция на крахмал
- •Блок информации
- •Классификация полисахаридов
- •Указания по выполнению самостоятельной работы № 8
- •Задания для тестового контроля
- •Занятие № 15
- •Реакция на присутствие серусодержащих α-аминокислот
- •Блок информации
- •Классификация аминокислот белков
- •Основные виды взаимодействий, фиксирующих вторичную и третичную структуру пептидов и белков
- •Указания по выполнению самостоятельной работы № 9
- •Вопросы для тестового контроля
- •Занятие № 16 нуклеиновые кислоты. Омыляемые липиды
- •Щелочной гидролиз (омыление) жира
- •Занятие № 17 итоговое занятие по теме «углеводы, аминокислоты, пептиды, белки, нуклеиновые кислоты, омыляемые липиды»
- •Занятие № 18 стероиды. Алкалоиды. Зачёт по практическим навыкам
- •План изучения материала
- •Общие реакции на алкалоиды
- •Блок информации
- •Родоначальные структуры стероидов
- •Классификация алкалоидов
- •Перечень практических навыков, выносимых на зачётное занятие
- •Примерные экзаменационные вопросы по биоорганической химии
- •Литература Основная
- •Дополнительная
- •305041, Г. Курск, ул. К. Маркса, 3.
- •305041, Г. Курск, ул. К. Маркса, 3.
Влияние заместителей на последующее электрофильное замещение в ароматическом ядре
Орто-, пара-ориентанты |
Мета-ориентанты |
||
электронные эффекты |
заместители I рода |
электронные эффекты |
заместители II рода |
+ M> -I
+ M> -I
+ M> -I
+ M> -I
+I
+I
+ M< -I
|
активирующие
-OH
-NH2, -NHR, -NR2
-OR
-алкил (-CH3, -C2H5)
-арил (-Ar)
дезактивирующие галогены (-F, -Cl, -Br, -I) |
-I, -M
-I, -M
-I, -M
-I, -M
-I, -M
-I, -M
-I
-I, -M |
дезактивирующие
-NO2
-SO3H |
Приложение
Вопросы для тестового контроля
УКАЖИТЕ СООТВЕТСТВИЯ!
1. тип сопряжения примеры
π,π –сопряжение а) CH2=CH-CH2-CH=CH2 в) CH2=CH-NH2
p,π-сопряжение б) CH2=C-CH=CH2
| г) CH2=CH-O-CH3
CH3
д) CH2=CH-CH2-NH2
2.
тип сопряжения примеры
π
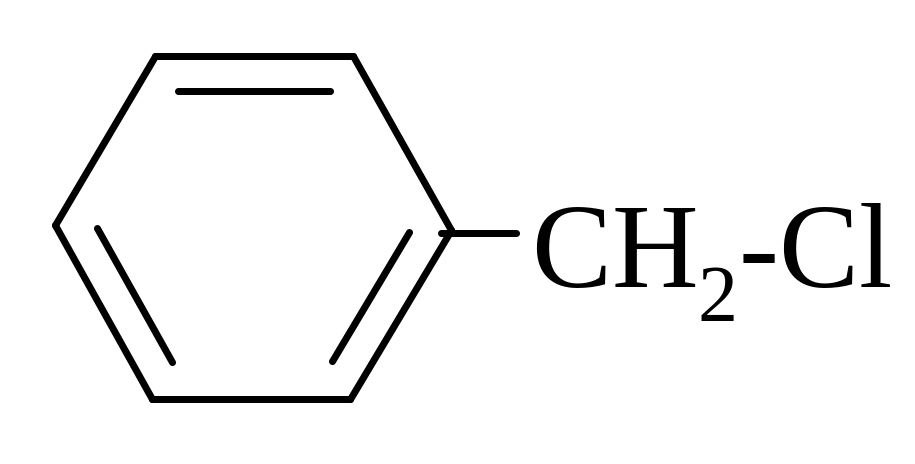 ,π
–сопряжение а) CH3-CH=CH-CH2-CH=CH2
в) CH2=C=CH2
,π
–сопряжение а) CH3-CH=CH-CH2-CH=CH2
в) CH2=C=CH2
2. p,π-сопряжение
б) CH2=CH-OCH3 г)
3.
тип сопряжения примеры
π,π –сопряжение а) CH2=CH-CH=CH-CH2-OH в) CH2=CH-CH3
p
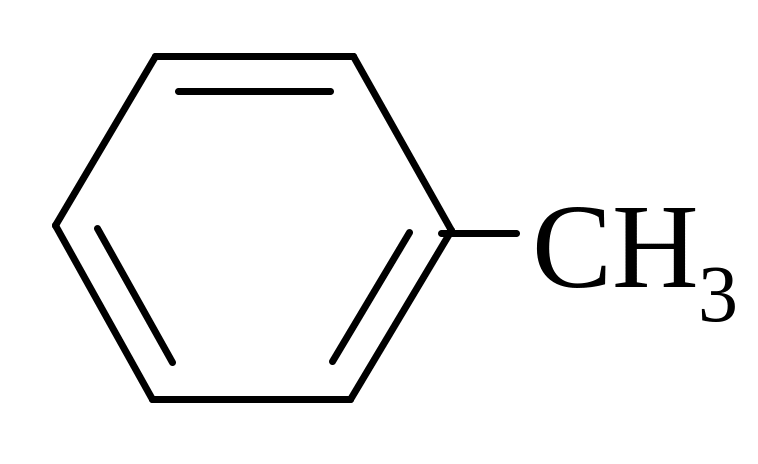 ,π-сопряжение
,π-сопряжение
б) CH2=CH-NH-CH3 г)
4.
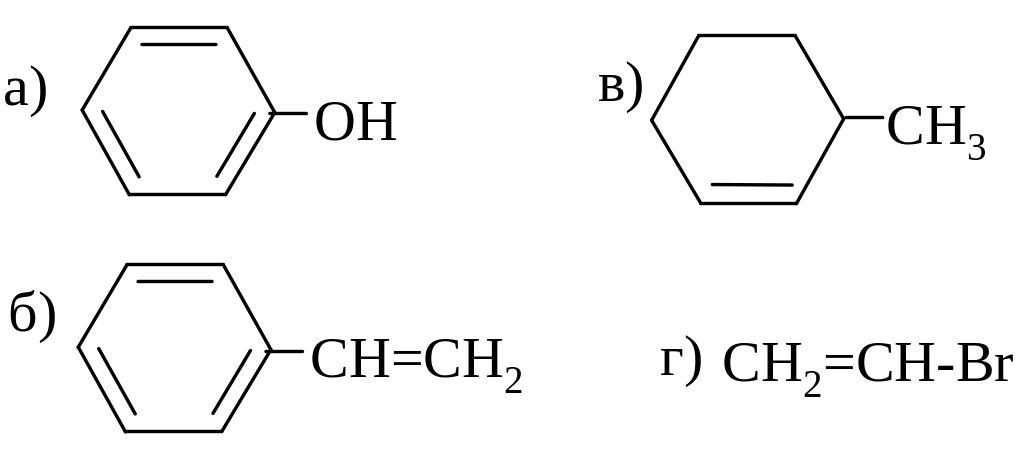 тип
сопряжения
примеры
тип
сопряжения
примеры
π,π –сопряжение
p,π-сопряжение
5. УКАЖИТЕ ПРАВИЛЬНЫЕ ОТВЕТЫ!
p,π-СОПРЯЖЕННЫМИ СИСТЕМАМИ ЯВЛЯЮТСЯ:

ВПИШИТЕ НЕДОСТАЮЩЕЕ ЧИСЛО!
6. В СОПРЯЖЁННОЙ СИСТЕМЕ АКРИЛОВОГО АЛЬДЕГИДА
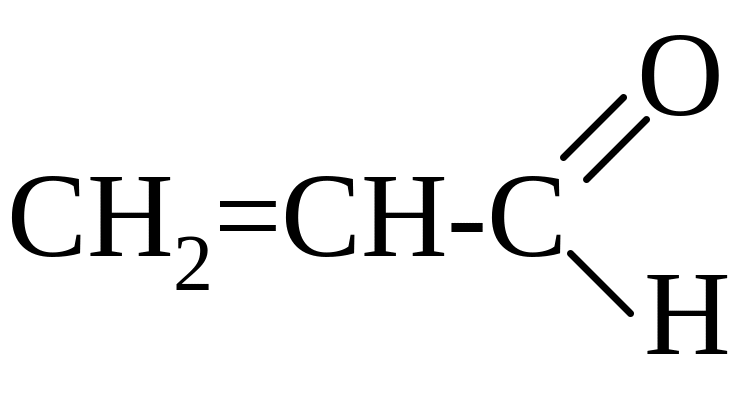
ДЕЛОКАЛИЗОВАНО ___ ЭЛЕКТРОНА
7.
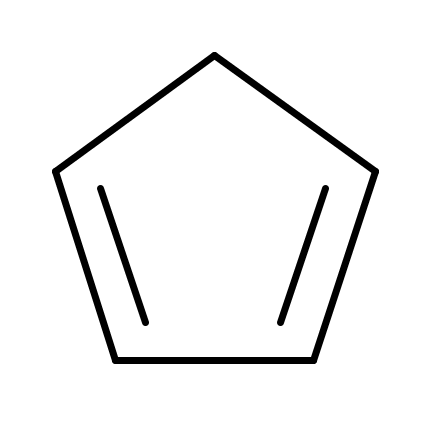 В СОПРЯЖЁННОЙ
СИСТЕМЕ ЦИКЛОПЕНТАДИЕНА-1,3
В СОПРЯЖЁННОЙ
СИСТЕМЕ ЦИКЛОПЕНТАДИЕНА-1,3
ДЕЛОКАЛИЗОВАНО ___ ЭЛЕКТРОНА.
8.
В СОПРЯЖЁННОЙ СИСТЕМЕ АКРИЛОВОЙ КИСЛОТЫ

ДЕЛОКАЛИЗОВАНО ___ ЭЛЕКТРОНА (ОВ)
9.
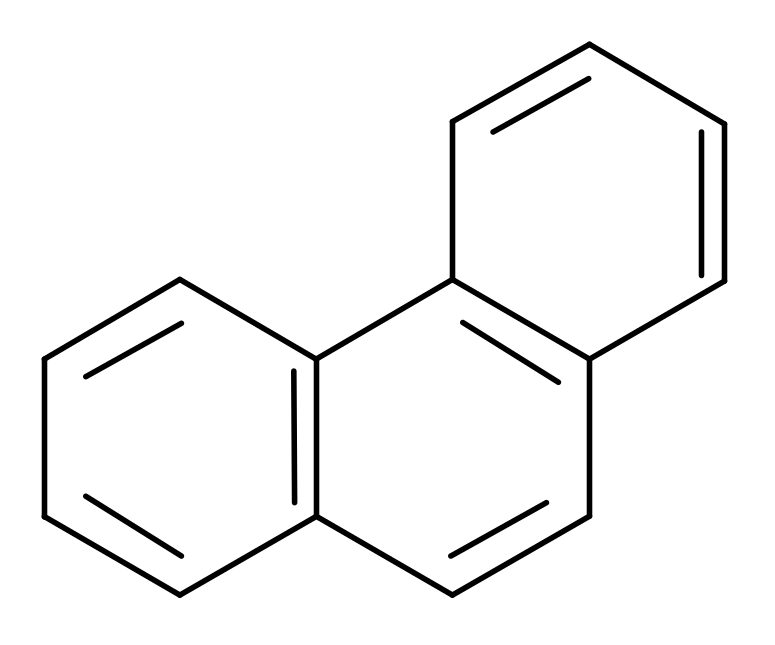
В СОПРЯЖЁННОЙ СИСТЕМЕ ФЕНАНТРЕНА
ДЕЛОКАЛИЗОВАНО ___ ЭЛЕКТРОНА (ОВ)
10.
В СОПРЯЖЁННОЙ СИСТЕМЕ ВИНИЛАМИНА
![]() ДЕЛОКАЛИЗОВАНО
___ ЭЛЕКТРОНА (ОВ).
ДЕЛОКАЛИЗОВАНО
___ ЭЛЕКТРОНА (ОВ).
11.
В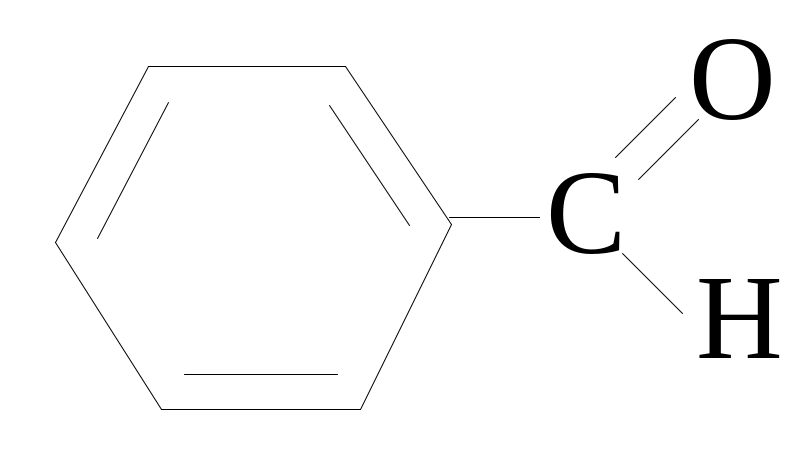 СОПРЯЖЁННОЙ СИСТЕМЕ БЕНЗАЛЬДЕГИДА
СОПРЯЖЁННОЙ СИСТЕМЕ БЕНЗАЛЬДЕГИДА
ДЕЛОКАЛИЗОВАНО ___ ЭЛЕКТРОНА (ОВ)
1 2.
2.
В СОПРЯЖЁННОЙ СИСТЕМЕ АНТРАЦЕНА
ДЕЛОКАЛИЗОВАНО ___ ЭЛЕКТРОНА (ОВ)
13.
В СОПРЯЖЁННОЙ СИСТЕМЕ ДИВИНИЛОВОГО ЭФИРА
![]() ДЕЛОКАЛИЗОВАНО
___ ЭЛЕКТРОНА(ОВ).
ДЕЛОКАЛИЗОВАНО
___ ЭЛЕКТРОНА(ОВ).
УКАЖИТЕ ПРАВИЛЬНЫЙ ОТВЕТ!
14. В РЕЗУЛЬТАТЕ СОПРЯЖЕНИЯ ЭНЕРГИЯ МОЛЕКУЛЫ:
1. повышается 2. понижается 3. не изменяется
15.
В РЕЗУЛЬТАТЕ СОПРЯЖЕНИЯ СТАБИЛЬНОСТЬ МОЛЕКУЛЫ:
1. повышается 2. понижается 3. не изменяется
ЗАПОЛНИТЕ СХЕМУ!
(вставьте в квадраты номера нужных ответов)
16. ВОЗРАСТАНИЕ ЭНЕРГИИ СОПРЯЖЕНИЯ
1 [ ] 2 [ ] 3 [ ] 1. бутадиен-1,3
2. гексатриен-1,3,5
3. бензол
17.
ВОЗРАСТАНИЕ СТАБИЛЬНОСТИ СОЕДИНЕНИЙ
1 [ ] 2 [ ] 3 [ ] 1. гексадиен-1,3 3. гексадиен-1,4
2. гексатриен-1,3,5
18. ВПИШИТЕ НЕДОСТАЮЩИЕ СЛОВА!
АРОМАТИЧНОСТЬ – ЭТО СОВОКУПНОСТЬ СВОЙСТВ ЗАМКНУТЫХ СОПРЯЖЁННЫХ СИСТЕМ, ПРОЯВЛЯЮЩАЯСЯ В ИХ УСТОЙЧИВОСТИ К РЕАКЦИЯМ ______________________ И ________________________ .
19.
ДЛЯ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ ХАРАКТЕРНЫ РЕАКЦИИ, ПРОТЕКАЮЩИЕ ПО МЕХАНИЗМУ _______________________ ____________________ .
УКАЖИТЕ ПРАВИЛЬНЫЕ ОТВЕТЫ!
20. КВАНТОВО-МЕХАНИЧЕСКИЕ КРИТЕРИИ АРОМАТИЧНОСТИ:
наличие плоского цикла
наличие длинной открытой цепи сопряжения
наличие замкнутой сопряжённой системы
в молекуле должно быть (4n+2) атома, где n – целое число
в сопряжённой системе должно быть (4n+2) электрона, где n –целое число
в сопряжённой системе должно быть (4n+2) электрона, где n – количество циклов
21.
А РОМАТИЧЕСКИЕ
СОЕДИНЕНИЯ:
РОМАТИЧЕСКИЕ
СОЕДИНЕНИЯ:
22. УКАЖИТЕ ПРАВИЛЬНЫЙ ОТВЕТ!
РЕАКЦИИ, ХАРАКТЕРНЫЕ ДЛЯ БЕНЗОЛА:
электрофильное присоединение 3. радикальное замещение
электрофильное замещение 4. окисление
. УКАЖИТЕ СООТВЕТСТВИЯ!
23. реакция реагент
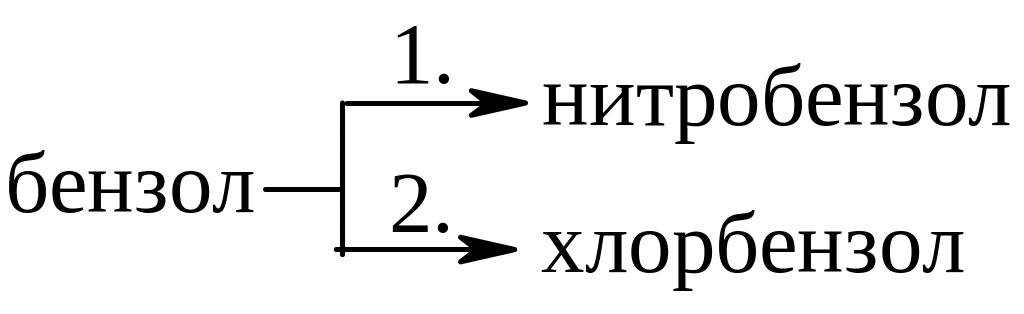 а)
конц. HNO3+
H2SO4
г) HCl
а)
конц. HNO3+
H2SO4
г) HCl
б) разб. HNO3 д) Cl2 + FeCl3
в) HNO2 е) Cl2 + H2O
24.
СХЕМА МЕХАНИЗМА РЕАКЦИЙ SE:
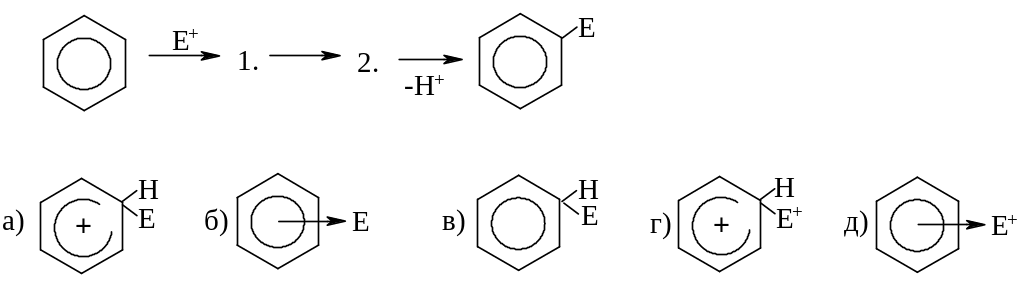
25.
СХЕМА МЕХАНИЗМА РЕАКЦИЙ SE:
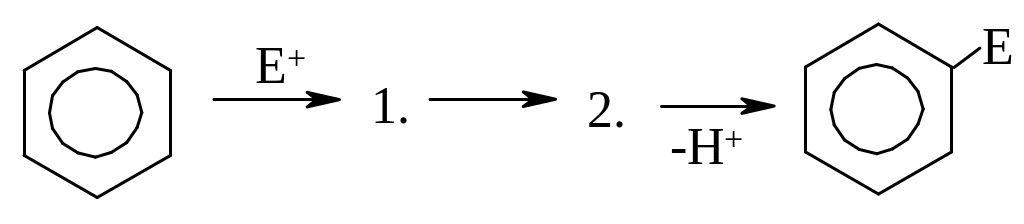
НАЗВАНИЕ ПРОМЕЖУТОЧНОЙ ЧАСТИЦЫ И ЕЁ ХАРАКТЕРИСТИКА
а) σ-комплекс в) ароматическая структура
б) π-комплекс г) неароматическая структура
26.
МЕХАНИЗМ РЕАКЦИИ НИТРОВАНИЯ БЕНЗОЛА:
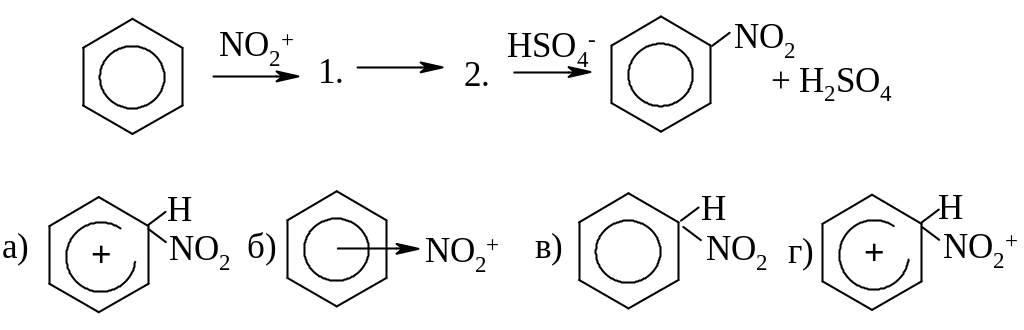
27.
РЕАКЦИЯ СУЛЬФИРОВАНИЯ БЕНЗОЛА ОЛЕУМОМ:
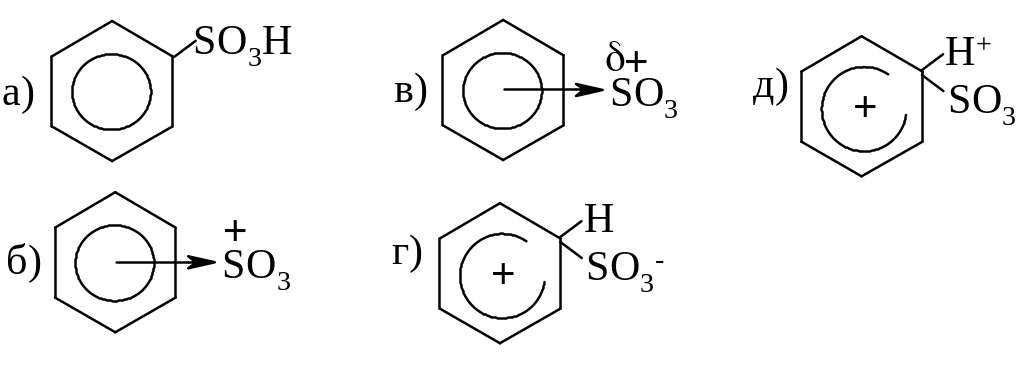 промежуточная
частица её
структура
промежуточная
частица её
структура
π-комплекс
σ-комплекс
28.
МЕХАНИЗМ РЕАКЦИИ МЕТИЛИРОВАНИЯ БЕНЗОЛА:
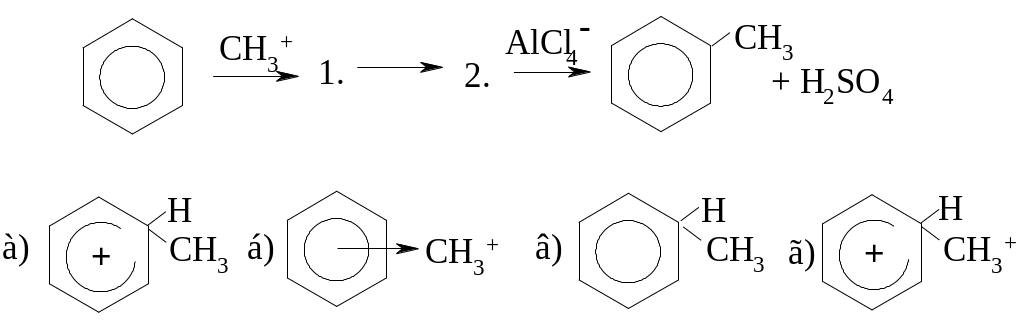
УКАЖИТЕ ПРАВИЛЬНЫЙ ОТВЕТ!
29. КАТАЛИЗАТОРОМ РЕАКЦИИ НИТРОВАНИЯ БЕНЗОЛА ЯВЛЯЕТСЯ:
1. конц. HNO3 3. AlCl3 5. облучение
2. конц. H2SO4 4. FeBr3
30.
КАТАЛИЗАТОРОМ РЕАКЦИИ ХЛОРИРОВАНИЯ БЕНЗОЛА ЯВЛЯЕТСЯ:
1. конц. HNO3 3. AlCl3 5. облучение
конц. H2SO4 4. Ni
31.
КАТАЛИЗАТОРОМ РЕАКЦИИ АЛКИЛИРОВАНИЯ БЕНЗОЛА ЯВЛЯЕТСЯ:
1. конц. HNO3 3. FeCl3 5. УФ-облучение
2. конц. H2SO4 4. Pt
32.
КАТАЛИЗАТОРОМ РЕАКЦИИ ПОЛУЧЕНИЯ ТОЛУОЛА ИЗ БЕНЗОЛА ЯВЛЯЕТСЯ:
1. конц. HNO3 3. УФ-облучение 5. кислота Льюиса
2. конц. H2SO4 4. Pt
УКАЖИТЕ СООТВЕТСТВИЯ!
33. ЭЛЕКТРОННЫЕ ЭФФЕКТЫ ПОДЧЕРКНУТЫХ ЗАМЕСТИТЕЛЕЙ
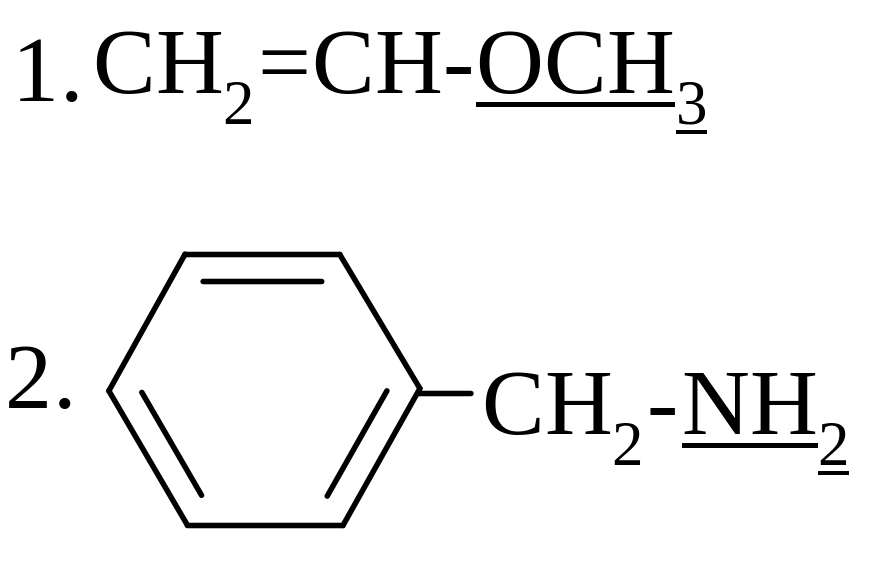
а) -I
б) +I
в) -I, +M
г) –I, -M
д) +I, +M
34.
ЭЛЕКТРОННЫЕ ЭФФЕКТЫ ПОДЧЕРКНУТЫХ ЗАМЕСТИТЕЛЕЙ
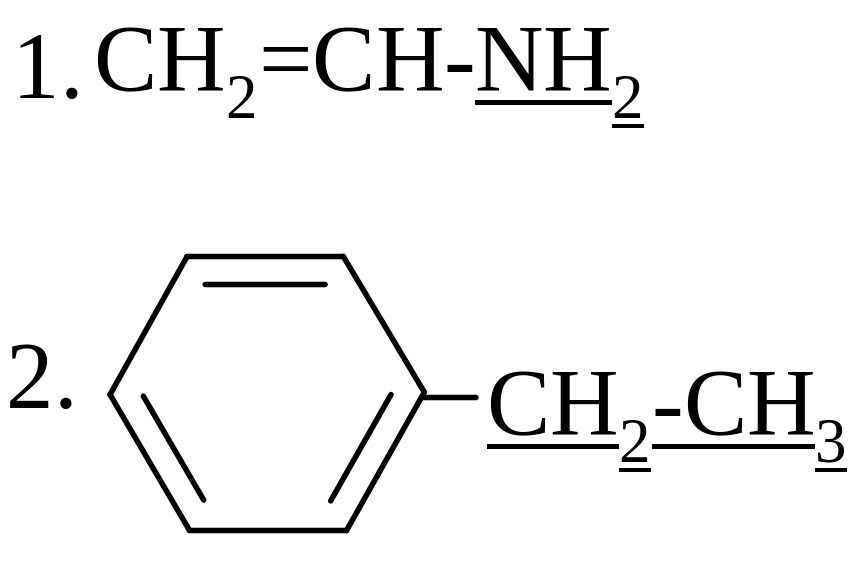 а)
-I
а)
-I
б) +I
в) -I, +M
г) –I, -M
д) +I, +M
35.
ЭЛЕКТРОННЫЕ ЭФФЕКТЫ ПОДЧЕРКНУТЫХ ЗАМЕСТИТЕЛЕЙ
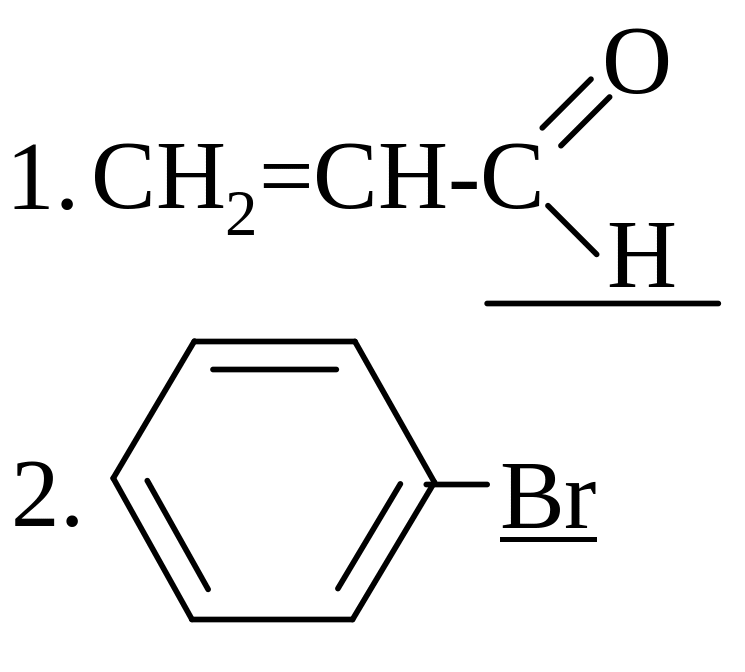
а) -I
б) +I
в) -I, +M
г) –I, -M
д) +I, +M
36.
ЭЛЕКТРОННЫЕ ЭФФЕКТЫ ПОДЧЕРКНУТЫХ ЗАМЕСТИТЕЛЕЙ

а) -I в) –I, +M д) +I,+M
б) +I г) –I,-M
37.
ЭЛЕКТРОННЫЕ ЭФФЕКТЫ ПОДЧЕРКНУТЫХ ЗАМЕСТИТЕЛЕЙ
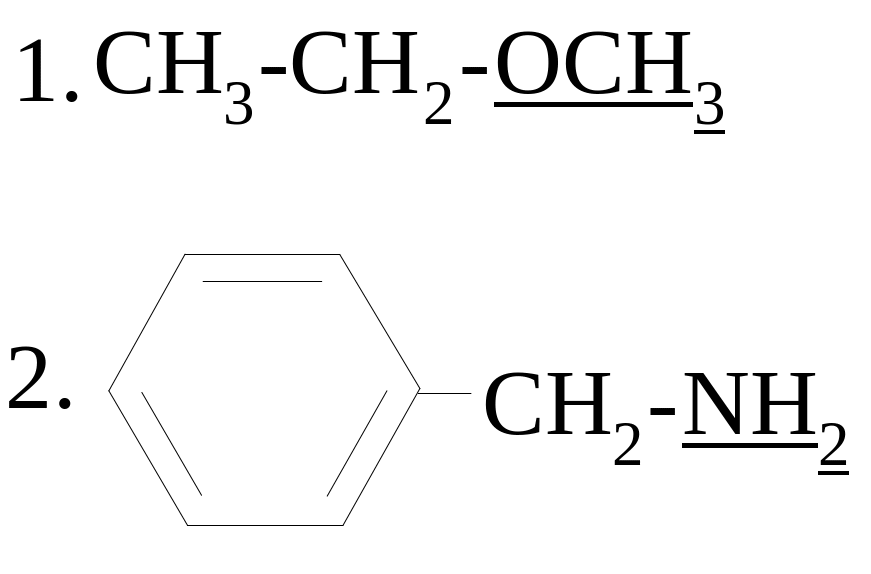 а)
-I
а)
-I
б) +I
в) -I, +M
г) –I, -M
д) +I, +M
38.
заместитель 1 рода a) CH3 в) SO3H д) NO2
заместитель 2 рода б) NH2 г) OH
39.
заместитель 1 рода a) Cl в) COOH д) OH
заместитель 2 рода б) NH2 г) C2H5
40.
заместитель 1 рода a) Br в) COOH д) OCH3
заместитель 2 рода б) NO2 г) CH2CH2CH3
41.
![]()
заместитель 1 рода a) б) NH2 г) SO3H
заместитель 2 рода в) NO2 д) CH3
42.
влияние в реакциях SE заместитель
активатор a) Cl в) COOH д) OH
дезактиватор б) NH2 г) C2H5
43.
влияние в реакциях SE заместитель
активатор a) CH3 в) SO3H д) NO2
дезактиватор б) NH2 г) OH
44.
влияние в реакциях SE заместитель
облегчает реакцию a) Br в) OCH3 д) COOH
затрудняет реакцию б) C2 H5 г) OH
45.
влияние в реакциях SE заместитель
облегчает реакцию a) Cl в) COOH д) OH
затрудняет реакцию б) NO2 г) C2H5
. ЗАПОЛНИТЕ СХЕМУ!
(вставьте в квадраты номера нужных ответов)
46. ВОЗРАСТАНИЕ АКТИВНОСТИ СОЕДИНЕНИЙ В РЕАКЦИЯХ SE:
1 [ ] 2 [ ] 3 [ ] 1. бензойная кислота
2. фенол
3. бензол
47.
ВОЗРАСТАНИЕ АКТИВНОСТИ СОЕДИНЕНИЙ В РЕАКЦИЯХ SE:
1 [ ] 2 [ ] 3 [ ] 1. хлорбензол
2. анилин (аминобензол)
3. бензол
48.
ВОЗРАСТАНИЕ АКТИВНОСТИ СОЕДИНЕНИЙ В РЕАКЦИЯХ SE:
1 [ ] 2 [ ] 3 [ ] 1. нитробензол 3. бензол
2. толуол
49.
ВОЗРАСТАНИЕ АКТИВНОСТИ СОЕДИНЕНИЙ В РЕАКЦИЯХ SE:
1 [ ] 2 [ ] 3 [ ] 1. хлорбензол
2. фенол
3. бензол
50.
ВОЗРАСТАНИЕ АКТИВНОСТИ СОЕДИНЕНИЙ В РЕАКЦИЯХ SE:
1 [ ] 2 [ ] 3 [ ] 1. нитробензол
2. 1,3-динитробензол
3. бензол
51.
ВОЗРАСТАНИЕ АКТИВНОСТИ СОЕДИНЕНИЙ В РЕАКЦИЯХ SE:
1 [ ] 2 [ ] 3 [ ] 1. нитробензол
2. анилин (аминобензол)
3. м-динитробензол
52.
ВОЗРАСТАНИЕ АКТИВНОСТИ СОЕДИНЕНИЙ В РЕАКЦИЯХ SE:
1 [ ] 2 [ ] 3 [ ] 1. нитробензол 3. бензол
2. этилбензол
УКАЖИТЕ ПРАВИЛЬНЫЙ ОТВЕТ (ОТВЕТЫ)!
53.
ПРОДУКТЫ РЕАКЦИИ МОНОБРОМИРОВАНИЯ АНИЛИНА:
1. o-броманилин 2. м-броманилин 3. п-броманилин 4. бромбензол
54.
ОСНОВНЫМ ПРОДУКТОМ РЕАКЦИИ БРОМИРОВАНИЯ НИТРОБЕНЗОЛА
ЯВЛЯЕТСЯ:
1. бромбензол 3. 1-бром-2-нитробензол
2. 1-бром-3-нитробензол 4. 1-бром-4-нитробензол
55.
КАТАЛИЗАТОРОМ РЕАКЦИИ НИТРОВАНИЯ ХЛОРБЕНЗОЛА ЯВЛЯЕТСЯ:
1. конц. HNO3 3. AlCl3 5. облучение
2. конц. H2SO4 4. FeBr3
56.
ПРИ ВЗАИМОДЕЙСТВИИ ФЕНОЛА (ОКСИБЕНЗОЛА)
С ИЗБЫТКОМ БРОМНОЙ ВОДЫ ОБРАЗУЕТСЯ:
1. м-бромфенол 4. 1,3,5-трибромбензол
2. смесь о- и п-бромфенола 5. 3,5-дибромфенол
3. 2,4,6-трибромфенол
57.
ПРИ ОКИСЛЕНИИ ПРОПИЛБЕНЗОЛА ОБРАЗУЕТСЯ:

58.
ПРОДУКТОМ ОКИСЛЕНИЯ ЭТИЛБЕНЗОЛА ЯВЛЯЕТСЯ:
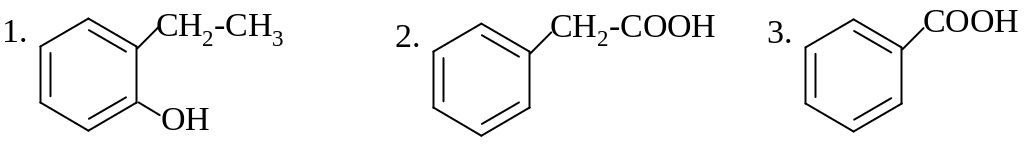
59.
СТРУКТУРНЫМИ ИЗОМЕРАМИ СОСТАВА C8H10 ЯВЛЯЮТСЯ:
о-диметилбензол 4. 1,2-диметилциклогексан
п-диметилбензол 5. 1,4-диметилциклогексан
этилбензол 6. этилциклогексан
60.
ПРИ ВЗАИМОДЕЙСТВИИ БЕНЗОЛА С ХЛОРОМ ПРИ УЛЬТРАФИОЛЕТОВОМ ОБЛУЧЕНИИ ОБРАЗУЕТСЯ:
хлорбензол 3. гексахлорциклогексан (гексахлоран)
хлорциклогексан 4. о-дихлорбензол
УКАЖИТЕ СООТВЕТСТВИЯ!
61. реакции анилина продукт реакции

м-броманилин
б) смесь о- и п-броманилина
в) 2,4,6-триброманилин
г) 1,3,5-триброманилин
д) 3,5-диброманилин
6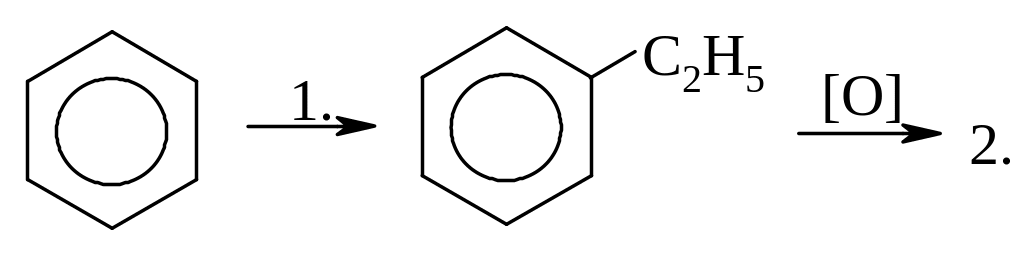 2.
а) С2H5OH
2.
а) С2H5OH
б) С2H5Br + AlBr3
в) C2H6
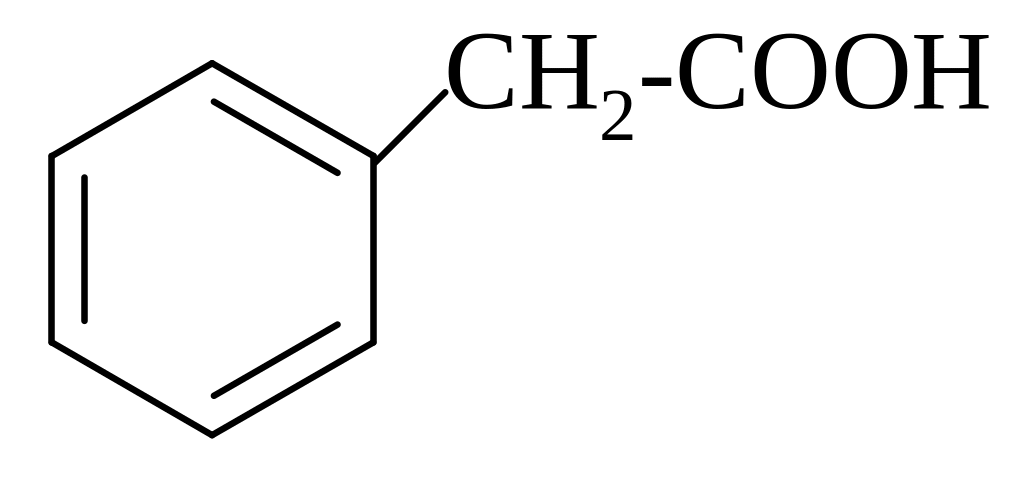
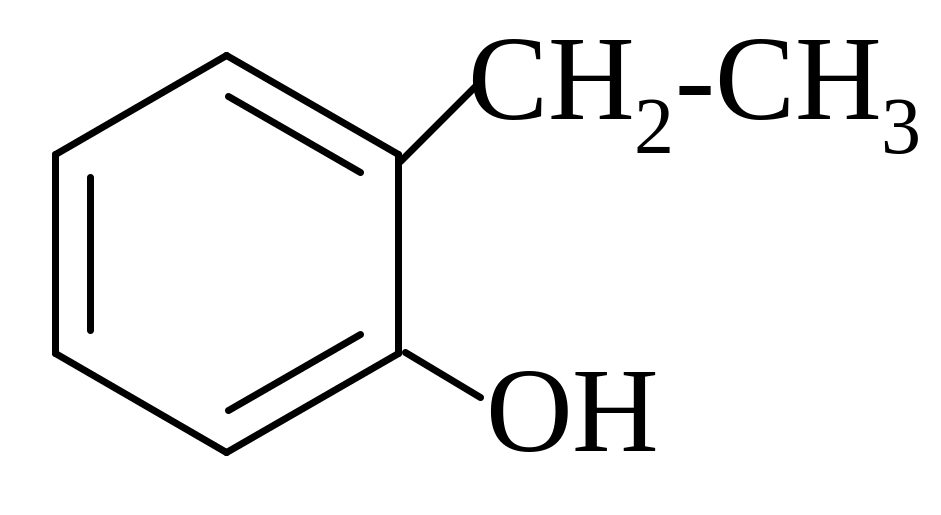
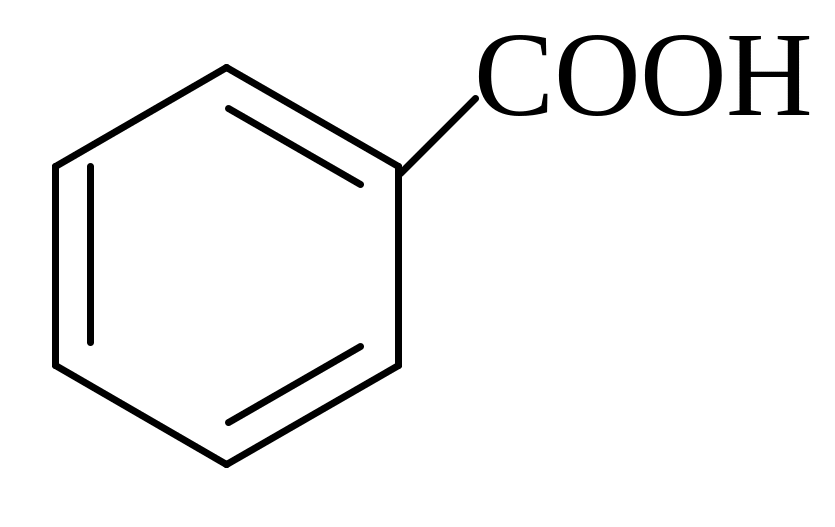 г)
г)
д) е)
63.
свет
 1
a) о-хлортолуол
1
a) о-хлортолуол
 толуол
+ Cl2
б) м-хлортолуол
толуол
+ Cl2
б) м-хлортолуол
FeCl3 в) п-хлортолуол
г) бензилхлорид
д) хлорбензол
ВПИШИТЕ НЕДОСТАЮЩЕЕ СЛОВО!
64. В РЕАКЦИИ СУЛЬФИРОВАНИЯ НАФТАЛИНА ПРИ ТЕМПЕРАТУРЕ 160ОС ОБРАЗУЕТСЯ _____________________________________ .
65.
ОСНОВНОЙ ПРОДУКТ РЕАКЦИИ НИТРОВАНИЯ НАФТАЛИНА - ______________________ .
66.
В РЕАКЦИИ СУЛЬФИРОВАНИЯ НАФТАЛИНА ПРИ ТЕМПЕРАТУРЕ 80ОС ОБРАЗУЕТСЯ _____________________________________ .