
- •Содержание
- •Введение
- •Объекты анализа материалов микроэлектроники
- •1. Основы качественного анализа
- •Классификация анионов
- •2. Аналитические реакции катионов
- •Лабораторная работа № 1 Частные реакции катионов I - II групп Опыт 1. Обнаружение катиона калия
- •Опыт 2. Обнаружение катиона натрия
- •Опыт 3. Обнаружение магния в растворе
- •Опыт 4. Определение иона аммония
- •Реакции катионов I группы
- •Опыт 5. Обнаружение катиона бария
- •Опыт 6. Обнаружение катиона стронция
- •Опыт 6. Обнаружение катиона стронция
- •Опыт 7. Обнаружение катиона кальция
- •Лабораторная работа № 2 Анализ смеси катионов I и II групп
- •3. Аналитические реакции катионов III группы
- •Лабораторная работа № 3 Частные реакции катионов III группы Опыт 1. Обнаружение катиона алюминия
- •Опыт 2. Обнаружение хрома
- •Реакции хромат- и бихромат-ионов
- •Опыт 3. Обнаружение железа
- •Опыт 5. Обнаружение цинка в растворе
- •Опыт 6. Обнаружение кобальта
- •Опыт 7. Обнаружение никеля
- •Лабораторная работа № 4 Анализ смеси катионов III, II и I групп
- •4. Аналитические реакции катионов IV и V групп
- •Опыт 2. Обнаружение катионов кадмия
- •Опыт 3. Обнаружение катионов висмута
- •Подгруппа мышьяка Опыт 5. Обнаружение ионов мышьяка
- •Реакции катионов подгруппы меди
- •Обнаружение арсенит-ионов
- •Обнаружение арсенат-ионов
- •Опыт 6. Обнаружение ионов сурьмы
- •Обнаружение ионов сурьмы (III)
- •Обнаружение ионов сурьмы (V)
- •Опыт 7. Обнаружение ионов олова
- •Обнаружение ионов олова (II)
- •Обнаружение ионов олова (IV)
- •Лабораторная работа № 6 Анализ смеси катионов IV группы
- •Лабораторная работа № 7 Частные реакции катионов V группы Опыт I. Определение катионов серебра
- •Опыт 2. Обнаружение катионов свинца
- •Лабораторная работа № 8 Анализ смеси катионов V - I групп
- •Реакции катионов V группы
- •5. Аналитические реакции анионов
- •Опыт 2. Определение аниона со32–
- •Опыт 3. Определение аниона ро4–
- •Опыт 4. Определение аниона SiO32–
- •Опыт 5. Определение аниона f –
- •Вторая аналитическая группа анионов Опыт 6. Определение аниона с1–
- •Опыт 7. Определение аниона Вr –
- •Опыт 8. Определение аниона I –
- •Опыт 9. Определение аниона s2–
- •Третья аналитическая группа анионов Опыт 10. Определение аниона no3–
- •Опыт п. Определение анионов no2–
- •6. Количественный анализ
- •7. Гравиметрия
- •Весовые методы определения некоторых элементов
- •Лабораторная работа № 10 Весовое определение серы в сульфиде кадмия
- •Оборудование и реактивы
- •Описание определения
- •Определение серы
- •Лабораторная работа №11 Весовое определение никеля и железа в резистивных сплавах Определение никеля
- •Оборудование и реактивы
- •Описание определения
- •Определение железа
- •Оборудование и реактивы
- •Описание определения
- •8. Титриметрия
- •Растворение образца.
- •Описание определения
- •Лабораторная работа № 16 Определение стехиометрического состава сверх проводящей керамики ( система y-Ba-Cu )
- •Определение бария
- •Реактивы
- •Описание определения
- •Иодометрическое титрование
- •Стандартизация раствора тиосульфата натрия по бихромату калия
- •Реактивы
- •Описание определения
- •Определение меди
- •Реактивы
- •Описание определения
- •Определение иттрия комплексонометрическим титрованием
- •Реактивы
- •Описание определения
- •Расчет стехиометрии y1 Ва2 Cu3o7
- •9.Физико-химические методы анализа
- •А. Определение фосфора по желтой форме
- •Оборудование и реактивы
- •Описание определения
- •Б. Определение фосфора в виде фосфорномолибденовой сини
- •Оборудование и реактивы
- •Описание определения
- •В. Определение кремния
- •Оборудование и реактивы
- •Описание определения
- •Оборудование и реактивы
- •Описание определения
- •Б. Фотометрическое определение железа в виде роданидного комплекса
- •Оборудование и реактивы
- •Описание определения
- •Лабораторная работа № 19 Экстракционно – фотометрическое определение германия в полупроводниковых халькогенидных стеклах системы Te–As-Si-Ge
- •Оборудование и реактивы
- •Описание определения
- •Лабораторная работа № 20 Спектрофотометрическое определение хрома и марганца при совместном присутствии в контактных проводниковых сплавах
- •Оборудование и реактивы
- •Описание определения
- •Лабораторная работа № 21 Спектрофотометрическое определение висмута в присутствии свинца
- •Оборудование и реактивы
- •Описание определения
- •11. Люминесцентный анализ
- •Оборудование и реактивы
- •Описание определения
- •12. Инфракрасная спектроскопия
- •Лабораторная работа № 23 Измерение толщины пленок диоксида и нитрида кремния методом икс
- •Применение икс для исследования материалов микроэлектроники
- •Оборудование и реактивы
- •Описание определения
- •В отчете долж ны быть представлены:
- •Пример расчета:
- •13.Эмиссионный спектральный анализ
- •Лабораторная работа № 24 Определение примесей металлов методом трех эталонов
- •А. Фотографирование спектров трех эталонов и образцов Оборудование и реактивы
- •Описание определения
- •Характерные группы линий железа на планшетах атласа
- •В. Измерение почернений линий примесей на микрофотометре и построение калибровочных графиков
- •Оборудование и реактивы
- •Описание определения
- •Форма записи результатов наблюдений
- •Последовательность фотографирования образцов
- •Форма записи результатов наблюдений
- •Длины волн определяемых примесей
- •14. Электрохимические методы анализа
- •15.Потенциометрия
- •Прямая потенциометрия (ионометрия)
- •Оборудование и реактивы
- •Описание определения
- •Результаты ионометрического определения ионов в воде
- •Б. Определение фторид-ионов
- •Оборудование и реактивы
- •Описание определения
- •Лабораторная работа № 27 Определение рН в водных растворах
- •Оборудование и реактивы
- •Описание определения
- •Потенциометрическое титрование (пт)
- •Результаты титрования
- •Лабораторная работа № 28 Определение соляной кислоты в травильной ванне
- •Оборудование и реактивы
- •Описание определения
- •Лабораторная работа № 29 Определение соляной и уксусной кислот в растворе при совместном присутствии
- •Оборудование и реактивы
- •Описание определения
- •Лабораторная работа № 30 Определение соляной и борной кислот в растворе при совместном присутствии
- •Оборудование и реактивы
- •Описание определения
- •Лабораторная работа № 31 Определение содержания кобальта (II) в растворе
- •Оборудование и реактивы
- •Описание определения
- •Лабораторная работа № 32 Определение концентрации хлорида железа (III)
- •Оборудование и реактивы
- •Описание определения
- •16. Кондуктометрическое титрование
- •Лабораторная работа № 33 Дифференцированное определение солей железа (п) и(ш) в травильных растворах
- •Оборудование и реактивы
- •Описание определения
- •17. Вольтамперометрия
- •Лабораторная работа № 34 Определение примеси цинка в фосфоре
- •18. Инверсионная вольтамперометрия
- •Лабораторная работа № 36 Определение примесей цинка, кадмия, свинца и меди методом инверсионной вольтамперометрии
- •Оборудование и реактивы
- •Описание определения
- •19. Хроматография
- •Раздельное вымывание примесей с катионита ку-2
- •Лабораторная работа № 37 Определение меди и цинка при их совместном присутствии на катионите ку-2
- •Оборудование и реактивы
- •Описание определения
- •Описание определения
- •Определение кадмия
- •Результаты хроматографического определения ионов кадмия
- •Определение теллура
- •20. Рекомендуемая литература
- •Реакции катионов III группы
- •Реакции ионов подгруппы мышьяка
Описание определения
Построение калибровочного графика. Стандартные растворы висмута и свинца по 2; 3; 3,5; 4 мл помещают в мерные колбы емкостью 50 мл. в эти же колбы прибавляют по 20 мл 0,001 М раствора ЭТДА, разбавляют водой до метки, перемешивают. Измеряют оптические плотности растворов на спектрофотометре СФ-26 по отношению к воде для висмута при =265 нм, для свинца при =240 нм в кюветах с толщиной слоя 1 см, строят калибровочные графики для этих длин волн. Исследуемый раствор, содержащий висмут и свинец, в количестве 0,2– 0,4 мг помещают в колбу на 50 мл и добавляют 20 мл 0,001 М раствора ЭТДА. Затем измеряют оптическую плотность этого раствора при =265 и 240 нм при толщине кюветы ℓ=1 см. По калибровочному графику определяют концентрацию висмута и свинца в исследуемом растворе.
В случае единичного определения висмута и свинца можно, измерив оптическую плотность одного эталона при =265 и 240 нм, рассчитать коэффициент поглощения, например:
![]() и
и
![]()
Зная 265 и 240 и измерив оптическую плотность исследуемого раствора при =265 и 240 нм, определяют концентрацию висмута и свинца в пробе по формулам:
![]() и
и
![]()
Метод применим в интервале концентраций, в котором светопоглощение подчиняется закону Бугера – Ламберта – Бера.
11. Люминесцентный анализ
Люминесценция - это вторичное излучение, т.е. явление, когда энергия возбуждения, определяемая уравнением Планка отдается в виде света.
Е2 – Е1 = hυ
При флуоресцентном анализе используют обычные приемы аналитической химии, связанные с выделением определяемой примеси, если основное вещество мешает, и созданием оптимальных условий произведения флуоресцентной реакции.
Флуоресцентные реакции можно разделить на две группы:
- реакции с использованием неорганических реагентов (собственная флуоресценция лантаноидов, солей уранила, некоторых солей тяжелых металлов);
- реакции с использованием органических реагентов.
Количественное определение неорганических веществ с помощью органических реагентов основано на возникновении флуоресценции комплексного соединения, образующегося при взаимодействии определяемого катиона с не флуоресцарупцим (либо флуоресцирующим другим цветом) реагентом.
Для количественного анализа особый интерес представляет зависимость интенсивности флуоресценции от концентрации флуоресцирующего вещества. Соблюдение основного закона светопоглощения характеризуется прямолинейной зависимостью между концентрацией поглощающего свет раствора и его оптической плотностью.
Прямолинейная зависимость между интенсивностью флуоресценции и концентрацией сохраняется при малых значениях концентрации.
IФл = KС
Именно эта область используется для количественного анализа. Для большинства веществ эта область охватывает концентрации порядка
10–7 – I0–4 моль/л. Таким образом, флуоресцентный метод применим для определения незначительного количества вещества в растворе. Начиная с некоторой пороговой концентрации, наблюдается уменьшение интенсивности флуоресценции, называемое концентрационным гашением.
Количественные определения могут быть выполнены с помощью калибровочного графика или методом добавок. Если в анализируемом растворе присутствуют частично гасящие флуоресценцию примеси, пользуются методом добавок. Форма записи результатов представлена в табл. 11.1.
Таблица 11.1
Форма записи результатов определения
Параметры |
Растворы |
|||
"холостой" |
с первой добавкой |
со второй добавкой |
исследуемый |
|
концентрация С, г/мл интенсивность флуоресценции |
|
|
|
|
Лабораторная работа № 22
Определение алюминия с салициаль-о-аминофенолом в
тетрахлориде германия
Летучесть тетрахлорида германия облегчает получение аналитического концентрата примесей при анализе германия и его соединений. Поэтому в качестве метода концентрирования примесей обычно используют удаление основы в виде летучего соединения GeCl4. Примеси посторонних элементов в тетрахлораде германия определяют различными физико-химическими методами анализа.
В основе флуоресцентного определения алюминия лежит реакция с салициаль-о-аминофенолом по схеме:
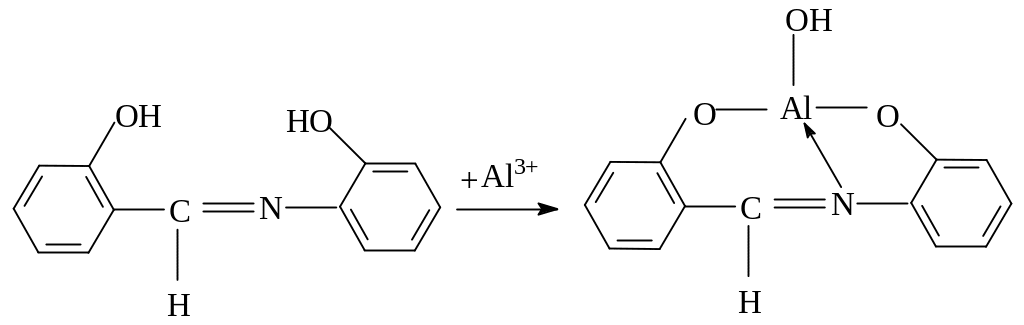
При возбуждении образующегося комплекса ультрафиолетовым светом возникает зеленая флуоресценция.
От основного вещества - тетрахлорида германия - освобождаются выпариванием его в кварцевом перегонном аппарате. Остающиеся следы германия не мешают определению алюминия. Определение алюминия в тетрахлориде германия осложняется тем, что после выпаривания остается плохо растворимый остаток. Поэтому остаток после выпаривания смачивают 0,2-0,3 мл очищенной соляной кислоты и снова выпаривают.
Спектр флуоресценции комплексного соединения представляет собой бесструктурную полосу в интервале длин волн 440-640 нм с максимумом флуоресценции 520-530 нм. Чувствительность метода составляет 0,0025 мкг алюминия в 5 мл раствора. Оптимальное значение рН раствора для выполнения реакции равно 5,0-6,2. Пропорциональная зависимость между интенсивностью флуоресценции и концентрацией алюминия наблюдается до тех пор, пока сохраняется соотношение 0,5 мкг алюминия в 5 мл раствора.

 Кроме
алюминия, никакие другие катионы в
количествах до 25 мкг в 5 мл раствора не
вызывают флуоресценции. Катионы меди
и железа в количествах, больших 0,1 мкг
в 5 мл, гасят флуоресценцию, поэтому при
определении алюминия целесообразно
применять
метод добавок, позволяющий выполнять
анализы без предварительного
выделения меди и железа из анализируемого
раствора.
Кроме
алюминия, никакие другие катионы в
количествах до 25 мкг в 5 мл раствора не
вызывают флуоресценции. Катионы меди
и железа в количествах, больших 0,1 мкг
в 5 мл, гасят флуоресценцию, поэтому при
определении алюминия целесообразно
применять
метод добавок, позволяющий выполнять
анализы без предварительного
выделения меди и железа из анализируемого
раствора.
Время развития максимальной интенсивности флуоресценции равно 45-50 мин.
