
- •Курс физики
- •Механика глава 1. Кинематика и динамика частицы § 1. Путь и перемещение
- •§ 2. Скорость и ускорение
- •§ 3. Сила и работа
- •Глава 2. Кинематика и динамика вращения твердого тела § 4. Угловая скорость и угловое ускорение
- •§ 5. Средняя скорость и среднее ускорение
- •§ 6. Момент силы
- •Глава 3. Законы сохранения § 7. Механическая энергия. Закон сохранения механической энергии
- •§ 8. Импульс. Закон сохранения импульса
- •§ 9. Момент импульса. Закон сохранения момента импульса
- •Глава 4. Механические колебания § 10. Гармонические колебания
- •§ 11. Затухающие колебания
- •§ 12. Вынужденные колебания
- •Глава 5. Механические волны § 13. Гармонические волны
- •§ 14. Плоская гармоническая волна
- •Экзаменационные вопросы 1
- •Контрольные задания 1 Вариант 1
- •Вариант 2
- •Вариант 3
- •Вариант 4
- •Вариант 5
- •Вариант 6
- •Вариант 7
- •Вариант 8
- •Вариант 9
- •Вариант 10
- •Вариант 11
- •Вариант 12
- •Вариант 13
- •Вариант 14
- •Вариант 15
- •Вариант 16
- •Вариант 17
- •Вариант 18
- •Вариант 19
- •Вариант 20
- •Вариант 21
- •Вариант 22
- •Вариант 23
- •Вариант 24
- •Вариант 25
- •Вариант 26
- •Вариант 27
- •Вариант 28
- •Вариант 29
- •Вариант 30
- •Приложение а
- •Молекулярная физика глава 6. Кинетическая теория газов § 15. Уравнение состояния идеального газа
- •§ 16. Внутренняя энергия идеального газа
- •§ 17. Распределение Максвелла
- •§ 18. Барометрическая формула
- •§ 19. Распределение Больцмана
- •§ 20. Явления переноса
- •Глава 7. Термодинамика § 21. Термодинамическая система и термодинамический процесс
- •§ 22. Первый закон термодинамики
- •§ 23. Теплоемкость идеального газа
- •§ 24. Адиабатический процесс
- •§ 25. Энтропия
- •§ 26. Второй и третий законы термодинамики
- •Глава 8. Реальные газы § 27. Силы межмолекулярного взаимодействия в газах
- •§ 28. Агрегатное состояние вещества
- •§ 29. Уравнение Ван-дер-Ваальса
- •§ 30. Внутренняя энергия реального газа
- •Экзаменационные вопросы 2
- •Контрольные задания 2 Вариант 1
- •Вариант 2
- •Вариант 3
- •Вариант 4
- •Вариант 5
- •Вариант 6
- •Вариант 7
- •Вариант 8
- •Вариант 9
- •Вариант 10
- •Вариант 11
- •Вариант 12
- •Вариант 13
- •Вариант 14
- •Вариант 15
- •Вариант 16
- •Вариант 17
- •Вариант 18
- •Вариант 19
- •Вариант 20
- •Вариант 21
- •Вариант 22
- •Вариант 23
- •Вариант 24
- •Вариант 25
- •Вариант 26
- •Вариант 27
- •Вариант 28
- •Вариант 29
- •Вариант 30
- •Приложение б
- •Электромагнетизм глава 9. Электрическое поле в вакууме § 31. Напряженность поля
- •§ 32. Поток вектора
- •§ 33. Теорема Гаусса для поля вектора
- •§ 34. Циркуляция вектора
- •§ 35. Потенциал поля
- •§ 36. Связь между φ и
- •Глава 10. Электрическое поле в диэлектрике § 37. Диполь в электрическом поле
- •§ 38. Поляризация диэлектрика
- •§ 39. Вектор
- •Глава 11. Энергия электрического поля § 40. Электроемкость
- •§ 41. Электроемкость плоского конденсатора
- •§ 42. Энергия электрического поля
- •Глава 12. Электрический ток § 43. Электрический ток
- •§ 44. Закон Ома для проводника
- •§ 45. Обобщенный закон Ома
- •§ 46. Закон Джоуля – Ленца
- •Глава 13. Магнитное поле в вакууме § 47. Магнитная индукция
- •§ 48. Закон Био – Савара
- •§ 49. Теорема Гаусса для поля вектора
- •§ 50. Теорема о циркуляции вектора
- •§ 51. Магнитное поле в соленоиде
- •§ 52. Закон Ампера
- •Глава 14. Магнитное поле в веществе § 53. Контур с током в магнитном поле
- •§ 54. Намагничивание магнетика
- •§ 55. Вектор
- •Глава 15. Энергия магнитного поля § 56. Индуктивность
- •§ 57. Электромагнитная индукция
- •§ 58. Энергия магнитного поля
- •Глава 16. Электромагнитные волны § 59. Вихревое электрическое поле
- •§ 60. Ток смещения
- •§ 61. Система уравнений Максвелла
- •§ 62. Электромагнитные волны
- •Глава 17. Волновая оптика § 63. Свет
- •§ 64. Интерференция света
- •§ 65. Дифракция света
- •§ 66. Поглощение света
- •§ 67. Рассеяние света
- •§ 68. Поляризация света
- •§ 69. Закон Малюса
- •§ 70. Вращение плоскости поляризации
- •Контрольные задания 3 Вариант 1
- •Вариант 2
- •Вариант 3
- •Вариант 4
- •Вариант 5
- •Вариант 6
- •Вариант 7
- •Вариант 8
- •Вариант 9
- •Вариант 10
- •Вариант 11
- •Вариант 12
- •Вариант 13
- •Вариант 14
- •Вариант 15
- •Вариант 16
- •Вариант 17
- •Вариант 18
- •Вариант 19
- •Вариант 20
- •Вариант 21
- •Вариант 22
- •Вариант 23
- •Вариант 24
- •Вариант 25
- •Вариант 26
- •Вариант 27
- •Вариант 28
- •Вариант 29
- •Вариант 30
- •Экзаменационные вопросы 3
- •Приложение в
- •Квантовая физика глава 18. Квантовая оптика § 71. Тепловое излучение
- •§ 72. Закон Кирхгофа
- •§ 73. Законы теплового излучения черного тела
- •§ 74. Формула Планка
- •§ 75. Фотоэффект
- •§ 76. Формула Эйнштейна для фотоэффекта
- •§ 77. Фотон
- •§ 78. Эффект Комптона
- •Глава 19. Квантовая механика § 79. Волны де Бройля
- •§ 80. Волновая функция
- •§ 81. Соотношение неопределенностей Гейзенберга
- •§ 82. Уравнение Шредингера
- •§ 83. Микрочастица в потенциальном ящике
- •Глава 20. Атомная физика § 84. Атом водорода
- •§ 85. Излучение и поглощение света атомом водорода
- •§ 86. Пространственное квантование
- •§ 87. Принцип Паули
- •Глава 21. Зонная теория твердых тел § 88. Металлы, полупроводники и диэлектрики
- •§ 89. Электронно-дырочная проводимость полупроводников
- •§ 90. Примесные полупроводники
- •Глава 22. Ядерная физика § 92. Строение атомного ядра
- •§ 93. Энергия связи ядра
- •§ 94. Радиоактивность
- •Контрольные задания 4 Вариант 1
- •Вариант 2
- •Вариант 3
- •Вариант 4
- •Вариант 5
- •Вариант 6
- •Вариант 7
- •Вариант 8
- •Вариант 9
- •Вариант 10
- •Вариант 11
- •Вариант 12
- •Вариант 13
- •Вариант 14
- •Вариант 15
- •Вариант 16
- •Вариант 17
- •Вариант 18
- •Вариант 19
- •Вариант 20
- •Вариант 21
- •Вариант 22
- •Вариант 23
- •Вариант 24
- •Вариант 25
- •Вариант 26
- •Вариант 27
- •Вариант 28
- •Вариант 29
- •Вариант 30
- •Экзаменационные вопросы 4
- •Приложение г
- •Оглавление
§ 30. Внутренняя энергия реального газа
Выражение для внутренней энергии идеального газа
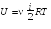
(30.1)
было получено без учета взаимодействия молекул. Для реального газа в выражении (30.1) необходимо прибавить потенциальную энергию П взаимодействия молекул газа:
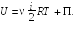
(30.2)
Потенциальная
энергия П обусловлена силами
межмолекулярного взаимодействия
молекул. Найдем П для газа, удовлетворяющего
уравнение Ван-дер-Вальса. При увеличении
объема от
![]() до
до
![]() газ совершает работу против сил взаимного
притяжения молекул
газ совершает работу против сил взаимного
притяжения молекул
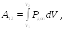
(30.3)
где Pдоп — дополнительное давление, испытываемое газом вследствие сил межмолекулярного притяжения. Подставляя формулу (29.3) в выражениях (30.3) и интегрируя, имеем
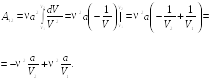
(30.4)
Так
как эта работа идет на приращение
потенциальной энергии взаимодействия
молекул
![]() можем написать
можем написать
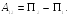
(30.5)
Сравнивая соотношение (30.4) и (30.5), получаем выражение для потенциальной энергии взаимодействия молекул:
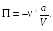
(30.6)
Подставляя формулу (30.6) в соотношение (30.2), получаем выражение для внутренней энергии газа:
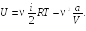
(30.7)
Экзаменационные вопросы 2
1. Уравнение состояния идеального газа.
2. Внутренняя энергия идеального газа.
3. Распределение Максвелла.
4. Барометрическая формула.
5. Распределение Больцмана.
6. Явления переноса.
7. Первый закон термодинамики.
8. Теплоемкость идеального газа при постоянном объеме.
9. Теплоемкость идеального газа при постоянном давлении.
10. Адиабатический процесс.
11. Энтропия.
12. Второй и третий законы термодинамики.
13. Силы межмолекулярного взаимодействия в реальных газах.
14. Уравнение Ван-дер-Ваальса.
15. Внутренняя энергия реального газа.
Контрольные задания 2 Вариант 1
1.
Баллон емкостью V
= 30 л содержит сжатый воздух при
![]() .
После того как, часть воздуха выпустили,
давление понизилось на
.
После того как, часть воздуха выпустили,
давление понизилось на
![]() Определить массу
Определить массу
![]() выпущенного
воздуха, если температура воздуха
осталась прежней.
выпущенного
воздуха, если температура воздуха
осталась прежней.
2.
Какое количество тепла
![]() надо сообщить кислороду массой
M = 30 г
для его изобарического нагревания на
надо сообщить кислороду массой
M = 30 г
для его изобарического нагревания на![]() ?
?
3.
Водород массой M = 6 г
расширяется изотермически от давления
![]() до давления
до давления
![]() .
Найти приращение
.
Найти приращение
![]() энтропии.
энтропии.
Вариант 2
1.
Полагая температуру воздуха и ускорение
свободного падения не зависимой от
высоты, определить, на какой высоте
![]() над уровнем моря плотность воздуха
меньше своего значения на уровне моря
в
над уровнем моря плотность воздуха
меньше своего значения на уровне моря
в
![]() раз. Температуру воздуха положить равной
раз. Температуру воздуха положить равной
![]() .
.
2.
Молярная теплоемкость газа изменяется
в ходе некоторого процесса по закону
![]() Найти количество тепла
Найти количество тепла
![]() ,
полученное одним молем газа при нагревании
от
,
полученное одним молем газа при нагревании
от
![]() до
до
![]() .
.
3.
Как отношение термодинамических
вероятностей
![]() двух макросостояний связано с приращением
двух макросостояний связано с приращением
![]() энтропии
этих состояний?
энтропии
этих состояний?
Вариант 3
1.
Найти плотность ρ водорода при температуре
![]() и давлении
и давлении
![]() .
.
2.
Газ совершает процесс по закону
![]() где
где
![]() и α — положительные постоянные. Найти
совершенную газом работу
и α — положительные постоянные. Найти
совершенную газом работу
![]() ,
если его объем увеличился от
,
если его объем увеличился от
![]() до
до
![]() .
.
3.
Кислород массой
M = 10 г
нагревается от температуры
![]() до температуры
до температуры
![]() .
Найти приращение
.
Найти приращение
![]() энтропии, если нагревание происходит
изобарически.
энтропии, если нагревание происходит
изобарически.
