- •Курс физики
- •Механика глава 1. Кинематика и динамика частицы § 1. Путь и перемещение
- •§ 2. Скорость и ускорение
- •§ 3. Сила и работа
- •Глава 2. Кинематика и динамика вращения твердого тела § 4. Угловая скорость и угловое ускорение
- •§ 5. Средняя скорость и среднее ускорение
- •§ 6. Момент силы
- •Глава 3. Законы сохранения § 7. Механическая энергия. Закон сохранения механической энергии
- •§ 8. Импульс. Закон сохранения импульса
- •§ 9. Момент импульса. Закон сохранения момента импульса
- •Глава 4. Механические колебания § 10. Гармонические колебания
- •§ 11. Затухающие колебания
- •§ 12. Вынужденные колебания
- •Глава 5. Механические волны § 13. Гармонические волны
- •§ 14. Плоская гармоническая волна
- •Экзаменационные вопросы 1
- •Контрольные задания 1 Вариант 1
- •Вариант 2
- •Вариант 3
- •Вариант 4
- •Вариант 5
- •Вариант 6
- •Вариант 7
- •Вариант 8
- •Вариант 9
- •Вариант 10
- •Вариант 11
- •Вариант 12
- •Вариант 13
- •Вариант 14
- •Вариант 15
- •Вариант 16
- •Вариант 17
- •Вариант 18
- •Вариант 19
- •Вариант 20
- •Вариант 21
- •Вариант 22
- •Вариант 23
- •Вариант 24
- •Вариант 25
- •Вариант 26
- •Вариант 27
- •Вариант 28
- •Вариант 29
- •Вариант 30
- •Приложение а
- •Молекулярная физика глава 6. Кинетическая теория газов § 15. Уравнение состояния идеального газа
- •§ 16. Внутренняя энергия идеального газа
- •§ 17. Распределение Максвелла
- •§ 18. Барометрическая формула
- •§ 19. Распределение Больцмана
- •§ 20. Явления переноса
- •Глава 7. Термодинамика § 21. Термодинамическая система и термодинамический процесс
- •§ 22. Первый закон термодинамики
- •§ 23. Теплоемкость идеального газа
- •§ 24. Адиабатический процесс
- •§ 25. Энтропия
- •§ 26. Второй и третий законы термодинамики
- •Глава 8. Реальные газы § 27. Силы межмолекулярного взаимодействия в газах
- •§ 28. Агрегатное состояние вещества
- •§ 29. Уравнение Ван-дер-Ваальса
- •§ 30. Внутренняя энергия реального газа
- •Экзаменационные вопросы 2
- •Контрольные задания 2 Вариант 1
- •Вариант 2
- •Вариант 3
- •Вариант 4
- •Вариант 5
- •Вариант 6
- •Вариант 7
- •Вариант 8
- •Вариант 9
- •Вариант 10
- •Вариант 11
- •Вариант 12
- •Вариант 13
- •Вариант 14
- •Вариант 15
- •Вариант 16
- •Вариант 17
- •Вариант 18
- •Вариант 19
- •Вариант 20
- •Вариант 21
- •Вариант 22
- •Вариант 23
- •Вариант 24
- •Вариант 25
- •Вариант 26
- •Вариант 27
- •Вариант 28
- •Вариант 29
- •Вариант 30
- •Приложение б
- •Электромагнетизм глава 9. Электрическое поле в вакууме § 31. Напряженность поля
- •§ 32. Поток вектора
- •§ 33. Теорема Гаусса для поля вектора
- •§ 34. Циркуляция вектора
- •§ 35. Потенциал поля
- •§ 36. Связь между φ и
- •Глава 10. Электрическое поле в диэлектрике § 37. Диполь в электрическом поле
- •§ 38. Поляризация диэлектрика
- •§ 39. Вектор
- •Глава 11. Энергия электрического поля § 40. Электроемкость
- •§ 41. Электроемкость плоского конденсатора
- •§ 42. Энергия электрического поля
- •Глава 12. Электрический ток § 43. Электрический ток
- •§ 44. Закон Ома для проводника
- •§ 45. Обобщенный закон Ома
- •§ 46. Закон Джоуля – Ленца
- •Глава 13. Магнитное поле в вакууме § 47. Магнитная индукция
- •§ 48. Закон Био – Савара
- •§ 49. Теорема Гаусса для поля вектора
- •§ 50. Теорема о циркуляции вектора
- •§ 51. Магнитное поле в соленоиде
- •§ 52. Закон Ампера
- •Глава 14. Магнитное поле в веществе § 53. Контур с током в магнитном поле
- •§ 54. Намагничивание магнетика
- •§ 55. Вектор
- •Глава 15. Энергия магнитного поля § 56. Индуктивность
- •§ 57. Электромагнитная индукция
- •§ 58. Энергия магнитного поля
- •Глава 16. Электромагнитные волны § 59. Вихревое электрическое поле
- •§ 60. Ток смещения
- •§ 61. Система уравнений Максвелла
- •§ 62. Электромагнитные волны
- •Глава 17. Волновая оптика § 63. Свет
- •§ 64. Интерференция света
- •§ 65. Дифракция света
- •§ 66. Поглощение света
- •§ 67. Рассеяние света
- •§ 68. Поляризация света
- •§ 69. Закон Малюса
- •§ 70. Вращение плоскости поляризации
- •Контрольные задания 3 Вариант 1
- •Вариант 2
- •Вариант 3
- •Вариант 4
- •Вариант 5
- •Вариант 6
- •Вариант 7
- •Вариант 8
- •Вариант 9
- •Вариант 10
- •Вариант 11
- •Вариант 12
- •Вариант 13
- •Вариант 14
- •Вариант 15
- •Вариант 16
- •Вариант 17
- •Вариант 18
- •Вариант 19
- •Вариант 20
- •Вариант 21
- •Вариант 22
- •Вариант 23
- •Вариант 24
- •Вариант 25
- •Вариант 26
- •Вариант 27
- •Вариант 28
- •Вариант 29
- •Вариант 30
- •Экзаменационные вопросы 3
- •Приложение в
- •Квантовая физика глава 18. Квантовая оптика § 71. Тепловое излучение
- •§ 72. Закон Кирхгофа
- •§ 73. Законы теплового излучения черного тела
- •§ 74. Формула Планка
- •§ 75. Фотоэффект
- •§ 76. Формула Эйнштейна для фотоэффекта
- •§ 77. Фотон
- •§ 78. Эффект Комптона
- •Глава 19. Квантовая механика § 79. Волны де Бройля
- •§ 80. Волновая функция
- •§ 81. Соотношение неопределенностей Гейзенберга
- •§ 82. Уравнение Шредингера
- •§ 83. Микрочастица в потенциальном ящике
- •Глава 20. Атомная физика § 84. Атом водорода
- •§ 85. Излучение и поглощение света атомом водорода
- •§ 86. Пространственное квантование
- •§ 87. Принцип Паули
- •Глава 21. Зонная теория твердых тел § 88. Металлы, полупроводники и диэлектрики
- •§ 89. Электронно-дырочная проводимость полупроводников
- •§ 90. Примесные полупроводники
- •Глава 22. Ядерная физика § 92. Строение атомного ядра
- •§ 93. Энергия связи ядра
- •§ 94. Радиоактивность
- •Контрольные задания 4 Вариант 1
- •Вариант 2
- •Вариант 3
- •Вариант 4
- •Вариант 5
- •Вариант 6
- •Вариант 7
- •Вариант 8
- •Вариант 9
- •Вариант 10
- •Вариант 11
- •Вариант 12
- •Вариант 13
- •Вариант 14
- •Вариант 15
- •Вариант 16
- •Вариант 17
- •Вариант 18
- •Вариант 19
- •Вариант 20
- •Вариант 21
- •Вариант 22
- •Вариант 23
- •Вариант 24
- •Вариант 25
- •Вариант 26
- •Вариант 27
- •Вариант 28
- •Вариант 29
- •Вариант 30
- •Экзаменационные вопросы 4
- •Приложение г
- •Оглавление
§ 16. Внутренняя энергия идеального газа
Внутреннюю
энергию
![]() газа определяют
как сумму кинетической энергии теплового
движения молекул и потенциальной энергии
межмолекулярного взаимодействия.
газа определяют
как сумму кинетической энергии теплового
движения молекул и потенциальной энергии
межмолекулярного взаимодействия.
Получим выражение для внутренней энергии идеального газа. В идеальном газе пренебрегают силами межмолекулярного взаимодействия. Поэтому внутренняя энергия идеального газа равна кинетической энергии его молекул.
Расчет дает, что средняя кинетическая энергия молекул
![]()
(16.1)
где
![]() — температура газа;
— температура газа;
![]() — постоянная
Больцмана
— постоянная
Больцмана
(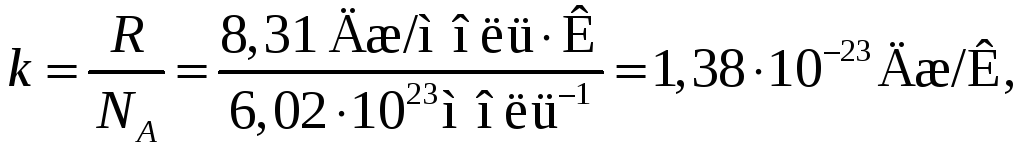 где NA
— число Авогадро — число молекул в
одном моле газа);
где NA
— число Авогадро — число молекул в
одном моле газа);
![]() — число
степеней свободы —
число независимых координат, с помощью
которых может быть задано положение
молекул в пространстве. Для определения
положения в пространстве одноатомной
молекулы достаточно трех координат
— число
степеней свободы —
число независимых координат, с помощью
которых может быть задано положение
молекул в пространстве. Для определения
положения в пространстве одноатомной
молекулы достаточно трех координат
![]() .
Следовательно, для
одноатомной молекулы
.
Следовательно, для
одноатомной молекулы
![]() .
Для определения
положения в пространстве двухатомной
молекулы достаточно трех координат
.
Для определения
положения в пространстве двухатомной
молекулы достаточно трех координат
![]() центра молекулы и двух значений углов
φ и υ, фиксирующих направление оси
молекулы. Следовательно, для
двухатомной молекулы
центра молекулы и двух значений углов
φ и υ, фиксирующих направление оси
молекулы. Следовательно, для
двухатомной молекулы
![]() .
Для определения
положения трехатомной и более молекулы
в пространстве достаточно трех координат
.
Для определения
положения трехатомной и более молекулы
в пространстве достаточно трех координат
![]() центра молекулы и трех значений углов
φ, υ и ψ, фиксирующих направление оси
молекулы. Следовательно, для
трехатомной и многоатомной молекулы
центра молекулы и трех значений углов
φ, υ и ψ, фиксирующих направление оси
молекулы. Следовательно, для
трехатомной и многоатомной молекулы
![]() .
.
Пусть в сосуде находится N молекул идеального газа. Тогда с учетом выражения (16.1) внутренняя энергия идеального газа
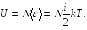
(16.2)
Учитывая, что
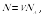
можем написать
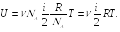
(16.3)
Отметим,
что внутренняя энергия является функцией
состояния. Это означает, например, что
при переходе газа из состояния 1 (с
температурой
![]() )
в состояние 2 (с температурой
)
в состояние 2 (с температурой
![]() )
приращение внутренней энергии
)
приращение внутренней энергии
![]() ,
т. е. не зависит от способа перехода газа
из состояния 1 в состояния 2, а определяется
только разностью значений внутренней
энергии газа в состояния 1 и 2.
,
т. е. не зависит от способа перехода газа
из состояния 1 в состояния 2, а определяется
только разностью значений внутренней
энергии газа в состояния 1 и 2.
Пример
16.1. Водород,
находящийся при нормальных условиях в
закрытом сосуде объемом V
= 5 л, охладили на
![]() .
Найти приращение внутренней энергии
газа.
.
Найти приращение внутренней энергии
газа.
|
Дано:
V = 5 л
|
Решение
|
|
|
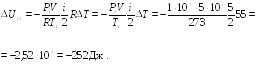
Ответ:
![]()
Пример
16.2. Водород
занимает объем
![]() при давлении
при давлении
![]() Его нагрели при постоянном объеме до
давления
Его нагрели при постоянном объеме до
давления
![]() Определить приращение
Определить приращение
![]() внутренней энергии газа.
внутренней энергии газа.
|
Дано:
|
Решение
|
|
|
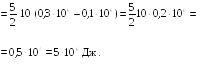
Ответ:
![]()
§ 17. Распределение Максвелла
Назовем состояние газа равновесным, если параметры состояния газа при отсутствии внешних воздействий остаются неизменными во времени.
Пусть
газ находится в равновесном состоянии
при температуре
![]() .
Молекулы газа, непрерывно сталкиваясь
между собой, меняют свои скорости как
по направлению, так и по величине. Мы не
можем сказать, с какой скоростью станет
двигаться произвольно выбранная молекула
в тот или иной момент времени. В то же
самое время мы можем говорить о некотором
стационарном (устойчивом) распределении
молекул по скоростям: одни молекулы
движутся быстро, другие медленно. Но на
всякий интервал скоростей, например от
10 до 20 м/с или от 20 до 30 м/с, будет приходиться
в среднем (по времени) некоторое
определенное число молекул. При отсутствии
внешних воздействий установившееся
при данной температуре распределение
молекул по скоростям в дальнейшем не
изменяется.
.
Молекулы газа, непрерывно сталкиваясь
между собой, меняют свои скорости как
по направлению, так и по величине. Мы не
можем сказать, с какой скоростью станет
двигаться произвольно выбранная молекула
в тот или иной момент времени. В то же
самое время мы можем говорить о некотором
стационарном (устойчивом) распределении
молекул по скоростям: одни молекулы
движутся быстро, другие медленно. Но на
всякий интервал скоростей, например от
10 до 20 м/с или от 20 до 30 м/с, будет приходиться
в среднем (по времени) некоторое
определенное число молекул. При отсутствии
внешних воздействий установившееся
при данной температуре распределение
молекул по скоростям в дальнейшем не
изменяется.
Определим
вероятность того, что модуль скорости
молекулы лежит между v
и v + dv.
Пусть
![]() — общее число молекул в единице объема
газа, а
— общее число молекул в единице объема
газа, а
![]() — число молекул в единице объема газа,
скорости которых лежат между v
и v + dv.
Тогда искомая вероятность
— число молекул в единице объема газа,
скорости которых лежат между v
и v + dv.
Тогда искомая вероятность
.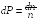
(17.1)
Введем величину
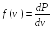
(17.2)
— плотность вероятности, которая является функцией модуля скорости молекулы, в связи с чем ее называют функцией распределения вероятности молекул по скорости или просто функцией распределения молекул по скоростям.
Комбинируя формулы (17.1) и (17.2), получаем
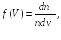
(17.3)
откуда
(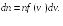 17.4)
17.4)
Зная вид функции f(v), можно, интегрируя выражение (17.4), определить количество молекул в единице объема газа, скорости которых лежат в любом интервале скоростей.
Максвелл теоретически получил вид функции распределения молекул по скоростям:
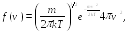
(17.5)
где
![]() и
и
![]() — масса молекулы и температура газа;
— масса молекулы и температура газа;
![]() — постоянная Больцмана.
— постоянная Больцмана.
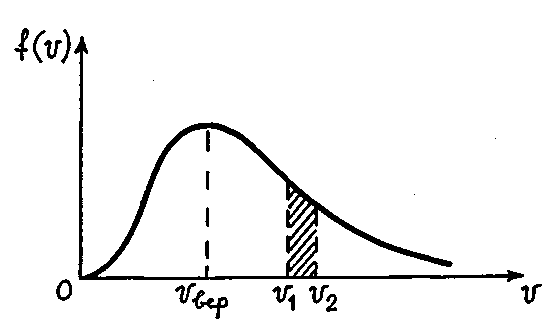
Рис. 17.1
Из графика видно, что вероятность обнаружения в газе молекулы со скоростью, лежащей в интервале от v1 до v2 (см. формулу (17.2))
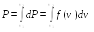
равна заштрихованной площади под кривой f(v).
Вероятность
обнаружения в газе молекул с любой
скоростью от 0 до
![]()
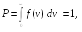
(17.6)
т. е. площадь под всей кривой f(v) равна единице. Выражение (17.6) называют условием нормировки вероятности.
Скорость, соответствующая максимуму функции распределения f(v), будет наиболее вероятной vвер скоростью молекул. Найдем эту скорость.
Для
![]() очевидно
очевидно
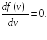
Продифференцируем выражение (17.5) по v и приравняем к нулю.
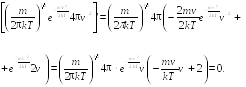
При v = 0 и v = ∞ функция f(v) минимальна. Следовательно, эти значения отбрасываем. Остается
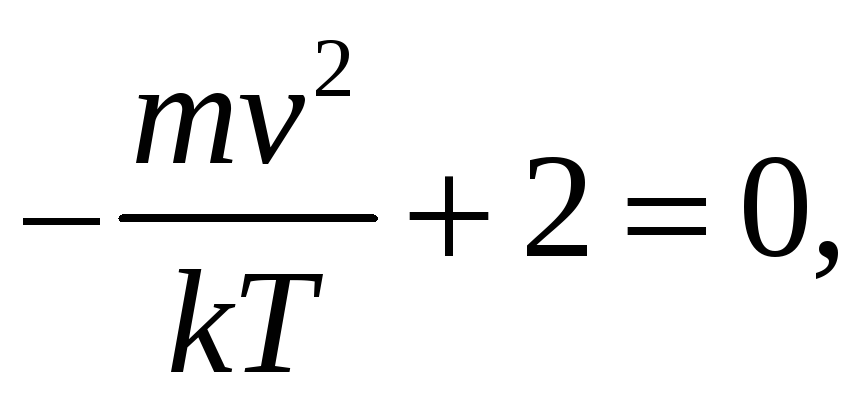
откуда
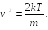
Откуда получаем
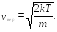
(17.7)
Используя
функцию распределения (17.5), можно найти
среднюю
![]() и среднюю
квадратичную vкв
скорости молекул:
и среднюю
квадратичную vкв
скорости молекул:
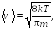
(17.8)
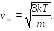 (17.9)
(17.9)

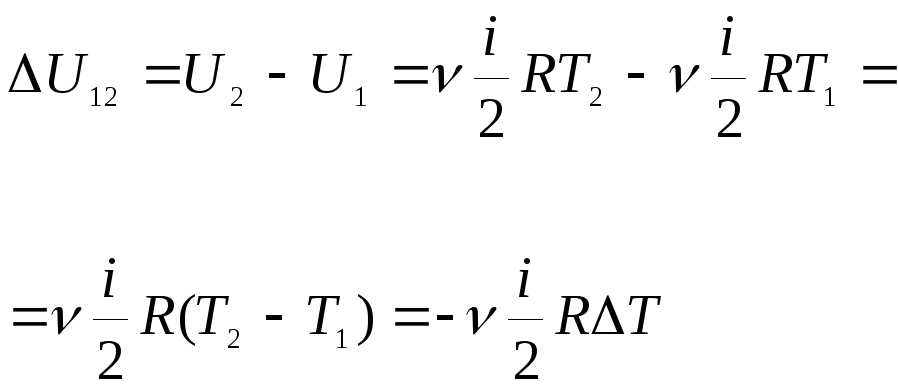
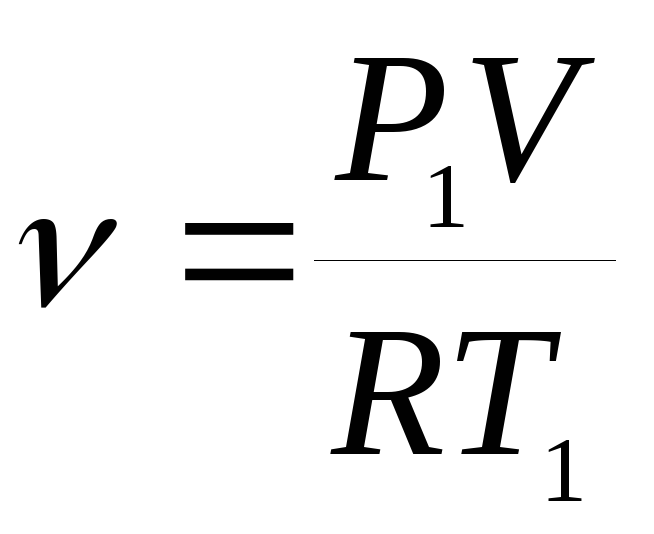 .
.